Актуальные вопросы подготовки к государственной итоговой аттестации по химии 2020 года
Проверка качества обученности выпускников основной и средней школы в России осуществляется в форме ГИА (ОГЭ и ЕГЭ).
Нормативные правовые документы, регламентирующие проведение ГИА
- Федеральный закон от 29.12.2012 № 273-ФЗ «Об образовании в Российской Федерации»;
- Постановление Правительства Российской Федерации от 28.07.2018 № 885 «Об утверждении Положения о Федеральной службе по надзору в сфере образования и науки и признании утратившими силу некоторых актов Правительства Российской Федерации»;
- Постановление Правительства Российской Федерации от 31.08.2013 № 755 «О федеральной информационной системе обеспечения проведения государственной итоговой аттестации обучающихся, освоивших основные образовательные программы основного общего и среднего общего образования, и приема граждан в образовательные организации для получения среднего профессионального и высшего образования и региональных информационных системах обеспечения проведения государственной итоговой аттестации обучающихся, освоивших основные образовательные программы основного общего и среднего общего образования» (вместе с прилагаемыми Правилами формирования и ведения федеральной информационной системы обеспечения проведения государственной итоговой аттестации обучающихся, освоивших основные образовательные программы основного общего и среднего общего образования, и приема граждан в образовательные организации для получения среднего профессионального и высшего образования и региональных информационных систем обеспечения проведения государственной итоговой аттестации обучающихся, освоивших основные образовательные программы основного общего и среднего общего образования (далее – Правила формирования и ведения ФИС/РИС);
- Приказ Минпросвещения России и Рособрнадзора от 07.11.2018 № 189/1513 «Об утверждении Порядка проведения государственной итоговой аттестации по образовательным программам основного общего образования» (зарегистрирован Минюстом 10.12.2018 регистрационный № 52953);
- Приказ Федеральной службы по надзору в сфере образования и науки от 17.12.2013 № 1274 «Об утверждении Порядка разработки использования и хранения контрольных измерительных материалов при проведении государственной итоговой аттестации по образовательным программам основного общего образования и Порядка разработки, использования и хранения контрольных измерительных материалов при проведении государственной итоговой аттестации по образовательным программам среднего общего образования».
Формирование КИМов по химии
КИМы ОГЭ и ЕГЭ по химии формируются ОИВ (Орган исполнительной власти субъекта Российской Федерации, осуществляющий государственное управление в сфере образования) с помощью открытого банка заданий и специализированного ПО (программного обеспечения).
Параметры доступа к открытому банку заданий, специализированному ПО, указаниям по работе с данным ПО, общим требованиям к сборке КИМ ОГЭ и ЕГЭ по химии, а также общим требованиям к форматированию вариантов КИМ предоставляются ФИПИ уполномоченному представителю ОИВ, ответственному за формирование КИМ ОГЭ и ЕГЭ по химии.
ОИВ обеспечивают информационную безопасность при хранении, использовании и передаче КИМ, в том числе определяют места хранения КИМ, лиц, имеющих к ним доступ, принимают меры по защите КИМ от разглашения содержащейся в них информации.
Спецификации Экзаменационных материалов по химии для проведения ОГЭ и ЕГЭ по химии размещаются на официальном сайте ФИПИ (http://fipi.ru/).
На всех этапах работы с КИМ ГИА ОИВ принимает меры по обеспечению их информационной безопасности.
Государственная итоговая аттестация по химии основного общего образования в форме основного государственного экзамена (ОГЭ)
Назначение контрольных измерительных материалов (КИМ) ОГЭ
Основной государственный экзамен (ОГЭ) представляет собой форму государственной итоговой аттестации, проводимой в целях определения соответствия результатов освоения обучающимися основных образовательных программ основного общего образования соответствующим требованиям федерального государственного образовательного стандарта. Для указанных целей используются контрольные измерительные материалы (КИМ), представляющие собой комплексы заданий стандартизированной формы. ОГЭ проводится в соответствии с Федеральным законом «Об образовании в Российской Федерации» от 29.12.2012 № 273-ФЗ и Порядком проведения государственной итоговой аттестации по образовательным программам основного общего образования, утверждённым приказом Минпросвещения России и Рособрнадзора от 07.11.2018 № 189/1513.
Документы, определяющие содержание КИМ ОГЭ по химии
Содержание КИМ определяется на основе Федерального государственного образовательного стандарта основного общего образования (приказ Минобрнауки России от 17.12.2010 № 1897) с учётом Примерной основной образовательной программы основного общего образования (одобрена решением Федерального учебно-методического объединения по общему образованию (протокол от 08.04.2015 № 1/15)). В КИМ обеспечена преемственность проверяемого содержания с Федеральным компонентом государственного стандарта основного общего образования по химии (приказ Минобразования России от 05.03.2004 № 1089 «Об утверждении Федерального компонента государственных образовательных стандартов начального общего, основного общего и среднего (полного) общего образования»).
Подходы к отбору содержания, разработке структуры КИМ ОГЭ по химии
Разработка КИМ осуществлялась с учётом следующих общих положений.
- КИМ ориентированы на проверку усвоения системы знаний, которая рассматривается в качестве инвариантного ядра содержания действующих программ по химии для основной школы. Требования к результатам обучения определяются в соответствии с Федеральным государственным образовательным стандартом основного общего образования.
- КИМ призваны обеспечивать возможность дифференцированной оценки подготовки выпускников. В этих целях проверка усвоения основных элементов содержания курса химии в VIII–IX классах осуществляется на трёх уровнях сложности: базовом, повышенном и высоком.
- Учебный материал, на базе которого строятся задания, отбирается по признаку его значимости для общеобразовательной подготовки выпускников основной школы. При этом особое внимание уделяется тем элементам содержания, которые получают своё развитие в курсе химии X–XI классов. Содержание заданий разработано по основным темам курса химии, объединённых в шесть содержательных блоков:
- «Основные понятия химии (уровень атомно-молекулярных представлений)»;
- «Периодический закон и Периодическая система химических элементов Д.И. Менделеева»;
- «Строение вещества»;
- «Многообразие химических реакций»;
- «Многообразие веществ»;
- «Экспериментальная химия».
Предлагаемая в 2020 г. модель КИМ является переходной, т.е. включающей задания как экзаменационной модели 2019 г., так и задания перспективной модели 2021 г. Такой подход позволяет постепенно переориентировать подготовку экзаменуемых на новые модели заданий. Главной особенностью экзаменационного варианта 2020 г. является наличие в нём двух заданий, предполагающих составление уравнений двух реакций и проведение в соответствии с ними реального химического эксперимента.
Важнейшей особенностью ФГОС является названный в качестве основного системно-деятельностный подход в обучении, который предусматривает активное включение обучающихся в деятельность, направленную на освоение новых и развитие имеющихся знаний и умений. Необходимым условием для реализации такого подхода является формирование у обучающихся общеучебных умений, которые нередко обозначают словосочетанием «умение учиться».
В ФГОС такие обобщённые способы учебной деятельности получили название «универсальных учебных действий» (УУД). Именно УУД (регулятивные, познавательные, коммуникативные) составили основу метапредметных результатов, которые включают также освоенные обучающимися меж- и метапредметные понятия, а также способность их использовать в учебной, познавательной и социальной практике, самостоятельно планировать и осуществлять учебную деятельность, организовывать учебное сотрудничества с педагогами и сверстниками. Актуальность контроля сформированности УУД обусловлена ещё и тем, что они являются одним из объектов оценивания в рамках международных мониторинговых исследований качества образования, таких как TIMSS (исследуется естественнонаучная подготовка) и PISA (исследуется естественнонаучная грамотность). Следует заметить, что знаниевый компонент данных исследований для российского образования менее актуален с точки зрения анализа результатов, т.к. содержание курса химии в российской школе имеет более предметноориентированную направленность. Вместе с тем, предлагаемое для изучения в российской школе химическое содержание предоставляет все возможности для формирования разнообразных умений, относящихся к разным группам УУД.
Поэтому бóльший интерес при анализе результатов данных исследований представляет проверяемый ими комплекс умений: давать научные объяснения явлениям окружающего мира, применять методы естественнонаучного исследования, интерпретировать данные и использовать научные доказательства для получения выводов и др.
Ещё одной важной особенностью данных исследований является наличие заданий, предусматривающих работу с информацией, предложенной в различной форме: текст, изображения, таблицы, графики, схемы и т.д. Причём содержание таких заданий, как правило, имеет практикоориентированную специфику. Таким образом, можно констатировать, что основным подходом, который реализуется в международных мониторинговых исследованиях оценки качества образования, является «компетентностно-ориентированный подход». Однако при всей важности его учёта при определении перспектив российского школьного химического образования не менее важным является сохранение традиционно сильной стороны нашего образования, предусматривающей формирование у обучающихся базовых системно-научных знаний, которые являются составляющей общего культурного уровня человека.
Не менее важным в процессе изучения курса химии также является усиление внимания прикладному аспекту химических знаний. Именно непонимание возможности применения школьных химических знаний в повседневной жизни является одной из причин низкой популярности данного предмета у школьников. Вместе с тем при всей значимости и кажущейся доступности для понимания школьников данного материала его включение в процесс обучения вызывает большие сложности.
Это обусловлено рядом причин. Например, тем, что многое из того, что относится к бытовым химическим знаниям, относится к разделам химии, изучаемым преимущественно в высшей школе, таким как: биохимия, физхимия, коллоидная химия, химия высокомолекулярных соединений и др., а, следовательно, вызовет серьёзные затруднения в понимании школьниками их научной составляющей. Кроме того, в учебных методических комплектах по химии изучению практикоориентированного материала уделено различное внимание и рассматриваются его разные аспекты, которые сопровождаются преимущественно красочными иллюстрациями-примерами применения веществ, без разъяснения логической цепочки:
состав — строение — свойства — применение.
В качестве ещё одной причины трудности включения вышеуказанного материала в учебный процесс является нарушение связей с другими предметами естественнонаучного цикла: программы физики и биологии часто не согласованы с точки зрения порядка изучения содержательных разделов курсов с курсом химии, что, например, затрудняет понимание материала о строении атома, общих свойствах металлов, роли микроэлементов в живых организмах, изменениях, происходящих с веществами в природе и др. Не является секретом и то, что времени на подробное изучение данного материала на уроках выделяется мало, т.к. предполагается, что он доступен для понимания и при самостоятельном изучении. Ещё больше затруднений вызывает включение прикладного и/или практикоориентированного материала курса химии в КИМ ОГЭ, особенно в аспекте вышеназванной специфики его изучения в основной школе.
Если в рамках текущего и рубежного (тематического) контроля учитель сам определяет принципы отбора, объём и глубину предъявления материала, решает вопрос о включении заданий межпредметной и метапредметной направленности, различной формы и уровня сложности прикладного материала, а, следовательно, и определяет требования к контролю и оцениванию, то его проверка на ОГЭ имеет другие особенности. Основной формой заданий в КИМ ОГЭ являются задания с кратким и развёрнутым ответом, которые должны соответствовать определённым требованиям:
во-первых, контролировать достижение предметных результатов;
во-вторых, иметь чёткую систему оценивания, которая в баллах отражает уровень сложности заданий, а также число мыслительных операций (действий), которые необходимо осуществить обучающимися для их выполнения.
С учётом вышеперечисленного комиссия разработчиков КИМ по химии разработана перспективная экзаменационная модель по химии для проведения основного государственного экзамена, которая полностью отвечает требованиям ФГОС ООО в 2020 году.
В КИМе ОГЭ с одной стороны сохранён системный подход к проверке химических знаний и умений, а с другой — увеличена доля заданий, которые предполагают работу с информацией, представленной в различной форме. Важным новшеством в экзаменационных вариантах также стало исключение заданий с выбором одного варианта ответа из четырёх возможных. Основными формами становятся задания с кратким ответом и с развёрнутым ответом.
Связь экзаменационной модели ОГЭ по химии с КИМ ЕГЭ по химии
При разработке КИМов ОГЭ важно было также учесть преемственность с формами заданий ЕГЭ. Даже в методической литературе ОГЭ нередко называют «малым ЕГЭ». И это в значительной степени оправдано, т.к. многое из того, что выпускники 9-го класса изучают в основной школе на этапе подготовки к ОГЭ, становится базой для последующей подготовки к ЕГЭ по химии. В связи с этим в экзаменационном варианте ОГЭ были сохранены некоторые задания, формулировки которых аналогичны заданиям экзаменационного варианта ЕГЭ.
Преемственность модели ОГЭ 2020 г. с КИМ ЕГЭ проявляется как в содержательной, так и в деятельностной составляющей экзаменационной модели. Это стало возможным, прежде всего благодаря использованию форм и формулировок заданий, аналогичных моделям заданий ЕГЭ. Так, для проверки сформированности усвоения понятий, изучаемых в систематическом курсе химии основной школы, предлагаются задания на сравнение или классификацию предлагаемых объектов, а также на их применение в процессе анализа химической информации. В вариант ОГЭ также включены задания, предусматривающие проверку умения прогнозировать возможность протекания химических реакций и состав образующихся продуктов реакций, описывать признаки их протекания или определять реактивы, необходимые для проведения качественных реакций. Так же, как и в варианте ЕГЭ, большое внимание уделено проверке сформированности системных знаний о химических свойствах неорганических веществ.
Например:
Пример1. (аналог задания 8 КИМ ЕГЭ). Установите соответствие между формулой вещества и реагентами, с которыми это вещество может вступать в реакцию: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.

Запишите в таблицу выбранные цифры под соответствующими буквами:
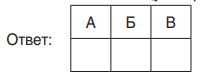
Пример 2. (аналог задания 9 КИМ ЕГЭ) Установите соответствие между реагирующими веществами и продуктами их взаимодействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.

Запишите в таблицу выбранные цифры под соответствующими буквами.
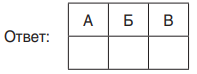
Не менее значимым стало сохранение направленности КИМ на проверку усвоения системы химических знаний, которые с одной стороны служат основой формирования общего культурного уровня человека, а с другой — обеспечивают возможность получения профильного химического образования. В этой связи КИМ были составлены с учётом преемственности с действующими моделями заданий ОГЭ и ЕГЭ, в которых данный подход был заложен изначально.
Характеристика структуры и содержания КИМ ОГЭ по химии
Работа состоит из двух частей.
Часть 1 содержит 19 заданий с кратким ответом, подразумевающих самостоятельное формулирование и запись ответа в виде цифры или последовательности цифр.
Часть 2 содержит 5 заданий. 3 задания этой части подразумевают запись развёрнутого ответа. 2 задания этой части предполагают выполнение реального химического эксперимента и оформление его результатов.
Распределение заданий по частям КИМ представлено в таблице 1.
Таблица 1
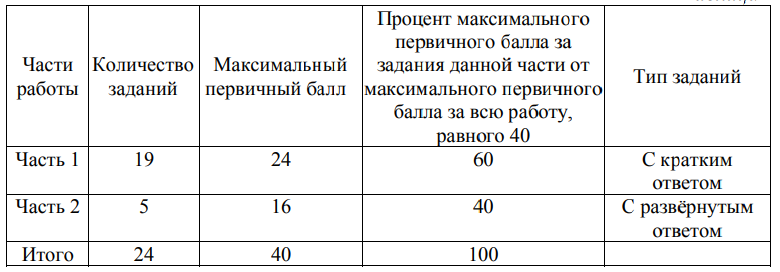
Распределение заданий КИМ ОГЭ по содержанию, проверяемым умениям и способам деятельности
При определении количества заданий КИМ ОГЭ, ориентированных на проверку усвоения учебного материала отдельных содержательных блоков/линий, учитывался, прежде всего, занимаемый ими объём в содержании курса химии.
Например, был принят во внимание тот факт, что в системе подготовки обучающихся основной школы наибольший объём знаний, определяющих уровень их подготовки, относится к таким содержательным блокам, как «Многообразие химических реакций» и «Многообразие веществ». По этой причине суммарная доля заданий (от общего количества всех заданий), проверяющих усвоение их содержания, составила 30% по каждому из разделов. Значительная доля заданий, включённых в вариант, относится также к разделу «Экспериментальная химия». Представление о распределении заданий по содержательным разделам даёт таблица 2.
Таблица 2
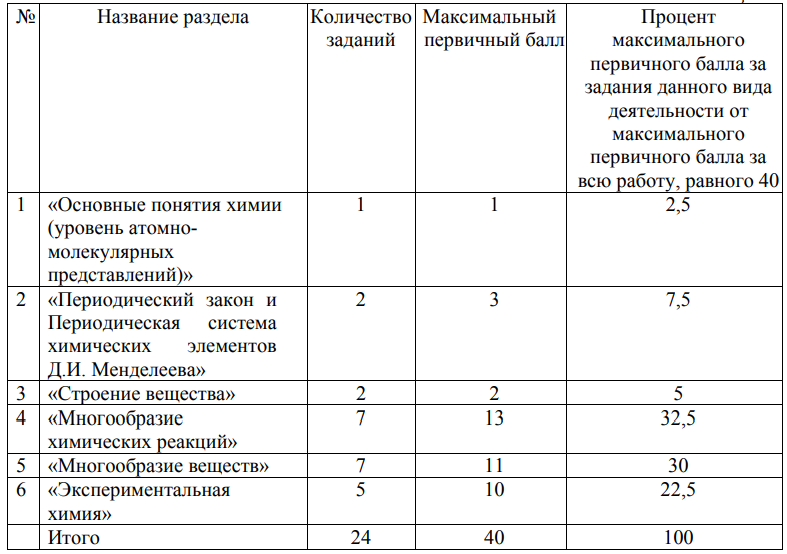
Распределение заданий КИМ ОГЭ по уровням сложности
Часть 1 КИМ содержит 14 заданий базового уровня сложности и 5 заданий повышенного уровня сложности.
Часть 2 содержит 5 заданий высокого уровня сложности.
Распределение заданий по уровням сложности представлено в таблице 3.
Таблица 3
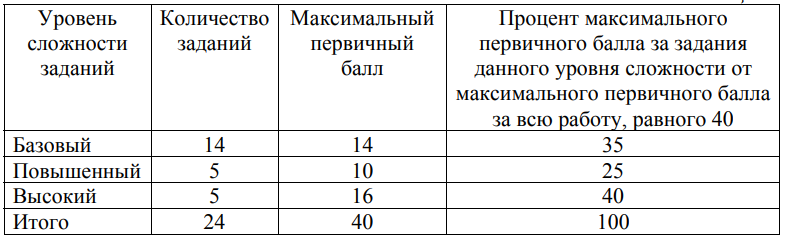
Продолжительность ОГЭ по химии
На выполнение работы по химии отводится 140 минут. Время, отводимое на решение заданий части 1, не ограничивается. Рекомендуемое время на выполнение заданий части 1 – 50 минут, а на выполнение заданий части 2 – 90 минут (1 час 30 минут), которые включают 25 минут, отводимые на выполнение заданий 23 и 24.
Дополнительные материалы и оборудование
Перечень дополнительных материалов и оборудования, пользование которыми разрешено на ОГЭ, утверждается приказом Минпросвещения России и Рособрнадзора.
На экзамене по химии разрешается использовать следующие материалы и оборудование:
- Периодическая система химических элементов Д.И. Менделеева;
- таблица растворимости солей, кислот и оснований в воде;
- электрохимический ряд напряжений металлов;
- непрограммируемый калькулятор;
- лабораторное оборудование для проведения химических опытов, предусмотренных заданиями.
Проведение лабораторных опытов при выполнении задания 24 осуществляется в специальном помещении – химической лаборатории, оборудование которой должно отвечать требованиям СанПиН.
Система оценивания выполнения отдельных заданий и работы в целом
Верное выполнение каждого из заданий 1–5, 7–9, 12, 14–17, 19 оценивается 1 баллом.
За полный правильный ответ на каждое из заданий 6, 10, 11, 13, 18 ставится 2 балла; если допущена одна ошибка, то ответ оценивается в 1 балл. Если допущено две и более ошибки или ответа нет, то выставляется 0 баллов.
Максимальное количество баллов, которое можно получить за выполнение заданий части 1, равно 24.
Проверка выполнения заданий 20–24 части 2 осуществляется предметной комиссией. При оценивании каждого из заданий эксперт на основе сравнения ответа выпускника с образцом ответа, приведённым в критериях оценивания, выявляет в ответе экзаменуемого элементы, каждый из которых оценивается 1 баллом.
Максимальная оценка за верно выполненное задание: за задания 20 и 22 – по 3 балла; за задания 21 и 23 – по 4 балла; за задание 24 – 2 балла.
Задания с развёрнутым ответом могут быть выполнены экзаменуемым разными способами. Поэтому приведённые в критериях оценивания образцы решений следует рассматривать лишь как один из возможных вариантов ответа. Это относится, прежде всего, к способам решения расчётных задач.
Максимальное количество баллов, которое можно получить за выполнение заданий части 2, равно 16. Максимальное количество первичных баллов, которое можно получить за выполнение всех заданий КИМ работы, равно 40. В соответствии с Порядком проведения государственной итоговой аттестации по образовательным программам основного общего образования (приказ Минпросвещения России и Рособрнадзора от 07.11.2018 № 189/1513 зарегистрирован Минюстом России 10.12.2018 № 52953):
64 Экзаменационные работы проверяются двумя экспертами. По результатам проверки эксперты независимо друг от друга выставляют баллы за каждый ответ на задания экзаменационной работы. В случае существенного расхождения в баллах, выставленных двумя экспертами, назначается третья проверка. Существенное расхождение в баллах определено в критериях оценивания по соответствующему учебному предмету. Третий эксперт назначается председателем предметной комиссии из числа экспертов, ранее не проверявших экзаменационную работу. Третьему эксперту предоставляется информация о баллах, выставленных экспертами, ранее проверявшими экзаменационную работу обучающегося. Баллы, выставленные третьим экспертом, являются окончательными». Существенным считается расхождение между баллами, выставленными двумя экспертами за выполнение любого из заданий 20–24, в 2 или более балла. В этом случае третий эксперт проверяет только те ответы на задания, которые вызвали столь существенное расхождение. На основе баллов, выставленных за выполнение всех заданий работы, подсчитывается общий балл, который переводится в отметку по пятибалльной шкале.
Изменения в КИМ ОГЭ по химии 2020 года по сравнению с 2019 годом
В экзаменационную работу 2020 г. по сравнению с работой 2019 г. внесены следующие изменения.
- В целях повышения деятельностной составляющей заданий и снижения вероятности случайного выбора правильного ответа увеличена доля заданий с множественным выбором ответа (6, 7, 12, 14, 15) и заданий на установление соответствия между позициями двух множеств (10, 13, 16).
- Добавлено задание 1, предусматривающее проверку умения работать с текстовой информацией, отражающей различия в содержательной нагрузке понятий. В задании требуется выбрать два утверждения, в которых химический термин используется в определённом смысловом значении.
- Из части 1 экзаменационного варианта исключено задание, проверяющее сформированность знаний по разделу «Первоначальные сведения об органических веществах».
- В часть 2 включено задание 21, предусматривающие проверку понимания существования взаимосвязи между различными классами неорганических веществ и сформированности умения составлять уравнения реакций, отражающих эту связь. Ещё одним контролируемым умением является умение составлять уравнения реакций ионного обмена, в частности сокращённое ионное уравнение.
- В экзаменационный вариант добавлена обязательная для выполнения практическая часть, которая включает в себя два задания: 23 и 24. В задании 23 из предложенного перечня необходимо выбрать два вещества, взаимодействие с которыми отражает химические свойства указанного в условии задания вещества, и составить с ними два уравнения реакций. Задание 24 предполагает проведение двух реакций, соответствующих составленным уравнениям реакций.
Минимальный набор оборудования, необходимый для проведения практических работ
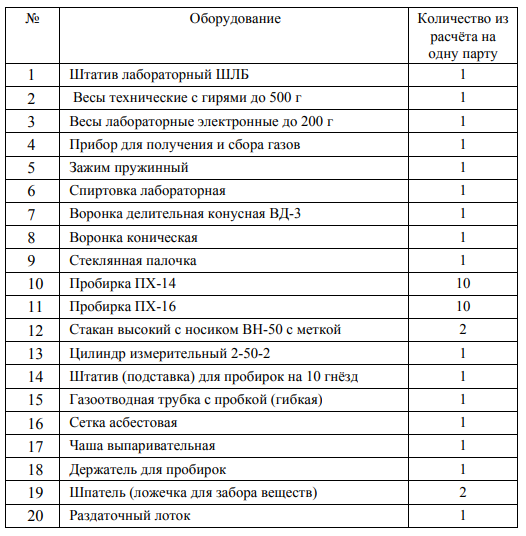
Оборудование для приготовления и хранения растворов в лаборатории
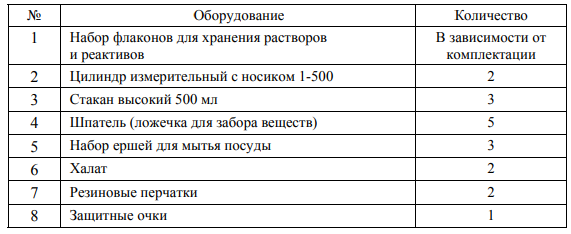
Расходные материалы, необходимые для проведения химических экспериментов

Минимальный набор реактивов, необходимый для проведения химического эксперимента на экзамене
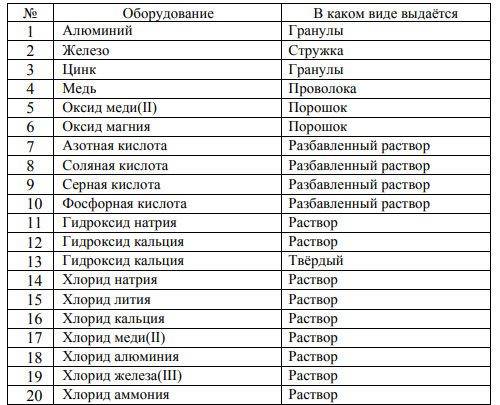
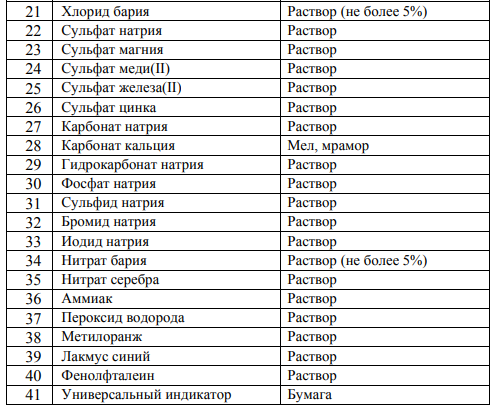
Методические рекомендации по подготовке к ОГЭ по химии в 2020 году
Задания части 1 позволяют проверить усвоение значительного количества элементов содержания:
- знание языка науки и основ химической номенклатуры,
- химических законов и понятий,
- закономерностей изменения свойств химических элементов и веществ по группам и периодам,
- общих свойств металлов и неметаллов, основных классов неорганических веществ, признаков и условий протекания химических реакций,
- особенностей протекания реакций ионного обмена и окислительно-восстановительных реакций,
- правил обращения с веществами и техники безопасности при работе с лабораторным оборудованием и др.
В экзаменационном материале части 2 задания с развернутым ответом наиболее сложные. Эти задания проверяют усвоение следующих элементов содержания: способы получения и химические свойства различных классов неорганических соединений, реакции ионного обмена, окислительно-восстановительные реакции, взаимосвязь веществ различных классов, количество вещества, молярный объем и молярная масса вещества, массовая доля растворенного вещества. Также задания части 2 проверяют практические умения обучающихся.
В экзаменационный вариант части 2 включено задание 21, предусматривающие проверку понимания существования взаимосвязи между различными классами неорганических веществ и сформированности умения составлять уравнения реакций, отражающих эту связь.
Ещё одним контролируемым умением является умение составлять уравнения реакций ионного обмена, в частности сокращённое ионное уравнение. Также, добавлена обязательная для выполнения практическая часть, которая включает в себя два задания: 23 и 24. В задании 23 из предложенного перечня необходимо выбрать два вещества, взаимодействие с которыми отражает химические свойства указанного в условии задания вещества, и составить с ними два уравнения реакций. Задание 24 предполагает проведение двух реакций, соответствующих составленным уравнениям реакций.
Рассмотрим пример, из демоверсии ОГЭ 2020 года.
- Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой
MnO2 + HBr → MnBr2 + Br2 + H2O
Определите окислитель и восстановитель.
Критерии оценивания:

Подчеркнём, что экзаменуемый должен корректно указывать степени окисления, не путать степень окисления с зарядом иона. Если экзаменуемый указывает, что окислителем является Mn4+ или восстановителем является Вr1- (для дихромата часто пишут окислителем является Cr6+ или Cr26+) такие варианты ответа засчитаны не будут. Подобных ионов в водном растворе не существует!
- Дана схема превращений:
Fe(NO3)2 → Fe(OH)2 → X → Fe2O3
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение реакции.
Критерии оценивания:

Экзаменуемый должен представить в работе только один вариант ответа, при наличии нескольких вариантов эксперт рассматривает только первый, записанный на бланке. Хотелось бы обратить особое внимание на особенности выполнения этого задания.
- При составлении сокращённого уравнения важно, чтобы коэффициенты в этом уравнении были минимальными.
Например, уравнение
2H+ + 2OH- = 2H2O
не может быть засчитано, в данном случае экзаменуемый должен записать:
H+ + OH- = H2O
- Запись заряда иона в ионных уравнениях должна быть корректной, например: Al3+, C1l-, SO42- . Неправильными будет считаться запись: Al+3, Cl-1, SO4-2. Подобных ионов в водном растворе не существует!
- После пропускания через раствор гидроксида натрия 2,24 л сернистого газа (н.у.) получили 252 г раствора сульфита натрия. Вычислите массовую долю соли в полученном растворе.
Критерии оценивания:

Подчеркнём, что экзаменуемый может решить задачу любым способом. Как, через количественное соотношение, так и используя метод пропорций. Главное, чтобы он пришел к верному ответу.
Практическая часть
Дан раствор сульфата магния, а также набор следующих реактивов: цинк; соляная кислота; растворы гидроксида натрия, хлорида бария и нитрата калия.
- Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата магния, и укажите признаки их протекания.
Критерии оценивания:

Подчеркнём, что экзаменуемый должен проанализировать свойства, и определить в каком из случаев соблюдается правило Бертолле (выделяется газ, выпадает осадок или образуется вода). Указывая, признаки реакции, важно указывать изменение цвета, цвет осадка, охарактеризовать характер запах (выпадение осадка белого цвета; выпадение осадка голубого цвета; малиновый раствор стал прозрачным; выделение газа без цвета и запаха…)
Важно, что именно эти две реакции экзаменуемый будет проводить практически в задании 24 (ему будет выдано две пробирки и предложена только одна возможность доказать экспериментально указанные в номере 23 реакции).
Допускаются и иные (чем указаны в критериях ответа) формулировки ответа, не искажающие его смысл.
- Проведите химические реакции между сульфатом магния и выбранными веществами в соответствии с составленными уравнениями реакции, соблюдая правила техники безопасности, приведённые в инструкции к заданию. Опишите изменения, происходящие с веществами в ходе проведённых реакций.
Следует отменить важность предварительной подготовки с обучающимися к данному практико-ориентированному заданию, необходимо проработать техники эксперимента, повторить технику безопасности, так как будут учитываться умения обучающегося проводить эксперимент в соответствии с правилами техники безопасности работы в химической лаборатории.
Критерии оценивания:

Пример 2 задания 23:
Дан раствор карбоната калия, а также набор следующих реактивов: растворы азотной кислоты, гидроксида натрия, хлорида кальция и нитрата натрия.
- Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата магния, и укажите признаки их протекания.
Возможный ответ:

Пример 3 задания 23:
Дан раствор сульфата лития, а также набор следующих реактивов: растворы фосфата натрия, нитрата бария, хлорида магния, гидроксида калия и азотной кислоты.
- Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата магния, и укажите признаки их протекания.
Возможный ответ:

Пример 4 задания 23:
Дан раствор хлорида магния, а также набор следующих реактивов: цинк, растворы сульфата натрия гидроксида лития, фторида калия и хлорида цинка.
- Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата магния, и укажите признаки их протекания.
Возможный ответ:

Государственная итоговая аттестация по химии среднего общего образования в форме единого государственного экзамена (ЕГЭ)
Назначение контрольных измерительных материалов (КИМ) ЕГЭ
Единый государственный экзамен (ЕГЭ) представляет собой форму государственной итоговой аттестации, проводимой в целях определения соответствия результатов освоения обучающимися основных образовательных программ среднего общего образования соответствующим требованиям федерального государственного образовательного стандарта или образовательного стандарта. Для указанных целей используются контрольные измерительные материалы (КИМ), представляющие собой комплексы заданий стандартизированной формы. ЕГЭ проводится в соответствии с Федеральным законом «Об образовании в Российской Федерации» от 29.12.2012 № 273-ФЗ и Порядком проведения государственной итоговой аттестации по образовательным программам среднего общего образования, утверждённого приказом Минпросвещения России и Рособрнадзора от 07.11.2018 № 190/1512.
Документы, определяющие содержание КИМ ЕГЭ
Содержание КИМ ЕГЭ определяется на основе Федерального компонента государственного стандарта среднего (полного) общего образования по химии, базовый и профильный уровни (приказ Минобразования России от 05.03.2004 № 1089).
Подходы к отбору содержания, разработке структуры КИМ ЕГЭ
Отбор содержания КИМ для проведения ЕГЭ по химии в 2020 г. в целом осуществлялся с учётом тех общих установок, на основе которых формировались экзаменационные модели предыдущих лет.
В числе этих установок наиболее важными с методической точки зрения являются следующие:
- КИМ ориентированы на проверку усвоения системы знаний, которая рассматривается в качестве инвариантного ядра содержания действующих программ по химии для общеобразовательных организаций. В стандарте эта система знаний представлена в виде требований к подготовке выпускников. С данными требованиями соотносится уровень предъявления в КИМ проверяемых элементов содержания.
- Стандартизированные варианты КИМ, которые будут использоваться при проведении экзамена, содержат задания, различные по форме предъявления условия и виду требуемого ответа, по уровню сложности, а также по способам оценки их выполнения. Задания построены на материале основных разделов курса химии. Как и в прежние годы, объектом контроля в рамках ЕГЭ 2020 г. является система знаний основ неорганической, общей и органической химии. К числу главных составляющих этой системы относятся: ведущие понятия о химическом элементе, веществе и химической реакции; основные законы и теоретические положения химии; знания о системности и причинности химических явлений, генезисе веществ, способах познания веществ. В стандарте эта система знаний представлена в виде требований к уровню подготовке выпускников.
- В целях обеспечения возможности дифференцированной оценки учебных достижений выпускников, КИМ ЕГЭ осуществляют проверку освоения основных образовательных программ по химии на трёх уровнях сложности: базовом, повышенном и высоком.
- Принципиальное значение при разработке КИМ имела реализация требований к конструированию заданий различного типа. Каждое задание строилось таким образом, чтобы его содержание соответствовало требованиям к уровню усвоения учебного материала и формируемым видам учебной деятельности. Учебный материал, на основе которого строились задания, отбирался по признаку его значимости для общеобразовательной подготовки выпускников средней школы. Особое внимание при конструировании заданий уделено усилению деятельностной и практико-ориентированной составляющей их содержания. Реализация этого направления имела целью повышение дифференцирующей способности экзаменационной модели.
Структура части 1 работы приведена в большее соответствие со структурой курса химии. Построение заданий, в первую очередь заданий базового уровня сложности, осуществлено таким образом, чтобы их выполнение предусматривало использование во взаимосвязи обобщённых знаний, ключевых понятий и закономерностей химии.
Структура КИМ ЕГЭ по химии
Каждый вариант экзаменационной работы построен по единому плану:
работа состоит из двух частей, включающих в себя 35 заданий.
Часть 1 содержит 29 заданий с кратким ответом, в их числе 21 задание базового уровня сложности (в варианте они присутствуют под номерами: 1–7, 10–15, 18–21, 26–29) и 8 заданий повышенного уровня сложности (их порядковые номера: 8, 9, 16, 17, 22–25).
Часть 2 содержит 6 заданий высокого уровня сложности, с развёрнутым ответом. Это задания под номерами 30–35.
Общие сведения о распределении заданий по частям экзаменационной работы и их основных характеристиках представлены в таблице 1.
Таблица 1. Распределение заданий по частям экзаменационной работы
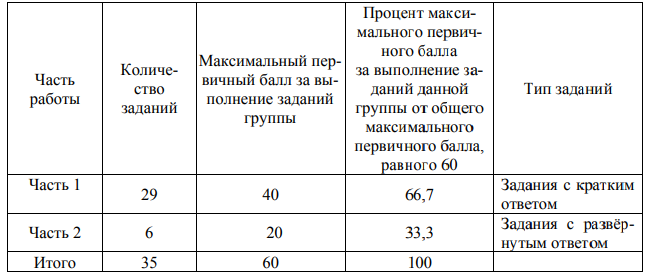
Количество заданий той или иной группы в общей структуре КИМ определено с учётом следующих факторов:
а) глубина изучения проверяемых элементов содержания учебного материала, как на базовом, так и на повышенном уровнях;
б) требования к планируемым результатам обучения – предметным знаниям, предметным умениям и видам учебной деятельности. Это позволило более точно определить функциональное предназначение каждой группы заданий в структуре КИМ. Так, задания базового уровня сложности с кратким ответом проверяют усвоение значительного количества (42 из 56) элементов содержания важнейших разделов школьного курса химии: «Теоретические основы химии», «Неорганическая химия», «Органическая химия», «Методы познания в химии. Химия и жизнь».
Согласно требованиям стандарта, к уровню подготовки выпускников эти знания являются обязательными для освоения каждым обучающимся. Задания данной группы имеют сходство по формальному признаку – по форме краткого ответа, который записывается в виде двух либо трёх цифр или в виде числа с заданной степенью точности. Между тем по формулировкам условия они имеют значительные различия, чем, в свою очередь, определяются различия в поиске верного ответа. Это могут быть задания с единым контекстом (как, например, задания 1–3), с выбором двух верных ответов из пяти, а также задания на «установление соответствия между позициями двух множеств». При этом важно заметить, что каждое отдельное задание базового уровня сложности независимо от формата, в котором оно представлено, ориентировано на проверку усвоения только одного определённого элемента содержания. Однако это не является основанием для того, чтобы отнести данные задания к категории лёгких, не требующих особых усилий для поиска верного ответа. Напротив, выполнение любого из этих заданий предполагает обязательный и тщательный анализ условия и применение знаний в системе.
Задания повышенного уровня сложности с кратким ответом, который устанавливается в ходе выполнения задания и записывается согласно указаниям в виде определённой последовательности четырёх цифр, ориентированы на проверку усвоения обязательных элементов содержания основных образовательных программ по химии не только базового, но и углубленного уровня. В сравнении с заданиями предыдущей группы они предусматривают выполнение большего разнообразия действий по применению знаний в изменённой, нестандартной ситуации (например, для анализа сущности изученных типов реакций), а также сформированность умений систематизировать и обобщать полученные знания. В экзаменационной работе предложена только одна разновидность этих заданий: на установление соответствия позиций, представленных в двух множествах. Это может быть соответствие между: названием органического соединения и классом/группой, к которому(-ой) оно принадлежит; названием или формулой соли и отношением этой соли к гидролизу; исходными веществами и продуктами реакции между этими веществами; названием или формулой соли и продуктами, которые образуются на инертных электродах при электролизе её водного раствора, и т.д.
Для оценки сформированности интеллектуальных умений более высокого уровня, таких как устанавливать причинно-следственные связи между отдельными элементами знаний (например, между составом, строением и свойствами веществ), формулировать ответ в определённой логике с аргументацией сделанных выводов и заключений, используются задания высокого уровня сложности с развёрнутым ответом. Задания с развёрнутым ответом, в отличие от заданий двух предыдущих типов, предусматривают комплексную проверку усвоения на углубленном уровне нескольких (двух и более) элементов содержания из различных содержательных блоков. Они подразделяются на следующие разновидности:
- задания, проверяющие усвоение важнейших элементов содержания, таких, например, как «окислительно-восстановительные реакции», «реакции ионного обмена»;
- задания, проверяющие усвоение знаний о взаимосвязи веществ различных классов (на примерах превращений неорганических и органических веществ);
- расчётные задачи.
- Задания с развёрнутым ответом ориентированы на проверку умений:
- объяснять обусловленность свойств и применения веществ их составом и строением, характер взаимного влияния атомов в молекулах органических соединений, взаимосвязь неорганических и органических веществ, сущность и закономерность протекания изученных типов реакций;
- проводить комбинированные расчёты по химическим уравнениям.
Распределение заданий КИМ ЕГЭ по содержанию, видам умений и способам действий
При определении количества заданий КИМ ЕГЭ, ориентированных на проверку усвоения учебного материала отдельных блоков / содержательных линий, учитывался, прежде всего, занимаемый ими объём в содержании курса химии.
Например, принято во внимание, что в системе знаний, определяющих уровень подготовки выпускников по химии, важное место занимают элементы содержания содержательных блоков «Неорганическая химия», «Органическая химия» и содержательной линии «Химическая реакция». По этой причине суммарная доля заданий, проверяющих усвоение их содержания, составила в экзаменационной работе 69% от общего количества всех заданий. Представление о распределении заданий по содержательным блокам / содержательным линиям даёт таблица 2.
Таблица 2. Распределение заданий экзаменационной работы по содержательным блокам / содержательным линиям курса химии
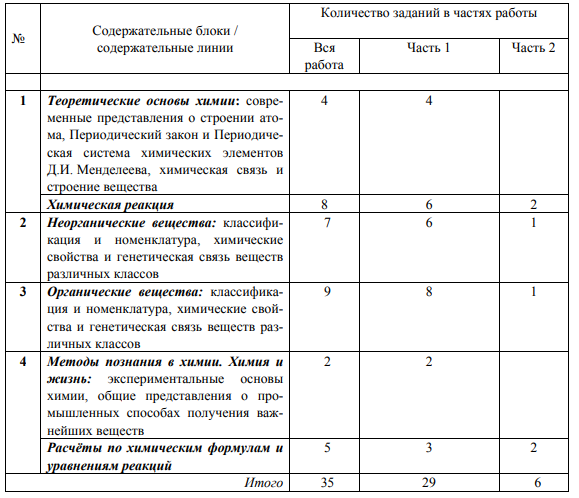
Соответствие содержания КИМ ЕГЭ общим целям обучения химии в средней школе обеспечивается тем, что предлагаемые в них задания проверяют наряду с усвоением элементов содержания овладение определёнными умениями и способами действий, которые отвечают требованиям к уровню подготовки выпускников. Представление о распределении заданий по видам проверяемых умений и способам действий даёт таблица 3.
Таблица 3. Распределение заданий по видам проверяемых умений и способам действий
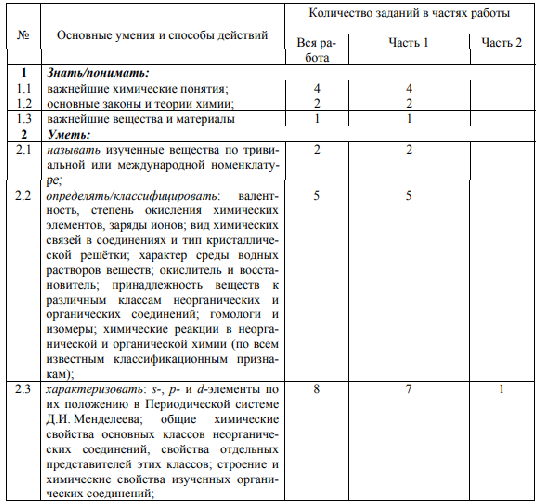

Распределение заданий КИМ ЕГЭ по уровню сложности
Распределение заданий КИМ по уровню сложности приведено в таблице 4.
Таблица 4. Распределение заданий по уровням сложности
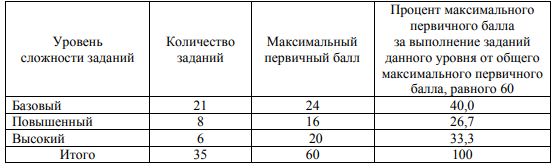
Продолжительность ЕГЭ по химии
Общая продолжительность выполнения экзаменационной работы составляет 3,5 часа (210 минут).
Примерное время, отводимое на выполнение отдельных заданий, составляет:
- для каждого задания базового уровня сложности части 1 – 2–3 минуты;
- для каждого задания повышенного уровня сложности части 1 – 5–7 минут;
- для каждого задания высокого уровня сложности части 2 – 10–15 минут.
Дополнительные материалы и оборудование
К каждому варианту экзаменационной работы прилагаются следующие материалы:
- периодическая система химических элементов Д.И. Менделеева; − таблица растворимости солей, кислот и оснований в воде;
- электрохимический ряд напряжений металлов. Во время выполнения экзаменационной работы разрешается использовать непрограммируемый калькулятор.
Перечень дополнительных устройств и материалов, пользование которыми разрешено на ЕГЭ, утверждается приказом Минпросвещения России и Рособрнадзора.
Система оценивания выполнения отдельных заданий и экзаменационной работы в целом
Ответы на задания части 1 оцениваются автоматизированно после сканирования бланков ответов № 1.
Ответы к заданиям части 2 проверяются предметной комиссией. За правильный ответ на каждое из заданий 1–6, 11–15, 19–21, 26–29 ставится 1 балл. Задание считается выполненным верно, если экзаменуемый дал правильный ответ в виде последовательности цифр или числа с заданной степенью точности. Задания 7–10, 16–18, 22–25 считаются выполненными верно, если правильно указана последовательность цифр. За полный правильный ответ на каждое из заданий 7–10, 16–18, 22–25 ставится 2 балла; если допущена одна ошибка – 1 балл; за неверный ответ (более одной ошибки) или его отсутствие – 0 баллов.
Задания части 2 (с развёрнутым ответом) предусматривают проверку от двух до пяти элементов ответа. Задания с развёрнутым ответом могут быть выполнены выпускниками различными способами. Наличие каждого требуемого элемента ответа оценивается 1 баллом, поэтому максимальная оценка верно выполненного задания составляет от 2 до 5 баллов в зависимости от степени сложности задания: задания 30 и 31 – 2 балла; 32 – 4 балла; 33 – 5 баллов; 34 – 4 балла; 35 – 3 балла.
Проверка заданий части 2 осуществляется на основе поэлементного анализа ответа выпускника в соответствии с критериями оценивания задания.
В соответствии с Порядком проведения государственной итоговой аттестации по образовательным программам среднего общего образования (приказ Минпросвещения России и Рособрнадзора от 07.11.2018 № 190/1512 зарегистрирован Минюстом России 10.12.2018 № 52952) «82. По результатам первой и второй проверок эксперты независимо друг от друга выставляют баллы за каждый ответ на задания экзаменационной работы ЕГЭ с развернутым ответом
В случае существенного расхождения в баллах, выставленных двумя экспертами, назначается третья проверка. Существенное расхождение в баллах определено в критериях оценивания по соответствующему учебному предмету. Эксперту, осуществляющему третью проверку, предоставляется информация о баллах, выставленных экспертами, ранее проверявшими экзаменационную работу». Существенным считается расхождение между баллами, выставленными первым и вторым экспертом, на 2 или более балла за выполнение любого из заданий 30–35. В этом случае третий эксперт проверяет только те ответы на задания, которые вызвали столь существенное расхождение. Максимальный первичный балл – 60.
На основе результатов выполнения всех заданий работы определяются первичные баллы, которые затем переводятся в тестовые по 100-балльной шкале.
Изменения в КИМ 2020 г. по сравнению с 2019 г.
Существенные изменения структуры и содержания КИМ отсутствуют. Лишь в задании 30-31 немного изменилась формулировка задания. В КИМах в № 30-31 введен признак реакции (далее мы рассмотрим эти изменения).
Методические рекомендации по подготовке к ЕГЭ по химии в 2020 году
Анализ сдачи ЕГЭ по химии в 2019 году, показал, что число участников ЕГЭ по химии в 2019 г. составило более 94 тыс. человек; средний тестовый балл в 2019 г.56,3 балла. Доля участников, не преодолевших минимального балла при сохранении его значения на уровне 13 первичных баллов (36 тестовых баллов) в 2019 г. составила 14,7% (в 2018 г. – 16,6%). Доля участников с результатами в диапазоне 61–80 баллов в 2019 г. – 32,5% и 81–100 баллов в 2019 г. – 11,2%. Следует отметить, что эти показатели выросли по сравнению с показателями сдачи ЕГЭ в 2018 году.
Наиболее успешно всеми участниками ЕГЭ 2019 г. выполнены задания 1, 2, 3, 10, 20, 21 и 22, которые проверяют сформированность следующих умений:
- применять основные положения химических теорий для анализа строения и свойств веществ;
- характеризовать s-, p- и d-элементы по их положению в Периодической системе Д.И. Менделеева;
- понимать смысл Периодического закона Д.И. Менделеева и использовать его для качественного анализа и обоснования основных закономерностей строения атомов, свойств химических элементов и их соединений;
- объяснять зависимость свойств химических элементов и их соединений от положения элемента в Периодической системе Д.И. Менделеева;
- понимать смысл важнейших понятий;
- определять валентность, степень окисления химических элементов, заряды ионов;
- объяснять влияние различных факторов на скорость химической реакции и на смещение химического равновесия;
- использовать важнейшие химические понятия для объяснения отдельных фактов и явлений.
Наименее успешно выполнены задания, предусматривающие проверку:
- знаний, формируемых в процессе химического эксперимента (задание 25);
- умений выбирать из перечня вещества, вступающие в окислительно-восстановительное взаимодействие, и составлять соответствующие уравнения реакций (задание 30), составлять реакции, отражающие химические свойства и взаимосвязь основных классов органических соединений (33), проводить комбинированные вычисления по формулам и уравнениям химических реакций (34 и 35).
Часть 1 экзаменационной работы 2019 г. содержала задания базового и повышенного уровней сложности. Эти задания были сгруппированы по четырем тематическим блокам:
«Строение атома. Периодический закон и Периодическая система химических элементов Д.И. Менделеева. Закономерности изменения свойств химических элементов по периодам и группам». «Строение вещества. Химическая связь»; «Неорганические вещества: классификация и номенклатура, химические свойства и генетическая связь веществ различных классов»; «Органические вещества: классификация и номенклатура, химические свойства и генетическая связь веществ различных классов»; «Химическая реакция»; «Методы познания в химии»; «Химия и жизнь»; «Расчеты по химическим формулам и уравнениям реакций».
Часть 2 экзаменационной работы содержит задания повышенного уровней сложности. Задания предполагают развернутые ответы. Задания с развёрнутым ответом, в отличие от заданий части 1, предусматривают комплексную проверку усвоения на углубленном уровне нескольких (двух и более) элементов содержания из различных содержательных блоков.
Они подразделяются на следующие разновидности:
- задания, проверяющие усвоение важнейших элементов содержания, таких, например, как «окислительно-восстановительные реакции» и реакции ионного обмена (задания №№ 30 и 31).
- задания, проверяющие усвоение знаний о взаимосвязи веществ различных классов (на примерах превращений неорганических и органических веществ);
Примеры:

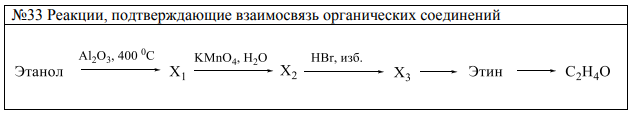
- расчётные задачи.
Задания с развёрнутым ответом ориентированы на проверку умений:
- объяснять обусловленность свойств и применения веществ их составом и строением, характер взаимного влияния атомов в молекулах органических соединений, взаимосвязь неорганических и органических веществ, сущность и закономерность протекания изученных типов реакций;
- проводить комбинированные расчёты по химическим уравнениям.

Комбинирование проверяемых элементов содержания в заданиях с развёрнутым ответом осуществляют таким образом, чтобы уже в их условии прослеживалась необходимость последовательного выполнения нескольких взаимосвязанных действий: выявления причинно-следственных связей между элементами содержания, формулирования ответа в определённой логике и с аргументацией отдельных положений. Отсюда становится очевидным, что выполнение заданий с развёрнутым ответом требует от выпускника прочных теоретических знаний, а также сформированных умений применять эти знания в различных учебных ситуациях, последовательно и логично выстраивать ответ, делать выводы и умозаключения, приводить аргументы в пользу высказанной точки зрения и т.п.
Выделение определённого числа элементов ответа осуществляется после разработки формулировки условия задания, изложения содержания верного ответа и критериев его оценивания.
Остановимся подробнее на особенностях формулировки условия задания с развёрнутым ответом. Важнейшей из них является чёткое описание тех компонентов, которые должны быть представлены в решении.
Так, например, в задании 32 описываются химические превращения, которые можно охарактеризовать уравнениями соответствующих реакций. Однако для однозначного понимания требований к ответу в конце формулировки задания приведена фраза, что уравнений должно быть записано именно четыре. Аналогичная ситуация в условии задания 33, содержательную основу которого составляет схема превращений органических веществ из пяти стадий.
Наиболее однозначно, с точки зрения понимания числа элементов ответа, в решении, сформулированы задания 30, 31 и 35. В условии каждого из них чётко указано, какие именно элементы должен содержать ответ экзаменуемого: запись электронного баланса, полного и сокращённого ионных уравнений, молекулярных уравнений реакций, структурной формулы вещества и т.п. В более обобщённом виде требования к ответу сформулированы в условии задания 34 — расчётной задаче, в которой обозначена лишь итоговая величина(-ы), которую(-ые) следует найти. Однако способ, которым должно быть выполнено задание, в условии не прописан, и, следовательно, обучающийся должен сам разработать алгоритм его выполнения. В таком случае количество элементарных действий в решении может быть существенно больше, чем максимальное число баллов, которое сможет получить экзаменуемый за задание.
Рассмотрим примеры заданий с развёрнутыми ответами.
Задание 30-31. В Экзаменационных материалах 2020 года произошли изменения в номере 30-31, обучающимся необходимо составить окислительно-восстановительную реакцию, протекающую с определённом признаком реакции (реакция, в которой выпал осадок бурого цвета; реакция протекает с изменением цвета раствора…). А в номере 31 предлагается выбрать определенное вещество для реакции ионного обмена или также указан конкретный признак протекания реакции.
Это сокращает возможность обучающемуся составить несколько вариантов ответов в заданиях 30-31.
Пример 1.
Для выполнения заданий 30, 31 используйте следующий перечень веществ: перманганат калия, гидрокарбонат натрия, сульфит натрия, сульфат бария, гидроксид калия, пероксид водорода. Допустимо использование водных растворов веществ.
30. Из предложенного перечня веществ выберите вещества, между которыми окислительно-восстановительная реакция протекает с изменением цвета раствора.Выделение осадка или газа в ходе этой реакции не наблюдается. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
Анализ возможных окислительно-восстановительных процессов:
окислители: восстановители: среда:
KMnO4 H2O2 Na2SO3 H2O2 KOH H2O
Схемы возможных реакций:
- KMnO4 + Na2SO3 + KOH → K2MnO4 + Na2SO4 + H2O
- KMnO4 + Na2SO3 + H2O → MnO2 + Na2SO4 + KOH
- KMnO4 + H2O2 → MnO2 + O2 + KOH + H2O
- H2O2 + Na2SO3 → Na2SO4 + H2O
Условию задания – изменение цвета раствора, осадок или газ не выделялся - соответствует только уравнение реакции 1.
Критерии оценивания:

Подчеркнём, что экзаменуемый должен корректно указывать степени окисления, не путать степень окисления с зарядом иона. Если экзаменуемый указывает, что окислителем является Mn7+ или восстановителем является S4+ (для дихромата часто пишут окислителем является Cr6+ или Cr26+), такие варианты ответа засчитаны не будут. Подобных ионов в водном растворе не существует! Также, важно, указывать единицу в степени окисления. (например: Вr-1, вместо простого ионаВr-) и степень окисления ноль в простых веществах (например: Вr20).
Недопустимы записи:
- Из предложенного перечня веществ выберите кислую соль и вещество, которое вступает с этой кислой солью в реакцию ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
Из предложенного перечня веществ только одно вещество является кислой солью – гидрокарбонат натрия, именно это вещество и необходимо использовать для составления уравнений реакций.
Критерии оценивания:

Экзаменуемый должен представить в работе только один вариант ответа.
Хотелось бы обратить особое внимание на особенности выполнения этого задания.
- Экзаменуемый должен проанализировать свойства и определить в каком из случаем соблюдается правило Бертолле (выделяется газ, выпадает осадок или образуется вода).
- При составлении полного ионного и сокращённого ионного уравнений важно, чтобы коэффициенты в этих уравнениях были минимальными.
Например, уравнение
2H+ + 2OH- = 2H2O
не может быть засчитано, в данном случае экзаменуемый должен записать:
H+ + OH- = H2O
- Запись заряда иона в ионных уравнениях должна быть корректной, например: Al3+, C1l-, SO42- . Неправильными будет считаться запись: Al+3, Cl-1, SO4-2. Подобных ионов в водном растворе не существует!
- Если в качестве одного из исходных веществ выбрана соль, то она должна быть растворима в воде (исключение – взаимодействие нерастворимых карбонатов с кислотами).
- Кислые соли диссоциируют ступенчато:
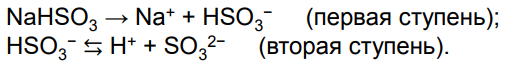
В ионном уравнении используется записи типа: Na+ + HSO3−.
Например:
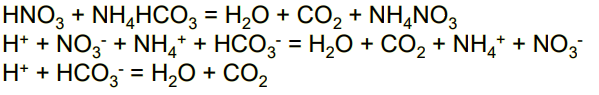
- Реакции образования гидроксокомплексов при взаимодействии растворов щелочей и растворимых солей цинка и алюминия также можно отнести к реакциям ионного обмена:
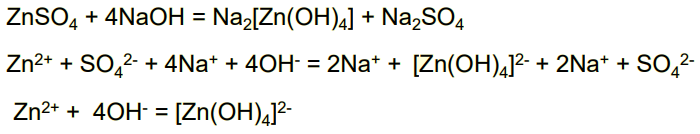
- При взаимодействии солей аммония со щелочами допустимы записи NH3 ∙H2O, NH3 + H2O, например:
Пример 2. Задания 30, 31.

В задании 30, с образованием двух кислот, возможна только одна реакция:
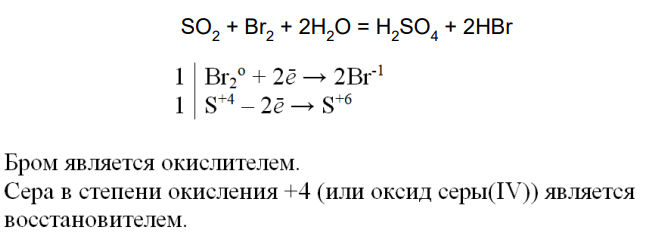
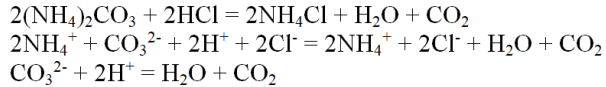
В задании 31, реакция ионного обмена с выделением газа протекает только между веществами:
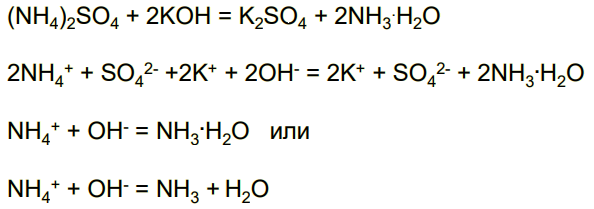
Пример 3. Задания 30, 31.

В задании 30, условию соответствует реакция:

Задание 31.
Вариант ответа:
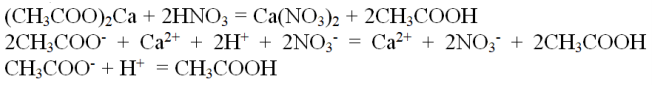
Не менее значимым является опыт в проведении химического эксперимента и при выполнении задания 32.
В задании 32 существенных изменений в 2020 году нет. В задании 32 (КИМ ЕГЭ 2019 г.) - выполнение задания высокого уровня сложности, проверяющего усвоение знаний взаимосвязи неорганических веществ, предусматривало написание уравнений реакций, соответствующих описанному в условии задания эксперименту.
Пример 1. Нитрат меди (II) прокалили. Образовавшуюся при этом смесь газов пропустили через воду, при этом образовалась кислота. В горячий концентрированный раствор этой кислоты поместили оксид железа (II). Образовавшуюся соль железа выделили и поместили в раствор карбоната калия. Напишите уравнения четырех описанных реакций.
Ответ к этому заданию предполагал запись следующих уравнений реакций:
1) 2Cu(NO3)2 = 2CuO + 4NO2 + O2
2) 4NO2 + O2 + 2H2O = 4HNO3
3) FeO + 4HNO3(конц.) = Fe(NO3)3 + NO2 + 2H2O
4) 2Fe(NO3)3 + 3K2CO3 + 3H2O = 2Fe(OH)3 + 3CO2 + 6KNO3
За каждое верно составленное уравнение реакции экзаменуемый получал 1 балл, за задание в целом – 4 балла. Наиболее часто встречались следующие ошибки. В первом уравнении в качестве продукта реакции вместо оксида меди (II) экзаменуемые записывали металлическую медь. Выпускники с низким уровнем подготовки затруднялись в написании второго уравнения реакции – получения азотной кислоты. В третьем уравнении реакции некоторые экзаменуемые не учитывали сильных окислительных свойств концентрированной азотной кислоты и составляли уравнение реакции обмена, в которой степень окисления железа не изменяется. Уравнение четвертой реакции зачастую ошибочно экзаменуемые записывали как реакцию обмена между солями с образованием карбоната железа (III), который отсутствует в растворе.
Несмотря на кажущуюся простоту представленных уравнений реакций, в каждом из них есть определённые тонкости («подсказки»), которые можно выявить и учесть только при внимательном прочтении условия задания, а также при наличии достаточного опыта в проведении лабораторных и практических работ. Именно в процессе их проведения формируются образы реальных химических превращений. Можно с уверенностью сказать, что существенное снижение времени, отводимого на выполнение ученического эксперимента, всё в большей степени влияет на число баллов, получаемых учащимися в рамках государственной итоговой аттестации (ОГЭ и ЕГЭ), т.к. количество практико-ориентированных вопросов в КИМ достаточно велико.
- (Демоверсия ЕГЭ 2020): При электролизе водного раствора нитрата меди (II) получили металл. Металл обработали концентрированной серной кислотой при нагревании. Выделившийся в результате газ прореагировал с сероводородом с образованием простого вещества. Это вещество нагрели с концентрированным раствором гидроксида калия. Напишите уравнения четырёх описанных реакций.
Критерии оценивания:
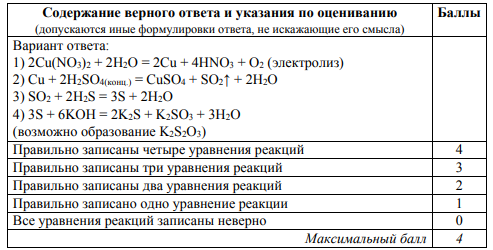
В задании 33 проверяемые ведущие элементы содержания:
- характерные химические свойства органических веществ различных классов;
- генетическая взаимосвязь органических веществ.
Существенных изменений по сравнению с КИМами 2019 года не произошло, однако в модели 2020 года в генетической связи предложено больше «зашифрованных» органических веществ. Обучающийся должен проанализировать последовательность реакций и определиться, какие вещества описаны в генетической связи.
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
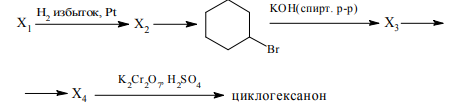
Критерии оценивания:
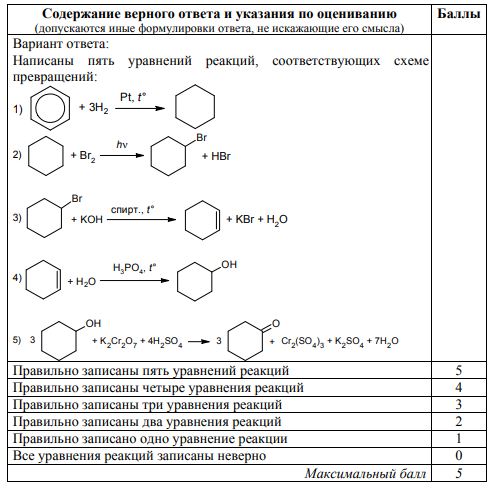
Подчеркнём, что экзаменуемый должен:
1.Корректно составлять формулы органических веществ (допустимы только структурные формулы).
- При написании уравнений реакций между органическими веществами важно указывать условия их протекания! Если экзаменуемый указал не верные условия осуществления реакций, то экзаменаторы могут снять баллы. В случае, если обучающийся не помнит условия реакции, то лучше их не писать, чем написать неверные условия течения реакций.
Важным условием успешного выполнения таких заданий (33 номер) является фокусирование внимания не на одной стадии, а на всех данных о веществах и условиях протекания реакций на всех этапах превращений – как предшествующих, так и последующих.
Так, например, получение на второй стадии бромциклогесана позволяет спрогнозировать, что исходным веществом, вступающим на первой стадии в реакцию с 4 моль водорода (реакция гидрирования), является ароматическое соединение – бензол. А образование на завершающем этапе циклогексанона в результате окисления вещества Х4 хромовой смесью позволяет предположить, что продуктом превращения на четвертой стадии является кислородсодержащее соединение – спирт – циклогексанол.
Одной из ошибок, которую допускают участники ЕГЭ при выполнении подобных заданий, является отсутствие подготовительного этапа к выполнению, включающему общий анализ химических свойств веществ, указанных в задании.
Первым шагом при выполнении заданий, проверяющих знание химических свойств органических и неорганических веществ, является определение принадлежности вещества к определенному (-ой) классу (группе). Именно такой подход позволяет исходя из общих свойств веществ, характерных для определенного (-ой) класса/группы веществ, спрогнозировать возможные варианты взаимодействия. На следующем этапе следует перейти к учету специфических свойств веществ, которые, как правило, могут быть связаны с особенностями строения.
Наиболее трудными для экзаменуемых оказываются расчетные задачи (задания 34 и 35). При выполнении задания 34 большинство экзаменуемых не могут составить уравнения реакций, о которых идет речь в условии задания, многие не могут правильно соотнести заданные физические величины с химической сутью задания и выстроить дальнейший логический путь решения задачи. Хотя, задание 35 экзаменуемые выполняют традиционно более успешно, чем задание 34.
Возможно одним из факторов, не позволивших успешно справиться с расчетными задачами, находящими в конце варианта, является нехватка времени на их выполнение. Поэтому обратим внимание на тот факт, что умение распределить свои время и силы в процессе выполнения экзаменационной работы является важным дифференцирующим фактором определения уровня подготовленности экзаменуемых. На этот фактор надо обратить внимание выпускников при организации их самостоятельной работы при подготовке к экзаменам. Например, можно ограничивать время на решение заданий: начать с более длительных временных отрезков, постепенно уменьшая их. Существенным моментом в процессе подготовки может стать отработка в решении моделей заданий, выходящих за рамки моделей ЕГЭ (задачи на электролиз, задачи на пластинки…). Это позволит сформировать умение самостоятельно разрабатывать алгоритм решения в случае нестандартных заданий.
В условии каждой из задач этой линии встречаются данные, которые должны быть учтены экзаменуемым, а для этого необходимо уметь учитывать все приведенные данные. Важным этапом на пути к этому является формирование умения записывать «дано», отработку которого нужно начинать на более простых условиях заданий, постепенно увеличивая количество приведенных в них данных. Грамотная запись «дано» с указанием единиц измерения физических величин позволяет также избежать и арифметических ошибок, которые нередко встречаются в решениях даже хорошо подготовленных экзаменуемых. Одни из ошибок свидетельствуют о непонимании взаимосвязи между величинами, а другие являются результатом наличия проблем в математической подготовке.
Таким образом, важнейшим фактором, определяющим успешность решения заданий экзаменационного варианта по химии, является реализация системного подхода к формированию химических знаний и отработке умения работать с информацией, представленной в условии заданий в различной форме (текст, формула, схема). В целях учета названных выше факторов в рамках текущего и рубежного контроля целесообразно применять различные формы заданий, направленных на проверку химических свойств веществ и предусматривающих анализ данных, их отбор с учетом сформулированных вопросов, и/или заданий, включающих описание результатов химических экспериментов. При этом очень важно предлагать выпускникам проговаривать или записывать алгоритм действий. Именно данный шаг обеспечивает систему и логику в решении заданий любого уровня сложности.
Общий вывод
Рекомендации руководителям методических объединений районов и школ
Для достижения более высоких результатов при сдаче ЕГЭ и ОГЭ по химии необходимо на совещаниях МО учителей химии:
- Провести анализ результатов ГИА по химии 2019 г.
- Рассмотреть на методических объединениях проекты кодификаторов, спецификаций и демоверсий ЕГЭ, ОГЭ по химии 2020 г.
- Обобщить опыт учителей, которые систематически показывают лучшие результаты ГИА по химии. Рекомендовать педагогам представить свой опыт работы по подготовке обучающихся к ГИА на семинарах учителей химии в марте 2020 г.
- Оказать консультационную помощь малоопытным учителям и рекомендовать педагогам курсы повышения квалификации.
- Организовать во втором полугодии пробное тестирование выпускников по химии в формате ЕГЭ и ОГЭ c последующим анализом результатов и выявлением проблем в подготовке обучающихся.
Методическую помощь учителям и обучающимся при подготовке к ОГЭ и ЕГЭ могут оказать материалы с сайта ФИПИ (www.fipi.ru):
- документы, определяющие структуру и содержание КИМ ОГЭ и ЕГЭ 2020 г.;
- открытый банк заданий ОГЭ и ЕГЭ;
- учебно-методические материалы для председателей и членов региональных предметных комиссий по проверке выполнения заданий с развернутым ответом экзаменационных работ ОГЭ, ЕГЭ;
- Методические рекомендации на основе анализа типичных ошибок участников ОГЭ, ЕГЭ прошлых лет (2015–2019 гг.);
- журнал «Педагогические измерения»;
- Youtube-канал Рособрнадзора (видеоконсультации по подготовке к ЕГЭ 2016 – 2019 гг.), материалы сайта ФИПИ.
Список литературы:
- Демонстрационный вариант контрольных измерительных материалов для проведения в 2020 году основного государственного экзамена по ХИМИИ (подготовлен Федеральным государственным бюджетным научным учреждением «ФЕДЕРАЛЬНЫЙ ИНСТИТУТ ПЕДАГОГИЧЕСКИХ ИЗМЕРЕНИЙ»).
- Демонстрационный вариант контрольных измерительных материалов единого государственного экзамена 2020 года по химии (подготовлен Федеральным государственным бюджетным научным учреждением «ФЕДЕРАЛЬНЫЙ ИНСТИТУТ ПЕДАГОГИЧЕСКИХ ИЗМЕРЕНИЙ»).
- Добротин Д.Ю., Свириденкова Н.В., Снастина М.Г. Методические рекомендации для учителей, подготовленные на основе анализа типичных ошибок участников ЕГЭ 2019 года. - ФЕДЕРАЛЬНЫЙ ИНСТИТУТ ПЕДАГОГИЧЕСКИХ ИЗМЕРЕНИЙ. – М. - 2019 г. - 34 с.
- Кодификатор проверяемых требований к результатам освоения основной образовательной программы основного общего образования и элементов содержания для проведения основного государственного экзамена по ХИМИИ 2020 г. (подготовлен Федеральным государственным бюджетным научным учреждением «ФЕДЕРАЛЬНЫЙ ИНСТИТУТ ПЕДАГОГИЧЕСКИХ ИЗМЕРЕНИЙ»).
- Кодификатор элементов содержания и требований к уровню подготовки выпускников образовательных организаций для проведения единого государственного экзамена по химии (подготовлен Федеральным государственным бюджетным научным учреждением «ФЕДЕРАЛЬНЫЙ ИНСТИТУТ ПЕДАГОГИЧЕСКИХ ИЗМЕРЕНИЙ»).
- Лёвкин А.Н., Домбровская С.Е. Методические рекомендации по подготовке к ГИА по химии в 2019 году. – М., СПбАППО. – 2019 г. – 25 с.
- Научно-методический журнал «Педагогические измерения». Электронный адрес редакции журнала «Педагогические измерения»
- Спецификация контрольных измерительных материалов для проведения в 2020 году основного государственного экзамена по ХИМИИ (подготовлена Федеральным государственным бюджетным научным учреждением «ФЕДЕРАЛЬНЫЙ ИНСТИТУТ ПЕДАГОГИЧЕСКИХ ИЗМЕРЕНИЙ»).
- Спецификация контрольных измерительных материалов для проведения в 2020 году единого государственного экзамена по ХИМИИ (подготовлена Федеральным государственным бюджетным научным учреждением «ФЕДЕРАЛЬНЫЙ ИНСТИТУТ ПЕДАГОГИЧЕСКИХ ИЗМЕРЕНИЙ»)
© ООО «Знанио»
С вами с 2009 года.
![]()
