
Конспект урока Тема: «Белки. Характеристика белков»
(Интегрированный урок по химии, биологии)
Класс: 10
Цель урока: формирование у обучающихся устойчивых знаний по теме: «Белки», развитие практических умений и навыков работы с лабораторным оборудованием и химическими веществами; расширение межпредметных связей по химии и биологии.
Задачи урока:
1. Углубить и расширить знания обучающихся о важнейшей роли белков в жизнедеятельности живых организмов на основе изучения их свойств и функций.
2. Дать представление о белках, как природных полимерах, объяснить строение макромелекул белка.
3. Продолжить формирование умений выявлять взаимосвязь между строением, химическими свойствами и функциями веществ на примере белков.
4. Продолжить формирование понимания обучающимися важности сохранения здоровья на биологическом и химическом уровне.
5. Совершенствовать у обучающихся практические умения и навыки работы с химическими реактивами и лабораторным оборудованием, анализировать, сравнивать, устанавливать причинно – следственные связи.
Тип урока: изучение нового материала
Методы и методические приемы: объяснительно – иллюстративные, практические, репродуктивные.
Активизация познавательной деятельности обучающихся: использование наглядности, дополнительной литературы, технических средств обучения, проведение демонстрационных опытов, выполнение лабораторной работы, сообщения обучающихся.
Оборудование и наглядность: таблицы «Строение белков», яйцо варенное и сырое, раствор сульфата меди (II), гидроксида натрия, водный раствор яичного белка, бусы, химические стаканы, спиртовка, спички, спирт, пробирки.
Сообщения детей: «История открытия белков», «Проблема рационального питания и современные диеты», «Ферменты».
Живые тела, существующие на Земле, представляют собой открытые саморегулирующиеся и самовоспроизводящиеся системы, построенные из биополимеров – белков и нуклеиновых кислот.
М. В. Волькенштейн Ход урока:
1. Организационный момент.
2. Изучение нового материала.
В одной из книг Библии сказано «Вначале было слово». Современная книга о происхождении жизни по аналогии могла бы начинаться фразой: « Вначале был белок». Проблема жизни – это проблема первичной организации материи в живых объектах. В.А. Энгельгардт.
Проблема:
• Почему белки играют такую большую роль в жизни живых организмов.
• Почему многие люди отождествляют понятие «белок» с понятием «жизнью». Какова же структура белка?
1. История открытия белков.
Вещества белковой природы известны с древних времен. Начало их изучения положено в середине 18 в. итальянцем Я. Беккари, но только через 100 лет ученым удалось систематизировать свойства белков и сделать вывод, что белки – это главный компонент живых организмов. Затем из белковых гидролизатов были получены продукты расщепления и возникли гипотезы о строении белков из аминокислот.
Немецкий химик Эмиль Фишер первым выяснил, как построены молекулы белков и заложил основы их химического синтеза. В начале 20 века Фишер доказал пептидную теорию строения белков, выдвинутую русским химиком Данилевским, синтезировав полипептиды состоящие из 3 – 18 аминокислотных остатков.
Белки различаются составом аминокислот, числом аминокислотных звеньев, порядком чередования их в полипептидной цепи.
2. Состав и строение белков.
Вопросы для обучающихся:
• Атомарный состав белков. Почему белки являются высокомолекулярными веществами?
• На какие две группы делятся белки по их форме?
• Как называется связь с помощью которой аминокислоты соединяясь друг с другом образуют белки? (показать на доске)
Обучающиеся самостоятельно работают с текстом учебника и готовят рассказ о различных структурах белковых молекул.
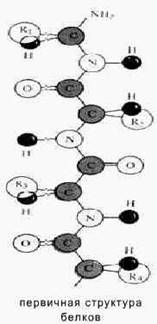
Первичная структура белка – это последовательное чередование АК (полипептидная цепь ППЦ).
Пространственная конфигурация белковой молекулы, напоминающая спираль образуется благодаря многочисленным водородным связям между группами: – СО– и –NH–
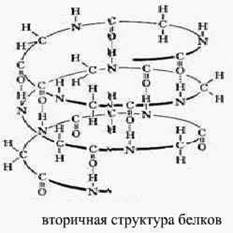
Такая структура белка называется вторичной. В пространстве закрученная спираль ППЦ образует третичную структуру белка, которая поддерживается взаимодействием разных функциональных групп ППЦ.
1. –S–S– (дисульфидный мостик)
2. –СООН и –ОН (сложноэфирный мостик)
3. –СООН и –NH2 (солевой мостик)
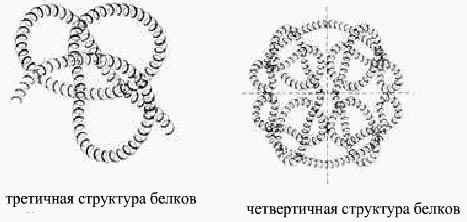
Некоторые белковые макромолекулами могут соединяться друг с другом и образовывать крупные молекулы. Полимерные образования белков называются четвертичными структурами (гемоглобин только при такой структуре способен присоединять и транспортировать О2 в организм).
3. Свойства белков (беседа с обучающимися) 1. Растворимость в воде (проводится опыт).
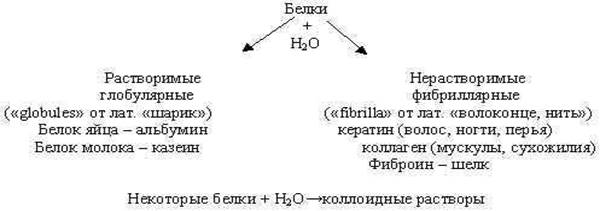
2. Денатурация. Для белков характерны реакции, в результате которых образуется осадок. Но в одних случаях полученный осадок при избытке воды растворяется, а в других – происходит необратимое свертывание белков, т.е. денатурация.
Денатурация – это изменение третичной и четвертичной структур белковой макромолекулы под влиянием внешних факторов (повышение температуры, давления, механического воздействия, действия химических реагентов, УФ – излучения, радиации).
Проблема: К чему может привести денатурация?
- нарушение антигенной чувствительности белка;
- блокирование ряда иммунологических реакций;
- нарушение обмена веществ;
- воспаление слизистой оболочки ряда органов пищеварения (гастриты, колит).
Какие еще реакции характерны для белков?
(Проведение лабораторной работы обучающимися по инструктивной карточке)
Лабораторная работа Тема: «Качественные реакция на белки» Биуретовая реакция:
Опыт 1. Белок куриного яйца растворите в 150 мл воды. Налейте в пробирку 3 -2 мл раствора гидроксида калия и 3-4 капли раствора сульфата меди (II). Что наблюдаете?
Белок + NaOH+CuSO4 > красно-фиолетовое окрашивание.

Ксантопротеиновая реакция.
Опыт 2. К раствору белка куриного яйца добавьте 0,5 – 1 мл раствора азотной кислоты смесь осторожно нагрейте. Отметьте наблюдаемое явление.
Белок + HNO3конц > ярко желтое окрашивание

4. Превращение белков в организме.
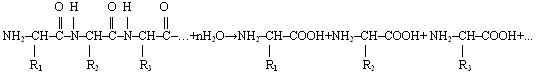
Гидролиз белка – это разрушение первичной структуры белковой молекулы. В лабораторных условиях этот процесс проводят в присутствии кислот и щелочей при нагревании, в организме он происходит под действием ферментов.
Белки – основа продуктов питания. На их фоне проявляются биологические свойства других пищевых продуктов. Биологическая ценность белков зависит от содержания незаменимых аминокислот. Недостаток белков или нарушение процессов их усвоения приводит к заболеваниям внутренних органов, болезням крови и ослаблению иммунитета.
Как происходит гидролиз белка в организме?
1. Под действием белков-ферментов в желудке происходит расщепление белковых молекул до мелких полипептидов.
2. В кишечнике полипептиды распадаются до отдельных аминокислот.
3. Смесь аминокислот всасывается слизистой оболочкой тонкого кишечника и через систему воротной вены попадает в печень, откуда разносится кровью по всем органам.
Вывод. Жизнь, безусловно, ушла вперед развиваясь от белковых молекул до человека. Белки необычайно сложны, имеют важнейшее значение для жизнедеятельности всего живого на Земле.
5. Функции белков.
Прочитайте соответствующий раздел учебника и заполните таблицу, охарактеризовав различные функции белков.
(заполнение таблицы)
Функции белков
|
№ |
Функции |
Значение |
|
|
Строительная |
Клеточные мембраны, покровные ткани, шерсть, перья, гора, волосы, хрящи |
|
|
Транспортная |
Накопление и транспорт по организму важнейших веществ |
|
|
Энергетическая |
Запас аминокислот для развития организма |
|
|
Двигательная |
Сократительные белки основа мышечных тканей |
|
|
Защитная |
Белки – антитела, антитоксины распознают и уничтожают бактерии и “чужеродные” вещества |
|
|
Каталитическая |
Белки – природные катализаторы (ферменты) |
|
|
Сигнальная |
Мембранные белки воспринимают внешние воздействия и передают сигнал о них внутрь клетки |
Белки - ферменты. Рациональное питание (беседа)
(Проведение лабораторной работы обучающимися по инструктивной карточке)
Лабораторная работа
Тема: «Расщепление пероксида водорода с помощью ферментов, содержащихся в клетках листа элодеи»
Цель: практически доказать каталитические функции белков.
Оборудование: микроскоп, предметные и покровные стекла, вода, пипетки, лист элодеи, перекись водорода.
Инструктивная карточка
1. Приготовить микропрепарат листа элодеи и рассмотреть его под микроскопом, зарисовать состояние клеток листа.
2. Капнуть на микропрепарат перекиси водорода и наблюдать за изменением состояния клеток элодеи.
3. Капнуть каплю перекиси водорода на пустое предметное стекло, отметить, что будет происходить.
4. Сравнить состояние капли перекиси водорода на чистом предметном стекле и на листе элодеи.
5. Сделать вывод о наличии в клетках листа элодеи особого фермента и его роли.
6. Заполнить таблицу:
|
Что делали |
Что наблюдали |
|
|
|
Вопросы к обучающимся:
- Какова цель предложенной вам лабораторной работы?
- Объясните, с чем связано выделение пузырьков газа на листе элодеи? - Почему не выделяются пузырьки газа в том случае, если капнуть перекись водорода на чистое предметное стекло?
3. Подведение итогов урока.
Вопросы для закрепления:
• Белок иначе называют… Что является мономерами белка?
• Сколько незаменимых АК известно?
• Какие вещества называются белками?
• Каков атомарный состав белков?
• Какая связь поддерживает вторичную структуру?
• Вторичная структура белковой молекулы в пространстве напоминает… За счет каких взаимодействий образуются третичная структура?
• Что в переводе с греческого означает “протеин”?
• На какие две группы делят белки по их отношению к Н2О?
• Что такое “денатурация”?
• Как называется процесс взаимодействия белков с Н2О?
Тест по теме урока:
1. Какие органические вещества в клетке на первом месте по массе?
а) углеводы; б) белки;
в) липиды; г) нуклеиновые кислоты.
2. Сколько аминокислот образует все многообразие белков?
а) 170; б) 26; в) 20; г) 10.
3. Сколько аминокислот являются незаменимыми для человека?
а) таких аминокислот нет; б) 20; в) 10; г) 7.
4. Какие белки называются неполноценными?
а) в которых отсутствуют некоторые аминокислоты?
б) в которых отсутствуют некоторые незаменимые аминокислоты?
в) в которых отсутствуют некоторые заменимые аминокислоты?
г) все известные белки являются полноценными.
5. В результате какой реакции образуется пептидная связь?
а) реакции гидролиза; б) реакции гидратации;
в) реакции конденсации; г) все вышеперечисленные реакции могут привести к образованию пептидной связи.
6. Между какими группировками аминокислот образуется пептидная связь?
а) между карбоксильными группами соседних аминокислот;
б) между аминогруппами соседних аминокислот;
в) между аминогруппой одной аминокислоты и радикалом другой;
г) между аминогруппой одной аминокислоты и карбоксильной группой другой.
7. Какие связи стабилизируют вторичную структуру белков?
а) ковалентные; б) водородные;
в) ионные; г) такие связи отсутствуют.
8. Какую структуру имеет молекула гемоглобина?
а) первичную; б) вторичную;
в) третичную; г) четвертичную.
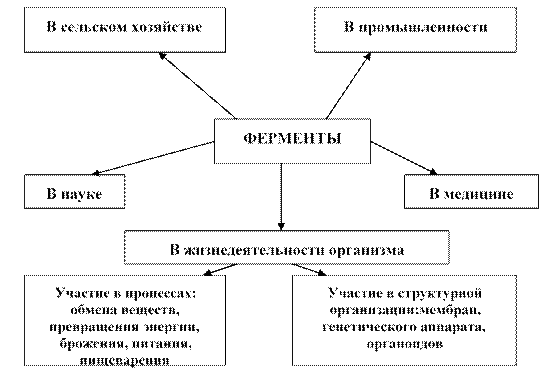
Беседа с обучающимися:
«Использование ферментов в хозяйстве, их роль в жизнедеятельности организма»
4. Домашнее задание.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.