
Сотенский УВК
Урок по химии 9 класс
«Метан представитель насыщенных углеводородов. Алканы»
Учитель химии
Сергеев А.А
Урок химии 9 класс с применением ИКТ по теме "Метан представитель насыщенных углеводородов. Алканы"
Цель урока:.
Образовательная: на примере метана познакомить учащихся с алканами, рассмотреть гомологический ряд насыщенных углеводородов, строение, физические и химические свойства, способы их получения, применение.
Развивающая: развить понятие о пространственном строении алканов; развитие познавательных интересов, творческих и интеллектуальных способностей, развитие самостоятельности в приобретении новых знаний с использованием новых технологий.
Воспитательная: показать единство материального мира на примере генетической связи углеводородов разных гомологических рядов.
Оборудование: компьютер, мультимедиа проектор, экран, презентация.
Ожидаемые результаты:
Ученики знают, какие углеводороды называют насыщенными; умеют составлять молекулярные и структурные формулы предельных углеводородов, исходя из общей формулы алканов; характеризовать физические и химические свойства метана, его применение.
Ход урока
I. Организационный момент.
Здравствуйте! Я рад вас всех видеть. Сегодня на уроке мы будем говорить о первом классе органических веществ. Я уверен, что наша продуктивная работа поможет нам достичь целей сегодняшнего урока.
II. Мотивация учебной деятельности.
Тему нашего урока вы сможете сформулировать, прослушав отрывок из стихотворения .
Уголь лихо били пики,
Рокотали молотки,
И мерцали на них лики,
Как на солнце лепестки.
И работа текла гладко,
Но не спал в пласте метан,
И готовился украдкой
Брызнуть в лаву, как фонтан.
Оставался час до смены,
И потом шабаш – домой,
Но метан внёс перемены,
Вспышкой грозной огневой.
IIІ. Обьявление темы урока.
Учитель
Тема урока: " Насыщенные углеводороды. Алканы". Слайд № 1
План изучения алканов. Слайд № 2
1. Определение. Общая формула класса углеводородов.
2. Гомологический ряд.
3. Строение алканов.
4. Физические свойства.
5. Химические свойства.
6. Распространение в природе.
7. Применение.
ІV. Актуализация знаний.
Фронтальный опрос: Что изучает органическая химия? Какие вещества называют органическими? Какие соединения называют углеводородами?
Составление кластера у доски «Классификация углеводородов».
 |
|||
V. Изучение нового материала.
Алканы. Насыщенные углеводороды. На примере метана.
Алканы - углеводороды в молекулах которых все атомы углерода связаны одинарными связями и имеют общую формулу: CnH2n+2 Слайд № 3
- Что такое гомологи?
Гомологи - это вещества, сходные по строению и свойствам и отличающиеся на одну или более групп СH2.
Гомологический ряд метана
СН4 метан
С2H6 этан
C3H8 пропан
C4H10 бутан
C5H12 пентан
C6H14 гексан
C7H16 гептан
C8H18 октан
C9H20 нонан
C10H22 декан Слайд № 4
Строение алканов. Слайд №5
Атом углерода во всех органических веществах находится в "возбуждённом" состоянии, имеет на внешнем уровне четыре неспаренных электрона.
Каждое электронное облако обладает запасом энергии: s- облако имеет меньший запас энергии, чем р-облако, в атоме углерода они находятся в разных энергетических состояниях. Поэтому при образовании химической связи происходит гибридизация, т. е. выравнивание электронных облаков по запасу энергии. Это отображается на форме и направленности облаков, происходит перестройка (пространственная) электронных облаков.
В результате sp3 - гибридизации все четыре валентных электронных облака гибридизованы: валентный угол между этими осями гибридизованных облаков 109° 28', поэтому молекулы имеют пространственную тетраэдрическую форму, форма углеродных цепей зигзагообразна; атомы углерода не находятся на одной прямой, т. к. при вращении атомов валентные углы остаются прежними.
Все органические вещества построены в основном за счёт ковалентных связей. Углерод - углеродные и углерод - водородные связи относятся к сигма - связям - это связь, образующаяся при перекрывании атомных орбиталей по линии, проходящей через ядра атомов. Возможно вращение вокруг сигма - связей, поскольку эта связь имеет осевую симметрию. Физические свойства. Слайд № 6
CH4 – молекулярная формула метана
- Графическая и электронная формулы метан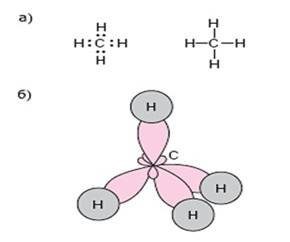 а
а
Мета́н бесцветный газ (в нормальных условиях) без запаха, малорастворим в воде, легче воздуха. При использовании в быту, промышленности в метан обычно добавляют одоранты со специфическим «запахом газа». Накапливаясь в закрытом помещении, метан становится взрывоопасен. Обогащение одорантами делается для того, чтобы человек вовремя заметил утечку газа. Взрывоопасен при концентрации в воздухе от 4,4 % до 17 %
Слайд № 7
СН4:C4Н10 - газы
T кипения: -161,6:-0,5 °C
T плавления: -182,5:-138,3 °C
С5Н12:C15Н32 - жидкости
T кипения: 36,1:270,5 °C
T плавления: -129,8:10 °C
С16Н34:и далее- твёрдые вещества
T кипения: 287,5 °C
T плавления: 20 °C
С увеличением относительных молекулярных масс предельных углеводородов закономерно повышаются их температуры кипения и плавления.
(Физкультминутка)
Распространение в природе. Слайд № 8
Основной компонент природного газа (77—99 %), попутных нефтяных газов (31—90 %), рудничного и болотного газов (отсюда произошли другие названия метана — болотный или рудничный газ). В анаэробных условиях (в болотах, переувлажнённых почвах, кишечнике жвачных животных) образуется биогенно в результате жизнедеятельности некоторых микроорганизмов.
Большие запасы метана сосредоточены в метаногидратах на дне морей в зоне вечной мерзлоты.
По современным данным, в атмосферах планет-гигантов солнечной системы в заметных концентрациях содержится метан.
Предположительно, на поверхности Титана в условиях низких температур (−180 °C) существуют целые озёра и реки из жидкой метано-этановой смеси.
Химические свойства Слайд №9
Для метана характерны следующие типы химических реакций:
1) Горение метана:
CH4 + 2O2 > CO2 + 2H2O + Q
2) Реакция галогенирования: Слайд №10
CH4 +Cl2 -> CH3Cl + HCl
Применение. Слайд №11
(Возможно, заранее подготовленные выступления учащихся.)
Широко используются в качестве топлива, в том числе для
двигателей внутреннего сгорания, а также при производстве сажи
(1 - картриджи; 2 - резина; 3 - типографическая краска), при получение органических веществ (4 - растворителей; 5 - хладогентов, используемых в холодильных установках; 6 - метанол; 7 - ацетилен) Слайд № 12
VI. Закрепление. Слайд №13
· Назовите 2 ближайших гомолога для пентана и назовите их.
· Определить предельный углеводород, плотность паров которого по воздуху равна 2. (C4H10).
· Создать 3D модель представителя гомологического ряда с помощью программы Avogadro
VII. Домашнее задание: Слайд №14
§ 25 Прочитать
Упражнение 287
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.