
МЕТОДИЧЕСКАЯ РАЗРАБОТКА ЗАНЯТИЯ

Разработала: преподаватель химии Ракчеева Наталия Александровна,
ГБПОУ «Ставрополь региональный многопрофильный колледж»
Тип занятия: изучение новых знаний и способов действий.
Методы: словесные, наглядные, проблемно-поисковые, самостоятельная работа.
Время: 80 минут
Цель занятия: формирование общих компетенций с использованием интерактивных методов обучения: по окончанию урока студент:
а) знает:
- строение глюкозы;
- физические и химические свойства;
- о роли углеводов в жизни человека и животных;
- области применения глюкозы.
б) умеет:
работать с информацией,
в) владеет рефлексией.
Задачи:
Воспитательная: продолжить формирование у обучающихся научно-материального мировоззрения, подтвердить единство природы, выражающегося во взаимных превращениях неорганических и органических веществ (фотосинтез); расширить и углубить кругозор об углеводах.
Образовательная: изучить строение глюкозы; выделить особые свойства глюкозы; выявить ее незаменимую роль в жизни человека и животных; научить самостоятельно составлять уравнения реакций.
Развивающая: развивать навыки экспериментальной работы, умения сравнивать, обобщать, делать самостоятельные выводы.
Методическая цель: продемонстрировать возможности использования на уроке информационно- коммуникационных технологий, педагогики сотрудничества, элементов современных развивающих методик.
Межпредметные связи: биология
Учебно-методическое обеспечение занятия:
Технические средства обучения: проектор, экран, компьютер, реактивы: глюкоза (кристаллическая), раствор гидроксида натрия, сульфата меди,
спиртовка, химическая посуда, штатив с пробирками, спиртовка, пробиркодержатель, спички, муляжи фруктов.
Наглядные пособия: схема “Классификация углеводов”
Дидактические материалы: инструкционная карта (приложение №1); задачи самостоятельной работы (приложение №2); тестовое задание (приложение №3); оценочный лист (приложение №4).
ХОД ЗАНЯТИЯ
I. Организационный момент (приветствие обучающихся, проверка их явки и готовности к занятию).
Вступительное слово преподавателя: Девизом сегодняшнего занятия я взяла слова
М. В.Ломоносова «Химик не такой должен быть, который дальше дыму и пеплу ничего не видит, а такой, который на основании опытных данных может делать теоретические выводы» (слайд3).
Мы продолжаем изучать представителей одного из классов органических соединений, которые находят широкое применение в различных отраслях народного хозяйства - в медицине, в пищевой, текстильной промышленности, играет незаменимую роль в жизни человека и животных и др.
II. Актуализация прежних знаний.
Разминка. Дать названия соединениям (слайд4). Названия и свойства этих соединений понадобятся нам при изучении нового материала.
III. Подготовка к изучению нового материала:
Вступительное слово преподавателя:
Сегодня мы с вами вспомним детство и послушаем сказку.
В большом царстве углеводородов случилась беда - разорился старый углеводород Гексан. От тоски и безысходности он начал чахнуть и болеть. Ему не могли ничем помочь самые лучшие лекари. И вдруг однажды перед ним оказалась красивая, белолицая девушка, она улыбнулась и сказала: "Не печалься, я помогу тебе вернуть богатство и силы! Я осыплю тебя серебром, только прикажи доставить сюда аммиачный раствор оксида серебра".
Удивился Гексан, но просьбу выполнил. И действительно, через некоторое время посыпались на пол серебряные монеты. От удивления старик даже рот открыл, сказать ничего не может. А девушка продолжает: "Чтобы твои силы восстановились - ешь виноград". Гексан кое-как вымолвил: "Кто ты? Как тебя зовут?" Девушка ответила, что она его дальняя родственница, поскольку у них одна углеродная цепь, а живет она в царстве кислородсодержащих соединений, и ее имя в переводе с греческого значит "сладкая". Больше она ничего не сказала, улыбнулась на прощание и исчезла. Только огромное количество серебра убеждало старика в том, что
эта встреча была явью, а не сном. А когда старик стал есть виноград, к нему действительно вернулись силы (слайд5).
Одна мысль не давала ему покоя - кто эта незнакомка? Позвал он лучшего сыщика, рассказал ему все и приказал узнать ее состав, строение и свойства. "А иначе, - говорит - не сносить тебе головы".
Сыщик взялся за дело с радостью, потому что хорошо знал греческий язык и сразу смекнул, что сладкая значит "glukus"(слайд6). После недолгих рассуждений он смог назвать ее имя - Глюкоза и то, что она содержится в винограде, помогло ему установить другое имя - виноградный сахар.
Определение физических свойств глюкозы (слайд7):
Преподаватель: Возьмем пробирку с глюкозой. Какого цвета это вещество? Каково его агрегатное состояние? (белый, кристаллический порошок). Проверим его на растворимость – добавим в пробирку воды. Что происходит? Определим рН среды
(опустим универсальную индикаторную бумагу в водный р-р глюкозы- изменение цвета бумаги не происходит, следовательно, рН среды- нейтральная).
Вывод: Глюкоза – белое порошкообразное вещество со сладким вкусом, хорошо растворимое в воде, рН среды- нейтральна.
IV.Объяснение нового материала.
Сыщик установил ее родословную - она относится к классу «Углеводы» - это старинное название этого класса органических веществ, их формула Cn(H2O)m..
Тема нашего занятия: «Углеводы. Моносахариды» (слайд 8). На сегодняшнем занятии мы рассмотрим следующие вопросы (слайд 9). (Тема и цели занятия формулируется вместе с обучающимися).
Далее дается классификация углеводов (слайд 10, 11).
Преподаватель: Сыщик еще кое-что узнал о глюкозе и составил досье на глюкозу (слайд 12).
|
Глюкоза реагирует |
Что наблюдается ? |
Вывод (какие функциональные группы содержатся в молекуле) |
|
1. с аммиачным р-ром Ag2О (слабое нагрев.) |
Выделяется серебро (реакция “серебряного зеркала”) |
|
|
2. с пятью молекулами уксусной кислоты |
Образуется сложный эфир, содержащий 5 остатков уксусной кислоты |
|
|
3. |
|
|
|
4. |
|
|
|
5. |
|
|
|
6. Специфические свойства: |
|
|
Окончательный вид досье принимает после беседы по соответствующим вопросам (см. ниже).
Вот такое досье сыщик представил Гексану через несколько дней. Рассердился углеводород, но дал ему время завершить начатое.
Сыщик понимал, что без знаний по химии ему голову на плечах не удержать. Ноги сами привели его в наш колледж, чтобы мы помогли сыщику дописать досье и сделать правильные выводы.
Преподаватель: Давайте вспомним все, что знаем о кислородсодержащих соединениях.
1.Какие вещества дают "реакцию серебряного зеркала"? (альдегиды);
2.Какая у них функциональная группа? (альдегидная).
3.Глюкоза также дает реакцию «серебряного зеркала» - следовательно какую группу она содержит? (альдегидную) Видеоопыт.
4. Какие вещества образуют с кислотами сложные эфиры? (спирты)
5. Какую функциональную группу они содержат? (-ОН).
6. О чем говорит тот факт, что глюкоза реагирует с 5 молекулами уксусной кислоты? (в ней пять групп - ОН).
7. К какому классу можно отнести глюкозу? (многоатомные спирты);
8.Какая реакция является качественной на многоатомные спирты? (взаимодействие с гидроксидом меди II).
9. Будет ли глюкоза вступать в реакцию с Cu(ОН)2 при обычных условиях? (да).Что можно сделать дальше? (Нагреть). Видеоопыт.
Обратите внимание на происходящие изменения:
t0 t0
ярко-синий раствор → желтый осадок → красный осадок
10. Какой вывод делаем? (Глюкоза - альдегид) (Запись в инструкционную карту- отмечаем появление осадка желтого, а затем красного цвета);
11. А какой факт из сказки поможет нам составить структурную формулу глюкозы? (Общая углеродная цепь с Гексаном); обучающиеся самостоятельно составляют структурную формулу глюкозы и делают вывод: глюкоза – альдегидоспирт (слайд 13).
11. Специфические свойства - спиртовое , молочнокислое, маслянокислое, полное брожение глюкозы изучается методом зигзага. (слайды 14-18).
Мини- проекты студентов:
1.Значение глюкозы в жизни растений и животных. Применение глюкозы.
(Вывод: глюкоза применяется в медицине, кондитерских изделиях, текстильной промышленности и содержится в организме и выполняет энергетическую функцию)- слайды 19-26.
2. Интересные факты о глюкозе (слайды 27-30).
V. Формирование умений и навыков.
Инструктаж по технике безопасности (слайд 31).
1.Эксперимент. Обнаружение глюкозы в ягодах и фруктах (слайды 32-33).
Оборудование: свежий виноград, разбавленные растворы сульфата меди (II) и гидроксида натрия, пробирка, пробиркодержатель, спиртовка.
Ход эксперимента: Выжать из винограда сок в широкую пробирку. Разбавить сок вдвое водой и прилить к полученному раствору равный объем щелочи и 1 мл раствора сульфата меди (II). Нагреть пробирку со смесью в пламени горелки. Образуется желтый, а затем красный осадок:
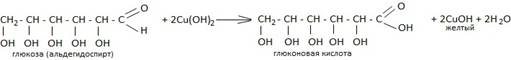
2СuОН = Сu2О + Н2О
Вывод: в виноградном соке содержится глюкоза.
2.Размышление-загадка (слайд 34).
Лаборант приготовила реактивы и вышла из кабинета. Здесь Трехатомный спирт, сойдя с полочки, подошел к столу и забрал свой реактив. Увидев это, Глюкоза возмутилась: “Что вы делаете, зачем берете чужое, это же мой распознаватель!”“Позвольте, позвольте, вмешаться в ваш спор”– промолвил Формальдегид, – “Это же мое вещество”.
Вопросы:
Кто был из них прав?
О каком веществе они спорили?
Как разрешить этот спор?
Задание:
1. Напишите формулы всех веществ, участвующих в споре (глицерин, глюкоза, формальдегид, гидроксид меди)
2. Запишите уравнения возможных реакций.
Преподаватель делает самопроверку (слайды 35-36).
1.
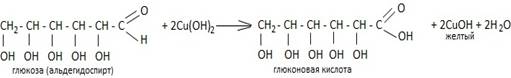
2СuОН = Сu2О + Н2О
красный
2
![]() СН2-СН-СН2
+ Cи(ОН)2 глицерат
меди (р-р ярко-синего цвета)
СН2-СН-СН2
+ Cи(ОН)2 глицерат
меди (р-р ярко-синего цвета)
ОН ОН ОН
3.
![]() Н-СОН + 2Cи(ОН)2 Н-СООН +
Си2О +2Н2О
Н-СОН + 2Cи(ОН)2 Н-СООН +
Си2О +2Н2О
3.Историческая загадка (слайд37).
Преподаватель: Вам, наверняка, известна такая историческая фигура как Григорий Распутин - полуграмотный крестьянин, обладавший невероятными, гипнотическими способностям, был вхож в царскую семью. Царь Николай II и его жена считали своим духовным отцом. Вся жизнь этого человека была окутана скандальными историями. Невероятна была и его смерть. Вначале его пытались отравить – подсыпав KCN в крем пирожных. Но яд почему-то не подействовал!! Что вызвало ужас и панику у заговорщиков!
- Попытайтесь объяснить эту историческую загадку, используя полученные сегодня знания.(C давних пор, при опасности отравления цианидами, рекомендовали держать за щекой кусочек сахара. Учеными было доказано, что глюкоза взаимодействует с цианидами с образованием нетоксичного соединения циангидрин глюкозы).
4. Дидактическая игра «Кот в мешке». Задачи для самостоятельного решения (слайд 38).
Обучающиеся вытаскивают текст задачи (уровень равноценный) для самостоятельного их решения (см. приложение№3).
В качестве справочных материалов – молярные массы веществ.
Преподаватель делает самопроверку (слайд 39).
VI.Закрепление изученного материала. Выполнить тест (приложение №2, слайд 40).
VII.Рефлексивное задание (слайд 41).
1.Продолжите фразу (слайд ):
Сегодня на занятии я узнал …
Теперь я могу …
Было интересно …
Полученные знания я смогу применить…
VII. Подведение итогов занятия.
1.Заполнение оценочных листов (слайд 42). Оценка складывается из баллов по 5 пунктам.
Обучающиеся выставляют баллы в оценочные листы (приложение №4) и сдают их преподавателю.
Усвоение учебного материала (слайд 43).
Если считать, что полное усвоение учебного материала урока соответствует дистанции,
А_____________________________________________В
то покажите точкой ваше место нахождения.
2.Сообщение о реализации цели учебного занятия (слайд 44), выставление оценок, информация о домашнем задании (слайд 45).
Домашнее задание:
конспект; осуществить превращения:
1 вариант:
Углерод → оксид углерода(IV) → глюкоза → сахароза
2 вариант:
Оксид кальция → карбид кальция → ацетилен→ углекислый газ→ глюкоза
Подготовить сообщение о применении полисахаридов (опережающее задание).
Литература
1.Химия. 10 класс: Учеб. для общеобразовательных. учреждений/ О.С. Габриелян, Ф.Н. Маскаев, С.Ю. Пономарев, В.И. Теренин; Под ред. В.И. Теренина. – 3-е изд., стереотип. – М.: Дрофа, 2012. – 304с.: ил.
2.Уроки химии в 10 – 11 классах: Методическое пособие для учителя/ Р.Г. Иванова, А.А. Каверина, А.С. Корощенко. – М.: Просвещение, 2012. – 190с.: ил.
3.Мультимедиа учебный курс «1С: Образовательная коллекция. Органическая химия».
|
Глюкоза реагирует |
Что наблюдается |
|
Вывод (какие функциональные группы присутствуют в молекуле)
|
|
1. с аммиачным р-ром Ag2О (слабое нагрев.) |
Выделяется серебро (реакция "серебряного зеркала") |
|
альдегидная |
|
2. с пятью молекулами уксусной кислот |
Образуется сложный эфир, содержащий 5 остатков уксусной кислоты |
|
5 гидроксильных групп
|
|
3. Cu(ОН)2 обычные усл. |
Ярко синий раствор |
|
гидроксильная
|
|
4. Cu(ОН)2 нагревание |
красный осадок |
|
альдегидная |
|
5.Структурная формула
|
|
|
|
|
6. Специфические свой-ства: Спиртовое брожение-
Молочнокислое-
Маслянокислое-
Полное брожение- |
2С2Н5ОН +2СО2
2С3Н6О3
С5Н7СООН+2СО2+2Н2
|
используют в получении алкогольных напитков кефира, кумыса и др.молочных продуктов.
для получения молочных продуктов: простокваши, творога, сметаны, сыра.
может быть причиной появления дефектов или даже порчи молочных продуктов.
выделяется энергия для обеспечения процессов жизнедеятельности организма. |
|
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.