
Лекция 46.
Тема «Углеродный скелет органической молекулы. Кратность химической связи.».
Органическая химия — это химия соединений углерода (органических соединений). Согласно другому определению органическая химия — это химия углеводородов и их производных. Основой органической химии является структурная теория, или теория химического строения органических соединений, которая была разработана во второй половине XIX в. и в которую огромный вклад внесла научная школа русского химика А. М. Бутлерова.
Основные положения структурной теории:
1) Атомы в органических молекулах соединены между собой в определенном порядке химическими связями в соответствии с их валентностью. Этот порядок называется химическим строением. Углерод во всех органических соединениях четырехвалентен.
2) Химическое строение можно выразить структурной формулой, в которой химические связи между атомами изображаются черточками. Общее число черточек, отходящих от каждого атома, равно его валентности.
3) Физические и химические свойства веществ зависят не только от их качественного и количественного состава, но и от строения молекул. Вещества, описываемые одинаковой молекулярной формулой (изомеры), могут иметь совершенно разные физические и химические свойства.
4) Атомы в молекуле оказывают друг на друга взаимное влияние. Свойства каждого атома зависят не только от его природы, но и от его окружения.
Для классификация органических соединений используют понятия «углеродный скелет» и «функциональная группа».
Углеродный скелет — это каркас органической молекулы; он представляет собой последовательность химически связанных между собой атомов углерода. Во многих органических реакциях углеродный скелет остается неизменным. Углеродные скелеты бывают циклические, в которых углеродная цепь замкнута в цикл, и алифатические, в которых углеродная цепь не замкнута. Кроме того, скелеты бывают разветвленные и неразветвленные: в неразветвленных скелетах каждый атом углерода связан с одним или двумя атомами углерода, а в разветвленных скелетах хотя бы один атом углерода связан с тремя или четырьмя атомами углерода.
Атомы углерода в скелетах различают по числу химически связанных с ними других атомов углерода. Если данный атом углерода связан с одним атомом углерода, то его называют первичным, с двумя — вторичным, тремя — третичным и четырьмя — четвертичным.
Органические соединения классифицируют также по кратности связи углерод-углерод. Соединения, содержащие только одинарные связи углерод-углерод, называют насыщенными, или предельными; соединения со связями С=С или С=С называют ненасыщенными, или непредельными. Соединения, в которых атомы углерода связаны только с атомами водорода, называют углеводородами.
Функциональные группы образуют все атомы, кроме водорода, или группы атомов, связанные с атомом углерода. Функциональные группы — это активные центры органических молекул. Именно они чаще всего испытывают химические превращения и определяют многие химические и физические свойства органических соединений.
Соединения, имеющие одинаковые функциональные группы, но отличающиеся числом атомов углерода, обладают весьма похожими физическими и химическими свойствами. Такие соединения называют гомологами. Гомологи — это соединения, принадлежащие одному классу, но отличающиеся друг от друга по составу на целое число групп —СН2. Совокупность всех гомологов образует гомологический ряд.
Одно из основных положений структурной теории связано с существованием изомеров. Изомеры это вещества имеющие одинаковый качественный и количественный состав (молекулярную формулу), но разное строение молекул.
Различают два вида изомерии — структурную и пространственную. Структурные изомеры отличаются друг от друга порядком соединения атомов. В пространственных изомерах порядок соединения атомов один и тот же, однако некоторые атомы благодаря электронным или геометрическим особенностям отличаются положением в пространстве относительно других атомов.
Структурные изомеры могут отличаться друг от друга: 1) строением углеродных скелетов; 2) положением функциональной группы; 3) положением кратной связи; 4) по классам органических соединений.
Пространственные изомеры (стереоизомеры) можно разделить на два класса: 1) цис-транс-изомеры; 2) оптические изомеры. Цис транс точерия связана с разным положением заместителей относительно двойной связи С=С или одинарной связи С—С в циклах. Оптическая изомерия характерна для молекул, которые не совпадают со своим зеркальным отображением. Таким свойством обладают любые молекулы, имеющие хотя бы один атом углерода, связанный с четырьмя различными заместителями.
Все атомы в органических молекулах находятся во взаимосвязи и испытывают взаимное влияние. Смещение электронных облаков (электронной плотности) в молекуле под влиянием заместителей называют электронными эффектами. Если атом или группа атомов смещают электронную плотность на себя, то говорят, что они обладают электроноакцепторными свойствами и проявляют отрицательный электронный эффект. В противном случае они обладают электронодонорными свойствами и проявляют положительный эффект.
Смещение электронной плотности по цепи одинарных связей называют индуктивным эффектом и обозначают буквой І; смещение электронной плотности, передаваемое по цепи кратных связей, называют мезомерным эффектом (М).
по составлению названия органического соединения по номенклатуре IUPAC (заместительная номенклатура)
Для составления названия органического соединения по номенклатуре IUPAC необходимо выполнить следующие операции:
1. Определите функциональную (характеристическую) группу, если она имеется, суффикс которой используют при составлении названия. При составлении названия используется суффикс только одной функциональной группы, называемой главной (исключение: суффиксы двойной или тройной связи). Все заместители, в том числе и другие младшие функциональные группы, указываются префиксами.
Некоторые характеристические группы, расположенные
в порядке уменьшения старшинства
|
КЛАСС |
Формула |
ПРЕФИКСЫ |
СУФФИКСЫ |
|
Карбоновые кислоты Альдегиды Кетоны Спирты Фенолы Амины Галогениды Нитро-соединения |
-СООН -СООН -СНО -СНО -(С)=О -ОН -ОН -NH2 F, Cl, Br, I —NO2 |
-карбокси - -формил -оксо -оксо -гидрокси -гидрокси -амино Фтор-, Хлор-, бром, иод Нитро |
-карбоновая кислота -овая кислота -карбальдегид -аль -он -ол -ол -амин Фторид, Хлорид, Бромид, Иодид |
2. Определите родовой гидрид:
а) для ациклических соединений родовым гидридом является самая длинная неразветвленная цепь, включающую главную функциональную группу а также двойные и (или) тройные связи. Родовой гидрид образуется прибавлением атомов водорода вместо заместителей или гетероатомов, присоединеннных к длинной цепи, чтобы получился насыщенный углеводород.
б) для циклических соединений родовым гидридом является насыщенный циклоалкан, например циклогексан или полностью ненасыщенный углеводород ( гетероциклическое соединение), например бензол, пиридин и т.д.
3. Назовите родовой гидрид вместе с суффиксом главной группы.
4. Пронумеруйте самую длинную цепь таким образом, чтобы атом углерода главной функциональной группы получил наименьший номер.
5. Назовите заместители вместе с цифрами (локантами), указывающими атомы углерода, при которых заместители находятся.
6. Название заместителей с их локантами по алфавиту присоедините к названию родового гидрида. Локанты двойной и (или) тройной связи и локант главной функциональной группы расположите перед соответствующими суффиксами.
Пример 1.
![]()
Главная группа: -ОН -ол
Родовой гидрид: Н3С–СН3 этан
Название: этанолэтан-1,2-диол
Пример 2: Пример 3:
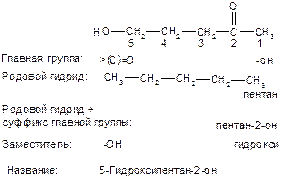
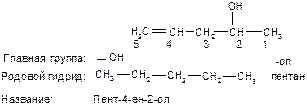
Пример 4:

Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.