
ОБЛАСТНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «РОСЛАВЛЬСКИЙ МЕДИЦИНСКИЙ ТЕХНИКУМ»
|
Рассмотрено на заседании ЦМК специальности 33.02.01 Фармация Протокол №________ « _____ » ______________ 2024 г. Председатель: ________________________________ /Т.А. Вишневская/ |
|
«УТВЕРЖДАЮ» Заместитель директора по учебно-методической работе
__________________________ /С.В. Новикова/ « _____ » ______________ 2024 г.
|
Учебно-методическое пособие
по МДК 02.02 Контроль качества лекарственных средств
ТЕМА: «ОПРЕДЕЛЕНИЕ ГАЛОГЕНИДОВ
ПРИ ИХ СОВМЕСТНОМ ПРИСУТСТВИИ
В ЛЕКАРСТВЕННЫХ ФОРМАХ»
Разработчик: зав. отделением
специальности 33.02.01 Фармация,
преподаватель высшей
квалификационной категории
Т.А. Вишневская
Рославль
2024 г.
Пояснительная записка
Особое место среди задач контроля качества лекарственных средств занимает анализ качества многокомпонентных лекарственных форм.
Сборником обязательных общегосударственных стандартов, нормирующих качество лекарственных средств, является Государственная фармакопея. Государственная фармакопея (греч. «pharmakon» – лекарство и «poieo» – делаю (искусство приготовления лекарств)) является официальным руководством для фармацевтов (провизоров), содержащим описание свойств, требования проверки подлинности и количественного содержания, условий хранения лекарств.
Государственная Фармакопея – это основной документ, регламентирующий фармацевтический анализ. Однако Фармакопея содержит положения, нормирующие качество лекарственных субстанций и однокомпонентных лекарственных средств. При этом выполняя испытания подлинности и количественного анализа лекарственных веществ, содержащихся в однокомпонентных лекарственных формах, обычно используют те же химические реакции, что и для соответствующих субстанций, указанных в фармакопейных статьях ГФ.
Характерной особенностью анализа многокомпонентных лекарственных форм является то, что способы определения индивидуальных веществ часто не дают положительных результатов при использовании их для анализа лекарственных смесей. Возникает необходимость подбирать условия, позволяющие анализировать одно лекарственное вещество в лекарственной смеси в присутствии другого, или предварительно отделять лекарственные вещества друг от друга или от вспомогательных веществ. При этом фармацевтический анализ осложняется, если каждый из компонентов смеси характеризуется сходными физическими и химическими свойствами, как в случае совместного присутствия галогенидов в лекарственных смесях.
Учебно-методическое пособие ориентировано на развитие общих и профессиональных компетенций, направленных на повышение квалификации фармацевтических кадров в области оценки и контроля качества многокомпонентных лекарственных форм.
Цель данного пособия заключается в формировании у студентов компетенции по анализу комбинированных лекарственных смесей, содержащих галогениды, на основе приобретенных ранее знаний о физических, физико-химических и химических свойствах лекарственных средств и методах их анализа.
Учебно-методическое пособие состоит из двух разделов (теоретического и практического), и содержит подробное описание работ по контролю качества многокомпонентных лекарственных форм, содержащих галогениды, необходимые для изучения и закрепления теоретического материала по контролю качества и приобретения практических навыков фармацевтического анализа лекарственных средств рассматриваемой группы. В пособии рассмотрен контроль качества лекарственных форм внутриаптечного и промышленного производства. Пособие включает задания для самоподготовки и самоконтроля, а также материалы, необходимые для оформления результатов контроля качества и ведения протоколов анализа.
Учебно-методическое пособие предназначено для самостоятельной подготовки студентов отделения специальности 33.02.01 Фармация, выполнения практических занятий. Методики анализа могут быть рекомендованы для использования в работе провизоров-аналитиков контрольно-аналитических лабораторий и аптек при химическом контроле качества лекарственных средств.
В процессе самоподготовки, теоретических и практических занятий студент должен знать:
- требования нормативной документации, предъявляемые к фармацевтическому анализу субстанций, однокомпонентных и многокомпонентных лекарственных смесей;
- методы качественного и количественного определения галогенидов.
В процессе самоподготовки, теоретических и практических занятий студент должен уметь:
- определять трудности, возникающие при определении галогенидов в случаях их совместного присутствия в лекарственных формах;
- выбирать приемы и методы, позволяющие преодолеть выявленные трудности, возникающие при определении галогенидов в случаях их совместного присутствия в лекарственных формах;
- составлять схемы методик качественного и количественного определения многокомпонентных лекарственных смесей галогенидов при их совместном присутствии;
- осуществлять контроль качества многокомпонентных лекарственных форм при совместном присутствии в них галогенидов.
ПЕРЕЧЕНЬ ОБЩИХ И ПРОФЕССИОНАЛЬНЫХ КОМПЕТЕНЦИЙ,
КОТОРЫМИ ДОЛЖЕН ОВЛАДЕТЬ СТУДЕНТ
ПО ИТОГАМ ВЫПОЛНЕНИЯ ПРАКТИЧЕСКОЙ ЧАСТИ
|
ПК 2.3 |
Владеть обязательными видами внутриаптечного контроля лекарственных средств |
|
ПК 2.4 |
Оформлять документы первичного учета по изготовлению лекарственных препаратов |
|
ПК 2.5 |
Соблюдать правила санитарно-гигиенического режима, охраны труда, техники безопасности и противопожарной безопасности, порядок действия при чрезвычайных ситуациях |
|
ОК 01 |
Выбирать способы решения задач профессиональной деятельности применительно к различным контекстам |
|
ОК 02 |
Осуществлять поиск, анализ и интерпретацию информации, необходимой для выполнения задач профессиональной деятельности |
|
ОК 03 |
Планировать и реализовывать собственное профессиональное и личностное развитие |
|
ОК 04 |
Работать в коллективе и команде, эффективно взаимодействовать с коллегами, руководством, клиентами |
|
ОК 05 |
Осуществлять устную и письменную коммуникацию на государственном языке Российской Федерации с учетом особенностей социального и культурного контекста |
|
ОК 07 |
Содействовать сохранению окружающей среды, ресурсосбережению, эффективно действовать в чрезвычайных ситуациях |
|
ОК 09 |
Использовать информационные технологии в профессиональной деятельности |
|
ОК 10 |
Пользоваться профессиональной документацией на государственном и иностранном языках |
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
КОНТРОЛЬ КАЧЕСТВА
ЛЕКАРСТВЕННЫХ СРЕДСТВ – ГАЛОГЕНИДОВ
1.1 Контроль качества лекарственных средств. Общие положения
Лекарственные средства, подлежащие обращению на территории Российской Федерации, при условии их использования в соответствии с рекомендациями врача и инструкцией по медицинскому применению в течение срока их годности и надлежащих условий хранения, должны соответствовать требованиям нормативной документации по показателям качества и не должны причинять вреда жизни или здоровью человека.
Требования к лекарственным средствам включают:
1. Требования к качеству и безопасности лекарственных средств;
2. Требования к упаковке и маркировке лекарственных средств.
Согласно Федерального закона от 12.04.2010 г. № 61-ФЗ (ред. от 03.07.2016) «Об обращении лекарственных средств» (с изм. и доп., вступ. в силу с 15.07.2016 г.) под качеством лекарственных средств понимают соответствие их государственному стандарту качества лекарственных средств.
Контроль качества лекарственных средств – это комплекс мероприятий, направленных на своевременное предупреждение и выявление ошибок, неточностей, возникающих при изготовлении, оформлении и отпуске лекарств. С целью обеспечения контроля качества лекарственных средств в аптеках организованы аналитические кабинеты или аналитические столы, оснащенные приборами, реактивами, справочной литературой.
Внутриаптечный контроль качества осуществляют провизоры-аналитики. Провизоры-технологи, в обязанности которых также входит проверка качества лекарств, имеют оборудованное рабочее место на ассистентском столе или рядом с ним. Заведующий аптекой и его заместители руководят работой по контролю качества лекарств. Они должны владеть всеми видами контроля, а в небольших аптеках сами выполнять функции провизора-технолога.
Непосредственный контроль в аптеке включает три основных направления:
1. Контроль качества лекарственных веществ, поступающих от промышленности.
2. Контроль качества очищенной воды.
3. Различные виды контроля качества лекарственных форм, изготовляемых в аптеке.
Внутриаптечному контролю подвергаются все изготовляемые в аптеке лекарственные формы.
Существуют несколько видов контроля, которые условно подразделяются на обязательные и выборочные. К обязательным относят письменный, органолептический, контроль при отпуске. К выборочным – опросный, физический. Химический контроль может быть обязательным и выборочным. Виды контроля качества лекарственных средств и показатели качества, по которым можно установить неудовлетворительность изготовленных лекарственных форм, регламентируются Приказом Министерства здравоохранения РФ от 22 мая 2023 г. № 249н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, имеющими лицензию на фармацевтическую деятельность».
Для обеспечения контроля качества лекарственных средств промышленного производства каждое предприятие-изготовитель, которому выдается лицензия на производство и оптовую реализацию лекарственных средств, обязано иметь отдел технического контроля.
Основной задачей ОТК является предотвращение производства и/или поставки потребителю некачественной готовой продукции. ОТК должен быть независимым от других структурных подразделений предприятия.
Начальник ОТК должен иметь соответствующую квалификацию и опыт работы. В составе ОТК должны находиться одна или несколько испытательных (контрольных) лабораторий.
Контроль качества лекарственных средств в ОТК предприятия включает работы, которые связаны с отбором проб, нормативной документацией (спецификациями, ФСП) и испытаниями, а также с методиками организации этих работ, их документированием и выдачей в установленном порядке разрешений, гарантирующих, что все необходимые соответствующие испытания действительно проведены.
1.2 Методы определения индивидуальных лекарственных средств
Эффективность действия лекарственного средства непосредственно связана с его природой, поэтому в определении качества лекарственного вещества одной из основных целей является установление его подлинности.
Под определением подлинности понимают установленное в нормативном смысле соответствие анализируемого лекарственного средства тому наименованию, под которым он поступил на анализ, и будет использоваться в медицинской практике.
Для определения подлинности лекарственных средств чаще всего используется химический метод, т.к. он не требует эталонирования и сводится к визуальному фиксированию результатов. Химический метод определения подлинности не требует дорогостоящего оборудования. В основе его лежит аналитическая реакция – реакция, идущая с аналитическим эффектом (образование осадка, изменение окраски, появления запаха, выделение газа).
К химическим реакциям, используемым для определения подлинности лекарственного средства, предъявляются следующие требования:
1. Реакция определения подлинности должна быть по возможности специфичной. Специфические реакции – это реакции, которые позволяют получить с данным реагентом характерный аналитический эффект, свойственный только для данного лекарственного средства.
2. Реакция определения подлинности должна быть избирательной. Избирательные (селективные) реакции – это реакции, которые, являясь групповыми, при выполнении определенных условий становятся избирательными к тому или иному веществу или структурной части.
3. Реакция определения подлинности должна быть чувствительной. Под этим термином понимается наименьшее количество определяемого вещества, которое может быть обнаружено данным реактивом с учетом разведения. Этот термин близок по смыслу к понятию «предел обнаружения», который обозначает наименьшее содержание, при котором по данной методике можно обнаружить присутствие определяемого компонента с заданной доверительной вероятностью.
4. Реакция определения подлинности должна быть быстрой и обязательно сопровождаться отчетливым аналитическим эффектом.
С целью обеспечения правильной дозировки лекарственного средства в ходе его анализа проводится количественное определение. Лекарственное вещество стандартизуется по содержанию в нем действующего вещества, обуславливающего терапевтический эффект.
В количественном анализе неорганических лекарственных веществ преимущества имеют химические методы, т.к. эти методы являются абсолютными и не требуют использования стандартных образцов.
Химические методы количественного определения лекарственных средств являются экономически обоснованными, не требуют дорогостоящего оборудования. Одной из основных операций в них является операция по измерению объема стандартного раствора (титриметрические методы количественного определения).
В объемном титровании количество определяемого вещества устанавливается по количеству израсходованного стандартного реагента.
К химическим реакциям, используемым для количественного определения подлинности лекарственного средства, предъявляются следующие требования:
1. Вещества, вступающие в реакцию количественного определения, должны реагировать в строго определенных количественных соотношениях (стехиометрических отношениях).
2. Реакции, протекающие между определяемыми лекарственными веществами и стандартными растворами, должны протекать быстро и практически до конца.
3. Посторонние вещества, присутствующие в исследуемом лекарственном средстве и переходящие вместе с основным определяемым компонентом в раствор, не должны мешать титрованию определяемого вещества.
4. Точка эквивалентности реакций количественного определения должна фиксироваться быстро и точно.
5. Химические реакции количественного определения, по возможности, должны протекать при комнатной температуре.
Методики качественного и количественного определения частовстречающихся элементов и структурных частей различных лекарственных средств унифицированы и изложены в нормативных документах общего характера. К таким нормативным документам относятся общие фармакопейные статьи (ОФС) «Общие реакции на подлинность» и ОФС «Количественного определения лекарственных средств».
В ОФС описываются методики определения частовстречающихся элементов и структурных частей с указанием их пределов содержания в пробе анализируемого лекарственного средства, позволяющих получить отчетливый аналитический эффект. В фармакопейных статьях (ФС) в этом случае даются лишь ссылки на ОФС.
Все реактивы, применяемые для определения подлинности и количественного определения лекарственных средств, должны отвечать требованиям действующих ГОСТов, причем их приготовление указано в ОФС «Реактивы», ОФС «Титрованные растворы», ОФС «Индикаторы, применяемые при объемных определениях».
Мерная посуда, используемая при проведении химических реакций, регламентируется ОФС «Мерная посуда».
1.3 Определение индивидуальных
лекарственных средств – галогенидов
Галогены – хлор, бром, йод – элементы главной подгруппы VII группы Периодической системы Д.И. Менделеева.
Неорганические лекарственные средства – производные галогенов классифицируют на две группы:
1. Препараты свободных галогенов: препараты свободного (в молекулярном состоянии) галогена – йода, известь хлорная (действующее вещество – кальция хлорид-гипохлорит), хлорамин и пантоцид (хлорпроизводные бензолсульфамида) (действие их основано на выделении молекулярного галогена – хлора). Препараты свободных галогенов применяют в качестве антисептиков. Препараты йода используют и перорально при лечении атеросклероза, хронических воспалительных процессов в дыхательных путях, гипертиреоза и некоторых других заболеваний, для профилактики эндемического зоба.
2. Лекарственные средства, являющиеся солями галогеноводородных кислот (галогениды натрия и калия: хлориды, бромиды и йодиды).
Натриевые и калиевые соли галогеноводородных кислот нашли широкое применение в медицине. Натрия хлорид – основная составная часть солевых и коллоидно-солевых растворов, применяемых в качестве плазмозамещающих жидкостей. Калия хлорид является антиаритмическим средством и источником ионов калия (при гипокалиемии). Он также входит в состав плазмозамещающих жидкостей.
Натрия и калия бромиды применяют в качестве седативных (успокаивающих) средств внутрь и внутривенно. Натрия и калия йодиды применяют при недостатке йода в организме (эндемическом зобе) и некоторых воспалительных заболеваниях.
Галогениды щелочных металлов являются лекарственными средствами неорганической природы. При их определении в субстанциях лекарственных веществ, а также в однокомпонентных лекарственных средствах практически проводится элементный анализ, основанный на обнаружении ионов. Это связано с тем, что атомы элементов в галогенидах связаны ионной связью. Для получения ионов, достаточно растворения вещества в воде, являющейся полярным растворителем и способствующей диссоциации вещества на ионы.
По физическим свойствам (табл. 1.1) галогениды представляют собой белые или бесцветные кристаллические вещества без запаха, соленого вкуса, легко (йодиды – очень легко) растворимые в воде. Йодиды легко растворимы в этаноле и глицерине, хлориды и бромиды менее растворимы в этих растворителях (Приложение 1).
Для определения подлинности галогенидов выполняют качественные реакции на соответствующие катионы и анионы, которые включены в ОФС и ФС Государственных фармакопей.
К химическим реакциям определения подлинности галогенид-ионов относятся:
1. Осадочная реакция с раствором нитрата серебра в азотнокислой среде (фармакопейная реакция). Образуются труднорастворимые соли (табл. 1.2) галогенидов серебра, которые отличаются по окраске и растворимости в растворе аммиака (Приложение 2).
2. Реакция окисления галогенидов до свободных галогенов с использованием различных окислителей (фармакопейная реакция). Образующиеся галогены извлекают хлороформом и наблюдают окраску хлороформного слоя. Бром окрашивает слой хлороформа в желто-бурый цвет, йод – в фиолетовый цвет.
Для качественного определения бромидов возможно применять нефармакопейную реакцию с раствором сульфата меди (II) и концентрированной серной кислотой – появляется черный осадок, исчезающий после добавления нескольких капель воды.
Реакции идентификации галогенидов проходят по общей схеме: качественный экспресс-анализ проводят на фильтровальной бумаге, предметном или часовых стеклах, на фарфоровой лодочке или в тигле, при этом расход анализируемого вещества составляет 0,001-0,01 г для порошка или 1-5 капель для жидкости. На фильтровальной бумаге проводят реакции, в результате которых образуются окрашенные соединения, если при этом не требуется применение концентрированных кислот или оснований.
Реакции, в результате которых образуются осадки белого цвета, выполняют на часовых или предметных стеклах, помещенных на темную поверхность.
Для количественного определения галогенидов применяют титриметрические методы осаждения – объемно-аналитические методы определения, основанные на реакции образования осадков малорастворимых соединений. Несмотря на то, что подобных реакций известно очень много, лишь некоторые из них могут быть использованы в объемном анализе. Такие реакции должны удовлетворять следующим условиям:
1. Осадок должен быть практически нерастворим.
2. Выпадение его должно происходить достаточно быстро.
3. Результаты титрования не должны в заметной степени искажаться явлениями адсорбции (соосаждения).
Перечисленные требования ограничивают круг реакций, практически применяемых в объемном анализе. Наибольшее значение для количественного определения галогенидов приобрели методы осаждения, связанные с образованием малорастворимых соединений серебра – осадительное титрование по методу Мора, Фольгарда, Фаянса (метод Мора – для определения хлоридов и бромидов, метод Фаянса – для определения йодидов являются фармакопейными).
В количественном определении используются растворы различных концентраций: 0,1; 0,05; 0,02; 0,01 моль/л. Навески жидких препаратов для титрования (1-3 мл) берут пипетками, навески порошков – на ручных аптечных весах (0,05-0,1 г). Навеску берут с таким расчетом, чтобы на титрование расходовалось 1-5 мл титрованного раствора. Для титрования используют микробюретки с делениями 0,02 мл или пипетки на 2,5 и 10 мл с делениями 0,05 мл. Титрование проводят в склянках на 10-20 мл.
1.3.1 Натрия и калия хлориды
Натрия и калия хлориды относятся к сильным электролитам. Их водные растворы имеют нейтральную реакцию среды, т.к. соли образованы
сильной кислотой и сильными основаниями и, поэтому, не подвергаются гидролизу. Химические свойства данных лекарственных веществ обусловлены наличием соответствующих ионов. Так, катионы натрия и калия окрашивают пламя соответственно в желтый и фиолетовый цвета.
Соли натрия образуют желтый кристаллический осадок (нерастворимый в кислоте уксусной) с цинка уранилацетатом.
Na+ + Zn2+ + [(UO2)3(CH3COO)8]2- + CH3COOH + 6H2O →
→ NaZn[(UO2)3(CH3COO)9]⋅ 6H2O↓ + H+
Образовавшиеся октаэдрические или тетраэдрические кристаллы желтого цвета рассматривают под микроскопом. Нонаацетат-триуранилат-цинкат (II) натрия (натрия цинкуранилацетат) обладает яркой флуоресценцией зеленого цвета. При содержании натрия менее 10 мкг свечение становится заметно лишь через 1-4 минут.
Гексагидроксостибат-ион в строго нейтральной среде образует с ионами натрия белый кристаллический осадок натрия гексагидроксостибата.
Na+ + [Sb(OH)6]− → Na[Sb(OH)6]↓
Соли калия с раствором гексанитрокобальтата (III) натрия образуют желтый кристаллический осадок гексанитрокобальтата (III) натрия и калия.
2K+ + Na3[Co(NO2)6] → NaK2[Co(NO2)6]↓ + 2Na+
Осадок не растворяется в кислоте уксусной; растворяется в минеральных кислотах. В сильнокислой среде образуется нестойкая кислота гексанитрокобальтовая H3[Co(NO2)6], разлагающаяся в момент выделения.
В щелочной среде образуется бурый осадок гидоксида кобальта (III). Проведению реакции мешают ионы аммония, также дающие с реактивом осадок. Для удаления ионов аммония соль калия предварительно прокаливают.
С раствором кислоты винно-каменной соли калия образуют осадок калия гидротартрата, который не растворяется в кислоте уксусной, но растворяется в минеральных кислотах и щелочах.
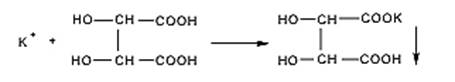
Добавление ацетата натрия обеспечивает необходимое значение рН в растворе, близкое к значению рК уксусной кислоты (4,75). В более кислых растворах осадок гидротартрата калия растворяется с выделением винной кислоты Н2С4Н4О6. В щелочной среде происходит замещение обоих протонов карбоксильных групп и образуется растворимая соль К2С4Н4О6.
Бесцветное пламя горелки в присутствии ионов К+ окрашивается в фиолетовый цвет (через синее стекло – окраска пурпурно-красная).
Хлорид-ион в данных лекарственных веществах определяют по взаимодействию с раствором серебра нитрата; образуется белый творожистый осадок.
Cl− + Ag+ → AgCl ↓
Реакцию проводят в присутствии кислоты азотной в качестве вспомогательного реактива, в котором не растворяются галогениды серебра. Особенность серебра хлорида, в отличие от бромида и йодида, заключается в способности легко растворяться в растворах аммиака, натрия карбоната и натрия тисосульфата.
AgCl + 2NH3 → [Ag(NH3)2]Cl
AgCl + (NH4)2CO3 → [Ag(NH3)2]Cl + CO2↑ + H2O
AgCl + 2Na2S2O3 → Na3[Ag(S2O3)2] + NaCl
Количественное определение индивидуальных натрия
хлорида и калия хлорида согласно ГФ проводят методом прямой аргентометрии по
Мору. Титрование ведут в нейтральной среде стандартным раствором серебра
нитрата в присутствии калия хромата в качестве индикатора. Серебра хлорид (ПРAgCl
= 1,78⋅10−10)
менее растворим, чем серебра хромат (![]() =
2⋅10−12),
поэтому хлорид-ионы осаждаются первыми.
=
2⋅10−12),
поэтому хлорид-ионы осаждаются первыми.
NaCl + AgNO3 → AgCl↓ + NaNO3
Далее, после полного осаждения хлорид-ионов, выпадает красно-оранжевый осадок серебра хромата.
2AgNO3 + K2CrO4 → Ag2CrO4↓ + 2KNO3
Обязательное условие проведения методики – соблюдение нейтральной или слабо щелочной реакции среды (рН 7,0-10,0). В противном случае, в кислой среде, хромат-ион переходит в дихромат-ион и чувствительность индикатора резко понижается. Если определение хлоридов методом Мора невозможно (например, при анализе лекарственных смесей, имеющих кислую реакцию среды, или содержащих вещества реагирующих, наряду с хлоридами, с ионами серебра), применяют метод обратного аргентометрического определения по Фольгарду. При этом хлориды осаждают избытком титрованного раствора серебра нитрата и оттитровывают остаток серебра нитрата стандартным раствором аммония тиоцианата.
AgNO3 + NaCl → AgCl↓ + NaNO3
AgNO3 (остаток) + NH4SCN → AgSCN↓ + NH4NO3
В качестве индикатора используют растворы солей трехвалентного железа, например аммония железа (III) сульфата (квасцы железоаммониевые − NH4Fe(SO4)2 ⋅ 12H2O), которые с избыточной каплей аммония тиоцината образуют комплексные соли красного цвета.
Fe3+ + nSCN− → [Fe(SCN)n]-3n
1.3.2 Натрия и калия бромиды
Бромиды натрия и калия – белые кристаллические порошки хорошо растворимые в воде; реакция среды водных растворов нейтральна. Натрия бромид гигроскопичен. Степень увлажнения его регламентируется путем определения потери в массе при высушивании.
Для идентификации применяют реакции на катионы и анионы, т.к. бромиды натрия и калия (как и хлориды) являются сильными электролитами. Бромиды с раствором серебра нитрата образуют желтоватый творожистый осадок.
Br− + Ag+ → AgBr↓
Серебра бромид, в отличие от серебра хлорида, не растворяется в растворе аммония карбоната и трудно растворяется в избытке концентрированного раствора аммиака.
AgBr + 2NH3 → [Ag(NH3)2]Br
Серебра бромид растворяется (как и хлориды и йодиды) в растворе натрия тиосульфата.
Бромиды окисляются до свободного галогена легче хлоридов, поэтому их идентифицируют по реакции выделения брома в результате окислительно-восстановительной реакции с хлорамином в кислой среде. Выделяющийся в результате реакции бром извлекают хлороформом, в котором он растворяется лучше, чем в воде, окрашивая его в желто-бурый цвет.
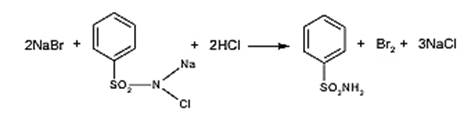
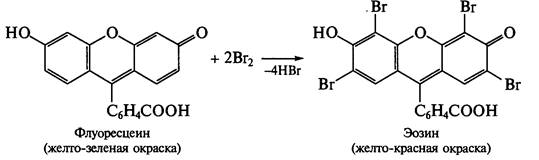
При добавлении к раствору бромида таких сильных окислителей, как соединений свинца (IV) (РbO2) или хрома (VI) (СrO3), в уксуснокислой среде происходит выделение паров брома, который реагирует с флуоресцеином, водно-спиртовым раствором которого пропитана фильтровальная бумага, помещенная над пробиркой с реакционной смесью.
2КВг + РЬO2 + 4СН3СООН → Рb(СН3СОО)2 + 2СН3СООК + Вг2 + 2Н2O
Количественное определение калия и натрия бромидов (как и калия и натрия хлоридов) по ГФ проводят методом прямого аргентометрического титрования по Мору.
1.3.3 Натрия и калия йодиды
Калия и натрия йодиды – бесцветные или белые кристаллические порошки; гигроскопичны, отсыревают на влажном воздухе. Являясь энергичными восстановителями, вступают в реакцию с кислородом воздуха, выделяя при этом йод, вследствие чего порошки и растворы данных лекарственных веществ желтеют при неправильном хранении. Свет, примеси тяжелых металлов, кислород воздуха инициируют процессы окисления йодидов.
ГФ рекомендует для открытия йодидов использовать раствор нитрита натрия или железа (III) хлорида. При определении бромидов и йодидов в качестве окислителей можно использовать также бромат- или йодат-ионы.
5Br- + BrO3- + 6Н+ → 3Вг2 + 3Н2О
Реакционную смесь встряхивают и дают отстояться. Хлороформный слой в случае бромида окрашивается в желтый цвет (Вr2), а в случае йодида – в малиновый (I2).
Общий способ количественного определения йодидов по ГФ – прямая аргентометрия с применением адсорбционного индикатора (метод Фаянса). Сущность метода заключается в том, что адсорбционный индикатор (по ГФ – натрия эозинат) не меняет своего окрашивания (желтовато-красного) до наступления точки эквивалентности. Затем, в точке эквивалентности, индикатор адсорбируется на осадке серебра йодида и цвет осадка становится красно-фиолетовым. Это объясняется тем, что до точки эквивалентности на осадке серебра йодида адсорбируется неоттитрованный йодид-ион (как ион, входящий в состав осадка).
Возникающий на поверхности осадка отрицательный заряд препятствует адсорбции на нем индикатора в виде аниона. После того как йодид будет оттитрован полностью – на поверхности осадка будут адсорбироваться ионы серебра (также входящие в состав осадка). При этом на поверхности осадка возникает вызванный ионами серебра положительный заряд и тогда происходит адсорбция анионов индикатора, вызывающая переход окрашивания осадка. В итоге соединение, находящееся в осадке, примет следующий вид: AgI ⋅ Ag+ ⋅ Ind−.
ПРАКТИЧЕСКАЯ ЧАСТЬ
ОПРЕДЕЛЕНИЕ ГАЛОГЕНИДОВ ПРИ ИХ СОВМЕСТНОМ ПРИСУТСТВИИ В ЛЕКАРСТВЕННЫХ СМЕСЯХ
2.1 Общие принципы анализа лекарственных смесей
Необходимость контроля качества лекарств обусловлена высокими требованиями к их качеству. Как было отмечено в первой главе, контроль качества лекарственных средств осуществляют в соответствии с требованиями нормативной документации (ГФ, ОФС, ФС, ФСП, спецификации).
В Государственной фармакопее РФ важное значение отведено анализу лекарственных форм. Методики качественного и количественного определения лекарственных субстанций изложены в ОФС «Общие реакции на подлинность» и ОФС «Количественное определение лекарственных средств».
Около 30% частных ФС содержат требования к качеству однокомпонентных лекарственных средств.
Количественное определение однокомпонентных лекарственных форм выполняют в несколько этапов: отбор пробы, подготовка к количественному определению, титрование, математическая обработка результатов, причем расчет концентрации лекарственного вещества в однокомпонентной лекарственной форме является наиболее простым (Приложение 3).
Расчет концентрации лекарственного вещества в однокомпонентной лекарственной форме прост и потому, что в частных ФС указаны нижний и верхний пределы содержания лекарственного вещества в граммах на определенное количество лекарственной формы. Для растворов приведены пределы содержания лекарственного вещества в 1 мл; для таблеток в пересчете на среднюю массу или в пересчете на содержание в одной таблетке.
Многокомпонентные лекарственные формы в отличие от однокомпонентных могут содержать два, три и более лекарственных вещества. Для таких лекарственных форм используют также термин «лекарственные смеси». При определении их качества выполняют испытания на подлинность и количественное определение каждого из лекарственных веществ, входящих в состав смеси.
При фармацевтическом исследовании многокомпонентной лекарственной смеси необходимо всесторонне учитывать физические и химические свойства всех входящих компонентов. В этой связи различают два подхода к анализу многокомпонентных лекарственных смесей:
1. Если лекарственные вещества, входящие в состав лекарственной смеси, характеризуются сходными физическими и химическими свойствами, необходимо разделение смеси на составляющие компоненты.
2. Если лекарственные вещества, входящие в состав лекарственной смеси, не обладают близкими физическими и химическими свойствами, что дает возможность их анализа без разделения смеси на составляющие компоненты. Применение химических методов определения основано на особенностях физических и химических свойств ингредиентов, входящих в состав многокомпонентной лекарственной формы, причем чем больше сходство в этих свойствах, тем труднее осуществить определение каждого из компонентов.
2.2 Трудности в определении галогенидов
при их совместном присутствии в лекарственных смесях
Соединения галогенов со щелочными металлами (галогениды) представляют собой лекарственные вещества неорганического происхождения и являются электролитами, поэтому фармацевтический анализ их осуществляют в растворах («мокрым путем»), и определение сводится не к идентификации растворенного вещества в целом, а к определению ионов (катионов или анионов, на которые оно диссоциирует).
Внутриаптечная рецептура лабильна и отличается разнообразием. В отличие от индивидуальных лекарственных средств создать нормативную документацию на каждую, встречающуюся в лечебной практике пропись, невозможно, что вызывает определенные трудности в работе провизора-аналитика.
При разработке схемы анализа лекарственных смесей целесообразно осуществить качественное и количественное определение на каждый ингредиент в отдельности. Однако галогениды характеризуются близкими физическими и химическими свойствами, ввиду чего предложить самостоятельные методы определения на каждый компонент при их совместном присутствии в лекарственной смеси зачастую оказывается невозможным.
Трудности в качественном определении галогенидов при их совместном присутствии в лекарственных смесях состоят в том, что один галогенид мешает обнаружению другого: так, реактив нитрат серебра, используемый как для качественного, так и для количественного определения галогенидов, одновременно реагирует с двумя или более компонентами смеси. Это происходит из-за отсутствия специфических реакций на каждый из галогенидов (аналитическая практика в целом располагает небольшим числом специфических реакций). Отсюда при проведении селективных реакций на галогениды при их совместном присутствии для создания условий, делающих реакцию специфической, предполагается использование одного или нескольких вспомогательных реагентов (например, возможно использование различной растворимости серебряных солей галогенидов в растворе аммиака и других растворителях).
Для качественного определения галогенидов в лекарственных смесях также можно применять и их способность окисляться до свободных галогенов.
Главная трудность количественного определения галогенидов при их совместном присутствии в лекарственных смесях состоит в том, что ГФ не регламентирует методику определения многокомпонентных лекарственных смесей. Для самостоятельного составления схемы количественного определения галогенидов при их совместном присутствии, а также в целях обеспечения точности определения и экономного расходования реактивов, провизору-аналитику необходимо иметь знания о физико-химических свойствах определяемых галогенидов, позволяющих применять сочетание различных титриметрических и физико-химических методов.
Из титриметрических методов для определения галогенидов при их совместном присутствии применяется большинство известных способов титрования. При количественном анализе нужно не только выбрать наиболее точный и удобный метод, исходя из индивидуальных свойств анализируемого галогенида, но и учесть вид лекарственной формы, установить, позволят ли сопутствующие компоненты обеспечить необходимую точность, учесть реакцию среды, наличие других галогенидов, определяемых аналогично, и т.д.
Способы расчета концентрации определяемых галогенидов зависят не только от вида лекарственной формы, но и от величин эквивалентов (особенно при определении по разности), что также создает определенные трудности при совместном определении галогенидов (при титровании разными методами эквиваленты галогенидов меняются).
2.3 Качественное определение галогенидов
при их совместном присутствии в лекарственных смесях
Галогенид-ионы обнаруживают реакцией осаждения раствором азотнокислого серебра. Все галогениды при действии раствора нитрата серебра в присутствии азотной кислоты дают творожистые осадки галогенида серебра белого или желтого цвета, что затрудняет одновременное определение хлоридов, бромидов и йодидов в одной навеске.
Сl- + AgNO3 → AgCl↓ + NO3- (белый осадок)
Br- + AgNO3 → AgBr↓ + NO3- (светло-желтый осадок)
I- + AgNO3 → AgI↓ + NO3- (желтый осадок)
Для качественного определения галогенидов при их совместном присутствии в лекарственной смеси возможно использовать различную растворимость их серебряных солей (1 способ) и различную окислительно-восстановительную активность (2 способ).
1 способ: для качественного определения галогенидов при их совместном присутствии в лекарственных смесях образующиеся осадки можно различить по растворимости в растворе аммиака NH3 или карбоната аммония (NH4)2CO3. Хлорид серебра легко растворяется в разбавленных растворах аммиака и карбоната аммония с образованием комплексных ионов [Ag(NH3)2]+. Бромид серебра не растворим в растворе карбоната аммония, мало растворим в разбавленных растворах аммиака, но легко растворяется в концентрированных растворах аммиака. Йодид серебра AgI не растворим ни в растворах аммиака, ни в растворах карбоната аммония.
Все галогениды серебра (AgCl, AgBr, AgI) не растворимы в азотной кислоте HNO3, но растворимы в растворах натрия тиосульфата Na2S2O3.
AgI↓ + 2Na2S2O3 → Na3[Ag(S2O3)2] + NaI
Так, в прописи 1 для определения хлоридов в присутствии бромидов возможно использование различной растворимости их серебряных солей в растворе аммиака.
ПРОПИСЬ 1 Натрия хлорида
Натрия бромида по 3,0
Воды очищенной 200 мл
Методика определения подлинности
Натрий-ион: графитовую палочку опускают в жидкость и вносят в бесцветное пламя. Пламя окрашивается в желтый цвет.
Хлорид- и бромид-ионы: к 1-2 каплям раствора прибавляют 1-2 капли раствора серебра нитрата. Образуется бело-желтый осадок (хлорид- и бромид-ионы).
NaСl + AgNO3 → AgCl↓ + NaNO3 (белый осадок)
NaBr + AgNO3 → AgBr↓ + NaNO3 (светло-желтый осадок)
Затем добавляют 1-2 капли раствора аммиака и осадок отфильтровывают (в осадке – серебра бромид).
AgCl↓ + 2NH3 → [Ag(NH3)2]Cl
К прозрачному фильтрату добавляют 2-3 капли раствора кислоты азотной разведенной; образуется белый осадок серебра хлорида.
[Ag(NH3)2]Cl + 2HNO3 → AgCl↓ + 2NaNO3
2 способ: для качественного определения галогенидов при их совместном присутствии в лекарственных смесях возможно использовать их различия в окислительно-восстановительных свойствах. Для обнаружения хлоридов, бромидов и йодидов при совместном присутствии целесообразно использовать их способность окисляться до свободных галогенов с различной силой и скоростью.
Чтобы определить каждый из галогенидов, реакцию необходимо проводить поэтапно, поскольку у них разные величины окислительно-восстановительных потенциалов E0.
E0 (Cl2/2Cl−) =1,359 V
E0 (Br2/2Br−) =1,087 V
E0 (I2/2I−) = 0,536 V)
В качестве окислителя возможно использовать калия перманганат KMnO4 (строго определенное количество), который в среде кислоты серной H2SO4 в первую очередь вступает в реакцию с йодидом (наиболее сильным восстановителем среди галогенидов) и окисляет его до свободного йода, окрашивающего хлороформный слой в красно-фиолетовый цвет.
При дальнейшем прибавлении калия перманганата идет более глубокое окисление йода до бесцветного йодат-иона.
I2 + 2KMnO4 + 3H2SO4 → 2HIO3 + K2SO4 + 2MnSO4 + 2H2O
Затем в реакцию вступает бромид-ион, и вследствие образования молекулярного брома хлороформный слой окрашивается в желто-бурый цвет. После полного окисления бромидов избыток калия перманганата KMnO4 разрушают прибавлением по каплям раствора водорода пероксида H2O2.
2KMnO4 + 5H2O2 + 3H2SO4 → 2MnSO4 + K2SO4 + 8H2O + 5O2
Хлорид-ион, как самый слабый восстановитель в ряду галогенидов, в данных условиях не взаимодействует (или не полностью взаимодействует) с калия пермаганатом и может быть обнаружен в водном слое по реакции с серебра нитратом.
ПРОПИСЬ 2 Кальция хлорида 5,0
Калия йодида
Калия бромида по 2,0
Воды очищенной до 100 мл
Методика определения подлинности
Хлорид-, бромид- и йодид- ионы: к 2 каплям раствора лекарственной смеси прибавляют по 10 капель воды и кислоты серной разведенной, 1 каплю 0,1% раствора калия перманганата и встряхивают. Хлороформный слой окрашивается в фиолетовый цвет (йодиды).
10KI + 2KMnO4 + 8H2SO4 → 5I2 + 2MnSO4 + 6K2SO4 + 8H2O
Затем продолжают прибавлять раствор калия перманганата (при встряхивании) до перехода фиолетового окрашивания хлороформного слоя в желто-бурое (бромиды).
10KBr + 2KMnO4 + 8H2SO4 → 5Br2 + 2MnSO4 + 6K2SO4 + 8H2O
После окрашивания водного слоя в устойчивый розовый цвет его сливают в другую пробирку и прибавляют к нему 10 капель хлороформа. Последний не должен окрашиваться. Если же хлороформный слой окрашивается в желтый цвет, добавляют по каплям раствор калия перманганата.
После полного окисления бромидов избыток калия перманганата разрушают прибавлением по каплям раствора водорода пероксида и далее прибавляют 2 капли раствора серебра нитрата. Образуется белый творожистый осадок (хлориды), растворимый при добавлении раствора аммиака.
СaСl2 + 2AgNO3 → 2AgCl↓ + 2NaNO3
AgCl↓ + 2NH3 → [Ag(NH3)2]Cl
2.4 Количественное определение галогенидов
при их совместном присутствии в лекарственных формах
Для количественного определения индивидуальных галогенидов ГФ рекомендует применять титриметрические методы осаждения, связанные с образованием малорастворимых соединений серебра, – методы Мора, Фольгарда, Фаянса, отдавая предпочтение прямым способам титрования. В основе перечисленных методов титрования лежит химическая реакция взаимодействия определяемых веществ с рабочим раствором серебра нитрата:
Сl- + AgNO3 → AgCl↓ + NO3-
Br- + AgNO3 → AgBr↓ + NO3-
I- + AgNO3 → AgI↓ + NO3-
Как было отмечено выше, количественное определение различных галогенидов при их совместном присутствии в лекарственных смесях ГФ не регламентирует. Для определения галогенидов при их совместном присутствии аналитику необходимо применять сочетание титриметрических и физико-химических методов, учитывая индивидуальные свойства анализируемых галогенидов, вид лекарственной формы, реакцию среды, величины эквивалентов.
2.4.1 Определение хлоридов
при их совместном присутствии
В случае совместного присутствия различных галогенидов в лекарственных смесях применение осадительных методов титрования для получения индивидуальных результатов не возможно ввиду одновременной реакции галогенидов с рабочим раствором нитрата серебра (сходство физико-химических свойств затрудняет раздельное определение галогенидов общепринятыми титриметрическими методами).
Таким образом, количественное определение галогенидов при их совместном присутствии в лекарственных смесях без разделения на составляющие компоненты методами осадительного титрования выполнено быть не может, но и разделение смеси не представляется возможным. Как исключение в подобных случаях допускается применять расчет количественного содержания галогенидов через средний ориентировочный титр для определения суммы компонентов.
Средний ориентировочный титр – это масса смеси определяемых веществ в граммах, соответствующая 1 мл титранта. Его величина зависит от значений титриметрических факторов пересчета ингредиентов лекарственной смеси и соотношения этих веществ в ней.
Существует несколько способов расчета среднего ориентировочного титра:
1. Расчет по упрощенной формуле:
![]() (2.7),
(2.7),
где Т1, Т2,…, Тn – титры соответствия определяемых веществ по используемому для количественного определения титрованному раствору, г/мл;
а1, а2, …, аn – содержание входящих в лекарственную форму ингредиентов (по прописи), определяемых по среднему титру, г [20, с. 4].
Средний ориентировочный титр, рассчитанный по формуле (2.7), недостаточно точен и может быть использован для предварительного расчета объема титранта, если им титруется одновременно несколько галогенидов в лекарственной форме.
В том случае, когда средний ориентировочный титр будет использован для расчета результатов титрования смеси галогенидов, которые невозможно оттитровывать раздельно, средний ориентировочный титр нужно рассчитывать по формулам, дающим более точное значение.
2. Расчет по более точным формулам:
![]() (2.8),
(2.8),
![]() (2.9),
(2.9),
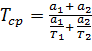 (2.10).
(2.10).
3. Точный и достаточно простой метод расчета среднего ориентировочного титра разработан на базе кафедры фармацевтической химии очного факультета Пермской государственной фармацевтической академии Н.Г. Савельевой (Приложение 4).
Использование в расчетах среднего ориентировочного титра удобно рассмотреть на примере раствора Рингера (пропись 3). Натрия и калия хлориды раздельно определить в данной прописи титриметрическими методиками, принятыми в экспресс-анализе, невозможно (кальция хлорид определяют комплексонометрически).
ПРОПИСЬ 3 Натрия хлорида 0,9
Калия хлорида
Кальция хлорида
Натрия гидрокарбоната по 0,02
Воды для инъекций до 100 мл
Согласно ФС, количественное определение индивидуальных компонентов лекарственной смеси проводят методом аргентометрии по методу Мора. Раздельное количественное определение галогенидов (натрия хлорида, калия хлорида и кальция хлорида) при совместном присутствии их в прописи невозможно (все вещества вступают в реакции осаждения с раствором серебра нитрата).
Количественное определение лекарственной смеси целесообразно начинать с определения содержания суммы галогенидов аргентометрическим методом: титруют навеску лекарственной смеси раствором серебра нитрата AgNO3, индикатор – калия хромат K2Cr2O7:
NaCl + AgNO3 → AgCl ↓ + KNO3
KCl + AgNO3 → AgCl ↓ + KNO3
CaCl2 + 2AgNO3 → 2AgCl ↓ + Ca(NO3)2
2AgNO3 + K2CrO4 → Ag2CrO4 ↓ + 2KNO3
Методика количественного определения
Натрия хлорид, калия хлорид и кальция хлорид: титруют 1 мл раствора 0,1 н. раствором нитрата серебра до оранжево-желтого окрашивания (индикатор – хромат калия).
1 способ: расчет среднего ориентировочного титра по Н.Г. Савельевой.
Навеска лекарственной смеси для количественного определения согласно требований экспресс-анализа составляет 1 мл (а = 1 мл). Если молярная концентрация раствора серебра нитрата 0,1 н., поправочный коэффициент равен 1,00 (К = 1,00), то расчет среднего ориентировочного титра по методике Н.Г. Савельевой будет следующим:
1. Титр по определяемому веществу рассчитывают по формуле (2.2):
![]() г/мл)
г/мл)
![]() г/мл)
г/мл)
![]() г/мл)
г/мл)
2. Содержание каждого галогенида в навеске лекарственной смеси, взятой для определения, составляет:
- для натрия хлорида q1 = 0,009 г;
- для калия хлорида q2 = 0,0002 г;
- для кальция хлорида q3 = 0,0002 г.
3. Сумму определяемых галогенидов, содержащихся в навеске, рассчитывают по формуле (2.11):
∑q = 0,009 + 0,0002 + 0,0002 = 0,0094 (г)
4. Объем титранта, который теоретически израсходуется на титрование каждого галогенида, рассчитывают по формуле (2.12):
![]()
![]()
![]()
5. Рассчитывают сумму объемов по формуле (2.13):
∑V = 1,540 + 0,027 + 0,018 = 1,585 (мл)
6. Отсюда средний ориентировочный титр рассчитывают по формуле (2.14):
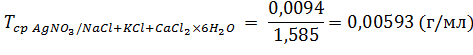
Согласно приведенных расчетов 1 мл 0,1 моль/л раствора нитрата серебра соответствует 0,00593 г суммы натрия хлорида, калия хлорида и кальция хлорида.
Расчет содержания действующих веществ ведут по формуле:
![]()
где 100 – общий объем лекарственной смеси, мл,
1 – навеска раствора, взятая для анализа, мл.
Кальция хлорид: к 10 мл раствора прибавляют 5 мл аммиачного буферного раствора, 0,05 г индикаторной смеси кислотного хром-темно-синего и титруют 0,01 н. раствором трилона Б до сине-фиолетового окрашивания.
Параллельно проводят контрольный опыт.
Титр по определяемому веществу рассчитывают по формуле (2.2):
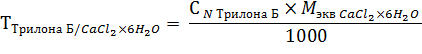
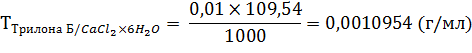
1 мл 0,01 н. раствора трилона Б соответствует 0,0010954 г кальция хлорида.
Содержание кальция хлорида в лекарственной смеси рассчитывают по формуле:
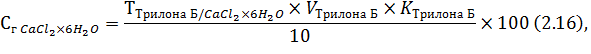
где 10,0 – навеска раствора, взятая для анализа, мл.
Содержание суммы натрия хлорида и калия хлорида находят по разнице содержания суммы хлоридов и содержания кальция хлорида.
2 способ: расчет среднего ориентировочного титра по упрощенной формуле.
Сумму хлоридов натрия и калия можно также рассчитать по упрощенной схеме, согласно которой значение среднего ориентировочного титра 0,1 н. раствора нитрата серебра для суммы натрия хлорида и калия хлорида рассчитывают по формуле (2.10):
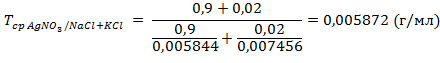
Содержание суммы натрия хлорида и калия хлорида также можно рассчитывать по формуле (при условии равных навесок для определения суммы хлоридов аргентометрическим методом и содержания кальция хлорида комплексонометрическим методом):
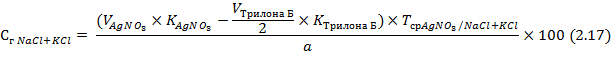
2.4.2 Определение йодидов в сочетании с хлоридами
Для количественного определения различных галогенидов при их совместном присутствии в лекарственных смесях применяется сочетание титриметрических и физико-химических методов.
Для определения йодидов в присутствии хлоридов (если хлориды находятся в виде соли с двухвалентным металлом, например кальция хлорид) можно использовать три метода титрования в различных комбинациях: метод комплексонометрии, методы осаждения и методы окислительно-восстановительного титрования.
На схеме 2.1 (Приложение 5) представлены различные способы количественного определения йодидов в присутствии хлоридов кальция (или других двухвалентных металлов).
Расчет содержания лекарственных веществ проводят по разности (в случае суммарного титрования йодидов и хлоридов), или по формуле прямого титрования (если йодиды и хлориды определяют отдельно).
В экспресс-анализе для количественного определения йодидов и хлоридов часто используют сочетание приведенных в схеме 2.1 титриметрических методов анализа, что можно проиллюстрировать на примере прописи 4.
ПРОПИСЬ 4 Кальция хлорида 3,0
Калия йодида 2,0
Воды очищенной 100,0 мл
1 способ: кальция хлорид определяют трилонометрически, калия йодид – по методу Фаянса с индикатором эозинатом натрия (хлорид-ионы не мешают титрованию с индикатором эозинатом натрия).
Методика количественного определения
Кальция хлорид: к 2 мл раствора прибавляют 5 мл аммиачного буферного раствора, 0,1 г индикаторной смеси кислотного хромтемно-синего и титруют 0,1 н. раствором трилона Б до сине-фиолетового окрашивания.
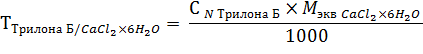
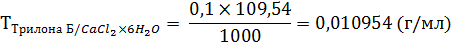
1 мл 0,1 н. раствора трилона Б соответствует 0,01095 г кальция хлорида.
Содержание кальция хлорида в лекарственной смеси рассчитывают по формуле:
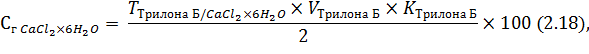
где 2 – навеска раствора, взятая для анализа, мл.
Калия йодид: к 2 мл раствора прибавляют 1 мл разведенной кислоты уксусной, 3-5 капель раствора натрия эозината и титруют 0,1 н. раствором серебра нитрата до ярко-розового окрашивания осадка.
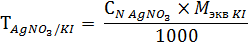
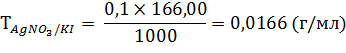
1 мл 0,1 н. раствора серебра нитрата соответствует 0,0166 г калия йодида.
Содержание калия йодида в лекарственной смеси рассчитывают по формуле:
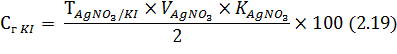
Аргентометрическое титрование йодидов можно проводить с применением внешнего индикатора – нитрозо-крахмальной бумаги.
2 способ: кальция хлорид определяют трилонометрически, а калия йодид – методом аргетометрии с применением внешнего индикатора. Определение конечной точки титрования основано на реакции йодидов с нитритом натрия в кислой среде.
2NaNO2 + 2NaI + 2H2SO4 → I2 + 2NO + 2Na2SO4 + 2H2O
Титрование стандартным раствором серебра нитрата проводят, пока капля реакционной среды, нанесенная на нитрозо-крахмальную бумагу, не будет вызывать ее посинения вследствие выделения йода. Определению йодидов по реакции с натрия нитритом не мешают хлориды и бромиды.
Кроме приведенных вариантов аргентометрического титрования, возможно определять сумму калия йодида и кальция хлорида по методу Фольгарда или Фаянса (с индикатором бромфеноловым синим), а затем содержание калия йодида рассчитывать по разности между объемом титрованного раствора, израсходованным на титрование суммы галогенидов, и объемом трилона Б, пошедшим на титрование кальция хлорида.
KI + AgNO3 → AgI↓ + KNO3
CaCl2 + 2AgNO3 → 2AgCl↓ + Ca(NO3)2
AgNO3(избыток) + NH4CNS → AgCNS↓ + NH4NO3
3NH4CNS + NH4Fe(SO4)2 → Fe(CNS)3 + 2 (NH4)2SO4
Содержание калия йодида в лекарственной смеси рассчитывают по формуле:
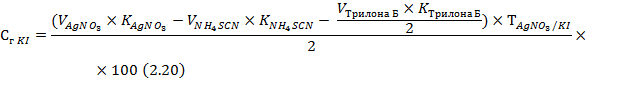
3 способ: йодкрахмальный метод Кольтгофа используют для определения йодидов в присутствии хлоридов и бромидов. В реакционную смесь, содержащую йодиды, прибавляют 1 каплю 0,1 н. раствора калия йодата КIO3, раствор крахмала и раствор серной кислоты разведенной H2SO4. В результате реакции образуется йод, окрашивающий крахмал в синий цвет:
5I- + IO3- + 6 H+ → 3I2 + 3H2O
Окрашивание йодкрахмального комплекса устойчиво лишь в присутствии йодид-ионов. Если их связать серебра нитратом, синяя окраска раствора исчезает.
Способ определения йодидов в присутствии хлоридов йодкрахмальным методом Кольтгофа дает хорошие результаты при титровании йодидов, если концентрация их не превышает концентрацию йодидов более, чем в три раза.
В присутствии бромидов титрование затруднено, а переход окраски от синей через серую до желтой наступает не резко. Поэтому до прибавления раствора кислоты серной к реакционной смеси приливают 5 мл 10% раствора аммония карбоната (NH4)2CO3.
Методика количественного определения
Калия йодид: к 2 мл микстуры прибавляют 10-15 мл воды, 1 каплю 0,1 н. раствора калия йодата, 2 мл свежеприготовленного раствора крахмала и по каплям серную кислоту разведенную до появления синего окрашивания жидкости. Титруют 0,1 н. раствором серебра нитрата до перехода синего окрашивания в желтое.
Расчеты содержания калия йодида и кальция хлорида аналогичны таковым в способе 1.
4 способ: количественное определение обоих компонентов можно провести методом меркуриметрии в одной навеске.
Калия йодид определяют безындикаторным методом Кольтгофа, основанным на растворении оранжевого осадка ртути дийодида HgI2 в избытке калия йодида KI с образованием бесцветного комплекса:
2KI + Hg(NO3)2 → HgI2↓ + 2KNO3
HgI2 + 2 KI → K2[HgI4]
После того как все свободные йодиды перейдут в комплекс тетрайодмеркурата калия K2[HgI4], избыточная капля титрованного раствора ртути (II) нитрата Hg(NO3)2, вступая во взаимодействие с частью комплексного иона, вновь образует нерастворимый оранжевый осадок ртути дийодида HgI2, свидетельствующий о конце титрования:
K2[HgI4] + Hg(NO3)2 → 2HgI2↓ + 2KNO3
При определении без индикатора йодид-ионы взаимодействуют фактически до комплексного соединения K2[HgI4], поэтому число эквивалентности равно ½.
Для определения кальция хлорида к оттитрованной жидкости прибавляют индикатор раствор дифенилкарбазона и титруют стандартным раствором ртути (II) нитрата до фиолетового окрашивания. При этом ртути (II) нитрат сначала разрушает полученное ранее комплексное соединение:
K2[HgI4] + Hg(NO3)2 → 2 HgI2↓ + 2KNO3
Затем взаимодействует с кальция хлоридом:
CaCl2 + Hg(NO3)2 → HgCl2 + Ca(NO3)2
Избыточная капля ртути (II) нитрата реагирует с дифенилкарбазоном, образуя комплекс фиолетового цвета.
Методика количественного определения
Калия йодид: 2 мл раствора титруют 0,1 н. раствором ртути (II) нитрата до появления не исчезающей красно-оранжевой мути.
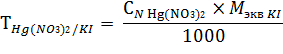
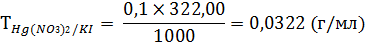
1 мл 0,1 н. раствора ртути (II) нитрата соответствует 0,0332 г калия йодида.
Содержание калия йодида в лекарственной смеси рассчитывают по формуле:
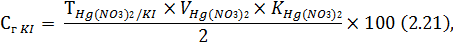
где 2 – навеска раствора, взятая для анализа, мл.
Кальция хлорид: к оттитрованной жидкости прибавляют 5-7 капель
раствора дифенилкарбазона, 1-2 капли раствора кислоты азотной разведенной и титруют 0,1 н. раствором ртути (II) нитрата до фиолетового окрашивания.
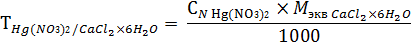
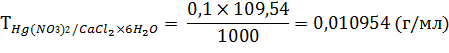
1 мл 0,1 н. раствора ртути (II) нитрата соответствует 0,010954 г кальция хлорида.
Содержание кальция хлорида в лекарственной смеси рассчитывают по формуле:
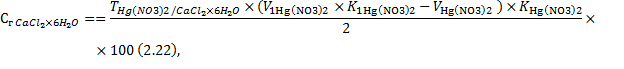
где ![]() – объем 0,1 н. раствора
ртути (II) нитрата, пошедший на титрование калия йодида, мл;
– объем 0,1 н. раствора
ртути (II) нитрата, пошедший на титрование калия йодида, мл;
![]() − объем 0,1 н.
раствора ртути (II) нитрата, пошедший на титрование суммы калия йодида и
кальция хлорида, мл.
− объем 0,1 н.
раствора ртути (II) нитрата, пошедший на титрование суммы калия йодида и
кальция хлорида, мл.
5 способ: кальция хлорид определяют трилонометрически, а калия
йодид – йодкрахмальным методом (с применением в качестве титрованного
раствора ртути (II) нитрата). Механизм реакции аналогичен титрованию йодидов по методу Кольтгофа с применением в качестве титранта раствора серебра нитрата. Точку эквивалентности устанавливают по исчезновению окраски йодкрахмального комплекса, синяя окраска которого изменяется через буроватую до чистой розовато-оранжевой:
5I− + IO3− + 6H+ → 3I2 + 3H2O
2KI + Hg(NO3)2 → HgI2↓ + 2KNO3
I2 + Hg(NO3)2 + H2O → HgI2↓ + 2HNO3
Методика количественного определения
Калия йодид: к 2 мл раствора прибавляют 2 мл воды, 1 каплю 0,1 н. раствора калия йодата, 0,5 мл раствора крахмала растворимого, по каплям серную кислоту разведенную до появления устойчивого синего окрашивания и титруют 0,1 н. раствором ртути (II) нитрата до перехода синего окрашивания (через бурое) в яркое розово-оранжевое.
1 мл 0,1 н. раствора ртути (II) нитрата соответствует 0,01660 г калия йодида.
Расчет содержания калия йодида аналогичен таковому в способе 4, кальция хлорида – в способе 1.
6 способ: кальция хлорид определяют трилонометрически, калия йодид – методом йодатометрии. Йодид-ионы окисляются калия йодатом KIO3 в среде кислоты хлористоводородной HCl до йода:
KIO3 + 5KI + 6HCl → 3I2 + 6 KCl + 3H2О
Затем выделившийся йод титруют до йодмонохлорида:
KIO3 + 2I2 + 6HCl → 5ICl + KCl + 3H2O
В расчетах число эквивалентности равно 3.
Методика количественного определения
Калия йодид: к 1 мл раствора добавляют 5 мл раствора кислоты хлористоводородной 1:1, 1 мл раствора крахмала растворимого и быстро титруют 0,1 н. раствором калия йодата до появления светло бурой окраски. Затем титрование проводят медленно, по каплям, до перехода окраски в лимонно-желтую.
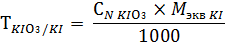
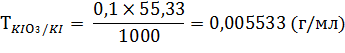
1 мл 0,1 н. раствора калия йодата соответствует 0,005533 г калия йодида.
Содержание калия йодида в лекарственной смеси рассчитывают по формуле:
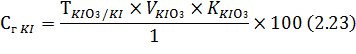
Расчет содержания кальция хлорида аналогичен таковому в способе 1.
7 способ: кальция хлорид определяют трилонометрически, калия йодид – броматометрически. Йодид-ионы окисляются калия броматом KBrO3 в среде кислоты хлористоводородной HCl до йодмонохлорида ICl:
KBrO3 + 3KI + 6HCl → 3ICl + KBr + 3KCl + 3H2O
Число эквивалентности равно 2.
Методика количественного определения
Калия йодид: к 1 мл раствора прибавляют 5 мл раствора кислоты хлористоводородной 1:1, 1 мл раствора крахмала и титруют 0,1 н. раствором калия бромата KBrO3 до перехода бурой окраски раствора в лимонно-желтую.
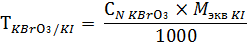
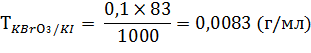
1 мл 0,1 н. раствора калия бромата соответствует 0,0083 г калия йодида.
Содержание калия йодида в лекарственной смеси рассчитывают по формуле:
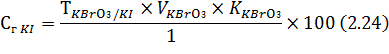
Расчет содержания кальция хлорида аналогичен таковому в способе 1.
8 способ: кальция хлорид определяют трилонометрически, калия йодид – методом перманганатометрии. Йодид-ионы окисляются калия перманганатом KMnO4 в среде кислоты хлористоводородной разведенной:
2KMnO4 + 5 KI + 16HCl → 5ICl + 7KCl + 2MnCl2 + 8HCl
Число эквивалентности равно 2.
Методика количественного определения
Калия йодид: к 1 мл микстуры прибавляют 5 мл раствора кислоты хлористоводородной 1:1 и титруют 0,1 н. раствором калия перманганата до появления светло-бурой окраски раствора. Затем прибавляют 1 мл раствора крахмала растворимого и снова титруют по каплям до перехода окраски в лимонно-желтую.
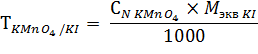
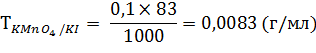
1 мл 0,1 н. раствора калия перманганата соответствует 0,0083 г калия йодида.
Содержание калия йодида в лекарственной смеси рассчитывают по формуле:
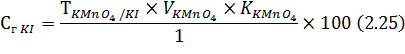
Расчет содержания кальция хлорида аналогичен таковому в способе 1.
Определение йодидов в присутствии хлоридов возможно осуществлять с использованием метода рефрактометрии. Вначале проводят трилонометрическое определение кальция хлорида шестиводного, а затем определяют показатель преломления лекарственной смеси относительно воды.
2.4.3 Определение бромидов в сочетании с хлоридами
Для количественного определения бромидов в сочетании с хлоридами в виде солей одновалентных металлов бромид-ионы окисляют калия перманганатом KMnO4 до свободного брома Br2:
10NaBr + 2KMnO4 + 8H2SO4 →
→ 5Br2 + 5Na2SO4 + K2SO4 + 2MnSO4 + 8H2O
Выделившийся бром далее удаляют путем превращения его в пентабромацетон:
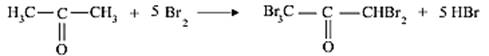
После этого в растворе остаются только хлорид-ионы, которые определяют по методу Фольгарда (пропись 5).
Для определения бромидов сумму галогенидов титруют по методу Мора, а далее определяют меркуриметрически.
ПРОПИСЬ 5 Натрия бромида
Натрия хлорида по 3,0
Воды очищенной до 100,0 мл
1 способ: определение натрия хлорида проводят после окисления бромид-ионов калия перманганатом KMnO4 и переведения образовавшегося брома Br2 в связанное состояние. Избыток калия перманганата удаляют водорода пероксидом H2O2 и проводят определение натрия хлорида по обратному методу Фольгарда, а сумму натрия хлорида и натрия бромида определяют аргентометрически по методу Мора.
Методика количественного определения
Натрия хлорид, натрия бромид: титруют 1 мл раствора 0,1 н. раствором серебра нитрата до оранжево-желтого окрашивания (индикатор – хромат калия).
Натрия хлорид: к 1 мл раствора прибавляют 3-5 мл воды, по 3 мл серной кислоты разведенной и ацетона и по каплям 5% раствор калия перманганата до устойчивого в течение 10 минут розового окрашивания.
Через 10 минут избыток калия перманганата удаляют осторожным прибавлением по каплям 3% раствора водорода пероксида:
5H2O2 + 2KMnO4 + 3H2SO4 → 2MnSO4 + K2SO4 + 8H2O + 5O2↑
К обесцвеченному раствору прибавляют 10 мл 0,1 н. серебра нитрата, 15-20 капель раствора квасцов железоаммониевых и титруют 0,1 н. раствором аммония роданида до буровато-оранжевого окрашивания раствора над осадком.
NaCl + AgNO3 → AgCl↓ + NaNO3
AgNO3 + NH4SCN → AgSCN + NH4NO3
3NH4SCN + Fe(NH4)(SO4)2 → Fe(SCN)3 + 2(NH4)2SO4
Титр
серебра нитрата по натрия хлориду (![]() ) рассчитан в п.п. 2.4.1.
) рассчитан в п.п. 2.4.1.
1 мл 0,1 н. раствора серебра нитрата соответствует 0,00585 г натрия хлорида.
Содержание натрия хлорида в лекарственной смеси рассчитывают по формуле:
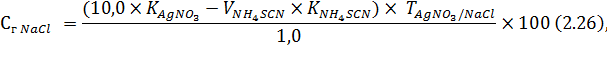
где 10 – объем избыточного раствора серебра нитрата, мл.
Содержание натрия бромида возможно находить по разности суммы натрия хлорида и натрия бромида и содержания натрия хлорида, а также воспользовавшись формулой:
![]()
где ![]() – объем 0,1 н. раствора
серебра нитрата, пошедшего на титрование суммы галогенидов, мл.
– объем 0,1 н. раствора
серебра нитрата, пошедшего на титрование суммы галогенидов, мл.
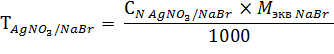
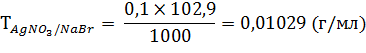
1 мл 0,1 н. раствора серебра нитрата соответствует 0,01029 г натрия бромида.
2 способ: натрия хлорид определяют по методу Фольгарда после предварительного окисления бромид-ионов, а сумму натрия хлорида и натрия бромида определяют меркуриметрически.
Методика количественного определения
Натрия хлорид, натрия бромид: к 1 мл микстуры прибавляют 5-8 капель раствора дифенилкарбазона, 1-2 капли кислоты азотной разведенной и титруют 0,1 н. раствором ртути (II) нитрата до фиолетового окрашивания.
Натрия хлорид: аналогично способу 1.
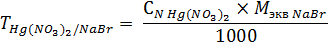
![]() г/мл)
г/мл)
1 мл 0,1 н. раствора ртути (II) нитрата соответствует 0,01029 г натрия бромида.
Содержание натрия бромида возможно находить по формуле [8, с. 31]:
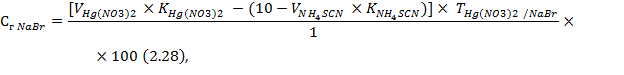
где ![]() – объем 0,1 н. раствора
серебра нитрата, пошедшего на титрование суммы галогенидов, мл.
– объем 0,1 н. раствора
серебра нитрата, пошедшего на титрование суммы галогенидов, мл.
2.4.4 Определение хлоридов, бромидов, йодидов
при их совместном присутствии
Более сложной задачей является анализ лекарственных смесей, содержащих одновременно йодид-, бромид- и хлорид-ионы. Часто в лекарственных смесях содержатся йоды и бромиды в виде солей одновалентных металлов, а хлориды – в виде солей двухвалентных металлов.
Для количественного определения их возможно сочетание методов осаждения и окислительно-восстановительных методов, представленных на схеме 2.2 (Приложение 6).
Более простым вариантом количественного определения из рассмотренных в схеме 2.2 является метод, основанный на различии окислительно-восстановительных свойств йодидов и бромидов (пропись 5).
Йодид как более сильный восстановитель окисляется стандартным раствором натрия нитрита NaNO2 (заместительное титрование с добавлением избытка титранта) до свободного йода I2.
2KI + 2NaNO2 + 4HCl → 2NaCl + 2KCl + I2 + 2H2O + 2NO
Избыток натрия нитрита удаляют с помощью мочевины H2N−CO−NH2 .
2NaNO2 + H2N−CO−NH2 + 2HCl → 2NaCl + 2N2 + CO2 + 3H2O
Выделившийся в эквивалентном количестве йод оттитровывают стандартным раствором натрия тиосульфата.
I2 + 2Na2S2O3 → 2NaI + Na2S4O6
ПРОПИСЬ 6 Калия йодида
Калия бромида по 2,0
Раствора кальция хлорида из 10,0 – 200,0 мл
Количественное определение основывается на сочетании рефрактометрии с титриметрическими методами анализа: кальция хлорид определяют методом трилонометрии, калия бромид – рефрактометрически. Калия йодид определяют методом йодометрии по способу заместительного титрования.
Методика количественного определения
Калия йодид: к 1 мл раствора прибавляют 5-6 капель кислоты серной разведенной, 0,04 г мочевины и медленно по каплям при частом перемешиваними 2 мл 0,05 н. раствора натрия нитрита и оставляют на 5-10 минут в темном месте в закрытой колбе для выделения молекулярного йода. Затем прибавляют 0,1 г калия йодида для растворения выделившегося йода и титруют 0,1 н. раствором натрия тиосульфата до полного обесцвечивания раствора. Возможно титрование в присутствии индикатора – крахмала. Его добавляют в конце титрования (когда раствор приобретает светло-желтую окраску) в количестве 2-3 капель. Раствор окрашивается в синий цвет (комплексное соединение крахмала с йодом), его дотитровывают до исчезновения синей окраски.
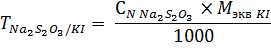
![]() г/мл)
г/мл)
1 мл 0,1 н. раствора натрия тиосульфата соответствует 0,0166 г калия йодида.
Содержание калия йодида в лекарственной смеси рассчитывают по формуле:
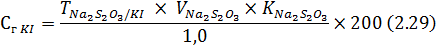
Кальция хлорид: 1 мл раствора помещают в мерный цилиндр емкостью
10 мл и объем доводят водой до метки. К 2 мл полученного раствора прибавляют 2 мл аммиачного буферного раствора, 0,02 г индикатора кислотного хром темно-синего и титруют 0,1 н. раствором трилона Б до сине-
фиолетового окрашивания.
Титр трилона Б по кальция хлориду (![]() ) рассчитан в п.п. 2.4.2.
) рассчитан в п.п. 2.4.2.
1 мл 0,1 н. раствора трилона Б соответствует 0,01095 г кальция хлорида.
Содержание кальция хлорида в лекарственной смеси рассчитывают по формуле (2.4):
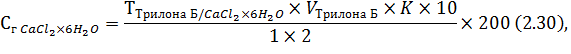
где 10 – общий объем разведения, мл;
2 – аликвота (часть разведения), взятая для анализа.
Калия бромид: определяют рефрактометрически.
Расчет содержания калия бромида осуществлять по формуле 2.6 нельзя ввиду присутствия калия йодида и кальция хлорида в лекарственной смеси.
Количественное содержание компонента, определяемое рефрактометрически, находят по формуле:
![]()
где n – показатель преломления испытуемого раствора;
С1, С2, Сn – концентрации веществ (%), найденных титриметрическими методами;
F1, F2, Fn – факторы показателей преломления растворов веществ, определяемых титриметрическими методами;
F – фактор показателя преломления вещества, определяемого рефрактометрическим методом.
Содержание калия бромида в рассматриваемой лекарственной смеси рассчитывают по формуле:
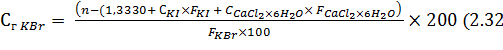 )
)
Фактор показателя преломления для всех концентраций раствора калия йодида равен 0,00130, для 5 % раствора кальция хлорида – 0,00117, для 1 % раствора калия бромида – 0,00120.
Для определения значений факторов показателей преломления растворов галогенидов одно- и двухвалентных металлов различных концентраций используют рефрактометрические таблицы (Приложение 7). При необходимости следует пользоваться интерполированием данных.
Вопросы для тестового контроля
1. По внешнему виду галогениды щелочных металлов представляют собой
1) белые кристаллические порошки с желтоватым оттенком
2) белые кристаллические порошки
3) белые аморфные порошки
2. В этаноле легко растворимы
1) йодиды
2) бромиды
3) хлориды
3. Йодиды легко растворимы в
1) воде
2) этаноле
3) глицерине
4) хлороформе
4.Катион натрия обнаруживают по
1) окрашиванию пламени
2) по реакции с пикриновой кислотой
3) по реакции с винной кислотой
5. Катион калия обнаруживают по
1) окрашиванию пламени
2) по реакции с пикриновой кислотой
3) по реакции с винной кислотой
4) по реакции с натрия гексанитрокобальтатом
6. Галогенид – ион можно обнаружить с раствором серебра нитрата в средах
1) щелочной
2) азотнокислой
3) аммиачно-буферной
7. Образующиеся осадки при взаимодействии солей галогеноводородных кислот с раствором серебра нитрата можно отличить друг от друга
1) по внешнему виду
2) по растворимости в азотной кислоте
3) по растворимости в растворе аммиака
4) по растворимости в растворе натрия тиосульфата
8. Из приведенных свойств выберите те, которые характерны для осадка серебра йодида
1) творожистый осадок белого цвета
2) мелкокристаллический белого цвета
3) растворим в 25% растворе аммиака
4) творожистый осадок желтого цвета
9. Окисление натрия и калия бромидов проводят в кислой среде в присутствии следующих окислителей
1) калия перманганата
2) хлорамина
3) калия бромата
4) натрия нитрита
10. Окисление натрия и калия йодидов проводят в кислой среде в присутствии
1) натрия нитрита
2) натрия бромида
3) калия йодата
4) калия бромата
11. При окислении бромидов хлорамином в кислой среде добавляют хлороформ с целью
1) как катализатор
2) для поддержания pН раствора
3) для извлечения выделившегося галогена
12. При количественном аргентометрическом методе определения натрия бромида в азотнокислой среде в качестве индикатора используют
1) эозинат натрия
2) хромат калия
3) железоаммониевые квасцы
4) бромфеноловый синий
13. При количественном аргентометрическом методе определения натрия хлорида в нейтральной среде в качестве индикатора используют
1) эозинат натрия
2) хромат калия
3) бромфеноловый синий
4) железоаммониевые квасцы
14. Возможные методы количественного определения калия бромида в кислой среде
1) Фаянса
2) Мора
3) Фольгарда
4) меркуриметрический
15. Возможные методы количественного определения калия йодида в нейтральной среде
1) меркуриметрический
2) Мора
3) Фольгарда
4) Фаянса
16. Условия меркуриметрического метода определения натрия хлорида
1) нейтральная среда
2) индикатор дифенилкарбазид
3) кислая среда
4) температура реагирующей смеси не выше +50 С
17. Метод Мора используется для количественного определения
1) только хлоридов
2) всех галогенидов
3) хлоридов и бромидов
4) только йодидов
18. Возможные методы количественного определения натрия йодида
1) метод Мора
2) метод Фаянса
3) метод Фольгарда
4) меркуриметрический
19. Меркуриметрическое определение хлоридов и бромидов осуществимо в средах
1) нейтральной
2) кислой
3) щелочной
4) аммиачно-буферной
20. При хранении во влажном воздухе меньшей гигроскопичностью отличаются
1) калия бромид
2) калия йодид
3) натрия бромид
22. Натрия хлорид хранят
1) в сухом месте в плотно укупоренных банках
2) в сухом месте в банках оранжевого стекла
3) в защищенном от света месте
23. Калия йодид хранят
1) в сухом месте в плотно укупоренных банках
2) в сухом месте в плотно укупоренных банках оранжевого стекла
3) в защищенном от света месте
24. Натрия хлорид применяется в медицине в виде
1) гипертонических растворов
2) изотонических растворов
3) седативного средства
4) при гипертиреозе
25. Натрия йодид применяется в медицине в виде
1) антиаритмического средства
2) изотонических растворов
3) седативного средства
4) при гипертиреозе
Контрольные вопросы
1. Какие трудности возникают в качественном определении галогенидов при их совместном присутствии в лекарственных формах?
2. Какие трудности возникают при количественном определения галогенидов при их совместном присутствии в лекарственных формах?
3. В каких случаях следует применять расчет среднего ориентировочного титра для определения содержания галогенидов в лекарственных формах?
4. В каких случаях совместного присутствия различных галогенидов в лекарственных формах их можно анализировать без разделения?
5. Приведите приемы, применяемые в фармацевтическом анализе для определения лекарственных смесей, содержащих одновременно йодиды, бромиды и хлориды.
Ситуационные задачи
1. Составьте схему определения и приведите методики определения галогенидов при совместном присутствии в лекарственных формах:
Пропись 1
Натрия тиосульфата 0,1
Кальция хлорида 0,3
Натрия хлорида 5,0
Воды для инъекций до 100 мл
Пропись 2
Калия хлорида 0,02
Кальция хлорида 0,02
Натрия хлорида 0,9
Глюкозы (в пересчете на б/в) 1,0 г
Раствора кислоты
хлористоводородной 0,1 М 0,5 мл
Воды для инъекций до 100 мл
Пропись 3
Натрия уксуснокислого 3,6
Натрия хлорида 4,75
Калия хлорида 1,5
Воды для инъекций до 1 л
Пропись 4
Натрия гидрокарбоната 4,0
Натрия хлорида 5,0
Калия хлорида 1,0
Воды для инъекций до 1 л
Пропись 5
Натрия хлорида 0,9
Натрия гидрокарбоната 0,02
Кальция хлорида 0,02
Калия хлорида 0,02
Воды для инъекций до 100 мл
2. Рассчитайте интервал объемов 0,1 н. раствора серебра нитрата (К = 1,0200), который обеспечит качество препарата по содержанию калия и натрия хлорида, если на анализ взяли 2,0 мл раствора следующего состава:
Натрия хлорида 0,35
Калия хлорида 0,15
Натрия гидрокарбоната 0,25
Глюкозы 2,0
Воды для инъекций до 100 мл
3. Рассчитайте примерный объем 0,1 моль/л раствора серебра нитрата (К= 0,9800), который пойдет на титрование 1,0 мл раствора Рингера:
Натрия хлорида 0,9
Калия хлорида 0,02
Кальция хлорида 0,02
Воды для инъекций до 100 мл
4. Рассчитайте содержание натрия хлорида, калия хлорида и кальция хлорида в растворе Рингера, если на суммарное титрование хлоридов натрия, калия, кальция в 1,0 мл лекарственной формы израсходовано 1,55 мл 0,1 н. раствора серебра нитрата с К= 1,0200, а на титрование кальция хлорида в 10,0 мл лекарственной формы – 0,95 мл 0,01 моль/л раствора трилона Б с К=0,9900.
5. Практическое задание на занятие: студент получая задание – анализ многокомпонентной лекарственной смеси, содержащей галогениды, должен:
- провести реакции подлинности;
- рассчитать содержание ингредиентов в лекарственной форме с использованием формул расчета;
- оформить отчетную документацию по форме (Приложение 8).
СПИСОК ЛИТЕРАТУРЫ
1. Федеральный закон МЗ РФ № 61 от 12.04.2010 г. «Об обращении лекарственных средств».
2. Приказ Министерства здравоохранения РФ от 22 мая 2023 г. № 249н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, имеющими лицензию на фармацевтическую деятельность».
3. Государственная фармакопея Российской федерации. ХIV издание. – М.: «Научный центр экспертизы средств медицинского применения», 2008;
4. Арзамасцев А.П. Анализ лекарственных смесей: учебное пособие для студ. фарм. ин-тов и фарм. фак. мед. ВУЗов / А.П. Арзамасцев и др. – М.: Компания Спутник, 2000.
5. Арзамасцев А.П. Фармацевтическая химия: учеб. пособие. – 3-е изд., испр. – М.: ГЭОТАР-Медиа, 2006.
6. Беликов В.Г. Лабораторные работы по фармацевтической химии: учебное пособие / В.Г. Беликов и др. – Пятигорск, 2003.
7. Беликов В.Г. Фармацевтическая химия. В 2 частях. Часть 1. Общая фармацевтическая химия: Учебник для фарм. ин-тов и фак. мед. ин-тов. – М.: Высшая школа, 2003.
8. Глущенко Н.Н. Фармацевтическая химия: Учебник для студ. сред. проф. учеб. заведений / Н.Н. Глущенко, Т.В. Плетенева, В.А. Попков. Под ред. Т.В. Плетеневой. – М.: Издательский центр «Академия», 2004.
9. Илларионова Е.А. Фармакопейный анализ неорганической лекарственных веществ: учебное пособие / Илларионова Е.А., Сыроватский И.П. – Иркутск, 2009.
10. Мельникова Н.Б. Фармакопейный анализ неорганических лекарственных веществ: Методические рекомендации к лабораторно-практическим занятиям / Мельникова Н.Б., Саликова Т.В., Гаврилова С.А., Жильцова О. Е. – Нижний Новгород: ГОУ ВПО «Нижегородская государственная медицинская академия», 2009.
11. Саенко О.Е. Аналитическая химия: учебник для средних специальных учебных заведений/ О.Е. Саенко. – Изд. 2-е, доп. и перераб. – Ростов-на-Дону: Феникс, 2011.
12. Сливкин А.И. Контроль качества экстемпоральных лекарственных форм: Учебное пособие / Сливкин А.И., Садчикова Н.П. – Воронеж: Изд-во Воронежского государственного университета, 2003.
13. Контроль качества лекарственных средств, изготовляемых в аптеках. Средний титр в анализе лекарственных препаратов. Учебно-методическое пособие для студентов фармацевтического факультета ГОУ ВПО «Нижегородская государственная медицинская академия» - Нижний Новгород, 2008 г.
14. Титриметрические методы в фармацевтическом анализе: практикум для студентов по специальности «Фармация» / О.Ф. Стоянова, И.В. Шкутина, В.Ф. Селеменев, М.В. Рожкова. – Воронеж: типография Воронежского государственного университета, 2005.
15. Фармацевтическая химия: руководство к практическим занятиям для студентов обучающихся по специальности «Фармация» / Е.С. Гагарина, А.В. Озерская, Н.В. Кувачева и др. – Красноярск: типография КрасГМУ, 2009.
Приложение 1
Таблица 1.1. Физико-химические свойства
хлоридов, бромидов, йодидов натрия и калия
|
Лекарственное вещество |
Химическая формула |
Описание |
|
Natrii chloridum Натрия хлорид |
NaCl |
Белые кубические кристаллы или белый кристаллический порошок запаха, соленого вкуса. |
|
Kalii chloridum Калия хлорид |
KCl |
Бесцветные кристаллы или белый кристаллический порошок без вкуса, без запаха, соленого вкуса. |
|
Natrii bromidum Натрия бромид |
NaBr |
Белый кристаллический порошок без запаха, соленого вкуса. Гигроскопичен. |
|
Kalii bromidum Калия бромид |
KBr |
Бесцветные или белые кристаллы или мелкокристаллический порошок без запаха, соленого вкуса. |
|
Natrii iodidum Натрия йодид |
NaI |
Белый кристаллический порошок без запаха, соленого вкуса. Гигроскопичен. |
|
Kalii iodidum Калия йодид |
KI |
Бесцветные или белые кубические кристаллы или белый мелкокристаллический порошок без запаха, солено-горького вкуса. Гигроскопичен. |
Приложение 2
Таблица 1.2. Труднорастворимые соли галогенидов серебра
|
Галогениды |
Цвет осадка |
Произведение растворимости |
Растворимость в растворе аммиака |
|
AgCl |
Белый |
1,8 · 10-10 |
Растворим |
|
AgBr |
Светло-желтый |
5,3 · 10-13 |
Мало растворим |
|
AgI |
Желтый |
8,3 · 10-17 |
Нерастворим |
Приложение 3
Формулы расчета концентрации лекарственного вещества
в однокомпонентной лекарственной форме
1. При прямом титровании концентрацию индивидуального лекарственного вещества в процентах рассчитывают по формуле:
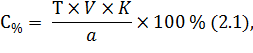
где С% – концентрация определяемого вещества, %;
V – объем титранта, пошедшего на титрование данного ингредиента, мл;
К – поправочный коэффициент титрованного раствора;
а – навеска анализируемого лекарственного вещества или лекарственной смеси, г [3, с. 29].
Титр по определяемому веществу рассчитывают по формуле:
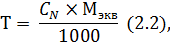
где CN – нормальная концентрация титранта, моль экв/л;
М экв. – молярная масса эквивалента определяемого вещества, г/моль [4].
2. При обратном титровании концентрацию в процентах рассчитывают по формуле:
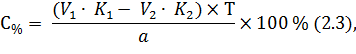
где V1 – объем первого титранта, взятого в избытке, мл;
К1 – коэффициент поправки на первый титрованный раствор;
V2 – объем второго титранта, затраченного на титрование избытка первого титрованного раствора, мл;
К2 – коэффициент поправки на второй титрованный раствор [3, с. 31].
Если при количественном определении предварительно делали разведение и для титрования использовали часть полученного разведения (аликвоту А), то концентрацию определяемого вещества при прямом титровании рассчитывают по формуле:
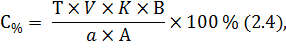
где В – объем мерной колбы, мл;
А – объем разведенного раствора, отобранный для титрования (аликвота), мл [4].
При необходимости выразить содержание анализируемого вещества в граммах, в числитель вместо цифры 100 подставляют величину общей массы (в г) или объема (в мл) лекарственной формы [5].
В случае определения содержания действующего вещества методом рефрактометрии используют расчет концентрации вещества в растворе по измеренному показателю преломления [4]:
![]() ,
,
где n и n0 – показатели преломления раствора и растворителя;
С% – концентрация вещества в растворе;
F – фактор показателя преломления (величина табличная) [4].
Содержание вещества в граммах рассчитывают по формуле:
![]() (2.6).
(2.6).
Приложение 4
Принцип расчета среднего ориентировочного титра по Н.Г. Савельевой
1. Рассчитывают содержание каждого компонента (галогенида) в навеске лекарственной смеси, взятой для определения в г (q1, q2, qх). При расчете можно исходить из любой навески в граммах или любого объема (мл).
2. Рассчитывают сумму определяемых компонентов (галогенидов) (∑q), содержащихся в навеске (г):
∑q = q1 + q2 + qх (2.11).
3. Рассчитывают объем титранта, который теоретически израсходуется на титрование каждого компонента (галогенида) (мл):
![]() ;
;
![]() ;
;
![]() (2.12).
(2.12).
Объемы рассчитывают с точностью до третьего знака после запятой, после чего третий знак округляется.
4. Рассчитывают сумму теоретических объемов титрантов (∑V), расходуемых на титрование каждого компонента (галогенида) (мл):
∑V = V1 + V2 + Vх (2.13).
5. Рассчитывают средний ориентировочный титр Тср:
![]() (2.14)
(2.14)
Приложение 5
Схема 2.1. Способы определения йодидов
в присутствии хлоридов в лекарственных смесях
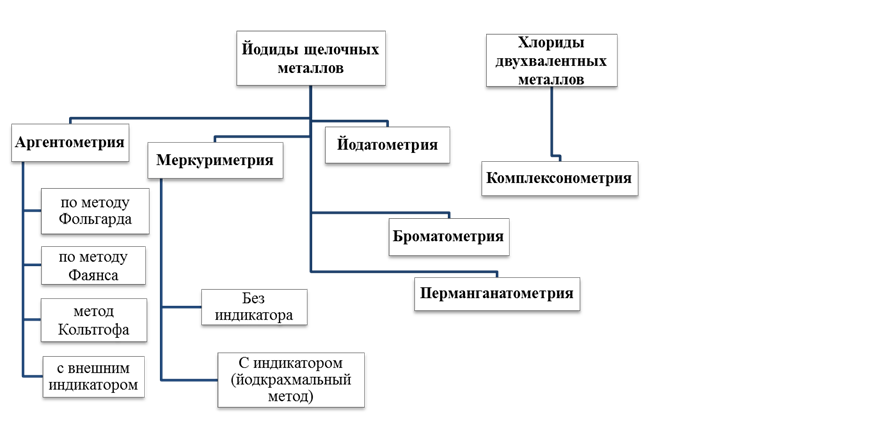
Приложение 6
Схема 2.2. Способы определения хлоридов, бромидов, йодидов
при их совместном присутствии в лекарственных смесях
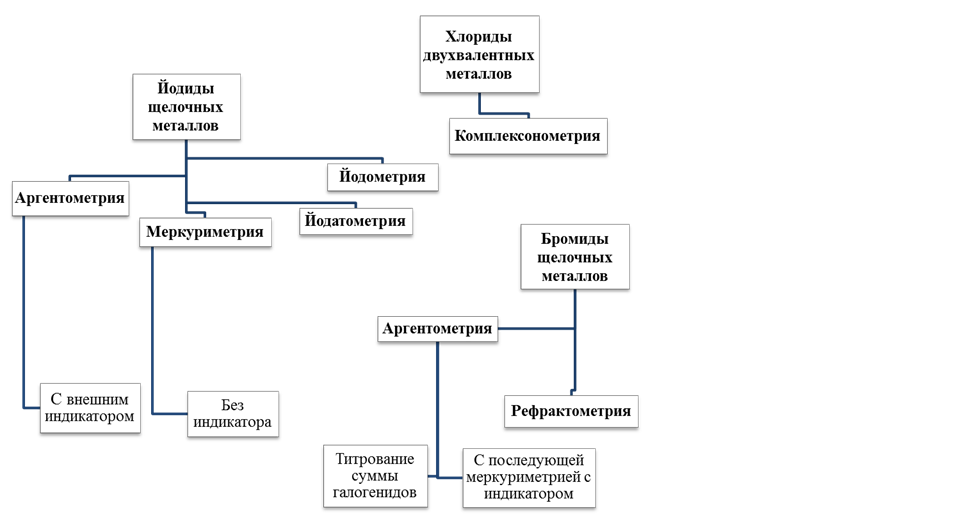
Приложение 7
Таблица 2.1. Факторы показателя преломления галогенидов
|
Натрия хлорид |
Натрия бромид |
Натрия йодид |
|||
|
Концентра-ция, % |
Показатель преломления |
Концентра-ция |
Показатель преломления |
Концентра-ция |
Показатель преломления |
|
1 |
0,00170 |
1 |
0,00131 |
1 |
Для всех концентраций 0,00143 |
|
5 |
0,00167 |
5 |
0,00133 |
5 |
|
|
10 |
0,00164 |
10 |
0,00132 |
10 |
|
|
15 |
0,00160 |
15 |
0,00131 |
15 |
|
|
20 |
0,00157 |
20 |
0,00130 |
20 |
|
|
Калия бромид |
Калия йодид |
Кальция хлорид |
|||
|
1 |
0,00120 |
1 |
Для всех концентраций 0,00130 |
1 |
0,00118 |
|
5 |
0,00119 |
5 |
5 |
0,00117 |
|
|
10 |
0,00118 |
10 |
10 |
0,00116 |
|
|
15 |
0,00117 |
15 |
15 |
0,00115 |
|
|
20 |
0,00116 |
20 |
20 |
0,00114 |
|
|
|
|
|
|
25 |
0,00113 |
Приложение 8
ПРОТОКОЛ АНАЛИЗА ЛЕКАРСТВЕННОЙ ФОРМЫ, ИЗГОТОВЛЕННОЙ ПО ИНДИВИДУАЛЬНОМУ РЕЦЕПТУ
№ ______ от ______________________
|
РЕЦЕПТ: |
|
|
|
Виды ВАК: |
|
|
|
Испытания проведены по НД: |
|
|
|
Упаковка: |
|||
|
Требование: |
Результат испытания: |
||
|
Заключение: |
Соответствует требованиям НД/ не соответствует требованиям НД |
||
|
Маркировка: |
|||
|
Требование: |
Результат испытания: |
||
|
Заключение: |
Соответствует требованиям НД/ не соответствует требованиям НД |
||
|
Описание: |
|||
|
Требование:
|
Результат испытания: |
||
|
Заключение: |
Соответствует требованиям НД/ не соответствует требованиям НД |
||
|
Определение подлинности: |
|||
|
Компонент 1 |
|||
|
Химическое название |
|
||
|
Химическая формула |
|
||
|
М.м. |
|
||
|
Компонент 2 |
|||
|
Химическое название |
|
||
|
Химическая формула |
|
||
|
М.м. |
|
||
|
Определение подлинности: |
|||
|
Компонет 1 |
|||
|
Реакция 1. |
|||
|
Методика, уравнение химической реакции:
|
Результат испытания: |
||
|
Реакция 2. |
|||
|
Методика, уравнение химической реакции:
|
Результат испытания: |
||
|
Компонент 2 |
|||
|
Реакция 1 |
|||
|
Методика, уравнение химической реакции:
|
Результат испытания: |
||
|
Реакция 2 |
|||
|
Методика, уравнение химической реакции:
|
Результат испытания: |
||
|
Заключение: |
Соответствует требованиям НД/ не соответствует требованиям НД |
||
|
Количественное определение: |
|||
|
Компонент 1 |
|||
|
Методика, уравнения химических реакций:
|
Расчеты, результат испытания: |
||
|
Компонент 2 |
|||
|
Методика, уравнения химических реакций:
|
Расчеты, результат испытания: |
||
|
Условия и сроки хранения: |
|||
|
|
|||
|
Заключение: лекарственная форма удовлетворяет/ не удовлетворяет требованиям НД. |
|||
|
Анализ провел: _____________________________________ |
Дата: __________________ |
||
|
Провизор-аналитик (преподаватель):________________________________ |
Подпись:____________________ |
СПИСОК СОКРАЩЕНИЙ
ГОСТ – Государственный стандарт
ГФ – Государственная Фармакопея
ОТК – отдел технического контроля
ОФС – Общая фармакопейная статья
ПР – произведение растворимости
ФС – Фармакопейная статья
ФСП – Фармакопейная статья предприятия
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.