
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
БИРСКИЙ ФИЛИАЛ
ФАКУЛЬТЕТ БИОЛОГИИ И ХИМИИ
КАФЕДРА ХИМИИ И МЕТОДИКИ ОБУЧЕНИЯ ХИМИИ
НАУЧНО-ИССЛЕДОВАТЕЛЬСКАЯ РАБОТА
Лыгин Сергей Александрович
Кабирова Лиана Рустамовна
ОЦЕНКА ЭКОЛОГИЧЕСКОГО СОСТОЯНИЯ
ТЕРРИТОРИИ КАРАИДЕЛЬСКОГО РАЙОНА
РЕСПУБЛИКИ БАШКОРТОСТАН
![]() Бирск-2016
Бирск-2016
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ
ГЛАВА I. ХЕМОМЕТРИКА КАК НАУЧНЫЙ ПОДХОД В ХИМИИ ДЛЯ ИНТЕРПРЕТАЦИИ МНОГОМЕРНЫХ ДАННЫХ
1.1 Понятие «хемометрика»
1.2 Методы обработки данных
1.2.1 Метод главных компонент
1.2.2 Регрессионный анализ
Вывод к главе I
ГЛАВА II. ЛЮТИК ЕДКИЙ – БИОИНДИКАТОР ТЯЖЕЛЫХ МЕТАЛЛОВ
2.1 Лютик едкий – биоиндикатор
2.1.1 Кресс-салат как тест - организм
2.2 Тяжелые металлы в почве
2.3 Физико-химические методы определения тяжелых металлов
2.3.1 Атомно - абсорбционный анализ
2.4 Географическое положение Караидельского района РБ
Вывод к главе II
ГЛАВА III. ВОДНЫЙ БАЛАНС ЗЕМЛИ И ОПРЕДЕЛЯЮЩИЕ ЕГО ФАКТОРЫ
3.1.1 Запах
3.1.2 Цветность
3.1.3 Прозрачность
3.2 Химические показатели
3.2.1 Водородный показатель (рН)
3.2.2 Растворенный кислород
3.2.3 Окисляемость (Химическое потребление кислорода)
3.2.4 Биохимическое потребление кислорода (БПК)
3.2.5 Азотная группа: нитраты, нитриты, аммоний
Вывод к главе II
ГЛАВА IV. ЭКСПЕРИМЕНТ И ЕГО ОБСУЖДЕНИЕ
4.1 Методика исследования почвы и результаты эксперимента
4.1.1 Результаты исследования автотрассы Байки-Бирск и прорастание семян кресс-салата
4.1.2 Результаты исследования автотрассы Байки-Акбуляк
4.1.3 МГК в установлении взаимосвязи между содержанием тяжелых металлов и показателями биоиндикации
4.2 Органолептические показатели воды рек Байкинка и Уфимка Караидельского района
4.3 Химические показатели воды рек Байкинка и Уфимка
4.3.1 Металлы исследуемой водной среды
4.3.2 Голубая глина в реке Байкинка в качестве адсорбента загрязняющих веществ
4.4 Регрессионный анализ в оценке уровня загрязненности рек Байкинка и Уфимка с помощью «К-фактора»
ЗАКЛЮЧЕНИЕ
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ И ЛИТЕРАТУРЫ
ВВЕДЕНИЕ
Атмосфера, гидросфера и педосфера тесно взаимодействуют между собой и показатели их загрязненности имеют огромное значение для оценки экологического состояния среды. Газы, пыль, тяжелые металлы и другие вещества, которые попадают в атмосферу, не только опасны для человеческого организма, но и также неблагоприятно влияют на круговороты многих компонентов на земле.
Основным источником загрязнения атмосферы территории Караидельского района является автотранспорт. Вместе с выхлопными газами свинец, образующийся при сгорании бензина, попадает в атмосферу. На территории района ведущее место занимает автомобиль. Он перевозит более 80% всех грузов и пассажиров. Проблема выбросов вредных веществ в атмосферу все больше возрастает, т.к. идет интенсивный рост автомобилей. Наиболее приемлемой формой контроля и определения наличия тяжелых металлов как в воздухе, так и в почве является биоиндикация.
Почвы представляют тройной интерес: как начальное звено пищевых цепей, как интегральный показатель экологического состояния окружающей среды и как источник вторичного загрязнения приземного слоя атмосферы, поверхностных и грунтовых вод. Вот почему необходимо постоянно проводить анализ почвы. Именно с почвы необходимо нормировать содержание тяжелых металлов, так как почвы влияют на химический состав природных вод, воздуха, растения, на продукты природного происхождения, а, следовательно, и на здоровье человека.
Мы живем на планете с очень ограниченным количеством полезных ресурсов. И вода, как один из наиболее важных природных ресурсов, стоит на первом месте. Проблема ее чистоты волнует жителей всей планеты, а жителей исследуемой территории волнует чистота реки Уфимка, с ее притоками рек Юрюзань, Кирзя, Байки, Урюш - как одной из значимых водных ресурсов района.
Трудно представить себе развитие науки без проведения экспериментов, получения достоверной информации и правильной интерпретации данных. Анализ данных необходим в любой области науки. Многомерные данные содержат информацию о двух или более признаках для каждого изучаемого объекта. В дополнение к той информации, которую можно извлечь из одномерных наборов, многомерные данные можно использовать для получения информации о том, существует ли простая зависимость между этими признаками, насколько они взаимосвязаны.
Актуальность: хемометрика является современным научным подходом к моделированию многомерных процессов и явлений, основанная на применении проекционных математических методов, позволяющих выделять в больших массивах данных скрытые переменные и анализировать связи, существующие в изучаемой системе.
Целью исследования является попытка оценить экологическое состояние одного из красивейших районов, расположенного на севере Башкортостана – Караидельского с помощью хемометрической обработки многомерных данных, полученных экспериментальным путем и выявить взаимосвязь между биологическими и химическими параметрами.
Для достижения поставленной цели необходимо выполнить следующие задачи:
- изучить учебную, учебно-методическую и научную литературу;
- установить химические факторы загрязнения почвы тяжелыми металлами, определяющие поведение тест-организмов: лютика едкого (свинец) и кресс-салата (медь, цинк, кобальт) автотрассы Акбуляк - Байки – Бирск, используя метод главных компонент;
- исследовать влияние определенных показателей (ионов ТМ, ХПК, БПК и аммонийной группы) на уровень загрязненности в точках отбора проб - д. Бердяш и д. Хорошаево р. Караидель, используя регрессионный анализ;
- на примере рек Караидель и Байкинка построить регрессионную модель и рассчитать значения обобщенного критерия загрязненности K для выбранных участков.
Объекты исследования:
- реки Уфимка и Байкинка Караидельского района республики Башкортостан и биоиндикаторы (Лютик едкий и кресс-салат).
ГЛАВА I. ХЕМОМЕТРИКА КАК НАУЧНЫЙ ПОДХОД В ХИМИИ ДЛЯ ИНТЕРПРЕТАЦИИ МНОГОМЕРНЫХ ДАННЫХ
Трудно представить развитие науки без проведения экспериментов, получения достоверной информации и правильной интерпретации данных. Анализ данных необходим в любой области науки. Можно выделить некие общие принципы анализа данных, общие методы обработки информации. Суть любого эксперимента заключается в конструировании оптимальной измерительной процедуры и в попытке получить как можно больше информации из результатов.
Можно выделить три основных этапа измерительной процедуры:
1) разработка метода (выбор метода и оптимизация);
2) проведение измерения (подготовка образца и сбор данных);
3) интерпретация данных (первичная обработка данных, перевод «сырых» данных в химическую информацию и переход от химической информации к потребительской).
Хемометрика касается первого и третьего этапов.
1.1 Понятие «хемометрика»
Наиболее часто хемометрика используется химиками-аналитиками. Большое количество примеров из литературы относится именно к анали-тической химии. Хотя само понятие «хемометрика» не имеет специального предназначения для какого-либо одного из направлений экспериментальной химии. Точного определения, что такое хемометрика, нет. В разных учебниках дается немного разная трактовка этого понятия. На сайте Российского хемометрического общества дается следующее определение: хемометрика - это научная дисциплина, находящаяся на стыке химии и математики, предметом которой являются математические методы изучения химиче-ских явлений.
Другое распространенное определение приводится в учебнике Массарта с соавторами: хемометрика - это химическая дисциплина, которая использует математические, статистические и другие методы, включая формальную логику, во-первых, для конструирования и выбора оптимальных измерительных процедур и экспериментов, во-вторых, для извлечения наиболее важной и достоверной химической информации при анализе химических данных [9].
1.2 Методы обработки данных
Методы многомерной статистики изучают взаимосвязи большого ко-личества признаков и большого количества объектов. Все методы можно условно разделить на несколько групп, среди которых важнейшими являются методы факторного, кластерного и дискриминантного анализа. На практике исследователь полагается в основном на компьтерные программы, которые часто предусматривают разные варианты вычислений. В идеале применение различных методов должно приводить к практически эквивалентным результатам.
Основными методами обработки данных являются метод главных компонентов и регрессионный анализ, которые будут рассмотрены ниже.
1.2.1 Метод главных компонент (Principal component analysis)
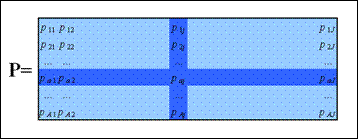
Метод главных компонент применяется к данным, записанным в виде матрицы X - прямоугольной таблицы чисел размерностью I строк и J столбцов (рис.1.1).
Рисунок 1.1
Матрица данных
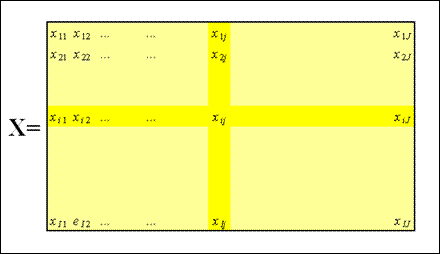
Традиционно строки этой матрицы называются образцами. Они нумеруются индексом i, меняющимся от 1 до I. Столбцы называются переменными, и они нумеруются индексом j= 1, …, J.
Цель МГК - извлечение из этих данных нужной информации. Что является информацией, зависит от сути решаемой задачи. Данные могут содержать нужную нам информацию, они даже могут быть избыточными. Однако, в некоторых случаях, информации в данных может не быть совсем [22].
В общем, многомерном случае, процесс выделения главных компонент происходит так:
- ищется центр облака данных, и туда переносится новое начало координат - это нулевая главная компонента (PC0);
- выбирается направление максимального изменения данных - это первая главная компонента (PC1);
- если данные описаны не полностью (шум велик), то выбирается еще одно направление (PC2) - перпендикулярное к первому, так чтобы описать оставшееся изменение в данных и т.д.
Часто удается упростить данные на порядки: от 1000 переменных перейти всего к двум. При этом ничего не выбрасывается - все переменные учитываются. В то же время несущественная для сути дела часть данных отделяется, превращается в шум. Найденные главные компоненты дают искомые скрытые переменные, управляющие устройством данных [9].
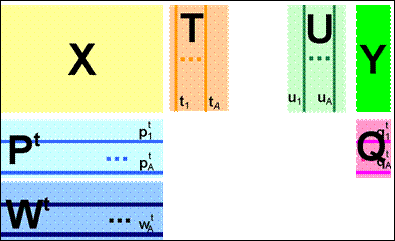
Суть метода главных компонент - это существенное понижение размерности данных. Исходная матрица X заменяется двумя новыми матрицами T и P, размерность которых, A, меньше, чем число переменных (столбцов) J у исходной матрицы X: X=TPT+E
Рисунок 1.2
Декомпозиция матрицы X
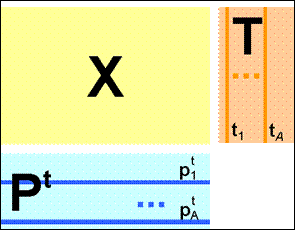
Матрица T и P называется матрицей счетов (scores) b матрицей нагрузок (loadings) соответственно (рис.1.2).
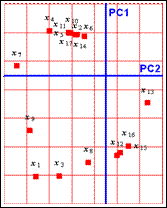
При исследовании данных методом МГК, особое внимание уделяется графикам счетов (рис.1.3). Они несут в себе информацию, полезную для понимания того, как устроены данные. На графике счетов каждый образец изображается в координатах (ti, tj), чаще всего - (t1, t2), обозначаемых PC1 и PC2. Близость двух точек означает их схожесть, т.е. положительную корреляцию. Точки, расположенные под прямым углом, являются некоррелироваными, а расположенные диаметрально противоположно - имеют отрицательную корреляцию[22].
Рисунок 1.3
График счетов
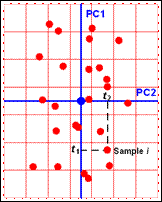
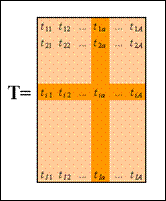
График нагрузок P применяется для исследования роли переменных. На этом графике (рис.1.4) каждая переменная xj отображается точкой в координатах (pi, pj), например (p1, p2). Анализируя его аналогично графику счетов, можно понять, какие переменные связаны, а какие независимы. Совместное исследование парных графиков счетов и нагрузок, также может дать много полезной информации о данных [9].
Рисунок 1.4
График нагрузок
1.2.2 Регриссионный анализ
Обобщением метода МГК является метод проекций на латентные структуры (Projection on Latent Structures, PLS), в котором проводится одновременная декомпозиция матриц X и Y. Проекция строится согласованно - так, чтобы максимизировать корреляцию между соответствующими векторами X-счетов ta и Y-счетов ua (рис.1.5).
Рисунок 1.5
Графическое представление метода главных компонент
Регрессионный анализ, основанный на предположении о нормальном распределении случайных величин, используется для построения модели, по которой можно было бы предсказывать значения одной случайной величины по значениям другой [22].
Вывод к главе I
Хемометрика несомненно является химической дисциплиной, несмотря на всевозможные и разнообразные приложения. Эта наука получила широкое распространение и применение вследствие того, что главной её целью является решение конкретных, в основном химических задач, и только затем разработка новых математических и статистических приемов и алгоритмов.
Появление в начале 70-х годов прошлого столетия вычислительной техники, ставшей повсеместно доступной ученым и инженерам, побудило к возникновению и бурному развитию хемометрики. Благодаря этому стало возможным воплощение многих сложных алгоритмов обработки данных, в особенности методов анализа с результатами многооткликовых и многофакторных экспериментов, что побудило производителей измерительных приборов к разработке оборудования, способного производить большее количество измерений. В целях извлечения полезной информации из возрастающего объема химических данных потребовались хемометрические методы.
Традиционные аналитические методы, которые требуют больших затрат дорогостоящих реактивов, уникального оборудования, времени, труда, могут быть заменены на косвенные хемометрические методы, являющиеся более быстрыми и дешевыми.
Начальные работы по хемометрике были посвящены анализам спектроскопических данных и построению калибровочных моделей с помощью метода главных компонент и метода проекций на латентные структуры. В настоящее время хемометрика является современной, стремительно развивающейся наукой и во многих вузах входит в перечень обязательных дисциплин в программе магистерского обучения.
ГЛАВА II. ЛЮТИК ЕДКИЙ - БИОИНДИКАТОР
ТЯЖЕЛЫХ МЕТАЛЛОВ
Рисунок 2.1
Объект исследования - Лютик едкий

Народное название: куриная слепота. Лютик едкий - многолетнее травянистое растение (рис. 2.1). Листья - нижние - длинночерешковые, длиной 5÷10 см, пятиугольные, пальчатораздельные; верхние - сидячие, трёхраздельные с линейными, зубчатыми долями. Цветки - ярко-жёлтого цвета, достигают 2 см в диаметре, одиночные или собраны в соцветие полузонтик. Формула цветка: *K5C5A∞G∞. Плод - многоорешек [1].
В популяциях разных видов лютиков вместе с нормальными цветками встречаются также махровые, с более пяти лепестками. Причиной мутации, то есть наличие гена махровости у Лютика едкого в работе заключается в том, что он растет в придорожной полосе, где интенсивное движение автотранспорта.
2.1 Лютик едкий – биоиндикатор
Биоиндикация представляет собой оценку состояния среды с помощью живых объектов (или систем), являющихся клетками, организмами, популяциями, сообществами, с помощью которых можно произвести оценку, как абиотических факторов, так и биотических.
Биоиндикаторы - это биологические объекты (от клеток и биологических макромолекул до экосистем и биосферы), используемые для оценки состояния среды. Когда хотят подчеркнуть то, что биоиндикаторы могут принадлежать к разным уровням организации живого, употребляют термин "биоиндикаторные системы" [2].
Критерии выбора биоиндикатора:
-·быстрый ответ;
-·надежность (ошибка <20%);
-·простота;
-·мониторинговые возможности (постоянно присутствующий в природе объект).
Биоиндикаторы принято описывать с помощью двух характеристик: специфичность и чувствительность.
При низкой специфичности биоиндикатор реагирует на разные факторы, при высокой - только на один. При низкой чувствительности биоиндикатор отвечает только на сильные отклонения фактора от нормы, при высокой - на незначительные [2].
Тест - организмы - это биоиндикаторы (растения и животные), которых используют для оценки качества воздуха, воды или почвы в лабораторных опытах (табл.2.1).
Одним из основных требований к тест - организмам является возможность получения культур из генетически однородных организмов. В таком случае отличия между опытом и контролем с большей вероятностью могут быть отнесены на счет нарушающего фактора, а не индивидуальных различий между особями [3].
В качестве тест - организма в данной работе выбран Лютик едкий (рис.2.2). Растение неприхотливо, не плохо растёт и на солнце и в полутени во влажной глинистой почве.
Таблица 2.1
Примеры тест – организмов
|
Изображение |
Примеры |
|
|
- одноклеточные зеленые водоросли (хлорелла, требоуксия из лишайников и пр.); |
|
|
-·простейшие: инфузория-туфелька;
|
|
|
-·членистоногие: рачки дафния и артемия;
|
|
|
-·мхи: мниум;
|
|
|
-·цветковые: злак плевел, кресс-салат, и др.
|
Рисунок 2.2
Лютик едкий (Ranunculus acris L.)

2.1.1 Кресс-салат как тест – организм
В настоящее время все чаще встречаются биоиндикаторы в домашних условиях, так называемая «лаборатория на кухне» с использованием семян кресс-салата. Наиболее часто используют сорт «Забава» вследствие его раннеспелости. Розетка листьев приподнятая, высотой 20-30 см, диаметром 8-10 см, число листьев 7-8. Листья среднего размера, зеленые, со слабым восковым налетом, удлиненно-овальной формы, перисто-рассеченные. Длина листовой пластинки составляет 11-18 см, ширина 3-4 см [21].
Кресс-салат является однолетним овощным растением, всхожесть которого заметно уменьшается в присутствии загрязнителей, побеги и корни подвергаются заметным морфологическим изменениям: задержка роста и искривление побегов, уменьшение длины и массы корней, а также числа и массы семян [15].
Кресс-салат (рис.2.3) как объект исследования удобен и обладает рядом достоинств:
- одновременность изучения действия стрессов на большом числе растений;
- малая площадь рабочего места (чашка Петри, кювета и т.п.);
- высокая скорость прорастания семян (прорастают уже на третий - четвертый день), их почти стопроцентная всхожесть;
- повышенная чувствительность к загрязнению, и возможность использования в качестве биоиндикатора.
Рисунок 2.3
Кресс - салат

2.2 Тяжелые металлы в почве
Тяжёлые металлы - группа химических элементов со свойствами металлов (в том числе и полуметаллы) и значительной атомной массой или плотностью. Список тяжелых металлов согласно разным определениям будет включать разные элементы. Используемым критерием может быть атомная масса свыше 50, и тогда в список попадают все металлы, начиная с ванадия, независимо от плотности. Другим часто используемым критерием является плотность, примерно равная или большая плотности железа (8 г/см3), тогда в список попадают такие элементы как свинец, ртуть, медь, кадмий, кобальт, а, например, более легкое олово выпадает из списка. Существуют классификации, основанные и на других значениях пороговой плотности или атомной массы. Некоторые классификации делают исключения для благородных и редких металлов, не относя их к тяжелым, некоторые исключают нецветные металлы (железо, марганец) [10].
Многие тяжелые металлы, такие как железо, медь, цинк, молибден, участвуют в биологических процессах и в определенных количествах являются необходимыми для функционирования растений, животных и человека микроэлементами. С другой стороны, тяжёлые металлы и их соединения могут оказывать вредное воздействие на организм человека, способны накапливаться в тканях, вызывая ряд заболеваний. Не имеющие полезной роли в биологических процессах металлы, такие как свинец и ртуть, определяются как токсичные металлы. Некоторые элементы, такие как ванадий или кадмий, обычно имеющие токсичное влияние на живые организмы, могут быть полезны для некоторых видов [15, 42].
2.3 Физико-химические методы определения тяжелых металлов
В настоящее время существуют две основные группы аналитических методов для определения тяжелых металлов:
- электрохимические;
- спектроскопические.
В последнее время с развитием микроэлектроники электрохимические методы получают новое развитие, тогда как ранее они постепенно вытеснялись спектрометрическими методами.
Среди спектрометрических методов определения тяжелых металлов первое место занимает атомно-абсорбционная спектроскопия с разной атомизацией образцов:
- атомно-абсорбционная спектроскопия с пламенной атомизацией (FAAS);
- атомно-абсорбционная спектроскопия с электротермической атомизацией в графитовой кювете (GF AAS).
Основными способами определения нескольких элементов одновременно являются атомная эмиссионная спектроскопия с индукционно связанной плазмой (ICP-AES) и масс-спектроскопия с индукционно связанной плазмой (ICP-MS).
Содержание тяжёлых металлов определяется и различными электрохимическими методами:
- полярографическим (вольтамперометрическим);
- потенциометрическим;
- кулонометрическим;
- кондуктометрическим и другими, а также сочетанием некоторых из перечисленных методов с титрованием.
В основу определения содержания тяжёлых металлов указанными методами положен анализ вольтамперных характеристик, потенциалов ион-селективных электродов, интегрального заряда, необходимого для осаждения искомого металла на электроде электрохимической ячейки (катоде), электропроводности раствора, а также электрохимический контроль реакций нейтрализации и других в растворах. С помощью этих методов можно определять тяжёлые металлы до 10-9 моль/л.
Эта группа методов позволяет определять содержание различных тяжёлых металлов в широком диапазоне концентраций с удовлетворительной точностью, но трудоемкость указанных методов также довольно высока.
Содержание тяжёлых металлов в очень малых (примесных) концентрациях - чаще радиоактивных изотопов соответствующих элементов, определяется рядом методов ядерной спектрометрии (бета-, гамма-спектрометрии, а также нейтронно-активационного анализа).
В некоторых случаях содержание тяжёлых металлов определяется комплексными методами, сочетающими спектральные и электрохимические - например, спектрополяриметрией.
К преимуществам спектральных методов относится их высокая чувствительность и, как следствие, небольшие количества пробы, необходимые для анализа содержания тяжёлых металлов в пробе. Вместе с тем, для осуществления ряда из них (атомный абсорбционный анализ, спектрофотометрия, спектрополяриметрия) пробу необходимо перевести в раствор, что обуславливает довольно высокую трудоемкость таких анализов на содержание тяжёлых металлов. Методы ядерной спектрометрии для анализа содержания тяжёлых металлов довольно специфичны [29].
2.3.1 Атомно - абсорбционный анализ
Атомно-абсорбционный анализ - метод количественного элементного анализа по атомным спектрам поглощения (абсорбции). Через слой атомных паров пробы, получаемых с помощью атомизатора, пропускают излучение в диапазоне 190-850нм. В результате поглощения квантов света атомы переходят в возбужденные энергетические состояния. Этим переходам в атомных спектрах соответствуют резонансные линии, характерные для данного элемента. Для получения результатов используется атомно-абсорбционный спектрометр (рис.2.4).
Достоинства атомно-абсорбционного анализа - простота, высокая селективность и малое влияние состава пробы на результаты анализа. Ограничения метода - невозможность одновременного определения нескольких элементов при использовании линейчатых источников излучения и, как правило, необходимость переведения проб в раствор.
Атомно-абсорбционный анализ применяют для определения примерно 70 элементов (главным образом металлов). Не определяют газы и некоторые другие неметаллы, резонансные линии которых лежат в вакуумной области спектра (длина волны меньше 190 нм). С применением графитовой печи невозможно определять Hf, Nb, Та, W и Zr, образующие с углеродом труднолетучие карбиды. Пределы обнаружения большинства элементов в растворах при атомизации в пламени 1-100мкг/л, в графитовой печи в 100-1000 раз ниже. Абсолютные пределы обнаружения в последнем случае составляют 0,1-100 пг. Относительно стандартное отклонение в оптимальных условиях измерений достигает 0,2-0,5% для пламени и 0,5-1,0% для печи. В автоматическом режиме работы пламенный спектрометр позволяет анализировать до 500 проб в час, а спектрометр с графитовой печью-до 30 проб. Оба варианта часто используют в сочетании с предварительным разделением и концентрированием экстракцией, дистилляцией, ионным обменом, хроматографией, что в ряде случаев позволяет косвенно определять некоторые неметаллы и орг. соединения.
Рисунок 2.4
Атомно-абсорбционный спектрометр

Метод атомно-абсорбционного спектрального анализа отличается высокой абсолютной и относительной чувствительностью. Метод позволяет с большой точностью определять в растворах примерно восьмидесяти элементов в малых концентрациях, поэтому он широко применяется в биологии, медицине (для анализа органических жидкостей), в геологии, почвоведении (для определения микроэлементов в почвах) и других областях науки, а также в металлургии для исследований и контроля технологических процессов [26].
2.4 Географическое положение Караидельского района РБ
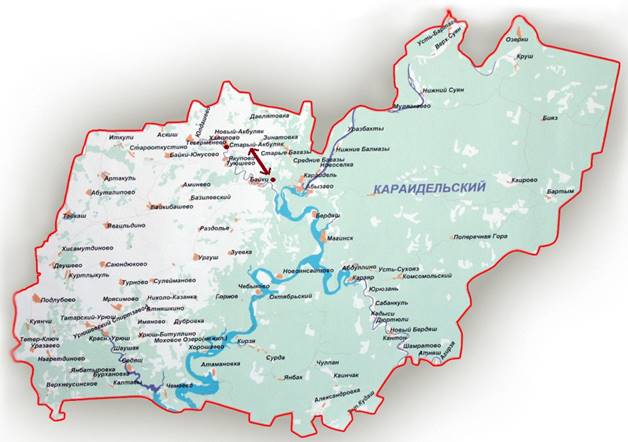
Караидельский район расположен на северо-востоке Республики Башкортостан. Граничит с Аскинским районом на север, Дуванским на восток, Нуримановским и Благовещенским на юг, Мишкинским на юго-запад, Балтачевским на северо-запад (рис.2.5). Район образован 20 февраля 1932г. в связи с упразднением Байкинского района и разукрупнением Аскинского и Мишкинского районов БАССР. Упразднен 4 июля 1956г. Территориально вошел в состав Байкибашевского района БАССР. Вновь образован 1 февраля 1963. Территория района составляет 3786км2. Административным центром является с. Караидель, находится в 217км к северо-востоку от Уфы и 110км. к юго-востоку от железнодорожной станции Щучье Озеро (Пермский край). В 99 населенных пунктах проживает 27,9 тысяч человек [43].
Рисунок 2.5
Карта Караидельского района РБ
Большая часть района расположена на Уфимском плато, на запад - окраине Прибельской увалисто-волнистой равнины. Район находится в пределах Башкирского свода. Территория подвержена карбонатному карсту, имеются месторождения нефти, глины, строительного камня щебенки, песчано-гравийной смеси. Климат умеренно континентальный, прохладный.
Гидрографическую сеть образуют реки Уфа (с притоками рек Юрюзань, Кирзя, Байки, Урюш), р. Юрюзань (с притоками Б. Бердяшка), один из самых крупных водоемов республики - Павловское водохранилище. Преобладают дерново-карбонатные почвы, серые лесные почвы, оподзоленные черноземы. Распространены темнохвойно-широколиственные леса, частично замещенные вторичными березняками и осинниками [43].
Площадь лесов Государственного лесного фонда Караидельского района составляет 235,5 тысяч га, из них 1/3 часть – категория защитных лесов.
Территорию района пересекает автомобильная дорога Бирск-Тастуба-Сатка. В 2001 году в с.Караидель через р. Уфа установлен понтонный мост.
Из-за обилия хвойных лесов, гор и Павловского водохранилища, реки Уфа (с притоками рек Юрюзань, Кирзя, Байки, Урюш), богатства животного мира и рыбного запаса район стал местом отдыха многих тысяч любителей природы и активного отдыха из республики и других регионов страны, а также в народе его прозвали «второй Швейцарией» [43].
Вывод к главе II
Таким образом, почва является основной средой, в которую попадают тяжёлые металлы, в том числе из атмосферы и водной среды. Она же служит источником вторичного загрязнения приземного воздуха и вод, попадающих из неё в Мировой океан. Из почвы тяжёлые металлы усваиваются растениями, которые затем попадают в пищу более высокоорганизованным животным, тем самым мониторинг почвенного покрова является обязательной процедурой контроля за загрязнением окружающей среды.
Среди многих негативных последствий хозяйственной деятельности человека особое место занимает загрязнение окружающей среды тяжелыми металлами. Многие тяжелые металлы являются чрезвычайно токсичными даже в минимальных количествах. Они способны концентрироваться в живых организмах, вызывая при этом различные патологии. В отличие от органических веществ, подвергающихся процессам разложения, металлы способны лишь перераспределяться между природными средами.
Автотранспортное загрязнение является одним из наиболее опасных, оказывающих жесткое влияние на придорожные экосистемы. В выхлопных газах обнаружено большое количество различных веществ, из которых только несколько нетоксичны. С работой автомобильного транспорта связано загрязнение почв в наибольших количествах свинцом, кадмием, цинком, оловом, бериллием и т.д.
ГЛАВА III. ВОДНЫЙ БАЛАНС ЗЕМЛИ
И ОПРЕДЕЛЯЮЩИЕ ЕГО ФАКТОРЫ
Вода - один из важнейших элементов окружающей среды, в значительной мере определяющий санитарные условия жизни и здоровья населения. Крупномасштабные глобальные изменения природной среды в настоящее время становятся все более очевидными, и все чаще их связывают с процессами глобального изменения климата. Глобальные изменения климата влекут за собой и достаточно серьезные изменения среды обитания человека. В связи с этим приходится рассматривать возможности устойчивого развития человеческого сообщества в неразрывной связи с устойчивостью среды обитания.
Зависимость экологических, и технологических процессов от климатической обстановки очевидна. В формировании последней, огромная роль принадлежит водному фактору, определяющему возможности жизнеобеспечения и прогрессивного развития современных и будущих поколений. Именно это определяет важность оценки современных и прогнозирования грядущих изменений водных ресурсов.
Все функционирующие на Земле живые системы содержат в своем составе воду. В растениях содержится до 85 - 95 % воды. В организме взрослого человека вода составляет в среднем 60 %. Биохимические реакции в организме человека протекают в воде, поскольку большинство органических соединений хорошо растворимы. Кроме того, вода участвует в терморегуляции организма и выведении токсических веществ (с потом, мочой) [5].
Под загрязнением водоемов понимают снижение их биосферных функций и экологического значения в результате поступления вредных веществ.
Метод определения состояния водного объекта путем его непосредственного осмотра. При органолептических наблюдениях особое внимание обращают на явления, необычные для данного водоема или водотока и часто свидетельствующие о его загрязнении: гибель рыбы и других водных организмов, растений, выделение пузырьков газа из донных отложений, появление повышенной мутности, посторонних окрасок, запаха, цветения воды, нефтяной пленки и пр. [17].
3.1.1 Запах
Свойство воды вызывать у человека и животных специфическое раздражение слизистой оболочки носовых ходов. Запах воды характеризуется видами запаха и интенсивностью запаха. Интенсивность запаха воды измеряется в баллах (табл. 3.1). Запах воды вызывают летучие пахнущие вещества, поступающие в воду в результате процессов жизнедеятельности водных организмов, при биохимическом разложении органических веществ, при химическом взаимодействии содержащихся в воде компонентов, а также с промышленными, сельскохозяйственными и хозяйственно-бытовыми сточными водами. На запах воды оказывают влияние состав веществ, температура, значения рН, степень загрязненности водного объекта, биологическая обстановка, гидрологические условия и т.д., [40].
3.1.2 Цветность
Показатель качества воды, характеризующий интенсивность окраски воды и обусловленный содержанием окрашенных соединений; выражается в градусах платиново-кобальтовой шкалы (табл. 3.1). Определяется путем сравнения окраски испытуемой воды с эталонами.
Цветность природных вод обусловлена главным образом присутствием гумусовых веществ и соединений трехвалентного железа. Количество этих веществ зависит от геологических условий, водоносных горизонтов, характера почв, наличия болот и торфяников в бассейне реки и т.п. Cточные воды некоторых предприятий также могут создавать довольно интенсивную окраску воды.
Высокая цветность воды ухудшает ее органолептические свойства и оказывает отрицательное влияние на развитие водных растительных и животных организмов в результате резкого снижения концентрации растворенного кислорода в воде, который расходуется на окисление соединений железа и гумусовых веществ [38, 40].
Таблица 3.1
Шкала оценки интенсивности запаха и цветности воды
|
Шкала оценки интенсивности запаха |
Шкала оценки цветности воды |
||
|
интенсивность запаха |
единица измерения, баллы |
цветность |
единица измерения, градус |
|
Нет |
0 |
Очень малая |
до 25 |
|
Очень слабая |
1 |
Малая |
> 25 до 50 |
|
Слабая |
2 |
Средняя |
> 50 до 80 |
|
Заметная |
3 |
Высокая |
> 80 до 120 |
|
Отчетливая |
4 |
Очень высокая |
> 120 |
|
Очень сильная |
5 |
||
3.1.3 Прозрачность
Мера прозрачности - высота столба воды, при которой можно наблюдать опускаемую в воду белую пластину определенных размеров (диск Секки) или различать на белой бумаге шрифт определенного размера и типа (шрифт Снеллена). Результаты выражаются в сантиметрах.
Определение прозрачности воды - обязательный компонент программ наблюдений за состоянием водных объектов. Увеличение количества грубодисперсных примесей и мутности характерно для загрязненных и эвтрофных водоемов [38].
3.2 Химические показатели
К химическим характеристикам можно отнести совокупность находящихся воде веществ, в различных химических и физических состояниях.
3.2.1 Водородный показатель
Водородный показатель (рН) - характеризует концентрацию свободных ионов H+ в воде и выражает степень кислотности или щелочности воды.
При пониженном содержании свободных ионов водорода (рН>7), - вода имеет щелочную реакцию, а при повышенном содержании - (рН<7) - кислую. В идеально чистой дистиллированной воде эти ионы будут уравновешивать друг друга. В таких случаях вода нейтральна и рН=7.
H2O ↔ [H]+ + [OH]- ; ═> [H]+ = [OH]-.
При растворении в воде различных химических веществ этот баланс может быть нарушен, что приводит к изменению уровня рН.
В зависимости от уровня рН воды можно условно разделить на несколько групп:
- сильнокислая вода (<3);
- кислая вода (3 – 5);
- слабокислая вода (5 – 6,5);
- нейтральная вода (6,5 – 7,5);
- слабощелочная вода (7,5 – 8,5);
- щелочная вода (8,5 – 9,5);
- сильнощелочная вода(>9,5).
Контроль над уровнем рН очень важен на всех стадиях водоподготовки, так как его изменение может не только сказаться на запахе, привкусе и внешнем виде воды, но и существенно повлиять на эффективность очистки воды.
При низком рН вода обладает высокой коррозионной активностью, а при высоких уровнях рН (>11) вода приобретает характерную мылкость [33].
3.2.2 Растворенный кислород
Поступление кислорода в водоем происходит путем растворения его при контакте с воздухом (абсорбции), а также в результате фотосинтеза водными растениями. Содержание растворенного кислорода зависит от температуры, атмосферного давления, степени турбулизации воды, минерализации воды и др.[36]. В поверхностных водах содержание растворенного кислорода может колебаться от 0 до 14 мг/л. Относительное содержание кислорода в воде, выраженное в процентах его нормального содержания и называется степенью насыщения кислородом. Этот параметр зависит от температуры воды, атмосферного давления и уровня минерализации [40].
Величина, характеризующая содержание в воде органических и минеральных веществ, окисляемых одним из сильных химических окислителей при определенных условиях. Существует несколько видов окисляемости воды: перманганатная, бихроматная, иодатная, цериевая. Наиболее высокая степень окисления достигается методами бихроматной и иодатной окисляемости воды. Выражается в миллиграммах кислорода, пошедшего на окисление органических веществ, содержащихся в 1 дм3 воды. Окисляемость подвержена закономерным сезонным колебаниям. Их характер определяется, с одной стороны, гидрологическим режимом и зависящим от него поступлением органических веществ с водосбора и, с другой,- гидробиологическим режимом. В водоемах и водотоках, подверженных сильному воздействию хозяйственной деятельности человека, изменение окисляемости выступает как характеристика, отражающая режим поступления сточных вод. Для природных малозагрязненных вод рекомендовано определять перманганатную окисляемость; в более загрязненных водах определяют, как правило, бихроматную окисляемость.
В соответствии с требованиями к составу и свойствам воды водоемов у пунктов питьевого водопользования величина ХПК не должна превышать 15 мгО/дм3; в зонах рекреации в водных объектах допускается величина ХПК до 30 мгО/дм3.
В программах мониторинга ХПК используется в качестве меры содержания органического вещества в пробе, которое подвержено окислению сильным химическим окислителем. ХПК применяют для характеристики состояния водотоков и водоемов, поступления бытовых и промышленных сточных вод (в том числе, и степени их очистки), а также поверхностного стока [37].
В поверхностных водах величины БПК5 изменяются обычно в пределах 0,5-4 мгO2/дм3 и подвержены сезонным и суточным колебаниям.
Сезонные изменения зависят в основном от изменения температуры и от исходной концентрации растворенного кислорода. Суточные колебания величин БПК5 также зависят от исходной концентрации растворенного кислорода, которая может в течение суток изменяться на 2,5 мг/дм3 в зависимости от соотношения интенсивности процессов его продуцирования и потребления. Весьма значительны изменения величин БПК5 в зависимости от степени загрязненности водоемов. Для водоемов, загрязненных преимущественно хозяйственно-бытовыми сточными водами, БПК5 составляет обычно около 70% БПКполн. [40].
В зависимости от категории водоема величина БПК5 регламентируется не более 6 мгO2 /дм3 для водоемов хозяйственно-бытового и культурного водопользования.
Oпределение БПК5 в поверхностных водах используется с целью оценки содержания биохимически окисляемых органических веществ, условий обитания гидробионтов и в качестве интегрального показателя загрязненности воды. Необходимо использовать величины БПК5 при контролировании эффективности работы очистных сооружений [27].
3.2.5 Азотная группа
Азот относится к числу биогенных элементов и его соединения имеют особое значение для развития жизни в водных объектах. При отсутствии азотсодержащих соединений в воде рост и развитие водной растительности прекращается, однако избыток этих соединений также приводит к негативным последствиям, вызывая процессы эвтрофикации водного объекта и ухудшение качества воды.
Минеральные формы азота в водных объектах представлены, главным образом нитритами, нитратами, ионами аммония.
Источниками поступления соединений азота в природные воды являются разложение клеток отмерших организмов, прижизненные выделения гидробионтов, атмосферные осадки, фиксация из воздуха в результате жизнедеятельности азотфиксирующих бактерий. Значительное количество азота может попадать в водные объекты с бытовыми, сельскохозяйственными и промышленными сточными водами.
В азотную группу входят такие соединения, содержащие ионы: нитрит, нитрат и аммония.
Нитриты представляют собой промежуточную ступень в цепи бактериальных процессов окисления аммония до нитратов (нитрификация - только в аэробных условиях) и, напротив, восстановления нитратов до азота и аммиака (денитрификация - при недостатке кислорода). Подобные окислительно-восстановительные реакции характерны для станций аэрации, систем водоснабжения и собственно природных вод. В поверхностных водах нитриты находятся в растворенном виде. В кислых водах могут присутствовать небольшие концентрации азотистой кислоты (HNO2) (не диссоциированной на ионы). Повышенное содержание нитритов указывает на усиление процессов разложения органических веществ в условиях более медленного окисления NO2- в NO3-, что указывает на загрязнение водного объекта, т.е. является важным санитарным показателем [35].
Концентрация нитритов в поверхностных водах составляет сотые (иногда даже тысячные) доли миллиграмма в 1 л.
Сезонные колебания содержания нитритов характеризуются отсутствием их зимой и появлением весной при разложении неживого органического вещества. Наибольшая концентрация нитритов наблюдается в конце лета, их присутствие связано с активностью фитопланктона (установлена способность диатомовых и зеленых водорослей восстанавливать нитраты до нитритов). Осенью содержание нитритов уменьшается.
Для нитритов ПДК установлена в размере 3,3 мг/л в виде иона NO2- или 1 мг/л в пересчете на азот.
В соответствии с требованиями глобальной системы мониторинга состояния окружающей среды (ГСМОС/GEMS) нитрит- и нитрат-ионы входят в программы обязательных наблюдений за составом питьевой воды и являются важными показателями степени загрязнения и трофического статуса природных водоемов [35].
Нитраты являются конечным продуктом минерализации органических азотсодержащих веществ,их содержание в воде, как правило, значительно превышает содержание аммонийного и нитратного азота. В незагрязненных водных объектах концентрация нитратного азота обычно не превышает десятков микрограммов в литре пробы. Для нитратов характерно уменьшение содержания в вегетационный период за счет потребления водными растениями и увеличение осенью при отмирании водных организмов и минерализации органических веществ. Максимальное содержание нитратов наблюдается в зимний период.
Понижение содержания соединений азота в водоемах связано, в основном, с потреблением их водными растениями. Некоторую роль в этом процессе играет денитрификация, т.е. перевод связанного азота в свободное состояние [32].
Аммонийный азот в водах находится, главным образом, в растворенном состоянии в виде ионов аммония и не диссоциированных молекул аммиака количественное соотношение которых имеет важное экологическое значение и определяется величиной рН и температурой воды. В то же время некоторая часть аммонийного азота может мигрировать в сорбированном состоянии на минеральных и органических взвесях, а также в виде различных комплексных соединений.
Присутствие в незагрязненных природных водах ионов аммония показано главным образом, с процессами биохимической деградации белковых веществ, дезаминирования аминокислот, разложения мочевины. Естественными источниками аммиака служат прижизненные выделения гидробионтов. Кроме того, ионы аммония могут образовываться в результате анаэробных процессов восстановления нитратов и нитритов [31].
Источником антропогенного загрязнения водных объектов ионами аммония являются сточные воды многих отраслей промышленности, битовые сточные воды, стоки с сельскохозяйственных угодий.
Сезонные колебания концентрации ионов аммония характеризуются обычно понижением весной, в период интенсивной фотосинтетической деятельности фитопланктона, и повышением летом при усилении процессов бактериального разложения органического вещества в периоды отмирания
водных организмов, особенно в зонах их скопления.
Не стабильность содержание ионов аммония указывает на ухудшение санитарного состояния водного объекта, причем, поскольку аммиак более токсичен, чем ионы аммония, опасность аммонийного азота для гидробионтов возрастает с повышением рН воды [6, 40, 44].
Вывод к главе III
В настоящее время водным ресурсам грозят истощение и порча. Человечество почти полностью зависит от поверхностных вод суши – рек и озер. Эта ничтожная часть водных ресурсов подвергается наиболее интенсивному воздействию. Вода рек и озер покрывает потребности человечества в питьевой воде, используется на орошение в сельском хозяйстве (на это уходит 73% всей пресной воды), в промышленности, служит для охлаждения атомных и тепловых электростанций.
Загрязнение вод проявляется в изменении физических и органолептических свойств (нарушение прозрачности, окраски, запаха, вкуса), увеличения содержания сульфатов, хлоридов, нитратов, токсичных тяжелых металлов, сокращении растворенного в воде кислорода воздуха, появлении радиоактивных элементов, болезнетворных бактерий и других загрязнителей. Наиболее часто встречаются химическое и бактериальное загрязнения. Значительно реже наблюдается радиоактивное, механическое и тепловое загрязнение.
ГЛАВА IV. ЭКСПЕРИМЕНТ И ЕГО ОБСУЖДЕНИЕ
4.1 Методика исследования почвы и результаты эксперимента
Исследования Лютика едкого проводились на территории Караидельского района дороги местного значения Байки - Акбуляк в период его цветения. Расчет результатов исследования и анализ почвы на содержание свинца проводились на кафедре химии и МОХ факультета биологии и химии БФ БашГУ.
В популяциях разных видов лютиков, наряду с нормальными цветками встречаются махровые цветки с 6-9 и более лепестками (рис. 4.1). Подтверждено [41], что этот признак появляется в результате мутации гена, определяющего развитие нормального цветка. Если принять во внимание, что это признак моногенный, тогда нормальный цветок – это признак доминантный (А), махровый – рецессивный (а). Исследования проводились из расчета, что признак моногенный (Аа).
Рисунок 4.1
Лютик едкий: А – нормальный (5 лепестков); Б – махровый (6 лепестков);
В – махровый (7 лепестков)



А Б В
Мутация растений - сложный генетический процесс. Чаще расщепление родительских признаков происходит у растений, полученных при скрещивании. Причиной мутации могут быть радиоактивные или химические вещества, механические повреждения или другие стрессовые ситуации [4].
Кроме изменения числа лепестков у лютиков существуют и другие виды мутации:
- нарушение числа чашелистиков;
- гофрированность лепестков;
- наличие вырезки на лепестках;
- наличие или отсутствие цветков-альбиносов;
- наличие или отсутствие темных пятен на оборотной стороне венчика;
- хлорофиллизация цветка и т. д.
Вблизи автострад с интенсивным движением транспорта в почве может накапливаться до 1г свинца на 1кг почвы, который и является мутагеном для цветка [12].
В недалеком прошлом топливо, которое использовалось для двигателя внутреннего сгорания, представляло собой смесь нескольких углеводородных жидкостей, в которые для лучшей детонации добавляли специальные присадки. Самое известное вещество, используемое для этого - тетраэтилсвине́ц Pb(CH3CH2)4-ядовитое металлоорганическое соединение, применяемое в основном как антидетонирующая присадка к моторному топливу, повышающая октановое число. Вот почему в бензине можно было обнаружить свинец. При сгорании 1л этилированного бензина в воздух попадало 200-400мг свинца [28].
В Российской Федерации с 2009 года введен запрет использования этилированного бензина [7].
Однако почва до сих пор содержит следы свинца. Тяжелые металлы накапливаются в почвенной толще, особенно в верхних гумусовых горизонтах. Период полуудаления тяжелых металлов из почвы (выщелачивание, эрозия, потребление растениями, дефляция) составляет в зависимости от типа почвы для: цинка - 70 - 510 лет; кадмия - 13 - 110 лет; меди - 310 - 1500 лет; свинца - 740 - 5900 лет [16].
Для того чтобы дать оценку влияния автотранспорта на содержание тяжелых металлов в почве был произведен качественный анализ почвы на содержание ионов тяжелых металлов автотрассы республиканского значения Байки - Бирск, где еще более интенсивное движение по сравнению с дорогой местного значения Байки-Акбуляк.
В качестве тест - организма также может выступать кресс-салат (рис.4.2).
Рисунок 4.2
Семена кресс-салата сорта «Забава»

4.1.1 Результаты исследования автотрассы Байки-Бирск
и прорастание семян кресс-салата
Исследуемый участок, протянулся в общей сложности более чем на 3,5 км. Пробы отбирались на 3 участках. А именно:
- автобусная остановка «с. Байки» (подножье подъема) - (Т-№1);
- середина подъема - (Т-№2);
- вершина подъема - (Т-№3).
Таким образом, были взяты пробы почвы с трех точек [8]. Анализы собранных образцов почвы проводились методом атомно-абсорбциооной спектроскопии в трех повторностях, что позволило получить достоверные сведения о содержании изучаемых элементов в почве.
Пробы отбирались по методике конверта. Метод конверта - наиболее распространенный способ отбора смешенных почвенных образцов и чаще всего применяется для исследования почвы гумусового горизонта, при этом из точек контролируемого элементарного участка берут 5 образцов почвы. Точки должны быть расположены так, чтобы, мысленно соединив их прямыми линиями, получить изображение запечатанного конверта (длина его стороны может составлять 1÷10м). Обычно при изучении почвы отбирают пробы гумусового горизонта с глубины примерно 20см, что соответствует длине штыка лопаты. Из каждой точки отбирают приблизительно 1кг почвы [15]. Почвенные образцы упаковывают в полиэтиленовые или полотняные мешочки и прилагают к ним этикетки (сопроводительные талоны).
Для анализов отбиралась почва с верхних горизонтов на глубине 0-10 см. Образцы почвы очищались от растительных остатков и живых частей растений. Затем ее поместили в пластиковую посуду с крышкой, что позволило изолировать почву от контакта с окружающей средой до начала эксперимента [8].
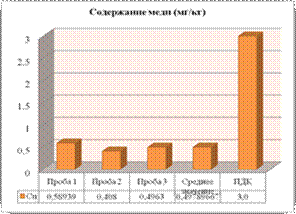
Рисунок 4.3
Содержание тяжелых металлов в почве у подножья подъема
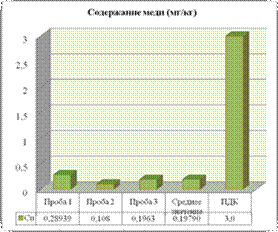
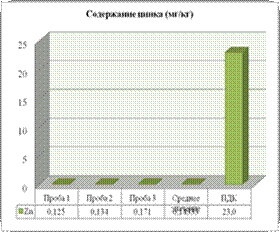
Анализ почвы - (Т-№1) показал, что содержание Cu, Zn, значительно меньше ПДК, это можно связать с тем большая часть (из 65 – 43) автомобиля за 30 мин начинают свое движение после стоянки на остановке «с. Байки», скорость не значительна сгорание топлива происходит практически полностью, а соответственно выбросы в атмосферу остаются минимальные (рис. 4.3).
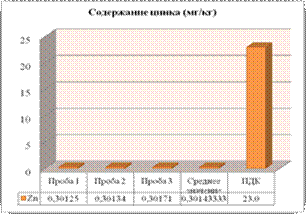
На (рис. 4.4) представлены результаты анализа почвы с середины подъема, которые свидетельствуют о том, что концентрация исследуемых металлов находится в пределах ПДК [15]. Но стоит отметить, что она несколько больше, чем на первом участке, так как перед предстоящим подъемом автомобиль набирает скорость, увеличивая нагрузку на двигатель, и в результате этого происходит не полное сгорание топлива [24].
Рисунок 4.4
Содержание тяжелых металлов в почве на середине подъема
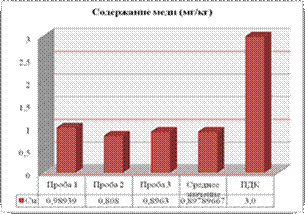
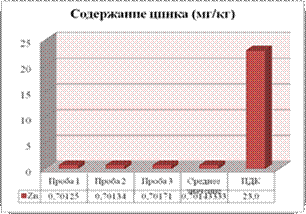
В (Т-№3) наблюдается снижение содержания ТМ по сравнению со средней частью начала подъема, но выше чем в начале подъема. Это можно связать с тем, что при выходе на вершину подъема у автомашин происходит сброс газа, уменьшается нагрузка на двигатель, а значит, происходит более полное сгорание топлива и содержание ТМ значительно уменьшается (рис.4.5).
Рисунок 4.5
Содержание тяжелых металлов в почве на вершине подъема
Что же касается исследования семян кресс - салата, в ходе эксперимента взято по 3 пробы снега с трех (выше указанных) участков и подготовлено 10 чашек Петри для опытов. Семена кресс - салата по 20 штук были помещены в подготовленные чашки и налит одинаковый объём талой воды, с указанием пробы воды и варианта. Семена находились в одинаковых условиях при температуре воздуха 22 - 24о С. Ежедневно проводились наблюдения в течение 7 дней за прорастанием семян [25].
Данные результаты сопоставимы с выше полученными.
Семена, находящиеся в чашке с талой водой из (Т-№1) растут быстрее всех (рис.4.6), а также по количеству проросших семян не уступает семенам, замоченным в других образцах воды. Значит, более благоприятной средой для прорастания семян, является талая вода, пробы которой были отобраны у подножъя подъема (рис.4.7).
Рисунок 4.6
Проросшие семена кресс-салата,
находящиеся в чашке с талой водой из (Т-№1)

Рисунок 4.7
Результаты эксперимента по числу проросших и не проросших семян,
и по средней длине проростков
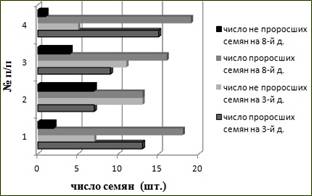
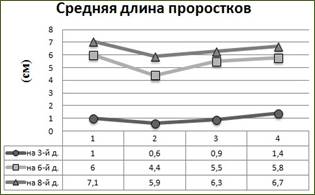
Семена, находящиеся чашке с талой водой из (Т-№3) является также «рекордсменами» по длине проросших семян, но отростки слабые тонкие, почти все лежат на вате. И меньше всех по размеру и количеству семян находится в талой воде из (Т-№2), наблюдается искривление некоторых побегов [21]. Значит наименее благоприятной средой для прорастания семян, является талая вода, пробы которой были отобраны у середины подъема (рис.4.7).
4.1.2 Результаты исследования автотрассы Байки-Акбуляк
На расстоянии 3 м от дороги (позиция 1) были определены 3 участка размером 10*10 м, общей площадью 100 м2. Определен объект исследования - Лютик едкий, с усредненным числом экземпляров, на каждом участке по 200 штук. Таким образом, в трех повторностях было изучено всего 600 штук.
В результате эксперимента было установлено, что в среднем каждый 8 Лютик едкий на 200 штук подвержен мутации и имеет махровость, которая выражается в увеличении числа лепестков с 5 до 6(7) штук, что составило в среднем на трех участках 4,0 % от общего числа [18].
Параллельно исследованным участкам, выше на 50 м (позиция 2) были определены 3 участка по 100 м2. Проводился подсчет лютиков по 200 штук на каждом участке, где махровость цветка выражена меньше: на 200 штук только каждый 5-й Лютик едкий проявлял махровость, что составило 2,5%. Это более чем на порядок ниже - позиции 1 [12].
Частоту встречаемости гена махровости у мутированных лютиков можно подсчитать используя математическое выражение Харди-Вайнберга:
p2AA + 2pqAa + q2aa = 1
Рисунок 4.8
Закон Харди - Вайнберга для двух аллелей
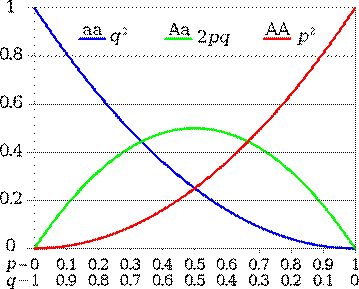
На рис.4.8 по оси абсцисс показаны частоты аллелей (p) и (q), по оси ординат - частоты генотипов. Каждая кривая соответствует одному из трех возможных генотипов.
Полученные данные позволяют определить частоту генов и генотипов, т.е. генетическую структуру популяции по изучаемому признаку [18].
На примере позиции 1 вариант-1 (В-1) приведены расчеты с учетом всех основных пунктов определения генов и генотипов Лютика едкого.
Рассчитано процентное содержание как нормальных, так и махровых цветков Лютика едкого, что составило: 94% и 6% или в долях 0,94 и 0,06 соответственно.
Таблица 4.1
Частота генов и генотипов в популяции Лютика едкого и
количественное содержание свинца в почве
|
Позиция |
Вариант |
Число растений
|
Форма цветка |
Частота генов в популяции |
Частота генотипов в популяции |
Pb (мг/кг) |
|||||
|
простая
доля |
махр-я
доля |
||||||||||
|
А, рА |
а, qa |
АА, р2AA |
Аа, 2pqAa |
аа, q2aa |
|||||||
|
На склоне горы (2) |
В-1 |
1-200 |
196 0,980 |
4 0,020 |
0,859 |
0,141 |
0,738 |
0,242 |
0,020 |
5,23±0,45 |
|
|
В-2 |
1-200 |
194 0,970 |
6 0,030 |
0,827 |
0,173 |
0,684 |
0,286 |
0,030 |
5,70±0,19 |
||
|
В-3 |
1-200 |
195 0,975 |
5 0,025 |
0,842 |
0,158 |
0,709 |
0,266 |
0,025 |
5,15±0,11 |
||
|
∑ср. |
200 |
195 0,975 |
5 0,025 |
0,842 |
0,157 |
0,710 |
0,265 |
0,025 |
5,36±0,25 |
||
|
У дороги (1) |
В-1 |
1-200 |
188 0,940 |
12 0,060 |
0,755 |
0,245 |
0,570 |
0.370 |
0.060 |
6,69±0,11 |
|
|
В-2 |
1-200 |
195 0,975 |
5 0,025 |
0,842 |
0,158 |
0,709 |
0,266 |
0,025 |
6,30±0,34 |
||
|
В-3 |
1-200 |
193 0,965 |
7 0,035 |
0,813 |
0,187 |
0,661 |
0,304 |
0.035 |
6,25±0,21 |
||
|
∑ср. |
200 |
192 0,960 |
8 0,040 |
0,803 |
0,197 |
0,647 |
0,313 |
0,040 |
6,41±0,22 |
||
|
Величина ПДК (мг/кг) |
6,0 |
||||||||||
Растения с махровыми цветками имели гомозиготный генотип – (аа).
По формуле a=√q2 частота генотипа (аа) в популяции составляет q2(0,060), а частота гена (а) составляет √q2 (0,245). Из формулы следует, что сумма частоты генов (А) и а есть величина постоянная pA+qa=1, тогда частота гена pA=1-qa =1-0,245=0,755 [24].
Растения с махровыми цветками имеют генотипы (АА) и (Аа). Частота генотипа AA=p2 (0,570) , частота генотипа Aa=2pq=2*0,755*0,245=0,370.
Результаты позиции 2 рассчитаны аналогично примеру позиции 1 В - 1. Таким образом, позиция 1, наиболее подвержена влиянию тяжелых металлов, чем позиция 2. Анализ почвы методом атомно-абсорбционной спектроскопии показал, что содержание свинца в придорожной полосе превышает ПДК. Полученные данные по генотипу, а также количественному содержанию свинца в почве представлены в табл.4.1.
Наиболее наглядно представлены результаты на рисунке 4.9.
Рисунок 4.9
Частота генотипов в популяции Лютика едкого и
количественное содержание свинца в почве
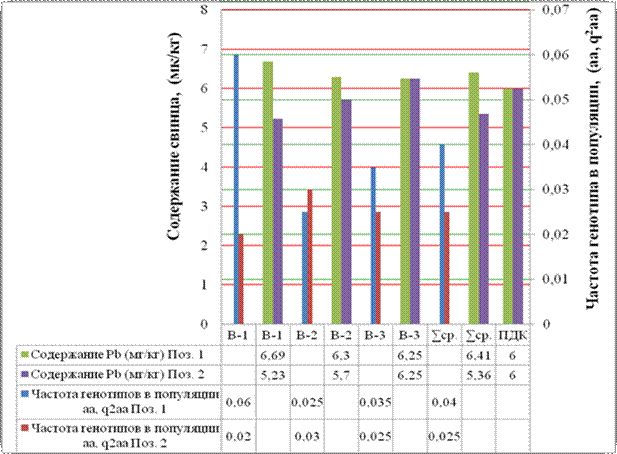
В результате эксперимента выявлено, что в придорожной полосе содержание свинца гораздо больше, чем на склоне горы и превышает ПДК в позиции 1 примерно на 7 %.
4.1.3 МГК в установлении взаимосвязи между содержанием тяжелых металлов и показателями биоиндикации
Данные обрабатывались в специализированном пакете программы Unscrambler® by CAMO ASA.
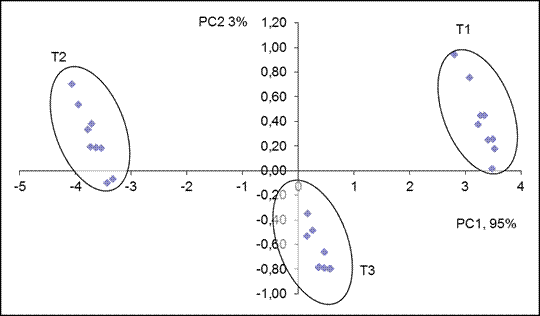
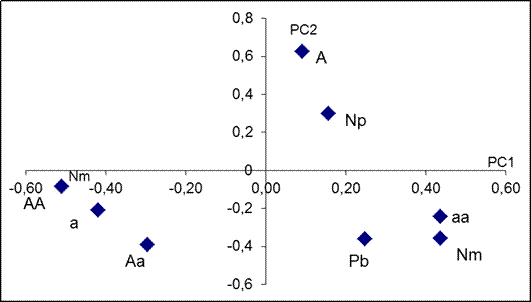
С помощью метода главных компонент удалось установить корреляцию биологических параметров с химическими. График счетов визуализирует данные, полученные экспериментальным путем, а график нагрузок устанавливает, как переменные влияют друг на друга. Как видно из рисунка 4.10 наибольшая концентрация тяжелых металлов (Zn, Cu) в пробах талой воды наблюдается в точке 2. Также можно заметить, что установлена прямая корреляция между количественным содержанием тяжелых металлов и дней, в которые семена не проросли в пробах [22].
Рисунок 4.10
График счетов и нагрузок
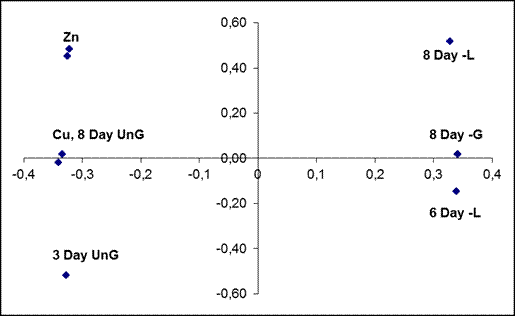
На изучаемых участках автотрассы Байки-Акбуляк установлена прямая корреляция между химическими (количественное содержание свинца в почве) и биологическими параметрами (доминантный и рецессивный ген, число махровых и нормальных цветков). Как видно из рисунка 4.11 наибольшее влияние свинец оказывает на число махровых цветков и развитие рецессивного гена махровости у Лютика едкого.
Рисунок 4.11
График нагрузок по Лютику едкому и содержанию свинца в почве
4.2 Органолептические показатели воды рек Байкинка и Уфимка
Караидельского района
С помощью изученных методик по определению органолептических свойств воды были определены органолептические показатели. Результаты занесены в таблицу 4.2.
Оценка интенсивности запаха реки Уфимка в исследуемых точках соответствует 1 баллу (запах, не замечаемый потребителем, но обнаруживаемый специалистом), согласно шкале интенсивности запаха, представленной в таблице 1 [6].
Исследования показали, что в реке Уфимка не наблюдается перегнивания растительности, в связи с чем цветность в ноябре - низкая (соответственно, прозрачность выше 30 см.) и оценивается до 25 градусов платино - кобальтовой шкалы, которая приведена в таблице 1, в апреле - очень высокая (прозрачность выше 15 см.) и оценивается более 120 градусов, в июле - малая (прозрачность ниже 30см.) и оценивается от 25-50 градусов [17].
Таблица 4.2
Органолептические показатели вод рек Уфимка и Байкинка
|
№ п/п |
Точка отбора пробы |
Органолептические показатели |
||||||||
|
цветность, град |
прозрачность, см |
запах, баллы |
||||||||
|
апрель |
Июль |
ноябрь |
апрель |
июль |
ноябрь |
апрель |
июль |
Ноябрь |
||
|
1 |
Т-1 |
165 |
40 |
20 |
15,3 |
30 |
>30 |
1 |
1 |
1 |
|
2 |
Т-2 |
106 |
36 |
21 |
16,7 |
29,7 |
>30 |
1 |
1 |
1 |
4.3 Химические показатели воды
рек Байкинка и Уфимка Караидельского района
В таблице 4.3 видно, что средние показатели pH в указанный период незначительно превышают ПДК. Вода обеих рек входит в группу щелочной воды, а также можно предположить, что вода обладает высокой коррозионной активностью.
Жесткость поверхностных вод подвержена заметным сезонным колебаниям, достигая наибольшего значения в конце зимы и наименьшего в период половодья [34]. Вода обоих рек относится к жесткой (табл. 4.3).
Таблица 4.3
Некоторые химические показатели
|
Показатели качества воды |
ПДК р/х (мг/л) |
Результаты анализа (мг/л) |
|
|
р. Байкинка |
р. Уфимка |
||
|
рН |
6,5-8,5 |
8,72±1,04 |
8,93±0,8 |
|
Общая жесткость |
7,00 |
8,20 |
7,59 |
По результатам проведенных исследований можно сказать, что биохимическое окисление органических веществ находится в пределах допустимой концентрации (рис.4.12).
Рисунок 4.12
Химические показатели: растворенный кислород, ХПК, БПК
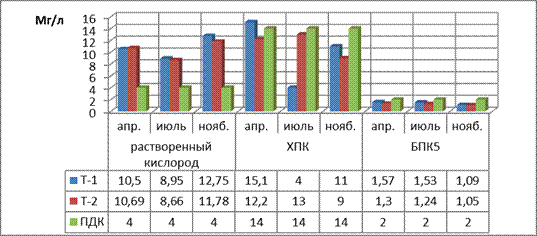
По результатам исследования выявилось, что ХПК не превышает ПДК, но наблюдается незначительное превышение в апреле (рис.4.11). Это может быть связано с тем что режим поступления сточных вод выше, чем в другие месяцы, из-за весеннего половодья.
Что же касается значений растворенного кислорода, то ПДК не должно быть менее 4 мг/л. В поверхностных водах содержание растворенного кислорода может колебаться от 0 - 14 мг/л, что соответствует данным на рис.4.11 [17].
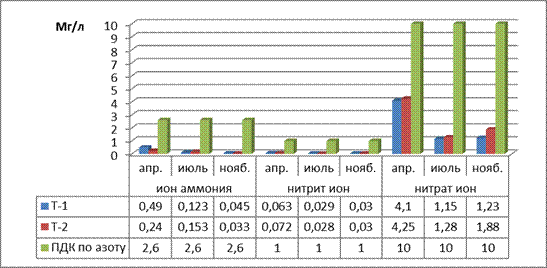
Исследования показали что, азотная группа находится значительно ниже ПДК и потверждают сезонные колебания этих ионов в реке (рис.4.13).
Рисунок 4.13
Химические показатели на азотную группу
4.3.1 Металлы исследуемой водной среды
Поступая в водную среду, тяжелые металлы вступают во взаимодействие с другими компонентами среды, образуя гидратированные ионы, оксигидраты, ионные пары, комплексные неорганические и органические соединения. Конкретная форма существования металлов зависит от их природы, природы ионов и молекул, от рН, температуры.
В результате проведенного эксперимента в водной среде рек Уфимка и Байкинка были обнаружены следующие металлы: железо, медь, кадмий, цинк, свинец [14].
Железо. В речных водах концентрация железа общего в большинстве случаев находится в пределах 0,01 ÷ 1,0 мг/л. Она подвержена сезонным изменениям, обусловленным участием этого металла в физико - химических и биологических процессах, активно протекающих в водной среде особенно в летний период. Основным природным источником поступления железа в поверхностные воды являются процессы химического выветривания горных пород. Значительная часть железа поступает также с подземным стоком. Антропогенное загрязнение водных объектов соединениями железа обусловлено их выносом со сточными водами предприятий горнодобывающей, металлургической и химической промышленности [19].
Содержание меди в природной пресной воде колеблется от 2 до 30 мкг/л, в морской - от 0,5 до 3,5 мкг/л. Повышенные концентрации меди (до нескольких граммов в литре) характерны для кислых рудничных вод. Основным источником поступления меди в природные воды являются сточные воды предприятий химической, металлургической промышленности, шахтовые воды, альдегидные реагенты, используемые для уничтожения водорослей. Также медь относиться к числу активных микроэлементов, участвующих в процессе фотосинтеза и влияющих на усвоение азота растениями. Недостаточное содержание меди в почвах отрицательно влияет на синтез белков, жиров и витаминов и способствует бесплодию растительных организмов. Вместе с тем избыточные концентрации меди оказывают неблагоприятные воздействия на растительные и животные организмы [14].
Цинк попадает в природные воды в результате протекающих в природе процессов разрушения и растворения горных пород и минералов (сфалерит, цинкит, госларит, смитсонит, каламин), а также со сточными водами рудообогатительных фабрик и гальванических цехов, производств пергаментной бумаги, минеральных красок, вискозного волокна и др.
В воде существует главным образом в ионной форме или в форме его минеральных и органических комплексов. Иногда встречается в нерастворимых формах: в виде гидроксида, карбоната, сульфида и др. Цинк относится к числу активных микроэлементов, влияющих на рост и нормальное развитие организмов. В то же время многие соединения цинка токсичны, прежде всего его сульфат и хлорид [19].
Кадмий: в природные воды поступает при выщелачивании почв, полиметаллических и медных руд, в результате разложения водных организмов, способных его накапливать. Соединения кадмия выносятся в поверхностные воды со сточными водами свинцово-цинковых заводов, рудообогатительных фабрик, ряда химических предприятий, гальванического производства, а также с шахтными водами. Понижение концентрации растворенных соединений кадмия происходит за счет процессов сорбции, выпадения в осадок гидроксида и карбоната кадмия и потребления их водными организмами. Растворенные формы кадмия в природных водах представляют собой минеральные комплексы. Основной взвешенной формой кадмия являются его сорбированные соединения. Значительная часть кадмия может мигрировать в составе клеток гидробионтов. В речных незагрязненных и слабозагрязненных водах кадмий содержится, в субмикрограммовых концентрациях Соединения кадмия играют важную роль в процессе жизнедеятельности животных и человека. В повышенных концентрациях токсичен, особенно в сочетании с другими токсичными веществами [14]. Свинец: источниками поступления свинца в поверхностные воды являются процессы растворения минералов. Существенными факторами понижения концентрации свинца в воде является адсорбция его взвешенными веществами и осаждение с ними в донные отложения. В числе других металлов свинец извлекается и накапливается гидробионтами. Свинец находится в природных водах в растворенном и взвешенном состоянии. В речных водах концентрация свинца колеблется от десятых долей до единиц микрограммов в 1 л. Свинец содержится в выбросах предприятий металлургии, металлообработки, электротехники, нефтехимии и автотранспорта [19].
В поверхностные воды соединения ртути могут поступать в результате выщелачивания пород, в районе ртутных месторождений, в процессе разложения водных организмов, накапливающих ртуть. Значительные количества поступают в водные объекты со сточными водами предприятий, производящих красители, пестициды, фармацевтические препараты, некоторые взрывчатые вещества.
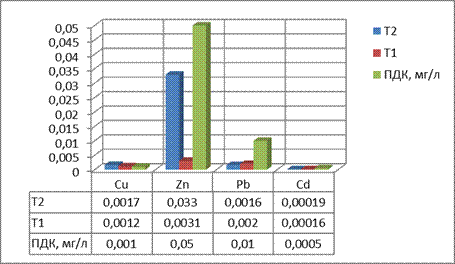
Показатели содержания кадмия, свинца и цинка укладываются в значение ПДК 0,005 мг/л, 0,01 мг/л, 0,05 мг/л соответственно, а вот медь немного превышает, как мы видим из рисунка 3, в связи с тем, что территория Башкортостана богата содержанием медных руд. В исследуемой пробе ртуть не обнаружена (рис. 4.14). Эти данные указывают на то, что вода исследуемой реки Уфимка и ее притока реки Байкинка не представляет токсической угрозы для жителей Караидельского района [14].
Рисунок 4.14
Содержание тяжелых металлов в реках Уфимка и Байкинка
4.3.2 Голубая глина в реке Байкинка в качестве адсорбента загрязняющих веществ
Территория Караидельского района в древности была дном древнего моря, и поэтому на территории района есть залежи осадочных пород, таких как глина, мел, известь, известняк, строительный камень [11].
Голубую глину добывают здесь же на реке Байкинка (в самой реке и по берегам), которая выходит на поверхность в пяти местах (рис.4.15).
Рисунок 4.15
Место выхода голубой глины на поверхность

Голубая глина была исследована по следующим показателям:
1) Чистота глины (отсутствие посторонних примесей):
а) для этого достаточно смочить глину водой и промять руками. Если руки ощущают камешки, песчинки - глина плохая;
б) поместить небольшое количество образца глины на предметное стекло, и рассматривать глину через лупу, на наличие песка и посторонних примесей[20]. Результаты представлены в таблице 4.4.
Таблица 4.4
Степень чистоты соответствующих образцов глины
|
№ п/п |
Степень чистоты образца |
Соответствующие образцы глины |
|
|
Образец |
1 |
Чистый |
|
|
2 |
Чистый |
||
|
3 |
Наличие примесей в виде речного песка более 40% |
||
|
4 |
Наличие примесей в виде речного песка менее 10% |
||
|
5 |
Чистый |
||
2) Способность глины растворяться в воде.
В стакане с водой растворить и перемешать образец глины, чтобы частицы пришли в движение, а вода замутилась, и следить, как глина будет оседать.
Если она это делает медленно, то глина маслянистая (частички жира не позволяют глине потонуть, поскольку не смачиваются водой), и оседает она хлопьями, нехотя - это хорошая глина [20]. А если глина сразу пошла на дно и через пять минут в стакане наблюдается два слоя – из глины и воды - это плохая глина (табл. 4.5).
Таблица 4.5
Осаждение и расслаивание частиц глины
|
№ п/п |
Степень осаждения и расслаивания частиц глины |
||
|
Образец |
1 |
Частицы |
Медленно оседают на дно, глина не расслаивается |
|
2 |
Медленно оседают на дно, глина не расслаивается |
||
|
3 |
Медленно оседают на дно, глина расслаивается на песок и глину |
||
|
4 |
Медленно оседают на дно, глина расслаивается на песок и глину |
||
|
5 |
Медленно оседают на дно, глина не расслаивается |
||
3) Исследование глины на пластичность.
Хорошую глину (не по составу, а по вязкости) можно определить без лабораторных исследований, просто на глаз. Есть очень несложный метод проверки.
Взять комок глины, обильно смочить водой и сделать из него форму в виде бублика. Хорошая глина мнется руками, принимая любую форму. Но основной показатель - это качество изделия после сушки. Положить «бублик» на солнце и подождать [20].
Если поверхность изделия потрескалась или появились непонятные разводы - глина плохая. Ее не стоит использовать. Если «бублик» остался ровным и прочным - глина хорошая. Настоящая глина чуть маслянистая на ощупь, вязкая (табл. 4.6).
Таблица 4.6
Пластичность соответствующих образцов глины
|
№ п/п |
Степень пластичности глины |
Образцы глины |
|
|
Образец |
1 |
Образец пластичный, без комочков, легко мнется и сворачивается в «бублик» |
|
|
2 |
Образец пластичный, без комочков, легко мнется и сворачивается в «бублик» |
||
|
3 |
Образец хрупкий, без комочков, легко мнется, плохо сворачивается в «бублик» |
||
|
4 |
Образец пластичный, без комочков, легко мнется и сворачивается в «бублик» |
||
|
5 |
Образец пластичный, без комочков, легко мнется и сворачивается в «бублик» |
||
4) Кислотность.
Кислотность образцов голубой глины проверена универсальной лакмусовой бумажкой (рис. 4.16), которая показала нейтральную среду (pH ≈ 7 - 8).
Рисунок 4.16
pH раствора образцов голубой глины

5) Адсорбционные способности.
Адсорбирующие способности голубой глины можно исследовать с помощью раствора перманганата калия (розовая окраска), и раствора йода (светло - коричневая окраска), обесцвечивание растворов проходило в течении определенного времени: - перманганата калия - один час; - йода примерно 5 часов[23].
6) Определение наличия ионов в глине:
а) SiO32-
Взвесить по 200мг навески (5 образцов), добавить к каждой по 10 мл раствора щелочи – 0,4% гидроксида натрия. Для количественного анализа отмерить по 5 мл полученных растворов. Затем к каждому образцу по каплям раствор соляной кислоты 1н до появления изменения в растворах. Используемый раствор соляной кислоты подкрашен метиловым оранжевым. Добавление соляной кислоты продолжить до появления изменений в растворе: окрашивания, помутнение, образование взвеси [20].
Результаты эксперимента на содержание силикат-иона показали, что во всех образцах содержится примерно одинаковое его количество (табл. 4.7)Таблица 4.7Появление окраски
|
№ пробы |
Появление розовой окраски (число капель) |
|
1 |
11 |
|
2 |
12 |
|
3 |
10 |
|
4 |
9 |
|
5 |
9 |
б) Cl-
Реагенты: 5% раствор AgNO3; азотная кислота (1н).
Выполнение анализа: к 10 мл пробы раствора глины прибавить 3 – 4 капли азотной кислоты и прилить 0,5 мл раствора нитрата серебра. Белый осадок выпадает при концентрации хлорид – ионов более 100 мг/л:
Cl- + Ag+ = AgCl↓
белый
Слабое помутнение растворов всех образцов, в результат, указывает что, хлорид – ионов более 1 мг/л.
в) SO42-
Реагенты: 10% BaCl2; 8% HCl (ρ=1,19 г/см3).
Выполнение анализа: к 10 мл пробы раствора глины прибавить 2 – 3 капли соляной кислоты и прилить 0,5 мл раствора хлорида бария. При концентрации сульфат – ионов более 100 мг/л выпадает осадок:
SO42- + Ba2+ = BaSO4↓
белый
Результат: наблюдается опалесценция, значит концентрация сульфат – ионов более 1 мг/л.
г) Fe3+
Реагенты: 20% КCNS; азотная кислота (конц.); 5% H2O2.
Условия проведения реакции: H2O2 необходим для окисления Fe (II) до Fe (III).
Выполнение анализа: к 10 мл пробы раствора глины прибавить 1 каплю азотной кислоты, затем 2 – 3 капли пероксида водорода и добавить 0,5 мл KCNS. При концентрации ионов железа более 2,0 мг/л появляется розовое окрашивание, при концентрации более 10 мг/л окрашивание становится красным:
Fe2+ + 3CNS- = Fe(CNS)3↓
красный
Результат: появляется розовое окрашивание, указывая, что концентрация ионов железа более 2,0 мг/л
д) Pb2+
Реагент: хромат калия (10г К2CrO4 растворить в 90 мл Н2О).
Выполнение анализа. В пробирку поместить 10мл пробы глины, прибавить 1 мл раствора реагента. Если выпадает жёлтый осадок, то содержание катионов свинца более 100 мг/л:
Pb2+ + CrO42- = PbCrO4↓
желтый
Если наблюдается помутнение раствора, то концентрация катионов свинца более 20 мл/л, а опалесценции – 0,1 мг/л [20].
Результат: катионов свинца не обнаружено.
Изучив свойства голубой глины, можно сделать следующий вывод:
- образцы глины - 1, 4, 5 хорошего качества (жирные на ощупь, пластичные, не содержат посторонних примесей и могут быть использованы в лечебных и косметических целях);
- образцы глины - 2, 3 не отвечают требованиям по качеству (образец - 2 добыт из воды и имеет неприятный запах; образец - 3 содержит большое количество речного песка).
Обнаружено на реке Байкинка и по ее берегам пять выходов голубой глины на поверхность, три из которых могут быть использованы в качестве источника добычи голубой глины.
Все образцы глины обладают в одинаковой степени адсорбционными свойствами.
В голубой глине исследованных образцов обнаружены:
-силикат – ионы;
- хлорид – ионы;
-сульфат – ионы;
-катионы железа (III);
-загрязнителей в виде ионов свинца не обнаружено. Что тоже подтверждает лечебные свойства голубой глины исследованных образцов [13].
4.4 Регрессионный анализ в оценке уровня загрязненности рек Байкинка и Уфимка с помощью «К-фактора»
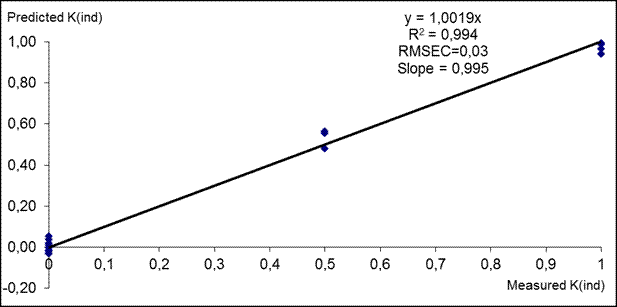
Для того чтобы получить экспрессную оценку качества воды была построена регрессионная модель по обобщенному критерию уровня загрязненности природных объектов - К критерию, приравненному для объектов с загрязненностью на уровне ПДК к 1, а к 0 для модельных образцов с наименьшими значениями. Коэффициент корреляции составляет 0.994 [22].
На графике ось абсцисс - это заданные значения индекса К, а ось ординат представляет собой найденные по модели значения К (рис. 4.17).
Установлено, что содержание вредных веществ на исследуемых участках не превышает ПДК, а значения К составляют не более 0,2 (табл. 4.8).
Таблица 4.8
Найденные значения К по модели
|
Real Sample |
K(ind) predicted, 3PCs |
|
T1 |
0,16 |
|
T1 |
0,13 |
|
T1 |
0,13 |
|
T2 |
0,21 |
|
T2 |
0,2 |
|
T2 |
0,11 |
Рисунок 4.17
Результаты ПЛС моделирования
ЗАКЛЮЧЕНИЕ
В ходе выполнения работы изучена учебная, учебно-методическая и научная литература.
Изучены методы определения органолептических и химических показателей воды. Главными органолептическими показателями являются запах, цветность и прозрачность воды, а химическими - pH, жесткость, ХПК, БПК5, растворенный кислород, азотная группа.
Проведен отбор воды рек Уфимка и Байкинка Караидельского района Республики Башкортостан в зимний, весенний и летний периоды. Эксперимент проводился трехкратно, с вероятной погрешностью 2-5 %. Всего было взято 6 проб и проведено более 100 экспериментальных исследований.
В результате определения органолептических и химических показателей воды этих рек установлено, что исследуемая река Уфимка с ее притоком р.Байкинка не представляет никакой токсической угрозы для жителей Караидельского района, т.к. органолептические и химические показатели выше указанных рек находятся в пределах ПДК.
Произведен учет мутированных цветков по признаку махровости и по формуле Харди-Вайнберга рассчитана частота генов и генотипов Лютика едкого, обитающего в разных экологических условиях. Махровость цветка Лютика едкого наблюдается в результате мутации. В среднем на каждые 200 штук приходится 8 махровых цветков у придорожной полосы, которая больше поражена выхлопными газами автотранспорта. На загрязненной территории махровость цветка Лютика едкого на 1,5% выше, чем на склоне горы.
Проведен анализ не только количественного содержания тяжелого металла (Pb) в почве придорожной полосы Байки-Акбуляк, но и анализ других тяжелых металлов (Cu, Zn,), содержащихся в почве дороги республиканского значения Байки-Бирск, где движение автотранспорта намного интенсивнее.
Содержание тяжелых металлов в придорожной полосе не превышает предельно допустимых значений для каждого металла, но оказывает влияние на растения. Тяжелые металлы аккумулируют не только в почве, но и в снеге, что сказывается на прорастании семян кресс-салата в талой воде, пробы которой были отобраны на тех же участках. Наличие гена махровости у Лютика едкого, заключается в том, что он растет в придорожной полосе, где интенсивное движение автотранспорта. С развитием технического прогресса, а в частности автомобильного транспорта, увеличилось воздействие антропогенного характера на окружающую среду, в частности растительный покров.
Исследовано влияние состава почвы и природной воды (рек Уфимка и Байкинка, талая вода снежного покрова) на показатели уровня загрязненности объектов окружающей среды с помощью хемометрики.
Используя МГК, установлены химические факторы загрязнения почвы тяжелыми металлами, определяющие поведение тест-организмов: лютика едкого (свинец) и кресс-салата (медь, цинк) автотрассы Акбуляк - Байки - Бирск.
Методом проекций на латентные структуры исследовали влияние определенных показателей (ионов ТМ, ХПК, БПК и аммонийной группы) на уровень загрязненности в точках отбора проб – р.Уфимка и р.Байкинка. В качестве обобщенного критерия уровня загрязненности природных объектов предложено использовать К критерий, который для объектов с загрязненностью на уровне ПДК приравнен к 1, низких - 0. На примере рек Уфимка и Байкинка построена регрессионная модель и рассчитаны значения K для выбранных участков. Установлено, что содержание вредных веществ на исследуемых участках не превышает ПДК, а значения К не более 0,2.
Таким образом, район является одним из самых экологически чистых и красивых уголков РБ, так как на территории района нет промышленных предприятий. Природная красота, широта лесного и водного пространства, обилие рыбных запасов нашего края является территорией отдыха для многочисленных туристов и любителей рыболовов не только из РБ, но и из других регионов страны.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ И ЛИТЕРАТУРЫ
1. Алексеев Ю.Е. Определитель высших растений Башкирской АССР. «Наука», 1989г.
2. Биоиндикация загрязнений наземных экосистем / Под ред. Р. Шуберт. - М.: Мир, 1988.
3. Биоиндикация как метод оценки состояния окружающей среды- [Электронный ресурс]- Режим доступа. - URL: http://knowledge.allbest.ru
4. Бородин П.М. Этюды о мутантах. М.: «Знание», 1983. - 109 с.
5. Бурлишин М. - Воду надо охранять от людей //. Природно-ресурсные Ведомости от 2008 года №4 (331).
6. Водные ресурсы Башкортостана и проблемы их использования. - [Электронный ресурс] - Режим доступа. - URL: http://otherreferats.allbest.ru/ecology/00113295_0.html
7. ГОСТ Р 51105-97. Топлива для двигателей внутреннего сгорания. Неэтилированный бензин. Издание с Изменением № 1,2,3,4; ИУС N10-99, N7-2000, N6-2004, N3-2005, дополнением ИУС N5-2009
8. ГОСТ 17.4.3.01-83 - Отбор проб
9. Дребущак Т.Н. Введение в хемометрику. Практика анализа экспериментальных данных: Учебное посрбие/ Новосибирск, 2011. 88 с.
10. Загрязнение биосферы тяжелыми металлами [Электронный ресурс]- Режим доступа. - URL: http://otherreferats.allbest.ru - Загрязнение биосферы тяжелыми металлами
11. Лыгин С.А., Кабирова Л.Р.- Анализ голубой глины окрестностей реки Байкинка Караидельского района республики Башкортостан, «Научное сообщество студентов XXI столетия. Естественные науки»: материалы Х студенческой международной заочной научно -практической конференции. (06 мая 2013 г.) — Новосибирск: Изд. «СибАК», 2013. – С.96-106.
12. Лыгин С.А., Кабирова Л.Р.- Влияние свинца на частоту генотипа лютика едкого (RANUNCULUS ACRIS L.), Материалы 51-й международной Научной студенческой конференции «Студент и научно-технический прогресс» 12–18 апреля 2013 г. Биология. Новосибирск 2013. С. 41.
13. Лыгин С.А., Кабирова Л.Р.- Голубая глина – дар господний, «Научная дискуссия: вопросы математики, физики, химии, биологии»: материалы V международной заочной научно-практической конференции. (11 июня 2013 г.) – Москва: Изд. «Международный центр науки и образования», 2013. – С. 109-116 (170с.)
14. Лыгин С.А., Кабирова Л.Р.- Ионы тяжелых металлов воды реки Уфа Караидельского района, Естественные и медицинские науки: научная дискуссия. Сборник материалов Международной научно-практической конференции (г.Киев, Украина, 7 февраля 2014 г.). Центр Научно-Практических Студий, 2014.-С. 140 – 143. (151 с.
15. Лыгин С.А., Кабирова Л.Р.- Качественный анализ почвы на содержание тяжелых металлов автотрассы Байки-Бирск, «Молодежный научный форум: Естественные и медицинские науки»: материалы I студенческой международной заочной научно-практической конференции. (20 марта 2013 г.) – Москва: Изд. «Международный Центр Науки и Образования», 2013.- С. 9-17.
16. Лыгин С.А., Кабирова Л.Р.- Материалы Международного дистанционного конференции – конкурса научных работ студентов, магистрантов и аспирантов им. Лилии Хайбуллиной «Современные аспекты изучения экологии растений», Уфа.- 2013.- С. 55-58.
17. Лыгин С.А., Кабирова Л.Р.- Органолептические и химические показатели реки Уфа Караидельского района республики Башкортостан, Журнал «Естественные и математические науки в современном мире: материалы XIV междунар. науч.-практ. конф. № 1 (13)». Новосибирск: Изд. «СибАК», 2014. – С. 89-96. (РИНЦ)
18. Лыгин С.А., Кабирова Л.Р.- Остаточное влияние свинца на частоту генов и генотипов лютика едкого (Ranunculus Acris L.), «Научная дискуссия: вопросы физики, химии, биологии»: материалы VI международной заочной научно-практической конференции. (31 января 2013 г.) – Москва: Изд. «Международный центр науки и образования»,2013.–С. 86-90 (112с.)
19. Лыгин С.А., Кабирова Л.Р, Пурина Е.С.- Практико-ориентированный проект по исследованию состава природных вод, Научно-методический журнал «Химия в школе» (ВАК) №3, 2016, с.56-61
20. Лыгин С.А., Кабирова Л.Р.- Химический анализ голубой глины окрестностей реки Байкинка Караидельского района Республики Башкортостан, Актуальные вопросы естественных и медицинских наук. Сборник материалов I Международной научно-практической заочной конференции (г. Киев, Украина. 19 сернтября 2013 г.). – Центр Научно-Практических Студий, 2013. –С. 41- 50
21. Lygin S.A., Kabirova L.R., Biotesting of snow cover at the roadside using watercress’seeds, The USA Journal of Applied Sciences, September 2015, №4 USA - pp.3-6
22. Lygin S.A., Kabirova L.R., Sidelnikov A.V.- Environmental pollution assessment using PCA/PLS analysis (through the example of soil and natural water of Karaidel' district of Bashkortostan republic), Tenth Winter Symposium on Chemometrics «Modern Methods of Data Analysis», February 29-March 4, 2016, Samara
23. Lygin S.A., Kabirova L.R., Karaidel district is a source of clay as natural “sterilizer” of cow’s milk, Austrian Journal of Technical and Natural Sciences, September-October, 2014. № 9-10. – pp. 10-14. Austria, Vienna.
24. Lygin S.A., Kabirova L.R., The assessment of environmental state Karaidel district of Bashkortostan, European science review, March-April, 2014, №2 – pp. 7-11. Austria, Vienna
25. Lygin S.A., Kabirova L.R., Watercress is bioindicator of water quality, European applied sciences, April, 2015, №4 Германия - pp.3-5
26. Методика выполнения измерений массовой доли элементов в пробах почв, грунтов, донных отложениях методами атомно-эмиссионной и атомно-абсорбционной спектрометрии (М-МВИ-80-2008)
27. Морозова О.Г. - Химия окружающей среды. // Красноярск: Сиб ГТУ, 2002.
28. Мотузова Г.В. Принципы и методы почвенно-геохимического мониторинга. – М.: Изд-во МГУ, 2006. 95 с.
29. Определение содержания тяжелых металлов физико-химическими методами - [Электронный ресурс] - Режим доступа. - URL: revolution.allbest.ru›Химия›00229171_0.html
30. ПНД. Ф. 14. 1:2: 3:4. 123 – 97. Методика выполнения измерений биохимической потребности в кислороде после n – дневной инкубации (БПКполн.) в поверхностных пресных, подземных (грунтовых), питьевых, сточных и очищенных сточных водах.
31. ПНД Ф 14. 1: 2. 1 – 95. Методика выполнения измерений массовой концентрации ионов аммония в природных и сточных водах фотометрическим методом с реактивом Несслера.
32. ПНД. Ф. 14. 1: 2. 4 – 95. Методика выполнения измерений массовой концентрации нитрат – ионов природных и сточных водах фотометрическим методом с салициловой кислотой.
33. РД. 52. 24. 495 – 2005. Водородный показатель. Методика выполнения измерений электрометрическим методом.
34. РД. 52. 24. 395 – 2007. Жесткость воды. Методика выполнения измерений титриметрическим методом с трилоном Б.
35. РД 52. 24. 381 – 2006. Массовая концентрация нитритов в водах. Методика выполнения измерений фотометрическим методом с реактивом Грисса.
36. РД. 52. 24. 419 – 2005. Массовая концентрация растворенного кислорода в водах. Методика выполнения измерений йодометрическим методом.
37. РД. 52. 24. 421 – 2007. Химическое потребление кислорода в водах. Методика выполнения измерений титриметрическим методом.
38. РД. 52. 24. 497 – 2007. Цветность и прозрачность поверхностных вод суши. Методика выполнения измерений фотометрическим и визуальным методами.
39. Российское хемометрическое общество - [Электронный ресурс] - Режим доступа.-URL: http://rcs.chemometrics.ru/Tutorials/pca.htm#Contents.ru.html
40. Справочник по гидрохимии - [электронный ресурс] - Режим доступа. - URL: http://shr.receptidocs.ru/v6559/?download=1.ru (дата обращения 13.09.2013)
41. Трошина А.И. Методическое пособие к проведению полевой практики по генетике. - Тобольск: ТГПИ им. Д.И. Менделеева, 2004. - 74 с.
42. «Тяжёлые металлы. Источники поступления в окружающую среду. Действие на организм человека» - [Электронный ресурс] - Режим доступа. URL:http://knowledge.allbest.ru/ecology/3c0b65635b3ad68a4c53b89521316c27_0.html
43. Электронный паспорт территориальной избирательной комиссии муниципального района Караидельский район. - [Электронный ресурс] - Режим доступа. - URL: http://www.admkaraidel.ru.html
44. Эльпинер Л.И. – Водные ресурсы, климат и здоровье // Научно - популяционный и образовательный журнал. Экология и жизнь 1(86) 2009 с. 82.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.