Самостоятельная работа на тему: «Элементы V группы» предназначена для учащихся 9 класса изучающих предмет по программе О. С. Габриелян (ФГОС). Данный материал позволяет закрепить и проверить знания полученные в ходе изучения темы. На выполнение самостоятельной работы учащимся отводится 15 минут.
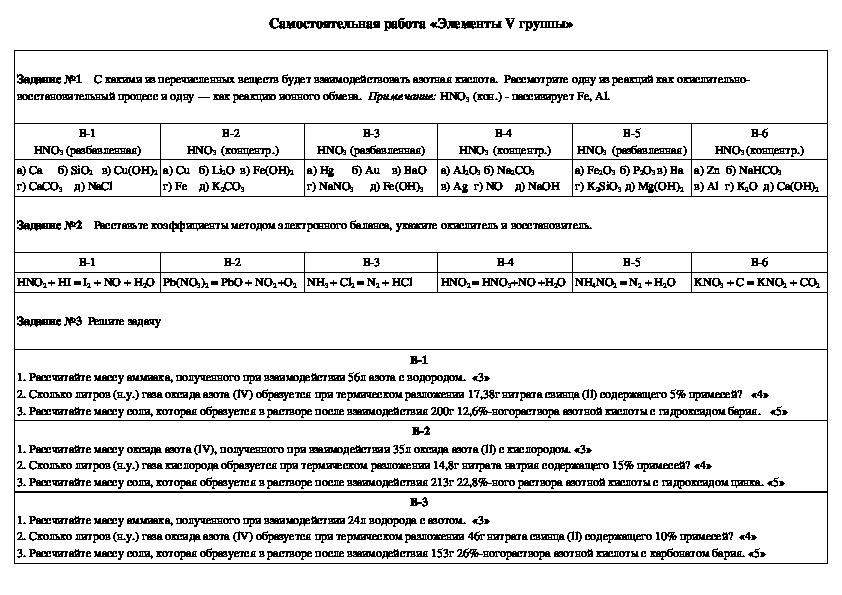
Самостоятельная работа «Элементы V группы»
Задание №1 С какими из перечисленных веществ будет взаимодействовать азотная кислота. Рассмотрите одну из реакций как окислительно
восстановительный процесс и одну — как реакцию ионного обмена. Примечание: HNO3 (кон.) пассивирует Fe, Al.
В1
В2
В3
В4
В5
В6
HNO3 (разбавленная)
HNO3 (концентр.)
а) Ca б) SiO2 в) Cu(OH)2
г) CaCO3 д) NaCl
а) Cu б) Li2O в) Fe(OH)2
г) Fe д) K2CO3
HNO3 (разбавленная)
а) Hg б) Au в) BaO
г) NaNO3 д) Fe(OH)3
HNO3 (концентр.)
а) Al2O3 б) Na2CO3
в) Ag г) NO д) NaOH
HNO3 (разбавленная)
а) Fe2O3 б) P2O3 в) Ba
г) K2SiO3 д) Mg(OH)2
HNO3 (концентр.)
а) Zn б) NaHCO3
в) Al г) K2O д) Ca(OH)2
Задание №2 Расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель.
В1
В2
В3
В4
В5
В6
HNO2 + HI = I2 + NO + H2O Pb(NO3)2 = PbO + NO2 +O2 NH3 + Cl2 = N2 + HCl
HNO2 = HNO3+NO +H2O NH4NO2 = N2 + H2O
KNO3 + C = KNO2 + CO2
Задание №3 Решите задачу
В1
1. Рассчитайте массу аммиака, полученного при взаимодействии 56л азота с водородом. «3»
2. Сколько литров (н.у.) газа оксида азота (lV) образуется при термическом разложении 17,38г нитрата свинца (ll) содержащего 5% примесей? «4»
3. Рассчитайте массу соли, которая образуется в растворе после взаимодействия 200г 12,6%ногораствора азотной кислоты с гидроксидом бария. «5»
В2
1. Рассчитайте массу оксида азота (lV), полученного при взаимодействии 35л оксида азота (ll) с кислородом. «3»
2. Сколько литров (н.у.) газа кислорода образуется при термическом разложении 14,8г нитрата натрия содержащего 15% примесей? «4»
3. Рассчитайте массу соли, которая образуется в растворе после взаимодействия 213г 22,8%ного раствора азотной кислоты с гидроксидом цинка. «5»
1. Рассчитайте массу аммиака, полученного при взаимодействии 24л водорода с азотом. «3»
2. Сколько литров (н.у.) газа оксида азота (lV) образуется при термическом разложении 46г нитрата свинца (ll) содержащего 10% примесей? «4»
3. Рассчитайте массу соли, которая образуется в растворе после взаимодействия 153г 26%ногораствора азотной кислоты с карбонатом бария. «5»
В31. Рассчитайте массу аммиака, полученного при взаимодействии 61л азота с водородом.«3»
2. Сколько литров (н.у.) газа оксида азота (lV) образуется при термическом разложении 71,83г нитрата свинца (ll) содержащего 7% примесей? «4»
3. Рассчитайте массу соли, которая образуется в растворе после взаимодействия 620г 15,1%ногораствора азотной кислоты с гидроксидом бария. «5»
В4
В5
1. Рассчитайте массу оксида азота (ll), полученного при взаимодействии 15л азота с кислородом. «3»
2. Сколько литров (н.у.) газа кислорода образуется при термическом разложении 34,2г нитрата лития содержащего 12% примесей? «4»
3. Рассчитайте массу соли, которая образуется в растворе после взаимодействия 261г 21,2%ного раствора азотной кислоты с гидроксидом алюминия. «5»
1. Рассчитайте массу оксида азота (lV), полученного при взаимодействии 75л оксида азота (ll) с кислородом. «3»
2. Сколько литров (н.у.) газа кислорода образуется при термическом разложении 184г нитрата натрия содержащего 25% примесей? «4»
3. Рассчитайте массу соли, которая образуется в растворе после взаимодействия 138г 5,8%ного раствора азотной кислоты с гидроксидом цинка. «5»
В6