
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ОБРАЗОВАНИЯ
«БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
Бирский филиал БашГУ
Факультет биологии и химии
Кафедра биологии, экологии и химии
Лыгин Сергей Александрович
Фараизов Ильнур Ильдарович
Научно-исследовательская работа
ТЕРПЕНЫ И ТЕРПЕНОИДЫ. РАСЧЕТ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ ТЕРПЕНОВ В ПРОГРАММЕ PASS ONLINE
БИРСК – 2021
ВВЕДЕНИЕ
ГЛАВА 1. ОБЩИЕ СВЕДЕНИЯ О ТЕРПЕНОВЫХ
УГЛЕВОДОРОДАХ И ИХ ПРОИЗВОДНЫХ
1.1 Классификация терпенов и их производных
1.2 Образование терпенов и смоляных кислот в растениях
1.3 Значение терпенов и смоляных кислот для промышленности
1.4 Физические свойства терпенов
1.5 Химические свойства терпенов
1.6 Способы идентификации терпенов и их производных
ГЛАВА 2. ПРОГНОЗ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ В ПРОГРАММЕ PASS ONLINE
2.1 Результаты расчета биологической активности
ЗАКЛЮЧЕНИЕ
СПИСОК ЛИТЕРАТУРЫ
Терпены и их производные являются обязательной составной частью почти всех эфирных масел, которые относятся к продуктам, известные еще в древности. Способы выделения эфирных масел из растений просты и ими уже давно пользуются в производстве.
Успехи, которые достигнуты в области химии терпенов, находятся в тесной связи с развитием органической химии. Со времени разработки А. М. Бутлеровым теории строения органических веществ появилась возможность быстрого развития химии терпенов, как, впрочем, и всех других областей органической химии.
Термин терпены применяют для обозначения соединений, которые содержат целое число изо-С5–фрагментов, при этом независимо содержаться ли в молекуле другие элементы. Терпеноиды – это органические соединения, содержащие помимо углерода и водорода еще и кислород, построенный из 22 изопреновых фрагментов, связанных между собой. Это исключительно многочисленный (больше 10 000 разновидностей) и многообразный по химическому строению класс природных соединений. К таким соединениям можно отнести: спирты, эфиры, альдегиды кетоны, хиноны. Терпены и терпеноиды распространены в растительном мире, к ним относятся: эфирные масла почти всех пахнущих растений, смолообразование хвойных растений под общим названием «живица». Живицы хвойных являются наиболее богатыми источниками самых различных терпенов.
Актуальность темы: значимость изучения данной темы имеет свое практическое, научное и теоретическое обоснование, так как терпены и их соединения имеют большое значение. В результате многочисленных соединений, осуществленных химиками и технологами, было установлено не только строение природных терпенов и терпеноидов, но также найдены пути синтеза их заменителей из доступных видов сырья. Возникли новые виды промышленности, возникло производство синтетических соединений данного семейства.
Цель работы:
-изучение строения и свойств терпенов и их производных;
-изучить принцип работы программы PASS Online;
-компьютерное прогнозирование спектра биологической активности терпенов и их производных в программе PASS Online.
Для решения цели необходимо выполнить следующие задачи:
-составить обзор литературы по теме исследования;
-изучить строение и свойства терпенов, а также структуру и состав;
-рассмотреть методы получения и применения терпенов и его производных;
-провести расчет биологической активности некоторых представителей терпенов в программе PASS Online.
Предмет исследования: терпены и терпеноиды.
Объект исследования: программа PASS Online.
Терпены – углеводороды, относятся к обширному классу природных соединений изопреноидов. Терпены являются обязательной составной частью почти всех эфирных масел. Экстрактивные вещества, выделяемые из листьев, плодов и других частей растений с помощью различных органических растворителей, в значительной степени состоят из терпенов. Особенно разнообразен состав терпеновых соединений, образуемых хвойными древесными породами. Монотерпены встречаются в очень многих эфирных маслах, например: камфен в масле можжевельника, петигрейн в масле сосны; дипентен в масле бергамота, кориандра, лимона; лимонен в масле бергамота, лимона, апельсина; пинен в масле кориандра, эвкалипта, сосны, розмарина; сильвестрен в масле кипариса, сосны и во многих других древесных маслах.
Терпены обладают антисептическим, болеутоляющим и согревающим кожу действием. Некоторые терпены широко используются в фармацевтической индустрии. Например, цитраль используют как антисептик и противовоспалительное средство. Он входит в состав лекарственных средств для глаз, применяется как душистое вещество в парфюмерии и ароматизатор в пищевой промышленности. Ментол используется в фармацевтических препаратах, предназначенных для лечения простуды, ревматизма, снятия мышечных болей, а также в составах косметических средств [Беликов В.Г. ,2007, с.327-336].
Скипидарное терпентинное масло используют в мазях для лечения травм и их последствий, ушибов и растяжений. Препараты скипидара при ревматоидном полиартрите проявляют мощное противовоспалительное действие. Химические свойства терпенов определяются, главным образом, наличием двойных связей и напряженных трех- и четырехчленных циклов.
Классифицируют терпены и терпеноиды по составу (по числу изопреновых звеньев) на монотерпены, сесквитерпены, ди-, сестер-, три-, тетра- и политерпены (Табл 1.1). Также классификация по строению углеродного скелета подразделяют на ациклические и циклические терпены.
Таблица 1.1
Классификация терепена и терпеноида

Примером ациклических монотерпенов являются структурные изомеры оцимен и мирцен (Рис 1.1). Это терпеновые УВ эфирного масла хмеля. Запись строения данных и других ациклических монотерпенов возможна в разных конформациях их молекул.
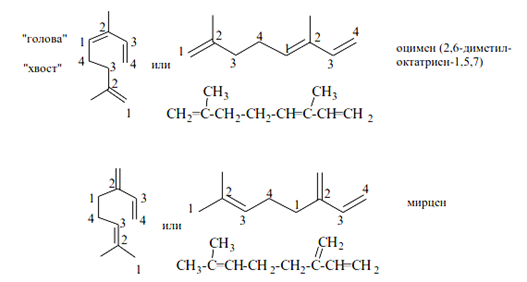
Рисунок 1.1 Структурные изомеры оцимен и мирцен
Моноциклические монотерпены. Родоначальным углеводородом этого класса терпенов и терпеноидов является ментан. Его строение соответствует "изопреновому правилу" [Майо П., 1963, с.494]. Важны производные ментана, которые представлены на рисунке 1.2. Например, лимонен (ментадиен-1,8), ментол (ментанол-3), терпин (ментадиол-1,8).
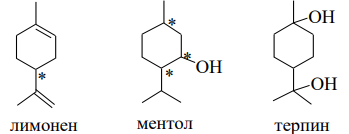
Рисунок 1.2 Производные ментана
Бициклические монотерпены многообразны по строению (Рис 1.3). Их классифицируют по строению изомерных друг другу структур. Более известны соединения ряда пинана и ряда камфана (борнана). Структура пинана образована конденсацией четырех и шестичленных циклов, в структуре камфана объединились два пятичленных цикла.
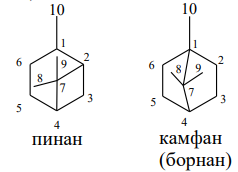
Рисунок 1.3 Бициклические монотерпены
Производными пинана и камфана являются a-пинен, стереоизомерные изоборнеол (камфанолы-2), борнеол и камфара (Рис 1.4).
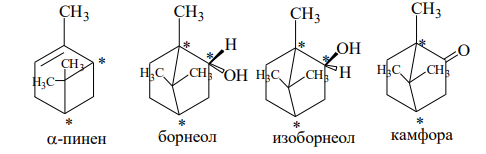
Рисунок 1.4 Производные пинана и камфана
Характерными реакциями для данного класса природных органических соединений являются окисление, присоединение, изомеризация углеродного скелета, в том числе и с раскрытием цикла. Реакции окисления терпенов изучались на различных соединениях, и многие процессы получения окисленных производных терпенов реализованы в промышленных масштабах для получения широкого набора ценных веществ [Майо П., 1963, с.494].
В настоящее время не установлено, каким образом образуются терпены и смоляные кислоты в растениях. Основой для образования терпенов служат ацетальдегид и ацетон. Конденсируясь, они образуют b-метилкротоновый альдегид, две молекулы которого дают цитраль.
Восстановлением цитраля образуется спирт гераниол или его диастереоизомер нерол. Эти два вещества и являются основой всех терпенов и смоляных кислот (Рис 1.5). Получение гераниола может быть представлено следующей схемой:
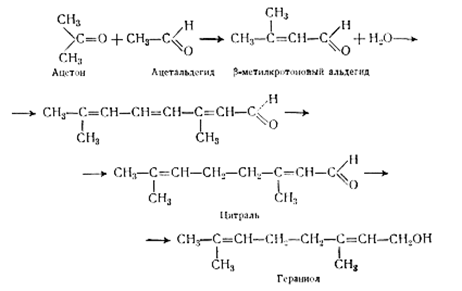
Рисунок 1.5 Схема образования цитраля и гераниола
Исходя из формулы гераниола, Рид построил схемы образования фелландрена, сабинена, терпинолена, Д3-карена и других терпенов [Никитин В.М., 1952, с.347]. Аскан основой для синтеза терпенов считал уксусный альдегид и ацетон, из которых образуется изопрен. Путем дальнейших превращений из изопрена получаются различные терпены (Рис 1.6). Образование, например, лимонена он представляет в виде следующей схемы:

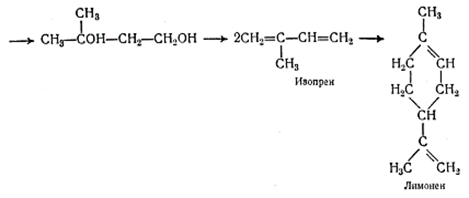
Рисунок 1.6 Схема образования лимонена
Синтез смоляных кислот (С20Н30О2) в растениях осуществляется путем полимеризации одной молекулы винилакриловой кислоты и трех молекул изопрена (Рис 1.7) [Никитин В.М., 1952, с.347].
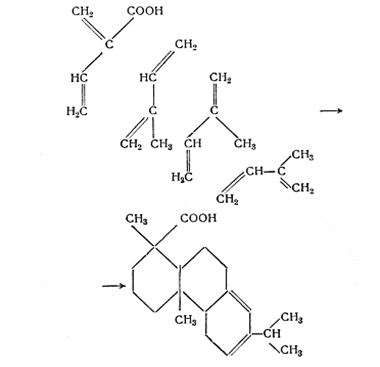
Рисунок 1.7 Синтез смоляных кислот
Как указывалось, терпены являются главной составной частью разных эфирных масел. С давних пор люди научились добывать эти вещества, содержащиеся в растениях. Из эфирных масел изготовляют духи, помады и прочие парфюмерные изделия. Некоторые эфирные масла используют в медицине в качестве лекарственных средств. Наибольшее значение для промышленности имеет скипидар, который получают из разных пород хвойных деревьев. Скипидар применяется в качестве растворителя для лаков и красок [Войткевич С.А. ,1994, с.594].
В настоящее время отдельные терпены, содержащиеся в скипидарах и эфирных маслах, служат сырьем для синтеза ценных химических продуктов. Из скипидара, например, получают: камфору, терпинеол, терпингидрат, флотационные масла (являющиеся смесью продуктов окисления терпеновых углеводородов, содержащихся в скипидаре).
Скипидары используют также для получения смол, лаков, различных душистых веществ, для получения метилстирола, синтетического каучука и многих других продуктов. Однако следует признать, что химическая природа терпенов до сих пор не использована промышленностью в достаточной степени и для этого потребуется еще большая работа химиков и технологов. Из природных продуктов, содержащих смоляные кислоты, наибольшее значение имеет канифоль, о способах получения которой будет сказано ниже. Большие количества канифоли потребляет лакокрасочная, бумажная и другие отрасли промышленности. Если раньше канифоль применяли обычно без всякой дополнительной химической обработки, то теперь большую роль начинают приобретать продукты химической переработки канифоли, более ценные, чем сама канифоль. В настоящее время разработаны методы получения гидрированной, хлорированной, окисленной канифоли, этерифицированной различными спиртами, а также полимеризованной канифоли. В результате изучения химических свойств смоляных кислот удалось расширить применение канифоли разных отраслях промышленности. [Никитин В.М., 1952, с.347]
Терпены и терпеноиды широко применяют в производствах парфюмерных композиций, косметических изделий, бумаги и картона. Применяют как пищевые эссенции, лекарственные средства, растворители, пластификаторы, инсектициды, например, полихлорпинен и полихлоркамфен, флотационное масло, иммерсионные жидкости и др. Медицинское применение терпеноидов основано на их антисептических, дезинфицирующих свойствах.
Все терпеноиды обладают спазмолитическим действием, седативные, отхаркивающие средства (терпингидрат), противовоспалительные и бактерицидные, возбуждающие сердечную деятельность и дыхание (камфора). Монотерпены оказывают бактерицидное, мочегонное, возбуждающее действие; обладают антивирусными свойствами; применяются в качестве фунгицидов (убивают грибки), антисептики, инсектициды. Полезные свойства сесквитерпенов достаточно разнообразны. Некоторые из них обладают приятным и устойчивым запахом, что позволяет использовать их в парфюмерии (пачулевый спирт, эфиры фарнезола, санталол) в качестве душистых компонент и фиксаторов запаха. Они оказывают обезболивающее, бактерицидное, противовоспалительное, успокаивающее, противовирусное действие; применяются как антибиотики, антисептики, противогрибковые средства; снимают мышечные боли (спазмолитики); понижают кровяное давление. По многим данным перспективными в качестве лекарственных препаратов являются сесквитерпеновые лактоны.
Спектр их действия достаточно широк: они обладают бактерицидной, фунгицидной, антифидантной и аттрактантной активностью; проявляют свойства регуляторов роста растений.
Биологическая активность дитерпенов ярко выражена. Они очень часто проявляют цитотоксическую активность, например, таксол – это потенциальное противовоспалительное лекарство. Некоторые дитерпеноиды обладают росторегуоирующим действием в растениях, проявляют антифунгицидную активность и антифидантную активность и др. Природные дитерпеноиды являются ценными лекарственными препаратами.
Гликозиды тритерпеноидов, т.е. сапонины, являются поверхностно-активными веществами, образуют устойчивую мыльную пену, обладают гемолитическим действием, ядовиты для животных, дышащих жабрами. Многие тритерпеновые гликозиды являются активными компонентами лекарственных растений восточной медицины, обеспечивая им противовоспалительный эффект, цитотоксическое действие и другие [Овчинников Ю.А., 1987, с.134].
При анализе разных эфирных масел и скипидаров большую роль играет определение физических свойств полученных фракций. Перегонка смесей терпенов с целью разделения их на фракции осуществляется обычно в вакууме. Для получения наиболее сравнимых данных производят дополнительную перегонку при нормальном давлении или определяют температуру кипения иными способами. Описание этих способов дано в специальных руководствах по анализу органических веществ. Обычная перегонка при нормальном давлении не дает, в случае терпенов, резкой температуры кипения, но в качестве предварительного исследования такую разгонку можно применять с достаточным успехом.
У терпеновых углеводородов можно наблюдать кое-какие закономерности в расположении точек кипения. Значительнее всех кипят алифатические терпены - 180÷192°С. Моноциклические терпены кипят в пределах 170÷180°С. Бициклические терпены имеют пределы кипения 155÷170°С, а трициклические терпены, которые не имеют двойных связей, кипят при еще более низкой температуре. Правда, и от этого правила имеются отдельные исключения. Таким образом, по температуре кипения нельзя установить строение терпена, но ее всегда следует учитывать при установлении структуры того или иного терпена.
По величине удельного веса терпена, как и по температуре кипения, возможно сделать некоторые выводы о его строении.
Наибольшим удельным весом обладают трициклические терпены. Бициклические терпены имеют удельный вес в пределах 0,860 ÷ 0,865, моноциклические - от 0,84 ÷ 0,85, а алифатические имеют наиболее низкие значения удельных весов, колеблющиеся в пределах 0,81 ÷ 0,83.
Показатель преломления является точно и быстро определяемой константой. Способы определения его подробно описываются в специальных руководствах по физико-химическим измерениям.
Для показателя преломления терпенов также имеются некоторые случаи. Наибольшим показателем преломления обладают алифатические терпены, которые имеют три двойные связи, наименее - трициклические терпены [Гуревич П.А., Сатарова Л.Ф., Струнин Б.П. ,2008, с.108].
Большинство молекул терпенов и терпеноидов обладают асимметрическими атомами углерода. Поэтому являются оптически активными. Из-за этого для характеристики отдельных терпенов часто пользуются измерением величины вращения плоскости поляризации.
Так, например, [α]D для D-α-пинена равна + 48°, а для L- α -пинена - 48°.
В природе чаще встречаются смеси, состоящие из этих двух оптических форм, в разных количественных соотношениях. Поэтому удельное вращение для разных образцов α -пинена различно и колеблется в пределах от + 48° до -48°. То же самое явление наблюдается и в отношении других терпеновых углеводородов и их производных.
Химические свойства терпенов обусловливается прежде всего наличием двойных связей, а также напряженных трех- и четырехчленных циклов. На начальном этапе исследования, легкость раскрытия циклов и связанные изомеризационные превращения терпенов (конформационной подвижности) затрудняли изучение химических свойств.
Терпены и его производные весьма реакциоспособны: легко могут окисляться на воздухе, особенно на свету, часто превращаясь при этом в кислородосодержащие соединения. Терпены вступают во все реакции окисления, которые характерны для ненасыщенных соединений. Для терпеноидов возможны реакции окисления, которые имеют уже функциональные группы. Терпены легко окисляются кислородом воздуха, образовывая гидроперекиси (Рис 1.8). Окисление идет в α-положение по отношению к двойной связи. Лимонен этой реакции образует гидроперекись лимонена. Полученный гидроперекись в дальнейшим превращаются в карвеол и карвон. α-Пинен в таких условиях образует вербенол и вербенон, которые применяются из-за своего приятного запаха в парфюмерии:
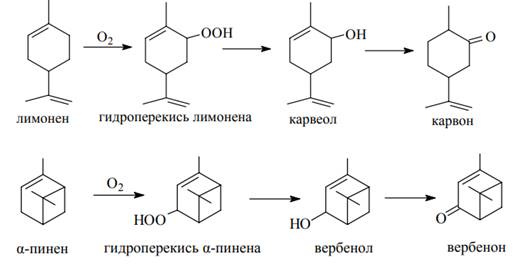
Рисунок 1.8 Окисление терпенов
с кислыми агентами при нагревании изомеризуются; диспропорционируют в присутствии катализаторов паладия, платины, никеля; легко гидрируются (Рис 1.9):
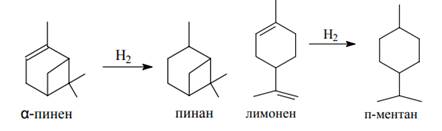
Рисунок 1.9 Гидрирование терпенов
присоединяют Hal, HHal (Рис 1.10);
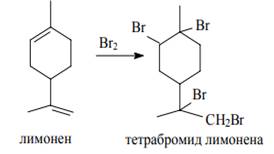
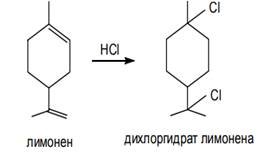
Рисунок 1.10 Реакции присоединение
при действии на карены хлороводорода (Рис 1.11) происходит разрыв трехчленного цикла в двух положениях и образуется смесь сильвестрендигидрохлорида, а также лимонендигидрохлорида:
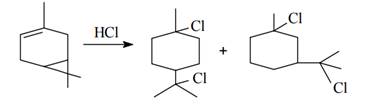
Рисунок 1.11 Действие хлороводорода на карены
α-Пинен при температуре ниже 0°С присоединяет хлороводорода, при этом образуется пиненгидрохлорид (Рис 1.12). В таких условиях изменения углеродного скелета не происходит:
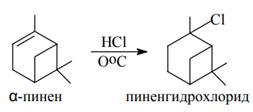
Рисунок 1.12 Образование пиненгидрохлорида
Терпены могут окисляться перманганатом калия, образовывая на первой стадии – гликоли (Рис 1.13). Таким образом, Вагнер окислением α-пинена синтезировал пиненгликоль, который в дальнейшем дал при окислении α-пиноновую, пиновую и норпиновую кислоты, соответственно [Дж. Харборна, 1968, с.342]:
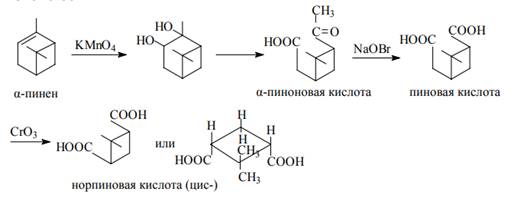
Рисунок 1.13 Окисление терпенов
Будучи ненасыщенными соединениями, терпены вступают в реакцию озонолиза, по продуктам реакции можно представить строение исходного соединения, поскольку кислород присоединяется по месту разрыва двойной связи (Рис 1.14):
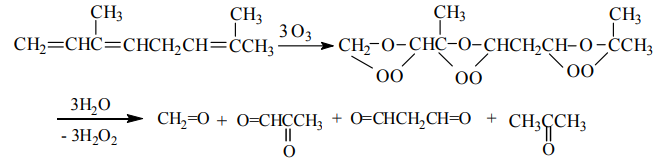
Рисунок 1.14 Озонолиз терпенов
Терпены также могут вступать в реакции окисления с участием функциональных групп (Рис 1.15). Например, нерол и гераниол при окислении образуют цитарль (альдегиды) — гераниаль и нераль:
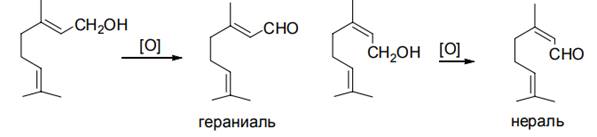
Рисунок 1.15 Реакции окисления с участием функциональных групп
При длительном нагревании без доступа воздуха (500˚С) кольца терпенов раскрываются, при этом из бициклических возможно получить моноциклические, а также алифатические (камфеновые перегруппировки). При сильном нагревании до 700˚С терпены разлагаются, образовывая сложную смесь продуктов (изопрен, ароматические УВ и др.). Из-за того, что терпены по функциональным признакам делятся на спирты, кетоны, альдегиды, по этим группам проходят характерные им реакции [Гуревич П.А., Сатарова Л.Ф., Струнин Б.П. ,2008, с.108].
Эфирными маслами называют смесь летучих, душистых веществ, которые образуются в растениях. Главной составной частью эфирных масел являются терпены и их кислородсодержащие производные, реже - ароматические и алифатические соединения. [Нестеров Д.В., 2016, с.100]
При большом многообразии терпеновых углеводородов и их производных необходимо было найти пути, которые позволили бы отличить одно вещество от другого. При большом сходстве в химическом строении и при одинаковом элементарном составе все терпеновые углеводороды довольно близки по своим физическим свойствам. И так как большинство их являются жидкостями, к ним трудно применить такой надежный метод очистки, как кристаллизация [Дж. Харборна, 1968, с.342].
Для идентификации терпеновых углеводородов и их производных получают разнообразные кристаллические производные. При этом используют химические свойства углеводородов, например наличие двойных связей, их расположение, легкость изомеризации циклов, способность к замещению водородных атомов и проч. В случае спиртов используют реакционность спиртового гидроксила, в случае альдегидов и кетонов - реакционную способность карбонила и т. д.
Для извлечения компонентов эфирных масел из растений существует несколько способов: мацерация, экстрагирование, перегонка с водяным паром, отжимание, анфлераж, а иногда сухая перегонка.
Перегонка с водяным паром. Данный способ является наиболее распространенным при получении эфирных масел из растений. Части растений, которые содержат эфирные масла, например: семена, листья, плоды, цветы, чаще всего предварительно измельченные, загружают в перегонный куб и через них пропускают водяной пар, который увлекает с собой эфирные масла. Выходя из куба, пары воды вместе с парами эфирных масел конденсируются в холодильнике и поступают в флорентин, где происходит расслаивание эфирных масел и воды (Рис 1.16). Перегонка с водяным паром широко используется как в лабораторных, так и в промышленных условиях. В данном методе температура не превышает обычно 100÷ 105°С [Писарев, Д.И., 2012, с.129].
Таким образом, терпены, которые составляют эфирные масла, мало изомеризуются. Если же перегонку провести при более высоких температурах, то в результате изомеризации, которые будут претерпевать терпены, возможно получить продукты, качественно значительно отличающиеся от тех, которые содержатся в самих растениях. Данным способом получают канифоль и скипидар из живицы различных хвойных пород. Например, если в теплое время года на сосне сделать надрез коры и заболони, то из раны сразу же начнет выделяться прозрачная смола, которую называют живицей. Живица состоит из летучих, с водяным паром, терпеновых углеводородов, называемых скипидаром, и нелетучей части, называемой канифолью, который состоит в основном из смеси изомерных смоляных кислот.
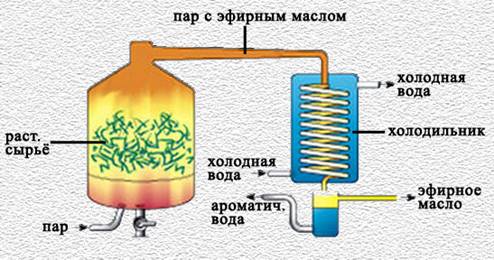
Рисунок 1.16 Перегонка водяным паром
Анфлераж. Данный метод применяют наиболее часто при извлечении эфирных масел из цветов (резеда, жасмин, ландыш, тубероза и др.). Для этого цветы насыпают на стеклянные листы (покрытые слоем чистого, лишенного запаха, жира), заключенные в деревянные рамы. Эфирные масла из цветов поглощаются слоем жира в течение 1 ÷ 3 суток. Затем увядшие цветы снимают, насыпают слой свежих цветов. Такую операцию повторяют 25÷30 раз, до тех пор, пока жир полностью не насытится эфирными маслами (Рис 1.17). Таким образом получают так называемую помаду, которая и поступает в продажу. Из помады эфирные масла могут быть выделены чистым спиртом, а также перегонкой с водяным паром.

Рисунок 1.17 Анфлераж растений
Мацерация. Подобен анфлеражу способ извлечения эфирных масел. Отличие состоит в том, что процесс идет уже при температуре 50 ÷ 70°, при которой жир становится жидким. Извлечение таким способом протекает быстрее. Помада, которая получена этим методом, по качеству близка к той, которая получается способом анфлеража. Из этой помады эфирные масла могут быть выделены таким же способом, как указывалось выше [Пономарёв, Д. А., 2014, с.56].
Экстракция также может быть использована для получения эфирных масел. Для экстракции применяют обычно серный эфир, петролейный эфир, дихлорэтан, и некоторые другие растворители.
Экстракцию эфирных масел из растений производят в специальных сосудах, называемых экстракторами, в которые загружают цветы или другие части растений и заливают их растворителем (Рис 1.18). Эфирное масло переходит при этом в растворитель. В результате экстракции получают экстракты консистенции растительного масла. Из таких экстрактов эфирное масло выделяют обычно отгонкой растворителя или каким-либо другим способом [Пигулевский Г.В. 1949, с.234].
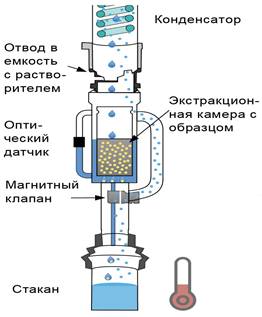
Рисунок 1.18 Экстрактор Сокслета
Выжимание применяют, например, при получении лимонных, бергамотных или других цитрусовых масел. Для этой цели корки плодов, богатые маслом, выжимают ручным способом или при помощи специальных прессов. Получающееся масло отделяют от воды, слизи и других примесей путем отстаивания и фильтрации.
Сухая перегонка. Этот способ сравнительно редко применяется для получения ценных эфирных масэл. Чаще к нему прибегают, например, для получения скипидара из древесины хвойных пород. В результате повышенной температуры, имеющей место при сухой перегонке, наблюдаются процессы изомеризации терпенов, находящихся в растениях, что является не всегда желательным явлением [Сур, С.В., 1990, с.50].
Полученные тем или иным способом эфирные масла обычно необходимо бывает обезводить. Для высушивания эфирных масел чаще применяют безводный сернокислый натрий. Хлористый кальций во многих случаях неприменим вследствие того, что некоторые спирты терпенового ряда дают с ним комплексные соединения.
Для разделения эфирных масел на составные части, т. е. для получения из них индивидуальных терпенов или их производных, высушенные эфирные масла подвергают фракционированной перегонке.
Чтобы возможно меньше изомеризовать терпеновые углеводороды,
перегонку ведут обычно в вакууме [Семёнов А.А., Карцев В. Г., 2009, Т-1].
Вследствие того, что эфирные масла представляют собой, как правило, сложные смеси веществ, с близкими друг к другу температурами кипения, то, даже при пользовании хорошими ректификационными колонками, после первой разгонки получается довольно грубое разделение и полученные фракции имеют сравнительно широкие пределы кипения. После первой перегонки проводят вторую из колбы меньшего размера.
В результате второй разгонки отбирают фракции веществ с более узкими пределами кипения. В случае необходимости такую перегонку повторяют несколько раз.
Спектром биологической активности мы предполагаем совокупность различных фармакологических эффектов, биохимических действий на организм, которые может проявить вещество при взаимодействии с биологическим объектом.
Новейшие лекарственные препараты находят при помощи скрининга синтезируемых соединений, которые выбираются для медико-биологических анализов те, которые достаточно эффективны по их прямому назначению, а также наименее вредны для организма. Большая часть новых синтезированных соединений оказывается в ряду неперспективных для фармакологии из-за ряда причин: низкой растворимости в воде, высокой токсичности, мутагенности, опасного влияния на организм продуктов распада.
Достаточно мощный метод компьютерного прогнозирования биологической активности органических соединений является метод, который основан на Байесовской вероятности.
Программа PASS (Prediction of Activity Spectra for Substances) – данная программа способна прогнозировать спектр биологической активности известных хим. соединений [Газетдинов Р.Р., Семенова Т.В., 2019, с.32-34].
Работа PASS основана на предположении, что Активность = Структура, в свою очередь, структура соединения описывается отдельными дескрипторами (функциональными элементами - Mulilevel Neighbourhoods of Atoms) – функциональными группами атомов, радикалами.
Результат прогноза биологической активности выдается в виде списка вероятных видов активности (вероятность наличия - Pa, отсутствие каждого вида активности Pi, значения которых варьируются 0÷1) (Рис 2.1).
Чем больше для конкретной активности значение Pa и чем меньше значение Pi, тем больше шанс обнаружить данную активность в эксперименте (Predictive services PASS online. URL. http://www.pharmaexpert.ru/PASSOnline/index.php).
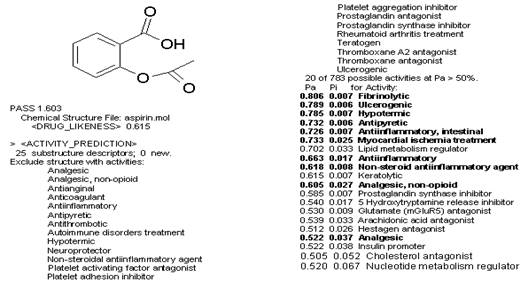
Рисунок 2.1 Химическая структура и вероятный спектр биологической активности ацетилсалициловой кислоты
Основываясь на данных компьютерного скрининга, исследователь может:
-выявить новые эффекты, а также механизм действия для ранее изученных веществ;
-установить, какие тесты наиболее пригодны для изучения биологической активности химического соединения;
-отобрать вероятную базовую структуру нового лекарственного средства с требуемым биологическим действием.
Данная система позволяет получить спектр биологической активности многих веществ на персональном компьютере менее чем за минуту. Так как прогноз выполняется по структуре химического соединения, он может быть выполнен на стадии планирования синтеза
Для прогнозирования спектра биологической активности индивидуальных соединений на основе их структурной формулы использовалась компьютерная система PASS ONLINE. Так как для описания структур органических соединений в программе PASS ONLINE выбрана двумерная структурная формула, был использован редактор химической графики ACD/ChemSketch (Рис 2.2).
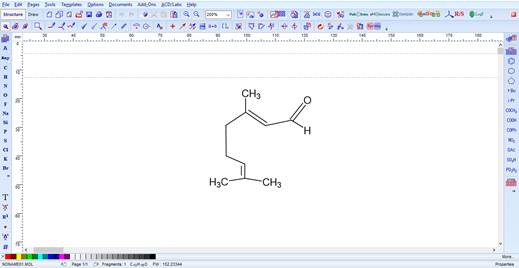
Рисунок 2.2 Химический редактор ACD/ChemSketch
Благодаря использованию программы PASS online был выполнен предварительный компьютерный скрининг природных соединений.
Прогнозирование спектра биологической активности было проведено для трех индивидуальных соединений терпенов и их производных (Табл 2.1):
- таксол – это дитерпен, потенциальное противовоспалительное лекарство;
- ментол – терпеноид, является основной составляющей рефлекторного сосудорасширяющего средства валидол;
- ингенол – это дитерпен, активное вещество против ВИЧ.
Таблица 2.1
Структурные формулы терпенов и терпеноидов
|
Название соединения |
Структурная формула |
|
Таксол (дитерпены) |
|
|
Ментол (терпеноид) |
|
|
Ингенол (дитерпены) |
|
Было выявлено, что следующие соединения, возможно, проявляют биологическую активность с высокой вероятностью.
Таблица 2.2 Возможная биологическая активность цитраля
|
Название соединения |
Pa |
Pi |
Активность |
|
Таксол |
0,977 |
0,003 |
Респираторный аналептик |
|
0,974 |
0,004 |
Противоопухолевый
|
|
|
0,925 |
0,003 |
Противоопухолевый (колоректальный рак) |
|
|
0,923 |
0,003 |
Противоопухолевые препараты (рак толстой кишки) |
|
|
0,917 |
0,003 |
Противоопухолевые препараты (рак груди) |
|
|
0,805 |
0,004 |
Противоопухолевые (рак легких) |
|
|
0,788 |
0,005 |
Антиканцерогенный |
Таблица 2.3 Возможная биологическая активность ментола
|
Название соединения |
Pa |
Pi |
Активность |
|
Ментол |
0,936 |
0,002 |
Вазопротектор |
|
0,923 |
0,003 |
Ингибитор ацилкарнитингидролазы |
|
|
0,759 |
0,005 |
Противозудное |
|
|
0,725 |
0,005 |
Лечение аденоматозного полипоза |
|
|
0,703 |
0,016 |
Иммунодепрессант |
|
|
0,679 |
0,004 |
Противозудное, аллергическое |
|
|
0,665 |
0,008 |
Противовирусный (грипп) |
Таблица 2.4 Возможная биологическая активность фарнезола
|
Название соединения |
Pa |
Pi |
Активность |
|
Ингенол |
0,905 |
0,001 |
Актиническое (солнечное) лечение кератозов |
|
0,886 |
0,000 |
Стимулятор протеин киназы C |
|
|
0,775 |
0,015 |
Противоопухолевый |
|
|
0,696 |
0,008 |
Дерматологические |
|
|
0,757 |
0,005 |
Антилейкемический |
|
|
0,585 |
0,004 |
Противоопухолевый (плоскоклеточный рак) |
|
|
0,565 |
0,004 |
Противоопухолевый (карцинома) |
Естественно, что при анализе данных веществ, прогнозируемых программой PASS ONLINE, необходимо учитывать реальные возможности экспериментального тестирования.
Необходимо отметить, что данная программа не может предсказать, станет ли конкретное соединение лекарственным препаратом, поскольку это зависит от ряда различных факторов. Однако, предсказание может помочь определить, на какие виды биологической активности следует протестировать анализируемое соединение в первую очередь.
По выполненной работе можно сделать выводы:
-терпены и их производные являются обязательной составной частью почти всех эфирных масел;
-терпены обладают антисептическим, болеутоляющим, противовоспалительным и согревающим кожу действием. Некоторые терпены широко используются в фармацевтической индустрии;
-терпены и терпеноиды широко применяют в производствах парфюмерных композиций, косметических изделий, бумаги и картона. Применяют как пищевые эссенции, лекарственные средства, растворители, пластификаторы, инсектициды, например, полихлорпинен и полихлоркамфен, флотационное масло, иммерсионные жидкости и другие;
-большинство молекул терпенов и терпеноидов обладают асимметрическими атомами углерода. Поэтому являются оптически активными;
-для извлечения компонентов эфирных масел из растений существует несколько способов: мацерация, экстрагирование, перегонка с водяным паром, отжимание, анфлераж, а иногда сухая перегонка;
-новейшие лекарственные препараты находят при помощи скрининга синтезируемых соединений, которые выбираются для медико-биологических анализов те, которые достаточно эффективны по их прямому назначению, а также наименее вредны для организма;
-при анализе данных веществ, прогнозируемых программой PASS ONLINE, необходимо учитывать реальные возможности экспериментального тестирования.
1. Беликов В.Г. Фармацевтическая химия: учебное пособие/В.Г.Беликов-Москва:2007. 327-336 с.
2. Войткевич С. А. 865 душистых веществ для парфюмерии и бытовой химии. - М.: Пищевая промышленность, 1994. -594 с.
3. Газетдинов Р.Р., Семенова Т.В. Расчет биологической активности азотсодержащих органических соединений в программе PASS // Доклады Башкирского университета. 2019. Т. 4. № 1. С. 32-34.
4. Гуревич П.А., Сатарова Л.Ф., Струнин Б.П. Введение в химию биологически активных соединений. Казань: Изд-во КГТУ, 2008. -108 с.
5. Дж. Харборна. Биохимия фенольных соединений; пер. с англ. – М., 1968. -342 с.;
6. Майо П., Терпеноиды, пер. с англ., М., Изд-во иностранной литературы, 1963. – 494с.;
7. Никитин В.М. Химия терпенов и смоляных кислот/ В. М. Никитин. М: Гослесбумиздат, 1952.- 347 с;
8. Нестеров Д.В. Биологически активные вещества: терпены и терпеноиды, флавоноиды: учебное пособие для студентов фармацевтического факультета и факультета промышленной технологии лекарств по дисциплинам: «Химия биологически активных веществ» и «Химия природных соединений». – СПб.: Изд-во СПХФА, 2016. – 100 с;
9. Овчинников Ю.А. Биоорганическая химия, Москва, «Просвещение», 1987 – 134 с.
10. Писарев, Д.И. Методы выделения и анализа эфирных масел / Д. И. Писарев, О.О. Новиков //Научные ведомости Белгородского государственного университета. Серия: Медицина. Фармация. - 2012. -№10-2.– Т.18. – 129 с;
11. Пономарёв, Д. А. Основы химии терпенов: учебное пособие / Д. А. Пономарёв, Э. И. Фёдорова; 2014. - 56 с.
12. Пигулевский Г.В. Химия терпенов. – Л.: Изд-во ЛГУ, 1949. 234 c;
13. Пигулевский Г. Ф. Терпены и кумарины. М., Наука, 1965. – 396 с.;
14. Племенков В. В. Введение в химию соединений, 2001 - 376 с.
15. Семенов А.А. Терпены хвойных растений, Новосибирск, 1987.- 79 с.
16. Семёнов А. А., Карцев В. Г. Основы химии природных соединений. - М.: ICSPF, 2009. -Т.1.
17. Семёнов А. А., Карцев В. Г. Основы химии природных соединений. - М.: ICSPF, 2009. -Т.2.
18. Сур, С.В. Методы выделения, идентификации и определения терпеновых соединений/ С.В. Сур //– 1990. – Т. 26, вып. 1. 42-50 с.
19. Predictive services PASS online [Электронный ресурс]. - Режим доступа: http://www.pharmaexpert.ru/PASSOnline/index.php, свободный. - (дата обращения: 18.06.2021).
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.