
Тест по темам «Теоретические основы химии», «Предмет химии», «Основные понятия и законы химии»
Вариант 1
Задание 1.
Массовые доли углерода, водорода и кислорода в органическом веществе равны соответственно 39,56%, 7,69% и 52,75%. Относительная плотность его паров по гелию составляет 45,5. Определите формулу этого вещества и назовите его.
А) Сорбит
Б) Глюкоза
В) Сахароза
Г) Глюконовая кислота
Задание 2.
При взаимодействии бутана объемом 13,44 дм3 с 288 г брома при освещении с выходом 73% образуется бромзамещенный алкан. Вычислите его массу (г). Ответ округлите до целого числа.
Ответ: ___ г.
Задание 3.
Массовые доли углерода, водорода и кислорода в органическом веществе равны
соответственно 40%, 6,67% и 53,33%. Относительная плотность паров этого вещества по гелию равна 15. Установите формулу этого вещества и назовите его
А) уксусная кислота
Б) муравьиная кислота
В) пропановая кислота
Г) стеариновая кислота
Задание 4.
Назовите вещество, имеющее следующую структурную формулу:
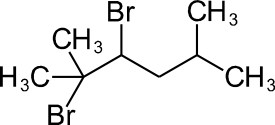
А) 2,3-дибром-2,5-диметилгексан
Б) 2,3-бром-2,5-метилгексан
В) 2,3-дибром-2,5-диметилгептан
Г) 2,4-диметил-4,5-дибромгептан
Задание 5.
Назовите вещество, имеющее следующую структурную формулу:
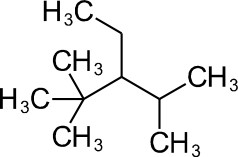
А) 2,2,4-триметил-3-этилпентан Б) 2,2,4-метил-3-этилпентан
В) 2,4,4-триметил-3-этилпентан
Г) 3-этил-2,4,4-метилпентан
Задание 6.
Составьте структурную формулу 1-бром-2,3,4-триметилпентана и укажите число σ-связей в его молекуле.
Ответ: __.
Задание 7.
Массовые доли углерода и хлора в соединении равны 7,8% и 92,2% соответственно. Установите формулу этого вещества, если известно, что его молярная масса в 5,5 раз больше, чем молярная масса этилена.
А) CCl4
Б) C2Cl4
В) C2Cl6
Г) C2Cl2
Задание 8.
Выберите верные утверждения, характеризующие метанол. А) Имеет молекулярную формулу C2H5OH .
Б) Соответствует общей формуле одноатомных спиртов СnH2n + 2О .
В) Представляет собой жидкость (н. у.) с характерным алкогольным запахом, растворим в воде, ядовит.
Г) С Cu(OH)2 образует ярко-синий раствор.
Д) В промышленности получают из синтез-газа.
Е) Тривиальное название древесный спирт; используется в производстве пластмасс, лекарственных препаратов, является хорошим растворителем.
Задание 9.
Из уксусной кислоты с выходом 92% получили аминоуксусную кислоту массой 89,7 г. На нейтрализацию избытка уксусной кислоты после отделения ее от продуктов реакции необходимо 52,2 г раствора гидроксида натрия (ω(NaOH) = 23%). Определите исходную массу (г) уксусной кислоты.
А) 96 г
Б) 92 г
В) 90 г
Г) 106 г
Задание 10.
При окислении 23,2 г неизвестного кислородсодержащего органического вещества получили 29,6 г насыщенной одноосновной карбоновой кислоты. При добавлении к этой порции кислоты питьевой соды NaHCO3 происходит выделение газа объемом 8,96 дм3. Определите исходное органическое вещество.
А) Пропаналь
Б) Этаналь
В) Метанол
Г) Этанол
Задание 11.
Определите массовую долю (%) ацетилена в смеси его с этиленом, если при сжигании 40,32 дм3 этой смеси выделилось 80,64 дм3 углекислого газа. Ответ округлите до целого числа.
Ответ: m = __%.
Задание 1. Правильный ответ: А
Задание 2. Правильный ответ: 129
Задание 3. Правильный ответ: А
Задание 4. Правильный ответ: А
Задание 5. Правильный ответ: А
Задание 6. Правильный ответ: 25
Задание 7. Правильный ответ: А
Задание 8.
Правильный ответ: Б, В, Д, Е
Задание 9. Правильный ответ: А
Задание 10. Правильный ответ: А
Задание 11.
Правильный ответ: 71
Тест по темам «Теоретические основы химии», «Предмет химии», «Основные понятия и законы химии»
Вариант 2
Задание 1.
При сгорании органического вещества массой 54,56 г образовались 69,44 дм3 углекислого газа и 66,96 г воды. Определите это вещество и вычислите относительную плотность его паров по водороду.
Ответ: DH2 = __.
Задание 2.
Составьте структурную формулу 1,1-дихлор-2,3,3-триметилбутана и укажите число σ-связей в его молекуле.
Ответ: __.
Задание 3.
Массовая доля углерода в молекуле алкана равна 80%. Определите его формулу и дайте ему название. А) этан
Б) бутан
В) пропан
Г) пентан
Задание 4.
При сплавлении пропионата натрия CH3CH2COONa массой 13 г с гидроксидом натрия с выходом 87% образовался углеводород. Вычислите объем (дм3) воздуха, необходимый для полного окисления полученного углеводорода. Ответ округлите до целого числа.
Ответ: __ дм3.
Задание 5.
При сплавлении ацетата натрия массой 20,75 г с гидроксидом натрия с выходом 92% образовался углеводород. Вычислите объем (дм3) воздуха, необходимый для полного окисления полученного углеводорода. Ответ округлите до целого числа.
Ответ: __ дм3.
Задание 6.
Установите соответствие между химическим знаком атома (иона) и общим числом электронов, числом электронов на внешнем слое и числом неспаренных электронов соответственно.
А) 10;8;0 Б) 12;6;0 В) 12;2;0 Г) 9;7;1 Д) 14;4;2 Е) 12;2;0
Варианты ответов:
1) S4+ 2) Mg 3) F– 4) Si
|
Ответ |
А |
Б |
В |
Г |
Д |
Е |
|
|
|
|
|
|
|
Задание 7.
Найдите верные утверждения.
А) Число электронных слоев в атоме соответствует номеру периода, в котором находится химический элемент.
Б) р-элементы – это элементы, которые имеют полностью заполненные p-орбитали.
В) Между двумя атомами может образоваться несколько σ- и только одна π-связь.
Г) σ-связь образована при перекрывании как s- так и p-орбиталей.
Д) Молекула, в которой атомы связаны ковалентными полярными связями, не всегда является диполем.
Е) Наличие на внешнем электронном слое свободных орбиталей и переход на них электронов является причиной переменной валентности химических элементов.
Задание 8.
Крахмал, полученный из 198,5 г кукурузы, подвергли гидролизу(выход продукта гидролиза составил 72%). К продукту гидролиза добавили дрожжи. В результате протекающей реакции выделился газ объемом 26,88 дм3. Вычислите массовую долю крахмала в кукурузе. А) 68%
Б) 66%
В) 70%
Г) 72%
Задание 9.
Установите соответствие между названием вещества и реагентом, с помощью которого можно его определить (провести качественную реакцию).
А) +Cu(OH)2 – окрашивание раствора в синий цвет Б) +Br2 – выпадение осадка белого цвета В) +Na – выделение газа Г) +O2 – горит коптящим пламенем Д) +CuO – изменение цвета проволоки с черного на красный Е) +KMnO4, H2O – обесцвечивание раствора
Варианты ответов:
1) Бензол 2) Этилен 3) Фенол 4) Глицерин 5) Этанол
|
Ответ |
А |
Б |
В |
Г |
Д |
Е |
|
|
|
|
|
|
|
Задание 10.
Массовая доля кислорода в составе сложного эфира 31,4%. При взаимодействии 13,8 г спирта, входящего в состав эфира, с избытком натрия выделяется 3,36 дм3 газа. Определите формулу сложного эфира и назовите его.
А) этиловый эфир пропановой кислоты
Б) пропиловый эфир уксусной кислоты
В) этилацетат
Г) метилпропионат
Задание 11.
В результате взаимодействия насыщенного одноатомного спирта массой 2,22 г с
бромоводородом образовался бромалкан массой 4,11 г. Определите формулу спирта и назовите его.
А) бутанол
Б) метанол
В) этанол
Г) пропанол
Задание 1. Правильный ответ: 44
Задание 2. Правильный ответ: 22
Задание 3. Правильный ответ: А
Задание 4. Правильный ответ: 44
Задание 5. Правильный ответ: 50 Задание 6.
|
Правильный ответ: |
А |
Б |
В |
Г |
Д |
Е |
|
3 |
|
1 |
|
4 |
2 |
|
|
Задание 7. Правильный ответ: А, Г, Д, Е Задание 8. Правильный ответ: А Задание 9. |
|
|
|
|
|
|
|
Правильный ответ: |
А |
Б |
В |
Г |
Д |
Е |
|
4 |
3 |
|
1 |
5 |
2 |
|
Задание 10. Правильный ответ: А
Задание 11.
Правильный ответ: А
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.