
Дата проведения__________
Класс 8
Матиев З.С.
Тема: Вычисления объёма, количества вещества газа по его известному количеству вещества или объёму
Цель
урока. Сформировать понятие о молярном объеме газов. Научить
производить расчеты, используя закон Авогадро и следствие из него.
Научить вычислять по химическим уравнениям объем газа (по известной массе или
количеству вещества), массу или количество вещества (по известному объему газа)
одного из вступивших в реакцию или получившихся в результате реакции веществ.
Сформировать понятие об относительной плотности газов. Научить производить
расчеты, используя понятие «относительная плотность газов». Сформировать умение
вычислять объемы газов, участвующих в химических реакциях.
Ход уока
1.
Организационный момент
2. Обсуждение результатов контрольной работы.
3. Актуализация опорных знаний
Обозначения:
n- количество вещества, (моль, кмоль, ммоль)
m – масса, ( г, кг, мг)
M – молярная масса, ( г/ моль, кг/ кмоль, мг/ ммоль)
V – объем, (л, м3, см3, мл)
Vм – молярный объем (л/ моль, м3/ кмоль, мл/ ммоль) для любого газа при нормальных условиях (н.у.) равен 22,4 л/моль
N- число частиц (атомы, молекулы, ионы)
NА- постоянная Авогадро равна 6,02.1023 частиц.моль-1
n= m/M n= V/VM n= N/NA
Задача 1. Сколько молекул озона О3 содержится в 72 г его?
|
Дано: m(О3)= 72г |
Решение 1) n (О3)=m/ M= 72г:48г/моль=1,5моль M(О3)=16.3= 48 г/моль 2) N (О3)=n NA= =1,5моль.6,02.1023молекул.моль-1=9.1023молекул Ответ: N (О3)= 9.1023молекул
|
|
Найти: N (О3)-? |
Задача 2. Какой объем занимают (при н.у.) 280 кг азота?
|
Дано: m(N2) = 280кг |
Решение 1. n (N2)=m/ M= 280кг:28кг/ кмоль =10кмоль M (N2) = 14.2= 28 г/моль= 28кг/ кмоль 2. V (N2)= n .Vм =10кмоль.22,4м3/ кмоль=224 м3 Ответ: V (N2)= 224 м3
|
|
Найти: V (N2) -?
|
Задача 3. Какую массу имеют 112л (при н.у.) углекислого газа?
|
Дано: V (СО2) = 112л |
Решение 1. n (СО2)=V/ Vм = 112л/ 22,4л/моль= 5 моль 2. m (СО2) = n.M= 5моль?(12+16.2) г/ моль= 5.44=220г
Ответ: m (СО2) =220г
|
|
Найти: m (СО2)-? |
Решите самостоятельно задачи:
1. Хлориду натрия массой 5,85 г соответствует количество вещества:
1) 1 моль; 2) 0,5 моль; 3) 0,1 моль; 4 ) 0,01 моль.
2. Оксиду кальция массой 28 г соответствует количество вещества:
1) 1 моль; 2) 0,1 моль; 3 )2 моль; 4) 0,5 моль.
3. Масса 0,25 моль хлорида меди (II) равна:
1) 64 г; 2) 24,75 г; 3) 24,875 г; 4) 33,75 г.
4. Какой объем при н.у. занимают 64г оксида серы (IV)?
5. Какую массу имеют 3 • 1024 молекул углекислого газа (оксида углерода (IV))?
6. Какую массу имеют 44,8 л при н.у. угарного газа (оксид углерода (II))?
7. Какой объем занимают 6 • 1023молекул сероводорода H2S?
9. Какой объем при н.у. занимают 96г озона О3?
10. Сколько молекул хлора CI2 cодержится в 284г его?
3. Изучение нового материала
Закон Авогадро: в равных объёмах различных газов при одинаковых условиях (температуре и давлении) содержится одинаковое число молекул. (1811 г, итальянский учёный Амедео Авогадро)
Так, 6,02 ∙ 1023 молекул (1 моль) любого газа и любой смеси газов при (н.у.) занимает объём равный 22,4 л.
Такой объём называется молярным объёмом и обозначается Vm
Молярный объём – это постоянная величина для веществ – газов при нормальных условиях (н.у.):
|
Vm = 22,4 л/моль н.у. – это p = 1амт (101325 Па) t = 0 ˚C (273 К) |
1. 1 моль любого газа при н. у. занимает одинаковый объём, равный 22,4 л. Этот объём называется молярный и обозначается Vm.
2.
Количество вещества (n) — отношение объёма газа при н.
у. к молярному объёму:
n = V/Vm=> Vm измеряется в л/моль.
3. Следовательно, количество вещества
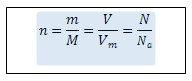
4. Дополните таблицу «Количественные характеристики веществ», делая необходимые вычисления.
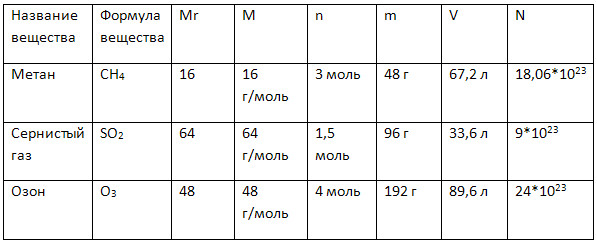
5.
Придумайте условие задачи, в которой нужно найти число молекул N, если известен
объём V.
Найти число частиц оксида азота(II), если его объём равен 67,2 л.
Решите задачу любым способом.
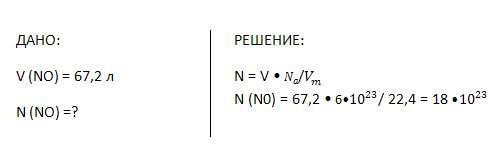
6. Вычислите массу 78,4 л (н. у.) хлора.
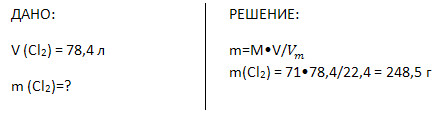
7. Найдите объём 297 г фосгена (COCl2).
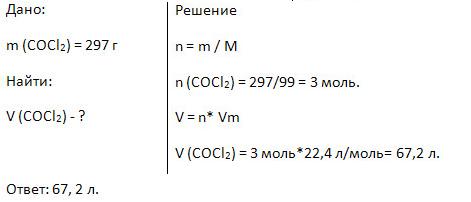
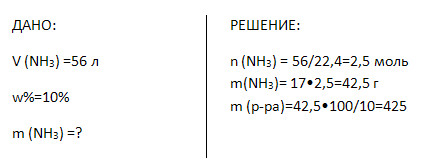
8. Вычислите массу 56 л аммиака, 10% -й водный раствор которого в медицине
известен под названием «нашатырный спирт».
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.