
• ![]() Измененние импульса молекулы или атома при каждом
столкновении со стенкой m0 – масса молекулы (атома)
Измененние импульса молекулы или атома при каждом
столкновении со стенкой m0 – масса молекулы (атома)
• ![]() Количество частиц на расстоянии d от стенки. В среднем половина этих частиц движется к стенке.
Количество частиц на расстоянии d от стенки. В среднем половина этих частиц движется к стенке.
• ![]() Количество частиц, движущихся к стенке (случайные скорости)
Количество частиц, движущихся к стенке (случайные скорости)
• ![]() Общий импульс передался стенке
Общий импульс передался стенке
• ![]() Сила удара о стенку
Сила удара о стенку
• ![]() Давление газа
Давление газа
• Средняя квадратичная скорость < v2 >
• Величина <v2> означает среднее значение квадрата средней скорости v2. Это среднее арифметическое значение.
• Возводя в квадрат скорости и извлекая квадратный корень, мы выбираем направленную составляющую скорости, и называем ее среднеквадратичной скоростью.
• Распределение скоростей в газе с использованием среднего квадрата x-составляющей скорости всех частиц.
• ![]() Наконец ... мы находим уравнение,
которое искали, используя треть среднего квадрата скорости:
Наконец ... мы находим уравнение,
которое искали, используя треть среднего квадрата скорости:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
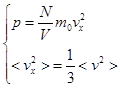
![]()
![]()
Ø Среднеквадратичная скорость
Среднеквадратичная скорость - это мера скорости частиц в газе.
Он определяется как корень квадратный из квадрата средней скорости молекул в газе (он не совсем равен средней скорости молекул).
Например:
Распределение Максвелла – Больцмана - это распределение вероятностей, используемое в физике (в частности, в статистической механике) для описания скоростей частиц в идеальных газах (для большого числа частиц).
На следующем
рисунке показано это распределение при разных температурах газообразного азота N2. Объясните графики.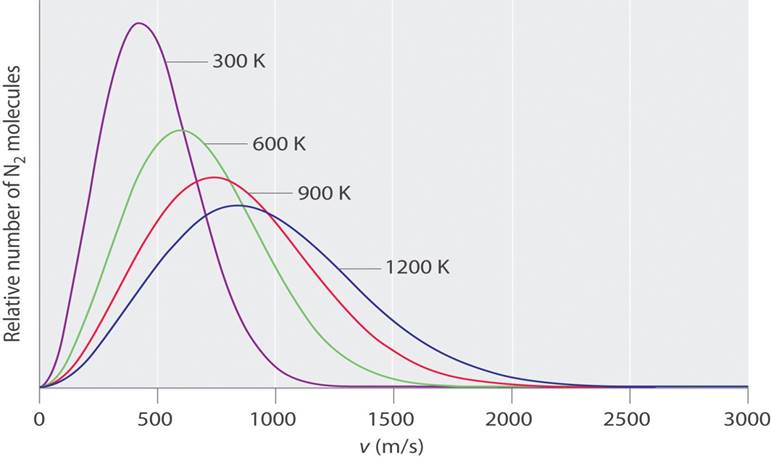
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.