
Подготовила учитель химии, биологии
Учитель ГОУ ЛНР «Краснолучская школа № 11»
Шкребтий Наталья Александровна
Моль, молярная масса
Цели:
1)Изучить новые понятия: количество вещества, молярная масса, постоянная Авогадро.
2) Научиться решать задачи с использованием этих понятий.
В химических процессах участвуют мельчайшие частицы – молекулы, атомы, ионы, электроны. Число таких частиц даже в малой порции вещества очень велико. Поэтому, чтобы избежать математических операций с большими числами, для характеристики количества вещества, участвующего в химической реакции, используется специальная единица – моль.
Моль - это такое количество вещества, в котором содержится определенное число частиц (молекул, атомов, ионов), равное постоянной Авогадро
![]()
Постоянная Авогадро NA определяется как число атомов, содержащееся в 12 г изотопа 12С:
![]()
Таким образом, 1 моль вещества содержит 6,02 • 1023 частиц этого вещества.
Исходя из этого, любое количество вещества можно выразить определенным числом молей ν (ню). Например, в образце вещества содержится 12,04 • 1023молекул. Следовательно, количество вещества в этом образце составляет:
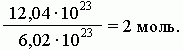
В общем виде:
![]()
где N –
число частиц данного вещества;
NA – число частиц, которое содержит 1 моль
вещества (постоянная Авогадро).
Молярная масса вещества (M) –
масса, которую имеет 1 моль данного вещества.
Эта величина, равная отношению массы m вещества к
количеству вещества ν, имеет размерность кг/моль или г/моль.
Молярная масса, выраженная в г/моль, численно равна относительной относительной
молекулярной массе Mr (для веществ атомного строения –
относительной атомной массе Ar).
Например, молярная масса метана CH4 определяется следующим
образом:
Мr(CH4) = Ar(C) + 4 Ar(H) = 12+4 =16
M(CH4)=16 г/моль, т.е. 16 г CH4 содержат 6,02 • 1023 молекул.
Молярную массу вещества можно вычислить, если известны его масса m и количество (число молей) ν, по формуле:
![]()
Соответственно, зная массу и молярную массу вещества, можно рассчитать число его молей:
![]()
или найти массу вещества по числу молей и молярной массе:
m = ν • M
Необходимо отметить, что значение молярной массы вещества определяется его качественным и количественным составом, т.е. зависит от Mr и Ar. Поэтому разные вещества при одинаковом количестве молей имеют различные массы m.
Вычислить массы метана CH4 и этана С2H6, взятых в количестве ν = 2 моль каждого.
Решение
Молярная масса метана M(CH4) равна 16 г/моль;
молярная масса этана M(С2Н6) = 2 • 12+6=30 г/моль.
Отсюда:
m(CH4)
= 2 моль • 16 г/моль = 32 г;
m(С2Н6) = 2 моль • 30 г/моль = 60
г.
Таким образом, моль – это порция вещества, содержащая одно и то же число частиц, но имеющая разную массу для разных веществ, т.к. частицы вещества (атомы и молекулы) не одинаковы по массе.
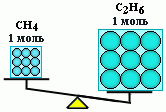
n(CH4) = n(С2Н6), но m(CH4) < m(С2Н6)Вычисление ν используется практически в каждой расчетной задаче.
Образцы решения задач
Задача №1. Вычислите массу (г) железа, взятого количеством вещества
0, 5 моль?
Дано: ν(Fe)=0,5 моль
Найти: m(Fe) — ?
Решение:
m = M · ν
M(Fe) = Ar(Fe) = 56 г/моль (Из периодической системы)
m (Fe) = 56 г/моль · 0,5 моль = 28 г
Ответ: m (Fe) =28 г
Задача №2. Вычислите массу (г) 12,04 · 1023 молекул оксида кальция CaО?
Дано: N(CaO)= 12,04 * 1023 молекул
Найти: m(СaO) — ?
Решение:
m = M · ν, ν= N/Na,
следовательно, формула для расчёта
m = M · (N/Na)
M(CaO) = Ar(Ca) + Ar(O) = 40 + 16 = 56 г/моль
m= 56 г/моль · (12,04 * 1023/6.02 · 1023 1/моль) = 112 г
Ответ: m= 112 г
Задания для закрепления
Задача 1. Вычислите массу воды (г),
взятой количеством вещества 5 моль?
Задача 2. Вычислите массу 24,08 *1023 молекул серной кислоты H2SO4?
Задача 3. Определите число атомов в 56 г железа Fe?
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.