
Объяснение свойств вещества на основе моделей строения газов, жидкостей и твёрдых тел
Из истории…
· Еще в Древней Греции, около 2,5 тысяч лет назад, была выдвинута гипотеза о том, что вещество состоит из мельчайших частичек – атомов и молекул.
· Основоположником идеи дискретного строения вещества считается древнегреческий философ Демокрит, живший около 470 года до новой эры. Демокрит считал, что все тела состоят из бесчисленного количества сверхмалых, невидимых глазу, неделимых частиц . "Они бесконечно разнообразны, имеют впадины и выпуклости, которыми сцепляются, образуя все материальные тела, а в природе существуют только атомы и пустота». В научную теорию эта гипотеза превратилась только XVIII – XIX веках.
· Если бы мы смогли рассмотреть окружающие нас тела через микроскоп, то увидели бы отдельные атомы и молекулы

Основные положения МКТ
Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химического вещества.
В основе молекулярно-кинетической теории лежат три основных положения:
· Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов («элементарных молекул»).
· Атомы и молекулы находятся в непрерывном хаотическом движении.
· Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало.
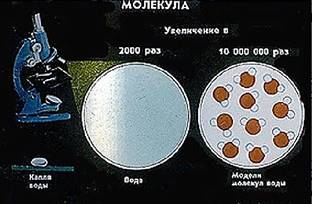
· Атомы очень малы. Их невозможно разглядеть не только простым глазом, но и с помощью даже самого мощного оптического микроскопа.
· В 1951 году Эрвин Мюллер изобрёл ионный микроскоп, позволивший в деталях разглядеть атомную структуру металла.
· Атомы различных химических элементов отличаются друг от друга.
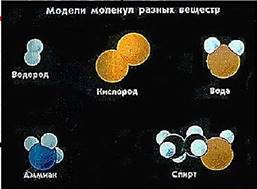
· Молекула - это мельчайшая частица вещества, обладающая свойствами этого вещества.
· Так, молекула сахара - сладкая, а соли – соленая.
· Молекулы различных веществ – различны,
· Молекулы одного вещества одинаковы
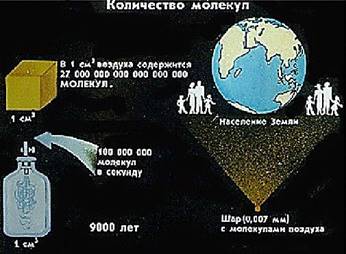
· Молекулы состоят из атомов.
· Размеры молекул ничтожно малы.
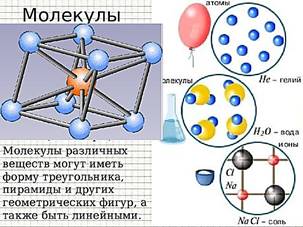
· У разных веществ молекулы могут состоять из одного атома (инертные газы) или из нескольких одинаковых или различных атомов, или даже из сотен тысяч атомов (полимеры).
· Молекулы различных веществ могут иметь форму треугольника, пирамиды и других геометрических фигур, а также быть линейными.

Строение вещества
· Между молекулами в веществе существуют промежутки.
· Доказательствами существования промежутков служат изменение объема вещества , т.е. расширение и сжатие вещества при изменении температуры, и явление диффузии.
· Частицы веществ способны притягиваться друг к другу. Однако это притяжение возникает лишь тогда, когда поверхности тел очень гладкие (для этого и понадобилась зачистка лезвием) и, кроме того, плотно прижаты друг к другу.
· Частицы веществ способны отталкиваться друг от друга . Это подтверждается тем, что жидкие, а особенно твердые тела очень трудно сжать.
· Притяжение или отталкивание частиц веществ возникает лишь в том случае, если они находятся в непосредственной близости.
· На расстояниях, чуть больших размеров самих частиц, они притягиваются.
· На расстояниях, меньших размеров частиц, они отталкиваются .
· Если же поверхности тел удалены на расстояние, заметно большее, чем размер частиц, то взаимодействие между ними не проявляется никак.

 Модели строения газов, жидкостей и
твердых
Модели строения газов, жидкостей и
твердых
В газах расстояния между молекулами обычно значительно больше их размеров, каждая молекула движется вдоль прямой линии до очередного столкновения с другой молекулой или со стенкой сосуда.
В жидкостях молекулы имеют значительно большую свободу для теплового движения. Они не привязаны к определенным центрам и могут перемещаться по всему объему жидкости. Этим объясняется текучесть жидкостей.
В твердых телах молекулы совершают беспорядочные колебания около фиксированных центров (положений равновесия).
Строение твердых, жидких и газообразных тел
· Большая часть вещества на Земле встречается в трех состояниях : твердом, жидком и газообразном . Часто эти состояния называют агрегатными .
· В зависимости от условий одно и тоже вещество находится в каком-либо из них.
· Например, лед, вода и водяной пар.
· Или другой пример: воздух в вашей комнате — газ, но если его охладить до -193°C, он станет жидкостью, а если охладить до -213°C — твердым телом.
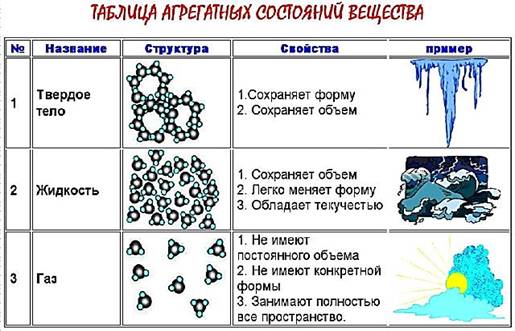 .
.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.