
Основные положения молекулярно-кинетической теории.
Размеры и масса молекул и атомов.
Строение вещества описывается с помощью молекулярно-кинетической теории.
В основу этой теории входят три положения:
1. Все вещества состоят из отдельных частиц молекул и атомов. Молекулы могут состоять как из одного атома, так и из нескольких. Они очень малы. Глаз человека не способен разглядеть атомы и промежутки между ними, поэтому любое вещество кажется нам сплошным.

Молекулы и атомы электрически нейтральные частицы, однако они могут приобретать дополнительный электрический заряд, то есть становиться положительным и отрицательным ионами.
2. Все эти частицы находятся в непрерывном беспорядочном движении. С ростом температуры скорость частиц вещества увеличивается, поэтому беспорядочное движение частиц принято называть тепловым. Это движение не зависит от внешних воздействий. Движение происходит в непредсказуемом направлении из-за столкновения молекул.
3. Молекулы и атомы взаимодействуют друг с другом с силами, имеющими электрическую природу. Частицы вещества одновременно и притягиваются, и отталкиваются друг от друга, и по этой причине располагаются на определенных расстояниях друг от друга.
![]()
Силы взаимодействия частиц у разных веществ различны. Этим объясняются различия многих свойств веществ, например их агрегатное состояние. Действие молекулярных сил возможно лишь на очень малых расстояниях, сравнимых с размерами самих частиц вещества. Гравитационным взаимодействием между этими частицами можно пренебречь.
Первое положение молекулярно-кинетической теории будет доказываться фотографиями веществ, выполненных с помощью специальных микроскопов, испарением веществ, уменьшением суммарного объема некоторых жидкостей в результате их смешивания друг с другом. Например, при смешивании спирта с водой маленькие молекулы воды займут промежутки между большими молекулами спирта (молекулы спирта в 2–3 раза крупнее молекул воды).
Второе положение молекулярно-кинетической теории будет доказываться броуновским движением и диффузией:
· Броуновское движение тепловое движение мельчайших частиц, взвешенных в жидкости или газе.
· Диффузия явление проникновение молекул одного вещества в промежутки между молекулами другого. Чем выше температура, тем быстрее происходит диффузия.

Третье положение молекулярно-кинетической теории будет доказываться существованием макроскопических тел.
Масса и размеры молекул
Размер молекул является величиной условной. Его оценивают следующим образом. Между молекулами наряду с силами притяжения действуют и силы отталкивания, поэтому молекулы могут сближаться лишь до некоторого расстояния. Расстояние предельного сближения центров молекул называют эффективным диаметром молекулы. (При этом условно считают, что молекулы имеют сферическую форму.)
С помощью многочисленных методов определения масс и размеров молекул установлено, что за исключением молекул органических веществ, содержащих очень большое число атомов, большинство молекул по порядку величины имеют диаметр 1· 10 - 10 м и массу 1· 10 - 26 кг.
Относительная молекулярная масса
Относительной молекулярной (или атомной) массой Мr (или Аr) называют величину, равную отношению массы молекулы (или атома) mо этого вещества к 1/12 массы атома углерода mоС, т.е.
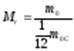
Относительная молекулярная (атомная) масса является величиной, не имеющей размерности.
Количество вещества. Молярная масса. Масса молекулы
Количеством вещества ν называют величину, равную отношению числа молекул (или атомов) N в данном теле к числу атомов NA в 0,012 кг углерода, т.е. ν = N/ NA (NA - число Авогадро).
Молярной массой М какого-либо вещества называют массу 1 моль этого вещества.
М = mо NA
Следовательно, массу молекулы (атома) можно определить из соотношения
mо = М / NA
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.