
ГБПОУ «Краевой многопрофильный техникум»
ХИМИЯ - ЭТО ИНТЕРЕСНО 
Пособие для педагогов и учащихся
Составитель: преподаватель химии Ветрова Нина Петровна
Откройте для себя мир химии! Ведь недаром Л. Полинг говорил, что химики – это те, кто на самом деле понимают мир!
Вы держите в руках пособие «Занимательная химия». В нём множество интересных рубрик, и каждый найдет себе по вкусу: от научно-познавательных до юмористических. Вы узнаете, кто получил кислород, что такое сапфир, познакомитесь с цветами-хамелеонами, разгадаете кроссворд, Вас ожидает юмористическая рубрика, галерея кристаллов и многое другое.
Надеюсь, Вам понравится!

Химия вокруг нас
Сапфир

Сапфи́р — одна из разновидностей минерала корунда, драгоценный камень разных оттенков, преимущественно синего цвета.
Формула: Al2O3(оксид алюминия)
Цвет: Синий и голубой различных оттенков. Реже бывает бесцветным, розовым, оранжевым, жёлтым, зелёным, фиолетовым, чёрным
Блеск: Стеклянный
Твёрдость: 9
Плотность: 3,95 — 4,00 г/см³
Показатель преломления: 1,766 — 1,774
Не так давно в ряде месторождений Африки, Шри-Ланки и др. стали добывать фантазийные сапфиры, обладающие александритовым эффектом смены цвета при изменении освещения с дневного на электрическое. Обычно такие камни меняют свой цвет в следующих пределах:
 · дневной свет -
синий,
· дневной свет -
синий,
электрический - пурпурный, фиолетовый;
· дневной свет - желтовато-зеленый,
электрический – коричневато - красный.
Это интересно:
· Самый крупный в мире из найденных на Шри-Ланке кристаллов сапфира весил более 18 кг (найден в 1986 г).
· Одним из самых крупных сапфиров является кристалл массой 1905 карат, найденный в США.
· В Алмазном фонде России хранится брошь (середина 19 века) с васильково-синим цейлонским сапфиром размером 3,9 х 3,4 х 2,2 см и массой 258,80 карат. Верхняя часть камня покрыта мелкими шестиугольными фасетами, создающими приятную игру.
Великие химики
Антуан-Лоран Лавуазье

Родился в Париже. Получив в 1774 г. кислород и сумев осознать значение этого открытия, Лавуазье создаёт кислородную теорию горения, которую излагает в 1777 г. В 1775-1777 гг. Лавуазье доказывает сложный состав воздуха, состоящего, по его мнению, из кислорода и азота. В 1781 г. доказывает также и сложный состав воды, установив, что она состоит из кислорода и водорода. В 1785 г. они же синтезируют воду из водорода и кислорода. Опираясь на свойства кислородных соединений, Лавуазье первый дал классификацию "простых тел". Основой его классификации химических веществ вместе с понятием о простых телах, служили понятия "окись", "кислота" и "соль". Это была первая классификация, давшая возможность с большой простотой обозреть целые ряды известных в то время в химии тел, но была узка и потому неправильна. Она дала Лавуазье возможность предугадать сложный состав таких тел как известь, барит, едкие щелочи, борная кислота и другие, считавшихся до него телами элементарными.
Новости мира химии
Аномерный эффект
 Ученые из Оксфордского университета
решили задачу, которой уже 50 лет о том, действительно ли, молекулы сахаров
меняют свою форму.
Ученые из Оксфордского университета
решили задачу, которой уже 50 лет о том, действительно ли, молекулы сахаров
меняют свою форму.
Уже давно известно, что молекулы сахаров могут принимать необычные формы. Некоторые ученые объясняют это влиянием неизменно присутствующей воды или других веществ. Чтобы проверить эту теорию, исследователи нашли способ отделения сахаров от всех других веществ, превращая их в газ. В таком состоянии они не подвержены влиянию примесей и за их поведением можно легко наблюдать.
Исследование показывает, что молекулы сохраняют свой необычный внешний вид, несмотря на их изоляцию. Это открытие может быть очень важным с точки зрения медицины, но еще более важным оно может быть для производства продукции, которое производится из нефти, запасы которого постоянно сокращаются.
Явление необычного поведения молекул сахаров было открыто в 1955 году и называется аномерным эффектом, в результате которого заместитель при аномерном атоме углерода стремится занять аксиальное положение.
Для доказательства существования аномерного эффекта изолировали молекулы сахара от всех других веществ, но по-прежнему присутствовали сахара необычной формы. Наши результаты также подтверждают предположение о том, что тип заместителя у атома углерода, так же имеет влияние на этот эффект.
![]()
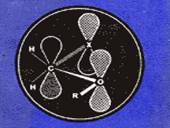 Это фундаментальное открытие,
поскольку оно распространяется на все сахара, и может иметь весьма далеко
идущие последствия. Многие химические соединения могут быть синтезированы из
молекул сахаров. На нашей планете их гораздо больше, чем нефти, которая сейчас
более популярна. Они не только играют огромную роль в питании человека, но и
являются основными составляющими веществами клеток растений и насекомых в виде
целлюлозы и хитина. В будущем можно будет использовать сахара для производства,
скажем, пластмассы или медицинских препаратов. В принципе, химики могут сделать
практически любые органические молекулы из них, и все, что вы можете сделать из
нефти, можно сделать из сахаров.
Это фундаментальное открытие,
поскольку оно распространяется на все сахара, и может иметь весьма далеко
идущие последствия. Многие химические соединения могут быть синтезированы из
молекул сахаров. На нашей планете их гораздо больше, чем нефти, которая сейчас
более популярна. Они не только играют огромную роль в питании человека, но и
являются основными составляющими веществами клеток растений и насекомых в виде
целлюлозы и хитина. В будущем можно будет использовать сахара для производства,
скажем, пластмассы или медицинских препаратов. В принципе, химики могут сделать
практически любые органические молекулы из них, и все, что вы можете сделать из
нефти, можно сделать из сахаров.
Последствия для медицины могут быть менее внушительными, нужно много дополнительных исследований. Мы гораздо меньше знаем о сахарах, чем о других более сложных молекулах, таких как ДНК и белки.
Полезные опыты
Как почистить серебро?
 Выбор метода чистки в первую очередь зависит от
степени окисленности и пробы металла. Высокопробные сплавы содержат большой
процент чистого серебра, и окислы, возникающие на их поверхности, имеют иной
характер, чем окислы низкопробных сплавов.
Выбор метода чистки в первую очередь зависит от
степени окисленности и пробы металла. Высокопробные сплавы содержат большой
процент чистого серебра, и окислы, возникающие на их поверхности, имеют иной
характер, чем окислы низкопробных сплавов.
 Если изделия высокой пробы
долгое время подвергались воздействию неблагоприятных факторов и покрылись
плотным слоем окислов, их целесообразно поместить на один час в раствор
нашатырного спирта (состав - 90% воды и 10% аммиака). При отсутствии нашатырного
спирта можно приготовить содовый раствор – на 100
г воды 30 г (примерно две чайных ложки) пищевой (двууглекислой) соды. В
раствор изделия опускаются на несколько часов до полного растворения окислов.
Процесс можно несколько ускорить, если подогревать раствор до кипения и
периодически протирать окисленные места мягкой зубной щеткой.
Если изделия высокой пробы
долгое время подвергались воздействию неблагоприятных факторов и покрылись
плотным слоем окислов, их целесообразно поместить на один час в раствор
нашатырного спирта (состав - 90% воды и 10% аммиака). При отсутствии нашатырного
спирта можно приготовить содовый раствор – на 100
г воды 30 г (примерно две чайных ложки) пищевой (двууглекислой) соды. В
раствор изделия опускаются на несколько часов до полного растворения окислов.
Процесс можно несколько ускорить, если подогревать раствор до кипения и
периодически протирать окисленные места мягкой зубной щеткой.
Изделия высокой пробы со слабыми следами окисления лучше всего чистить кашицей, составленной из трех компонентов - нашатырного спирта, пищевой (двууглекислой) соды и зубной пасты. Такая смесь должна ощущаться пальцами в виде мягкой жижи и не содержать твердых, царапающих частиц. Покрыв изделие составом, его следует растирать пальцами или мягкой щеткой, не прилагая при этом особых усилий.
 Новые изделия целесообразно,
время от времени, отмывать от " неосторожных прикосновений рук".
Заметно, что места прикосновений становятся точками, откуда начинается
коррозия.
Новые изделия целесообразно,
время от времени, отмывать от " неосторожных прикосновений рук".
Заметно, что места прикосновений становятся точками, откуда начинается
коррозия.
Изделия из низкопробных сплавов серебра, для которых в качестве лигатуры применяют медь, при сильном окислении зеленеют. Для их чистки наиболее подходит 10% - ный раствор трилона Б. После того как зеленый слой растворится и сойдет, чистку следует продолжить методом, принятым для высокопробного серебра - чистящей кашицей.
Химические фокусы
Цветок-хамелеон
Внешний эффект





 Исполнитель
показывает зрителям шесть тюльпанов: три красных и три синих. Отодвигает на
расстояние 10 шагов друг от друга два стула и на каждый ставит по стакану.
Затем дает красные тюльпаны одному из зрителей, а синие - другому и просит их
хорошенько запомнить цвета. После того, как все это проделано, он ставит
красные тюльпаны в один стакан, а синие - в другой. Оба стакана покрывает
яркими шелковыми платками и поручает зрителям-помощникам их охранять.
Исполнитель
показывает зрителям шесть тюльпанов: три красных и три синих. Отодвигает на
расстояние 10 шагов друг от друга два стула и на каждый ставит по стакану.
Затем дает красные тюльпаны одному из зрителей, а синие - другому и просит их
хорошенько запомнить цвета. После того, как все это проделано, он ставит
красные тюльпаны в один стакан, а синие - в другой. Оба стакана покрывает
яркими шелковыми платками и поручает зрителям-помощникам их охранять.
А теперь несколько минут терпения, которые можно занять разговором. "Волшебство наших тюльпанов заключается в том, - говорит фокусник, - что они сами без посторонней помощи меняют свои места, причем происходит все очень скрытно, как бы мы внимательно не следили". По прошествии времени вы просите помощника, охраняющего красные тюльпаны, снять платок и проверить - на своем ли месте то, что он сторожил. Ко всеобщему удивлению, красные тюльпаны неизвестным образом исчезли, а в стакане оказались синие. То же самое случилось и у второго зрителя: вместо синих у него в стакане стоят красные тюльпаны.





 Секрет фокуса
Секрет фокуса
 Из белой материи
сделайте шесть искусственных тюльпанов. Приготовьте два крепких настоя, один
красного лакмуса, другой - синего. Затем окрасьте каждую тройку в свой цвет.
Перед выступлением налейте в один стакан немного уксусной эссенции, в другой -
столько же нашатырного спирта. В стакан с уксусной эссенцией надо поставить
синие, а в стакан с нашатырным спиртом - красные тюльпаны.
Из белой материи
сделайте шесть искусственных тюльпанов. Приготовьте два крепких настоя, один
красного лакмуса, другой - синего. Затем окрасьте каждую тройку в свой цвет.
Перед выступлением налейте в один стакан немного уксусной эссенции, в другой -
столько же нашатырного спирта. В стакан с уксусной эссенцией надо поставить
синие, а в стакан с нашатырным спиртом - красные тюльпаны.
От действия уксусных паров синие тюльпаны будут постепенно краснеть, а от паров нашатырного спирта красный цвет изменится на синий.
Интересные факты
Почему светлячки светятся?!
Многие задавились этим вопросом, а доцент Факультета энтомологии и нематологии Флоридского университета Марк Бранхем решил пролить свет на столь интересующий вопрос.
Итак, он утверждает, что свечение светлячков вызывается химическим процессом биолюминесценции в их теле. Свет излучается, когда внутриклеточный кислород соединяется с кальцием, молекулой аденозинтрифосфата (АТФ), служащей хранилищем энергии, и пигментом люциферином в присутствии фермента лоюциферазы.

В отличие от ламп накаливания, выделяющих большое количество тепла, светлячки испускают «холодный свет». Если бы их светорождающий орган нагревался до температуры колбы лампочки, то насекомое погибло бы.
Химический юмор
Химия - это не только научные теории, синтезы, реакции и расчеты, Химия - это неисчерпаемая тема веселых шуток, забавных анекдотов и метких афоризмов. На страницах этого подраздела мы постарались собрать для вас все самое смешное и оригинальное, что есть в Химии. Читайте, смейтесь, улыбайтесь!!!
Женщина. Физико-химические свойства

Химический элемент: 115
Название: Женщина
Символ: Fm
Первооткрыватель: Адам
Атомная масса: 60 кг; также встречая изотопы от 40 до 250 кг.
Распространенность: Чрезвычайно распространен в природе
Физические свойства:
· Тает при определённом воздействии.
· Самопроизвольно закипает и без внешних причин охлаждается.
· Коэффициент расширения: увеличивается с годами.
· Меняется при сдавливании в определённых местах.
Химические свойства:
· Очень хорошо взаимодействует с Au, Ag, Pt и др. благородными металлами.
· Поглощает дорогостоящие вещества в больших количествах.
· Быстро насыщается этиловым спиртом.
· Реакционоспособность варьируется от времени суток.
· Может неожиданно взрываться.
Применение:
· Широко используется в декоративных целях, особенно в спортивных автомобилях.
· Является очень эффективным чистящим и моющим средством.
· Помогает расслабиться и снять стресс.
Качественная реакция: приобретает зеленую окраску, если рядом находится др. образец более высокого качества.
Меры предосторожности:
· При попадании в неопытные руки представляет серьёзную опасность.
· Не рекомендуется единовременно иметь более одного образца.
·
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.