
Тест по темам «Органическая химия», «Неорганическая химия», «Теоретические основы химии», «Хлор»
Вариант 1
Задание 1.
Для нейтрализации раствора массой 345 г, содержащего азотную и бромоводородную кислоты, необходимо 350 г раствора гидроксида натрия с массовой долей щелочи 0,377. При добавлении к такому же раствору кислот нитрата серебра образовалось нерастворимое вещество массой 303 г. Определите массовые доли (%) кислот в исходном растворе. Ответ округлите до целых чисел.
Ответ: ω(HBr) = __ %, ω(HNO3) = __ %.
Задание 2.
Дайте название веществу, имеющему следующее строение:
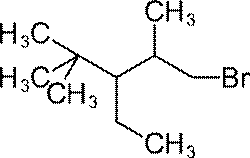
А) 1-бром-2,4,4-триметил-3-этилпентан
Б) 2,2-диметил-3-этил-4-метил-5-бромпентан
В) 4,4,2-триметил-3-этил-1-бромпентан
Г) 1-бром-2,4-метил-3-этилпентан
Задание 3.
Массовая доля атомов углерода в молекуле алкана составляет 83,33%. Определите формулу этого алкана.
А) C5H12
Б) C4H10
В) C2H6
Г) C3H8
Задание 4.
Сожгли этан объемом 8,064 дм3. Определите объем (см3) раствора гидроксида калия (ω(KOH) =
0,63; ρp-pa = 1,21 г/см3), который потребуется для полного поглощения выделившегося углекислого газа, если в результате образуется кислая соль. Ответ округлите до целого числа.
Ответ: Vp-pa(KOH) = __ см3.
Задание 5.
Сожгли пропан объемом 16,8 дм3. Определите объем (см3) раствора гидроксида натрия (ω(NaOH) = 0,48; ρp-pa = 1,09 г/см3), который потребуется для полного поглощения выделившегося углекислого газа, если в результате образуется кислая соль. Ответ округлите до целого числа.
Ответ: Vp-pa(NaOH) = ___ см3.
Задание 6.
Определите, какое число классов органических соединений представлено следующими веществами:
C4H6, глицерин, анилин, C3H8, C17H35COONa, ацетилен, этанол, ацетат калия, метиламин, метан,
С2H5NH2, CH3OH.
В ответе укажите это число.
А) 5
Б) 4
В) 7
Г) 6
Задание 7.
Массовая доля углерода в молекуле первичного насыщенного амина равна 61%. Определите формулу этого амина и назовите его.
А) Пропиламин
Б) Метиламин
В) Этиламин
Г) Анилин
Задание 8.
Укажите верные утверждения. Ответ представьте в виде последовательности чисел.
1) Аминокислоты в молекуле содержат две функциональные группы: Карбоксильную – СOOH иамино – NH2.
2) При добавлении фенолфталеина к раствору метиламина наблюдается желтое окрашивание.
3) C2H5NO2 – формула этиламина.
4) Амины являются органическими основаниями.
5) Анилин – ароматический амин – C6H5NH2.
6) При взаимодействии между собой остатки молекул аминокислот связываются пептиднымисвязями.
Ответ: ____.
Задание 9.
Укажите верные утверждения. Ответ представьте в виде последовательности чисел. 1) Амины можно рассматривать как производные аммиака, в которых атомы водорода замещены углеводородными радикалами.
2) Аминокислоты являются амфотерными органическими соединениями.
3) Способность молекул аминокислот взаимодействовать друг с другом лежит в основеобразования белковых молекул.
4) Раствор аминоуксусной кислоты окрасит лакмус в красный цвет.
5) Функциональной группой первичных аминов является группа – NH2 .
6) Амины и аминокислоты – изомеры.
Ответ: ____.
Задание 10.
Определите формулу углеводорода, плотность которого составляет 1,161 г/дм3, а массовая доля водорода – 7,7%.
А) C2H2
Б) C2H4
В) C2H6
Г) C6H6
Задание 11.
Укажите верные утверждения. Ответ представьте в виде последовательности чисел.
1) Буква n в формуле полимера показывает число полученных макромолекул.
2) Разрушение вторичной и третичной структуры белка под воздействием внешних факторов –денатурация.
3) Для раствора белков, как и для крахмала, характерны некоторые качественные (цветные) реакции.
4) Разрушение полимерных молекул называется реакцией полимеризации.
5) В образовании вторичной и третичной структуры белка участвуют водородные связи.6) В результате гидролиза белковых макромолекул разрушаются пептидные связи и образуются молекулы аминокислот.
Ответ: ____.
Задание 12.
Раствор глюкозы массой 540 г (ω(глюкозы) = 80%) подвергли спиртовому брожению.
Выделившийся газ пропустили через раствор гашеной извести Ca(OH)2, выпал осадок массой 284 г. Вычислите массовые доли (%) веществ в растворе после реакции брожения. Ответ округлите до целого числа.
Ответ: ω(C6H12O6) = __ %, ω(C2H5OH) = __ %.
Задание 13.
Определите объем (дм3) ацетилена, полученного из технического карбида кальция массой 47,78 г, в котором содержится 25% посторонних примесей.
А) V(C2H2) = 12,54 дм3
Б) V(C2H2) = 14,24 дм3
В) V(C2H2) = 15,42 дм3
Г) V(C2H2) = 4,18 дм3
Задание 14.
Выберите справедливые утверждения; ответ представьте в виде последовательности чисел:
1) В земной коре преобладают атомы неметаллов.
2) Электроотрицательность атомов металлов выше, чем неметаллов.
3) Существование некоторых элементов в виде нескольких простых веществ называетсяаллотропией.
4) К органогенам относятся неметаллы: С, H, O, N, P, S, Cl, F.
5) Атомы неметаллов могут выступать как в роли окислителя, так и в роли восстановителя.
6) В бинарных соединениях первым пишется элемент с меньшим значениемэлектроотрицательности.
7) Присоединяя электроны, атомы неметаллов повышают свою степень окисления.
Ответ: ____.
Задание 1.
Правильный ответ: 38, 31
Задание 2. Правильный ответ: А
Задание 3. Правильный ответ: А
Задание 4. Правильный ответ: 53
Задание 5. Правильный ответ: 172
Задание 6. Правильный ответ: А
Задание 7. Правильный ответ: А
Задание 8.
Правильный ответ: 1456
Задание 9.
Правильный ответ: 1235
Задание 10. Правильный ответ: А
Задание 11. Правильный ответ: 2356
Задание 12.
Правильный ответ: 43, 31
Задание 13. Правильный ответ: А
Задание 14.
Правильный ответ: 1356
Тест по темам «Органическая химия», «Неорганическая химия», «Теоретические основы химии», «Хлор»
Вариант 2
Задание 1.
Для нейтрализации раствора массой 220 г, содержащего соляную и фтороводородную кислоты, необходимо 260 г раствора гидроксида калия с массовой долей щелочи 0,431. При добавлении к такому же раствору кислот нитрата серебра образовалось нерастворимое вещество массой 208 г. Определите массовые доли (%) кислот в исходном растворе. Ответ округлите до целых чисел.
Ответ: ω (HCl) = __ %, ω(HF) = _ %.
Задание 2.
Массовая доля атомов углерода в молекуле алкана составляет 83,72%. Определите формулу этого алкана.
А) C6H14
Б) C4H10
В) C2H6
Г) C7H16
Задание 3.
Выберите верные утверждение, характеризующие алкены на примере этена. Ответ представьте в виде последовательности чисел.
1) Имеет молекулярную формулу СH2.
2) В молекуле содержится одна двойная связь.
3) Является гомологом этана.
4) Подчиняется общей формуле CnH2n.
5) Обесцвечивает бромную воду, что является качественной реакцией на кратную связь.
6) Имеет молекулярную формулу C2H4.
Ответ: ____.
Задание 4.
Дайте название веществу, имеющему следующее строение:
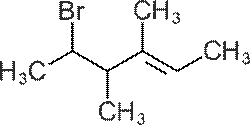
А) 5-бром-3,4-диметилгексен-2
Б) 2-бром-3,4-диметилгексен-4
В) 3,4-диметил-5-бромгексен-2
Г) 5-бром-3,4-метилгексен-3
Задание 5.
Выберите верные утверждения, характеризующие алканы на примере этана. Ответ представьте в виде последовательности чисел.
1) Имеет молекулярную формулу C2H6.
2) Обесцвечивает растворы брома или иода.
3) Подчиняется общей формуле CnH2n+2.
4) Является гомологом пентана.
5) Имеет два изомера.
6) Все химические связи в молекуле одинарные.
Ответ: ____.
Задание 6.
К раствору аминоуксусной кислоты массой 19,4 г с массовой долей кислоты 58% прилили раствор гидроксида калия массой 21 г с массовой долей щелочи 32%. Вычислите массовую долю (%) соли в полученном растворе. Ответ округлите до целого числа.
Ответ: ω(соли) = __ %.
Задание 7.
К раствору аминоуксусной кислоты массой 39,3 г с массовой долей кислоты 42% прилили раствор гидроксида натрия массой 43 г с массовой долей щелочи 28%. Вычислите массовую долю (%) соли в полученном растворе. Ответ округлите до целого числа.
Ответ: ω(соли) = __ %.
Задание 8.
Определите, какое число классов органических соединений представлено следующими веществами:
C6H6, С6H12, глицин, C6H12O6, HCOOH, пальмитиновая кислота, CH3–CH(NH2)–COOH, C3H7NH2,
C12H22O11, этилен, уксусная кислота, C17H33COOH. В ответе укажите это число.
А) 6
Б) 4
В) 5
Г) 7
Задание 9.
Массовая доля азота в молекуле первичного насыщенного амина равна 31%. Определите формулу этого амина и назовите его.
А) Этиламин
Б) Метиламин
В) Пропиламин
Г) Анилин
Задание 10.
Определите массу (г) бромбензола, полученного в результате бромирования технического бензола массой 25 г, содержащего 22% посторонних примесей.
А) m(C6H5Br) = 39,25 г
Б) m(C6H5Br) = 10,99 г
В) m(C6H5Br) = 35,92 г
Г) m(C6H5Br) = 29,35 г
Задание 11.
Вычислите относительную молекулярную массу целлюлозы, если число мономерных звеньев (степень полимеризации) равно 13000.
Ответ: _______.
Задание 12.
В результате спиртового брожения глюкозы получили спирт, который растворили в воде, при этом образовалось 360 г раствора (ω(спирта) = 45%). Определите массу (г) глюкозы. А) m = 317 г
Б) m = 371 г
В) m = 634 г
Г) m = 713 г
Задание 13.
Укажите справедливые утверждения. Ответ представьте в виде последовательности чисел.
1) Глюкоза, фруктоза, сахароза – моносахариды.
2) Жиры входят в состав животных организмов и растений (масла).
3) Сахароза в присутствии раствора йода окрашивается в синий цвет.
4) Мыла – это натриевые или калиевые соли высших карбоновых кислот.
5) Глюкоза и фруктоза – изомеры.
6) Твердые жиры образованы преимущественно предельными(насыщенными) карбоновымикислотами.
7) Глюкоза подвергается спиртовому и молочнокислому брожению.8) Формула сахарозы – C6H12O6 .
Ответ: _____.
Задание 14.
Вычислите объем (дм3) газа, выделившегося при взаимодействии 84,8 г карбоната натрия и 170,33 г раствора соляной кислоты с ω(HCl) = 30%.
А) V(CO2) = 15,68 дм3
Б) V(CO2) = 31,36 дм3
В) V(CO2) = 35,84 дм3
Г) V(CO2) = 17,92 дм3
Задание 1.
Правильный ответ: 24, 5
Задание 2. Правильный ответ: А
Задание 3.
Правильный ответ: 2456
Задание 4. Правильный ответ: А
Задание 5.
Правильный ответ: 1346
Задание 6. Правильный ответ: 34
Задание 7. Правильный ответ: 26
Задание 8. Правильный ответ: А
Задание 9. Правильный ответ: А
Задание 10. Правильный ответ: А
Задание 11.
Правильный ответ: 2106000
Задание 12.
Правильный ответ: А
Задание 13. Правильный ответ: 24567
Задание 14.
Правильный ответ: А
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.