
Химическая связь и её виды.
Химическая связь — это силы, с которыми атомы, ионы или молекулы связываются друг с другом с образованием более сложных устойчивых структур. Различают четыре вида химической связи.
|
Ионная |
Ковалентная неполярная |
Ковалентная полярная |
Металлическая |
|
1. Атомы инертных газов имеют идеально прочный внешний энергетический уровень. 2. Атомам металлов для прочности внешнего энергетического уровня энергетически выгоднее отдать электроны и превратиться в положительно заряженную частицу. 3. Атомам неметаллов для прочности внешнего энергетичес- кого уровня энергетически выгоднее принять недостающие электроны и превратиться в отрицательно заряженную частицу. 4. Положительно заряженные и отрицательно заряженные частицы называются ионами. 5. Между ионами возникает ионная связь. 6. Ионная связь, как правило, возникает между типичным металлом и типичным неметаллом. |
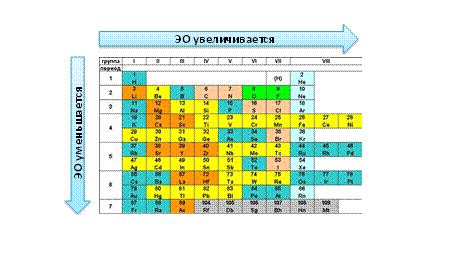
1. Ковалентная химическая связь возникает в результате образования общих электронных пар. 2. Атомы химических элементов обладают ЭО, которая изменяется периодически. 3. ЭО химических элементов в каждом периоде возрастает с увеличением порядкового номера элемента, а в каждой подгруппе — уменьшается. 4. Ковалентная неполярная связь возникает между атомами элементов с равной ЭО. 5. Между атомами химических элементов, в зависимости от их строения, могут возникнуть ковалентные связи — одинарная, двойная или тройная, имеющие определенную длину. 6. Химическая формула соединения может быть записана в молекулярном виде, в электронном или структурном виде. |
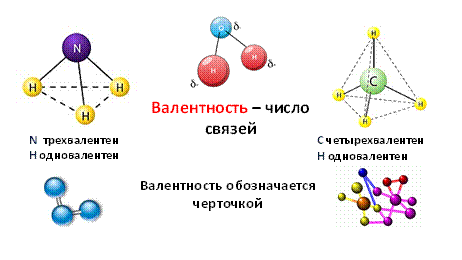
1. Ковалентная химическая связь образуется за счет общих электронных пар. 2. По числу общих электронных пар ковалентная связь бывает одинарной, двойной или тройной. 3. По ЭО химических элементов с ковалентной связью определяют ковалентную неполярную связь и ковалентную полярную связь. 4. Форма молекул в пространстве бывает линейной и угловой. Атомы химических элементов отличаются ЭО. |
1. 1.Для всех металлов характерна металлическая связь. Атомы металлов, в сравнении с атомами неметаллов, имеют большой атомный радиус и малое количество электронов на внешнем энергетическом уровне (1,2,3) 2. Металлическая связь возникает между атом- ионами металла и свободными электронами. 3. Общие физические свойства металлов обусловлены металлической связью. 4. В двухатомных молекулах металлов в парообразном состоянии возникает ковалентная неполярная связь.
|
|
Алгоритм записи схемы образования ионной связи 1.Составить схему строения и электронные формулы атомов химических элементов, образующих соединение. 2.Определить принадлежность элементов к металлам и неметаллам. 3. Составить схему перехода электронов и образования ионов. 4.Составить ионное соединение - формульную единицу. |
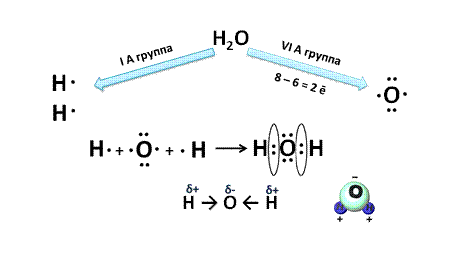
Алгоритм записи схемы образования ковалентной неполярной и полярной связи 1. Составить схему строения атома химического элемента и его электронную формулу. Определить число неспаренных электронов. 2. Записать знаки химических элементов, обозначая пары электронов и неспаренные электроны, так, чтобы непарные электроны были обращены к соседнему знаку. 3. Составить электронную формулу молекулы, определить кратность связи, то есть какая связь — одинарная, двойная или тройная. 4. Составить структурную формулу молекулы. |
Алгоритм записи схемы образования металлической связи. 1. Составить схему строения атома химического элемента и его электронную формулу. Определить число электронов внешнего уровня. 2. Me0 – nē ↔ Men+
|
|
|
ПРИМЕРЫ |
|||
|
|
|
|
|

Домашнее задание.
Задание #1
Вопрос:
Ковалентная неполярная связь образуется между:
Выберите один из 4 вариантов ответа:
1) между атомами металла и неметалла
2) между атомами различных неметаллов
3) одинаковыми атомами неметалла
4) различными атомами неметалла
Задание #2
Вопрос:
Образование молекулы водорода из атомов, можно изобразить:
Выберите один из 4 вариантов ответа:
1) H + H → H • H 2) H + • H → H •• H
3) H • + H → H • H 4) H • + • H → H •• H
Задание #3
Вопрос:
В результате образования ковалентной связи объединяются:
Выберите один из 4 вариантов ответа:
1) спаренные электроны 2) неспаренные электроны
3) ионы и неспаренные электроны 4) различные ионы
Задание #4
Вопрос:
Выберите пару, в которой первый элемент более электроотрицательный, чем второй:
Выберите один из 4 вариантов ответа:
1) С и Cl 2) F и O 3) P и O 4) Si и S
Задание #5
Вопрос:
Электротрицательность:
Выберите один из 4 вариантов ответа:
1) увеличивается по периоду слева направо
2) уменьшается по периоду слева направо
3) увеличивается в главных группах сверху вниз
4) уменьшается в группах снизу вверх
Задание #6
Вопрос:
При образовании ковалентной полярной связи электронная пара:
Выберите один из 4 вариантов ответа:
1) смещена влево
2) смещена вправо
3) равноценна между всеми атомами
4) смещена к более электроотрицательному элементу
Задание #7
Вопрос:
Ковалентная полярная связь образуется между:
Выберите один из 4 вариантов ответа:
1) между различными атомами металла
2) одинаковыми атомами неметаллов
3) различными атомами неметаллов
4) между атомами металла и неметалла
Задание #8
Вопрос:
Выберите молекулу с ковалентной полярной связью:
Выберите один из 4 вариантов ответа:
1) N2 2) P4 3) H2 4) CO2
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.