Предлагаемый методический материал является раздаточными дидактическими карточками с алгоритмами решения расчетных химических задач по определенной теме из школьного курса. Также материалы карточек могут быть использования для индивидуальных заданий на уроках химии, для повторения, обобщения или закрепления знаний, навыков решения задач разных типов, в качестве тренировочных тематических заданий при отработке заданий из ОГЭ или ЕГЭ.
Алгоритм решения задачи на определение молекулярной формулы
вещества по продуктам сгорания
ПОСЛЕДОВАТЕЛЬНОСТЬ
ДЕЙСТВИЙ
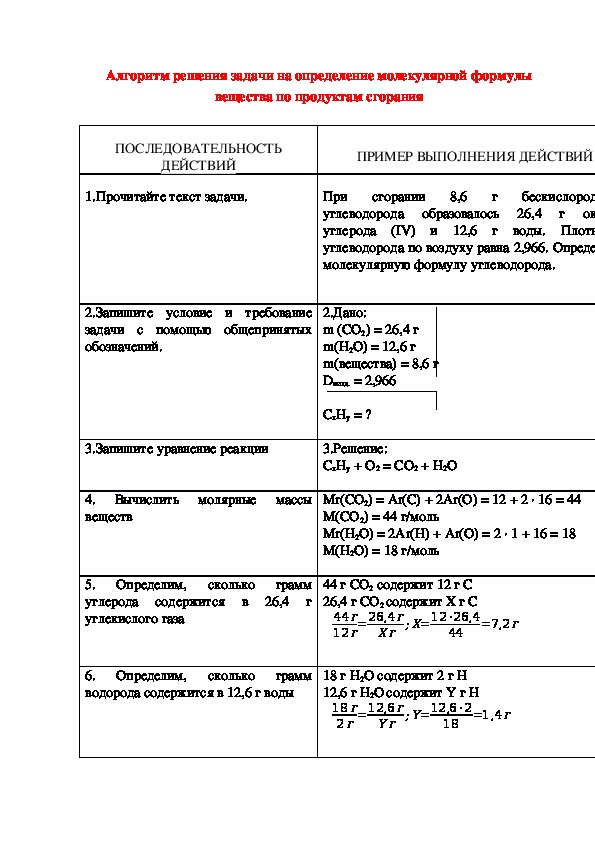
1.Прочитайте текст задачи.
ПРИМЕР ВЫПОЛНЕНИЯ ДЕЙСТВИЙ
При сгорании 8,6 г бескислородного
углеводорода образовалось 26,4 г оксида
углерода (IV) и 12,6 г воды. Плотность
углеводорода по воздуху равна 2,966. Определите
молекулярную формулу углеводорода.
2.Запишите условие и требование
задачи с помощью общепринятых
обозначений.
3.Запишите уравнение реакции
2.Дано:
m (CO2) = 26,4 г
m(H2O) = 12,6 г
m(вещества) = 8,6 г
Dвозд. = 2,966
СхHy = ?
3.Решение:
CxHy + O2 = CO2 + H2O
Вычислить молярные массы
4.
веществ
Mr(CO2) = Ar(C) + 2Ar(O) = 12 + 2 ∙ 16 = 44
M(CO2) = 44 г/моль
Mr(H2O) = 2Ar(H) + Ar(O) = 2 ∙ 1 + 16 = 18
M(H2O) = 18 г/моль
Определим,
5.
сколько грамм
углерода содержится в 26,4 г
углекислого газа
44 г CO2 содержит 12 г С
26,4 г CO2 содержит Х г С
;Х= 12·26,4
44г
12г=26,4г
Хг
44 =7,2г
Определим,
6.
водорода содержится в 12,6 г воды
сколько грамм
18 г H2O содержит 2 г Н
12,6 г H2O содержит Y г H
;Y=12,6·2
18г
2г=12,6г
Yг
18 =1,4г7. Находим количество вещества
углерода и водорода
ν(C)= 7,2г
12 г
моль
=0,6моль
ν(H)= 1,4г
1 г
моль
=1,4моль
8. Составляем пропорцию
Х : Y = 0,6 : 1,4
9. Избавляемся от десятичной дроби,
умножив на 10
Х : Y = 6 : 14
Записать
10.
формулу вещества
предполагаемую
С6H14
11. Рассчитать молярную массу
предполагаемого вещества
12. Рассчитать молярную массу
вещества по плотности воздуха
Mr(С6H14) = 6Ar(C) + 14Ar(Н) = 6 ∙ 12 + 14 ∙ 1 = 86
M(С6H14) = 86 г/моль
М(вещества) = Dвозд. ∙ 29 = 2,966 ∙ 29 = 86 г/моль
13. Сравнить полученные результаты М(вещества) = M(С6H14)
86 г/моль = 86 г/моль
14. Записать ответ
Ответ: формула вещества С6H14