
№______САБАҚТЫҢ ЖОСПАРЫ
ПЛАН ЗАНЯТИЯ №_______
Топ
Группа________________________________________
Күні
Дата____________________________________
Пәні
Дисциплина: Химия
Сабақтың тақырыбы:
Тема занятия: Аминокислоты. Изомерия и номенклатура аминокислот. Физические свойства аминокислот.
Цель урока: систематизировать знания учащихся о кислотах, аминах; дать представление об аминокислотах, познакомить со строением, амфотерными свойствами, физическими свойствами.
Задачи урока:
обучающая
- показать значение аминокислот. Рассмотреть биологическую роль аминокислот;
- научить учащихся записывать структурные формулы аминокислот, давать им названия;
развивающая
- развивать умение учащихся сравнивать, обобщать, проводить аналогию между неорганическими и органическими веществами;
- продолжить развитие навыков самообразования и самооценки;
- развивать общеучебные умения (умение работать с учебником, составлять таблицы, оформлять наблюдения в письменном виде, формулировать выводы во внутренней и внешней речи, осуществлять самоконтроль, проводить самоанализ и т.п.)
воспитывающая
- воспитывать устойчивый интерес к предмету через изучение некоторых моментов роли аминокислот для жизнедеятельности человека;
- воспитывать интерес к здоровому образу жизни.
Тип урока: изучение нового материала
Оборудование: Периодическая Система химических элементов Д.И. Менделеева, таблица аминокислот.
Ход урока
1. Организационный момент.
2. Проверка домашнего задания.
3. Актуализация знаний.
· Какую группу органических соединений мы начали изучать на прошлом уроке? (Азотсодержащие органические вещества).
· С каким классом соединений мы познакомились? (Амины)
· Сегодня мы продолжаем знакомиться с азотсодержащими органическими соединениями.
Постановка темы урока.
4. Изучение нового материала
Что же представляют собой аминокислоты с точки зрения химии?
Аминокислоты – органические бифункциональные соединения, в состав которых входят две функциональные группы: карбоксильная – СООН и аминогруппа -NH2.
Аминокислоты – амфотерные соединения.
Аминокислоты можно рассматривать как карбоновые кислоты, в молекулах которых один или несколько атомов водорода углеводородного радикала замещены аминогруппами.
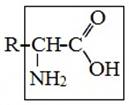
В природе встречаются в основном α-аминокислоты, составляющих белки (кроме пролина). Они имеют общую формулу
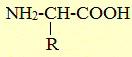
где R – углеводородный радикал, который может содержать различные функциональные группы (-SH, –OH, –COOH, NH2) и кольца.
Специфичность каждой аминокислоты определяется строением радикала R.
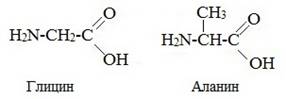
Простейший представитель – H2N-CH2-COOH - аминоуксусная кислота (глицин).
СТРОЕНИЕ АМИНОКИСЛОТ
Аминокислоты, в отличие от ранее изученных органических веществ, содержат две функциональнее группы.
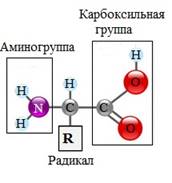
Каждая из 20 аминокислот имеет одинаковую часть (NH2-CH-COOH) и отличается от любой другой аминокислоты R-группой, или радикалом. Строение радикала у разных видов аминокислот — различное.
Структура лишь одной аминокислоты – пролина – не соответствует общей формуле. Это связано с тем, что пролин не является аминокислотой. Он представляет собой иминокислоту.
Например, в молекуле глицина R-радикал представлен атомом водорода:
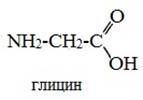
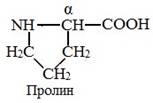
В молекуле пролина радикал связан с α-углеродным атомом и с аминогруппой, в результате чего молекула приобретает циклическую структуру.
НОМЕНКЛАТУРА АМИНОКИСЛОТ
Для названия аминокислот используют три типа номенклатуры –тривиальную, рациональнцю и IUPAC.
По систематической номенклатуре (IUPAC) названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино и указанием места расположения аминогруппы по отношению к карбоксильной группе.
Нумерация углеродной цепи начинается с атома углерода карбоксильной группы.
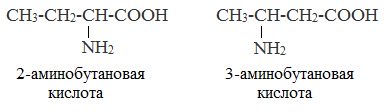
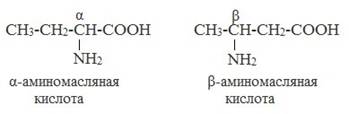
По рациональной номенклатуре к тривиальному названию карбоновой кислоты добавляется приставка амино с указанием положения аминогруппы буквой греческого алфавита.
Формулы и названия некоторых α-аминокислот, остатки которых входят в состав белков
Если в молекуле аминокислоты содержится две аминогруппы, то в ее названии используется приставка диамино, три группы NH2 – триамино и т.д.
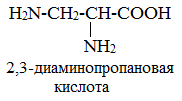
Наличие двух или трех карбоксильных групп отражается в названии суффиксом –диовая или -триовая кислота.
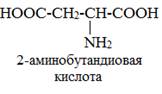
ИЗОМЕРИЯ АМИНОКИСЛОТ
Для аминокислот известны два вида изомерии: структурная и пространственная (оптическая изомерия).
Структурная изомерия
Структурная изомерия связана с особенностями строения углеродного скелета и взаимным расположением функциональных групп.
1. Изомерия углеродного скелета
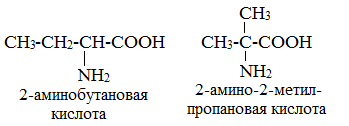
2. Изомерия положения аминогруппы
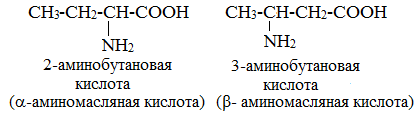
Оптическая изомерия
Все α-аминокислоты, кроме глицина H2N-CH2-COOH, содержат асимметрический атом углерода (a-атом) и могут существовать в виде оптических изомеров (зеркальных антиподов).
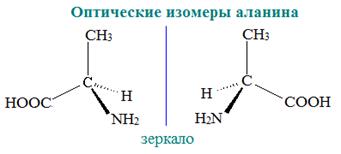
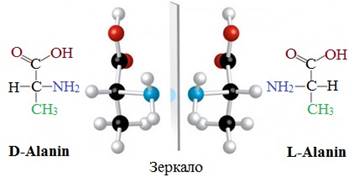
Оптическая изомерия природных α-аминокислот играет важную роль в процессах биосинтеза белка.
ФИЗИЧЕСКИЕ СВОЙСТВА АМИНОКИСЛОТ
Аминокислоты – бесцветные кристаллические вещества с высокой температурой плавления (выше 2500С). Плавление сопровождается разложением вещества. Аминокислоты хорошо растворимы в воде и малорастворимы в органических растворителях. Многие α-аминокислоты имеют сладкий вкус. Водные растворы аминокислот проводят электрический ток.
5. Закрепление изученного материала.
Рассмотрение и изучение формул основных аминокислот
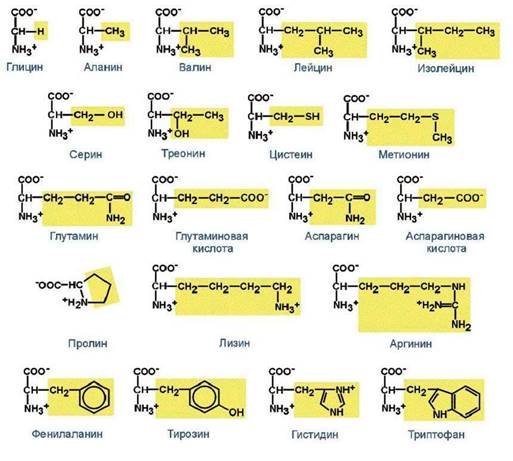
Задание
Напишите структурную формулу аминокислоты по названию и составьте изомер углеродного скелета, изомер положения аминогруппы, межклассовый изомер. Дайте название по систематической номенклатуре каждому веществу.
4-амино – 4- метилпентановая кислота
6. Подведение итогов урока. Рефлексия
7. Домашнее задание: Изучить формулы 20 основных аминокислот и физические свойства аминокислот. Повторить азотсодержащие органические соединения и их свойства.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.