
Зачет по теме «Химические реакции» - ХИМИЧЕСКИЕ РЕАКЦИИ - ПОУРОЧНЫЕ РАЗРАБОТКИ ПО ХИМИИ 11 класс - поурочные разработки - разработки уроков - авторские уроки - план-конспект урока - химия
Цели урока: проверить уровень усвоения теоретических знаний темы и умений их применять в выполнении расчетных задач и упражнений.
Оборудование: карточки заданий теории и практики на I—II варианты.
Ход урока
I. Организационный момент
Инструктаж выполнения зачета.
II. Зачет
Вариант 1
1. Определение скорости гомогенной химической реакции, формула единицы измерения. Как зависит скорость химической реакции: а) от концентрации; б) от катализатора. Дать обоснованный ответ.
2. Дать характеристику химической реакции по всем признакам классификации.
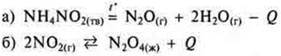
3. По термохимическому уравнению Н2 + Вr2 = 2НВr + 66,8 кДж рассчитать массу брома, вступившего в реакцию, если при этом выделилось 3,34 кДж теплоты.
4. В каком направлении сместится химическое равновесие в следующей системе:
![]()
а) при понижении температуры; б) при повышении давления.
Вариант II
1.
Определение химического равновесия. Константа химического равновесия. Как
влияет изменение концентрации веществ, температура на смещение химического
равновесия. Дать обоснованный ответ на примере реакции ![]()
2. Дать характеристику химической реакции по всем признакам классификации:
![]()
3.
Как изменится скорость химической реакции ![]() если
давление увеличить в 4 раза?
если
давление увеличить в 4 раза?
III. Подведение итогов урока
Ответы на вопросы практики
Вариант I
1. Вопрос теории.
2. ![]()
реакция разложения:
реакция ОВР

реакция гетерогенная — по фазе;
реакция эндотермическая — по тепловому эффекту;
реакция необратимая, некаталитическая.
б) ![]()
реакция изомеризации;
реакция не является ОВР;
по фазе — реакция гетерогенная, по тепловому эффекту — экзотермическая, реакция обратимая, некаталитическая.
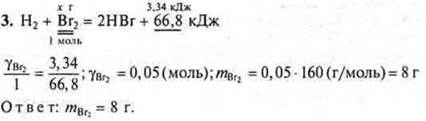
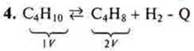
а) t°↓ в сторону экзотермической <- обратная.
б) Р↑ в сторону меньшего объема обратная.
Вариант II
1. Вопрос теории.
![]()
реакция соединения;

реакция гомогенная — по фазе;
реакция эндотермическая — по тепловому эффекту;
реакция обратимая;
реакция некаталитическая.
![]()
реакция обмена; реакция гетерогенная — по фазе;
реакция не ОВР; реакция некаталитическая;
реакция необратимая; тепловой эффект не указан.
![]() Р↑
в 4 раза
Р↑
в 4 раза
до
увеличения давления: ![]()
![]()
после
увеличения давления: ![]()
![]()
![]()
Ответ: скорость реакции возрастет в 64 раза.
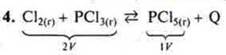
а) Р↑ в сторону меньшего объема, → (прямая);
б) ![]() →
(прямая) в сторону конечных продуктов реакции.
→
(прямая) в сторону конечных продуктов реакции.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.