
Пар – разновидность газообразного вещества. Газ не имеет объема он занимает весь предоставленный ему сосуд, у него нет формы, но пар образуется из жидкости. Понятие пара тесно связано с понятием жидкости.
Почему если имеется жидкость она будет испаряться? Что можно сказать о молекулах жидкости?
Они друг с другом взаимодействуют. Если бы молекулы жидкости не взаимодействовали друг с другом жидкость была бы газом. Из-за того, что между молекулами жидкости существуют силы притяжения довольно заметные жидкость, имеет определенный объем. Не имеет формы, но имеет объем.
Если жидкость имеет объем, но не имеет формы, мы можем сказать, что у жидкости есть свободная поверхность. Если мы наливаем жидкость в сосуд, то жидкость имеет определенный объем и если этот объем меньше чем объем сосуда образуется свободная поверхность жидкости. Об этой поверхности мы сегодня и будем вести речь
Молекулы жидкости взаимодействуют друг с другом
При попытке вытащить молекулу из жидкости “включаются” силы притяжения, которые будут втягивать молекулу обратно в жидкость.
Но почему же некоторые молекулы покидают жидкость, если они находятся на поверхности жидкости? Ведь они притягиваются к жидкости, они не должны улетать.
Когда Вы вытаскиваете молекулу из жидкости в вакуум с поверхности, то на эту молекулу действуют силы притяжения со стороны других молекул. Значит для того, чтобы вытащить молекулу нужно совершить работу. Можно говорить, и по-другому если молекула покидает жидкость, то силы притяжения которые втягивают молекулу обратно совершают работу.
Какой знак работы силы притяжения?
Знак работы силы притяжения “–” потому, что молекула движется от поверхности жидкости в вакуум, а силы притяжения направлены к жидкости. Такую же работу нужно, но уже положительную нужно совершить, если мы хотим вытащить молекулу из жидкости. Эта работа называется “Работа выхода молекулы из жидкости”
Работа всех сил действующих на тело равняется изменению кинетической энергии этого тела.
Молекулы жидкости движутся
Второе положение молекулярной кинетической теории: все молекулы находятся в состоянии непрерывное хаотического движения.
Если молекулы движутся, значит они обладают кинетической энергией, когда молекула вылетает с поверхности жидкости, значит мы можем вспомнить теорему о кинетической энергии. Работа всех сил действующих на тело равняется изменению кинетической энергии этого тела
Работа выхода это отрицательная величина (работа сил втягивающих молекулу обратно). Значит, когда молекула вылетает из жидкости, то это работа отрицательная приводит к уменьшению кинетической энергии (изменение кинетической энергии будет отрицательное).
Если все молекулы имеют кинетическую энергию больше чем работа выхода, что будет с этими молекулами?
Они все улетят. Потому, что работа выхода не сможет уменьшить их кинетическую энергию до 0.
Почему только некоторые молекулы жидкости улетают, превращаясь в молекулы пара?
Разные скорости. Хаотичность движения означает, что у молекул самая разная скорость. Если у данной молекулы находящейся на поверхности жидкости кинетическая энергия меньше чем работа выхода она не сможет из жидкости. Она может быть немножко удалится из поверхности на расстояние порядка размеров молекулы, но потом ее обратно втянет. Но если у какой-то молекулы оказалось, что кинетическая энергия оказалась больше чем работа выхода, она улетит, но таких молекул немного поэтому жидкость не вся превращается в газ, а лишь небольшая часть молекул жидкости покидает. А именно те молекулы у которых кинетическая энергия случайно оказалось больше чем модуль работы выхода, и они должны оказаться при этом у поверхности в результате происходит процесс парообразование с поверхности жидкости.
Как называется процесс парообразования, происходящий с поверхности жидкости?
Парообразование происходящее с поверхности жидкости называется испарением. Скорость испарения зависит от: температуры, площади свободной поверхности жидкости, какая жидкость и существует ли потоки воздуха над жидкостью.
Рассмотрим скорость испарение не со всей жидкости, а с единицы её площади, тогда получается, что скорость испарения от площади зависеть не будет (скорость испарения с единицы поверхности).
Каково влияние ветра, который над поверхностью жидкости существует, почему он испаряет быстрее?
Потому, что ветер (поток газа над поверхностью жидкости) те молекулы, которые уже стали молекулами пара удаляет, если нет ветра, то у этих молекул есть шанс вернуться обратно.
Скорость испарения зависит от рода жидкости и от температуры.
Почему скорость испарения (т.е. число молекулы улетающих с единицы свободной поверхности в единицу времени) зависит от рода жидкости?
Разный характер взаимодействия между молекулами разная работа выхода, работа выхода молекул из жидкости зависит от жидкости (эфир, вода, керосин или др. жидкость)
Почему скорость испарения зависит от температуры?
С ростом температуры увеличивается часть молекул, у которых кинетическая энергия больше чем работа выхода. Если мы возьмем воду, то скорость испарения зависит только от температуры.
Число молекул, вылетающих в единицу времени с единицы свободной поверхности жидкости зависит только от температуры (для данной жидкости).
Рассмотрим противоположный процесс.
Те молекулы, которые вылетели из жидкости могут находится над поверхности жидкости и может так случиться ведь они движутся хаотично, что их скорость направлена внутрь жидкости, они подлетят к поверхности жидкости и их тут же втянет. “Включатся” силы притяжения соседних молекул и молекула пара станет молекулой жидкости этот процесс называется конденсацией – процесс образования жидкостей из пара, обратный процесс испарению.
Для того, чтобы молекула покинула жидкость (сила притяжения совершает над ней работу) её энергия уменьшается, но вылетают все-таки самые быстрые молекулы. Если жидкость покинут самые быстрые молекулы, то в жидкости останутся более медленные молекулы. Жидкость из которой происходит испарение охлаждается, потому что энергия, которую получают молекулы, они получают за счет внутренней энергии жидкости.
Как сделать что бы температура не менялась в процессе испарения?
Нужно подводить тепло из вне. Не за счет внутренней энергии, а за счет подводимого кол-ва теплоты что бы внутреннюю энергию жидкости оставить прежней.
Для
того что бы испарения происходило при неизменной температуре нам необходимо
подводить какое-то количество теплоты – называется теплота парообразования. ![]()
где
L – удельная теплота парообразования (![]() )
)
m – масса жидкости превратившейся в пар
Удельная теплота парообразования – физическая величина равная количеству теплоты, которое нужно сообщить одному килограмму жидкости для превращения её в пар при неизменной температуре.
В пар могут переходить вещества даже из твердого состояния этот процесс называется сублимацией.
Сублимация
– переход вещества из твердого состояния в газообразное. Сублимация сухого льда
углекислота углекислый газ при атмосферном давлении оказывается если его
температура - ![]() он твердый и вот такой
т.н сухой лед он сразу превращается газообразный углекислый газ. На морозе
белье тоже сохнет, когда Вы выносите белье на мороз оно затвердевает вода
превращается в лед, но постепенно оно сохнет.
он твердый и вот такой
т.н сухой лед он сразу превращается газообразный углекислый газ. На морозе
белье тоже сохнет, когда Вы выносите белье на мороз оно затвердевает вода
превращается в лед, но постепенно оно сохнет.
Конденсация
Когда молекула пара приближается к поверхности жидкости её втягивает значит работа, совершаемая силами притяжения будет положительная и равна работе выхода, только с противоположным знаком.
Что будет с кинетической энергией молекулы, которую втянули в жидкость?
Она будет увеличиваться значит если мы пар будем вводить в воду, то вода будет нагреваться, а что бы поддерживать температуры воды постоянно нам нужно её охлаждать. При конденсации, то количество теплоты, которое было израсходовано на парообразование вернется обратно. т.е. количество теплоты, которое выделяется при конденсации
![]() или
или ![]()
От чего зависит скорость конденсации? т.е. количество молекул ежесекундно конденсирующихся на поверхности жидкости в единицу времени на единицу поверхности?
Скорость
конденсации и давление тесно связаны друг с другом. ![]()
![]() -
постоянная Больцмана. Если Вы увеличите в 2 раза концентрацию молекул при
постоянной температуре, то увеличится в 2 раза давление. Если увеличить
концентрацию молекул пара над жидкостью, то в 2 раза увеличится количество молекул,
ударяющихся о жидкость и превращающихся из пара в жидкость.
-
постоянная Больцмана. Если Вы увеличите в 2 раза концентрацию молекул при
постоянной температуре, то увеличится в 2 раза давление. Если увеличить
концентрацию молекул пара над жидкостью, то в 2 раза увеличится количество молекул,
ударяющихся о жидкость и превращающихся из пара в жидкость.
Вывод: скорость конденсации прямо пропорционально давлению пара над поверхностью жидкости.
Число молекул, конденсирующихся за единицу времени на единице поверхности жидкости прямо пропорционально давлению пара над поверхностью.
Рассмотрим пример:

Пусть в цилиндре находится жидкость накрытая поршнем (никакого зазора между жидкостью и поршнем нет) поршень плотно прилегает к жидкости (а) ,

Теперь
быстро поднимем поршень p=0.
Что будет между поршнем и поверхностью жидкости, что образуется сразу?
Вакуум там не будет ничего (б)  так
будет не долго
так
будет не долго
Оставим
поршень в том же самом положении и немного подождем,  поскольку
у нас на рис. б свободная поверхность начнется испарение
поскольку
у нас на рис. б свободная поверхность начнется испарение 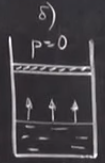 в
результате этого испарения часть жидкости превратится в пар
в
результате этого испарения часть жидкости превратится в пар 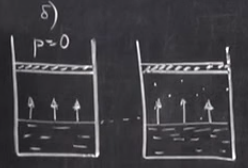 часть
жидкости испарится. Если часть жидкости испарилась, превратившись в пар, то эти
молекулы двигаясь хаотически будут ударяться о поршень, стенки цилиндра, но и о
поверхность жидкости. Попав на поверхность жидкости молекулы будут втянуты
обратно. В результате будет происходить обратный процесс испарения т.е.
конденсация
часть
жидкости испарится. Если часть жидкости испарилась, превратившись в пар, то эти
молекулы двигаясь хаотически будут ударяться о поршень, стенки цилиндра, но и о
поверхность жидкости. Попав на поверхность жидкости молекулы будут втянуты
обратно. В результате будет происходить обратный процесс испарения т.е.
конденсация  и при этом если
достаточно долго подождать, то количество молекул пара будет таким, что
скорость конденсации уравняется со скоростью испарения. Потому, что если
скорость конденсации была бы меньше чем скорости испарения, то число молекул
увеличивалось, а это приводило к увеличению скорости конденсации в ситуации (в)
установится какое-то давление p=p1
, которое определяется скоростью испарения. Значит давление пара будет зависит
от температуры t1
и при этом если
достаточно долго подождать, то количество молекул пара будет таким, что
скорость конденсации уравняется со скоростью испарения. Потому, что если
скорость конденсации была бы меньше чем скорости испарения, то число молекул
увеличивалось, а это приводило к увеличению скорости конденсации в ситуации (в)
установится какое-то давление p=p1
, которое определяется скоростью испарения. Значит давление пара будет зависит
от температуры t1  и
через некоторое время пар будет находится в равновесии со своей жидкость такой
пар называется насыщенным. Если подождать некоторое время, то здесь
будет насыщенный пар
и
через некоторое время пар будет находится в равновесии со своей жидкость такой
пар называется насыщенным. Если подождать некоторое время, то здесь
будет насыщенный пар
Пар находящийся в равновесии со своей жидкостью называется насыщенным.
Повысим температуру до
значения t2>t1.
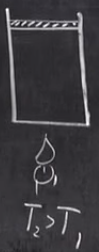 Нам
известно, что скорость температуры зависит от скорости испарения значит при
повышении температуры интенсивность процесса испарения увеличивается и это
приводит к росту количества молекул над жидкостью, но если молекул над
жидкостью (молекул пара стало больше), то интенсивность конденсации тоже
увеличилась, и давление P=P2
в случае (г) для более высокой температуры, давление насыщенного пара
станет больше. P2>Р1
Нам
известно, что скорость температуры зависит от скорости испарения значит при
повышении температуры интенсивность процесса испарения увеличивается и это
приводит к росту количества молекул над жидкостью, но если молекул над
жидкостью (молекул пара стало больше), то интенсивность конденсации тоже
увеличилась, и давление P=P2
в случае (г) для более высокой температуры, давление насыщенного пара
станет больше. P2>Р1

(д) Не
меняя температуру опустим поршень. 
Если мы уменьшим объем, то скорость конденсации преобладает над скоростью испарения и пар начнет конденсироваться до тех пор, пока концентрация молекул пара не уравняется с той которая была раньше при постоянном объеме.

Давление насыщенного пара данной жидкости не зависит от его объема, определяется только температурой.
Это значит, что мы можем зять воду тщательно измерить давление насыщенного пара воды при разных температурах составить таблицу и пользовать в дальнейшем этой таблицей. Тоже самое можно сделать для любой жидкости для эфира, ртути и т.п.
Приведем характерные численные значения насыщенного пара для воды
|
t1 |
Pн, кПа |
|
0 |
0,61 |
|
20 |
2,33 |
|
40 |
7,37 |
|
60 |
19,9 |
Если бы в сосудах был просто газ, а не пар менялось бы давление так стремительно?
Если бы был бы просто воздух, то давление определялось только температурой потому что концентрация была бы постоянной, а насыщенной пар всегда рядом с жидкостью должна присутствовать дикость. Если здесь присутствует жидкость, то при увеличении температуры давление пара растет за счет температуры и за счет роста концентрации. При увеличили температуры увеличивается давление во первых потому что увеличивается концентрации, а во вторых потому что увеличивается абсолютная температура.
При
0![]() = 273 К а при 60
= 273 К а при 60![]() =
333К отношение температур
=
333К отношение температур ![]() абсолютная температура
увеличилась в 1,22 раза , а давление
абсолютная температура
увеличилась в 1,22 раза , а давление ![]() раза. Это значит что за
счет температуры давление увеличилось на 22% а все остальное увеличение
обусловленно увеличением концентрации молекул.
раза. Это значит что за
счет температуры давление увеличилось на 22% а все остальное увеличение
обусловленно увеличением концентрации молекул.
![]() раза
раза
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.