
Предмет: химия
Класс: 8
Учитель: Пальчикова О.В., учитель высшей квалификационной категории МОАУ «СОШ № 40 с углубленным изучением математики» города Оренбурга
Тема: Кислоты
Тип урока: комбинированный.
Цель урока:
Образовательная: сформировать знания о составе и классификации неорганических кислот и их названиях, умения определять принадлежность веществ к классу кислот по формулам и называть их;
Развивающая: развивать навыки самостоятельного учения (планирование своей деятельности, ориентируясь на собственный уровень усвоения материала, работа с учебником и модульным пособием);
Воспитательная: воспитывать ответственное отношение к полученному заданию
Метод проведения: по учебным модулям, беседа, рассказ, демонстрация, элементы лабораторной работы.
Оборудование: таблица Д. И. Менделеева, карточки с заданием, технологическая карта урока; растворы важнейших неорганических и органических кислот: соляной, серной, азотной, уксусной, лимонной; индикаторы (лакмус, метиловый оранжевый, фенолфталеин); стеклянная химическая посуда.
На столах учащихся: штативы с пробирками, растворы кислот, индикаторы, кусочек лимона.
Технологическая карта модульного урока
по теме «Кислоты»
|
Номер учебного элемента, время работы. |
Учебный материал с указанием целей и заданий. |
Рекомендации по выполнению заданий. Освоение способов учебной деятельности. |
||||||||||||||||
|
УЭ – 0. 3 мин. (2 слайд) |
Интегрирующая цель урока: в процессе работы над учебными элементами вы должны:
|
Внимательно прочитайте цель урока.
|
||||||||||||||||
|
УЭ – 1 7 мин. (3 слайд)
(4 слайд) |
Входной контроль Цель: определить исходный уровень знаний необходимых для изучения модуля; переключать, вырабатывать умения быстро находить верные и отвергать неверные суждения. Сегодня вы покажите, как научились составлять формулы оксидов и оснований по их названиям. С этой целью проведем небольшую проверочную работу. ПРИЛОЖЕНИЕ № 1
|
Работайте индивидуально.
Выполняйте проверочную работу по вариантам.
Выполните взаимопроверку в парах в соответствии с ответами 4 слайда, оцените результат по количеству верно выполненных заданий (1 формула – 1 балл) |
||||||||||||||||
|
УЭ – 2. 20 мин.
(5 слайд)
(6 слайд)
(7 слайд)
(8 слайд)
(9 слайд)
(10 слайд)
(11 слайд) |
Цель: познакомить учащихся с новым классом неорганических соединений — кислотами, изучить их состав и классификацию, рассмотреть физические свойства кислот.
Сегодня на уроке мы продолжим знакомиться с многообразием веществ, на примере нового класса неорганических соединений – это КИСЛОТЫ.
I. Перед нами стоит ПЕРВАЯ учебная задача: Изучить состав нового класса неорганических веществ - кислот?
-На какие две группы можно разделить все вещества по их составу? -Какими по составу веществами являются кислоты?
1.Обратите внимание на ряд формул кислот в учебнике на странице 102 и перепишите их в тетрадь, дополнив этот список ещё двумя кислотами: соляная кислота и сероводородная кислота.
2.Важнейшие кислоты известны человечеству с древнейших времен, поэтому и названия исторические, тривиальные.
3.Кислоты в своем составе могут содержать как 2, так и 3 химических элемента. -Чем образована молекула серной кислоты? - А чем образована молекула соляной кислоты?
4. Давайте попробуем ответить на вопрос, какие вещества называются кислотами? Ответ. Кислоты – это сложные вещества, молекула которых состоит из одного или нескольких атомов водорода и кислотного остатка.
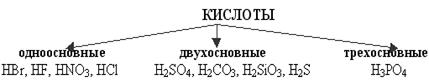
II. Теперь перед нами стоит ВТОРАЯ учебная задача: По каким признакам можно классифицировать кислоты? 1. Кислоты можно классифицировать по нескольким признакам. У вас на технологической карте изображено два ряда формул. - Какую закономерность вы видите? Какие могут быть кислоты? Кислоты можно классифицировать по содержанию кислорода: . (На 6 слайде раскрывается классификация кислот по наличию кислорода) --- Кислоты можно классифицировать по числу атомов водорода, т.е. по основности: Кислоты, имеющие один атом водорода, называют одноосновные, два – двухосновные, три – трехосновные.
(На 7 слайде раскрывается классификация кислот по числу атомов водорода) В технологической карте запишите вывод по поставленной задаче.
Вывод. Кислоты делятся на кислородсодержащие и бескислородные по наличию кислорода; на одноосновные, двухосновные и трехосновные по количеству атомов водорода.
III. Приступая к решению ТРЕТЬЕЙ учебной задачи, нам необходимо вспомнить технику безопасности при работе в кабинете химии.
Итак, третья учебная задача: Какие особенные физические свойства характерны для кислот?
1. Перед вами на столах стоят склянки с кислотами и лежит ломтик лимона. Какой он на вкус?
2. Подберите однокоренные слова к слову кислота. - Кисло, кислый.
3. Таким образом, само название класса указывает на одно из физических свойств кислот. Действительно кислоты имеют кислый вкус, его вы ощущаете, когда положите на язык ломтик лимона, в соке которого содержится небольшое количество лимонной кислоты. Но пробовать на вкус кислоты ни в коем случае нельзя – можно отравиться или получить сильный химический ожог, так как кислоты обладают разъедающим действием
4. (Демонстрация: “Действие концентрированной серной кислоты на лучину”).
5. Это свойство используется, например, при консервировании. Микроорганизмы, находящиеся в консервируемых продуктах, разрушаются под действием кислоты. Для этого используют чаще уксусную или лимонную кислоты. Обращаться с кислотами нужно очень осторожно, не допуская их попадания на кожу или одежду. Запишите в технологической карте физические свойства кислот, о которых сейчас было сказано (на 9 слайде раскрываются физические свойства кислот).
6. Ребята перед вами стоят две пробирки с растворами, но без этикеток. Среди них должна быть и кислота. ? Определите в какой пробирке находится кислота.
7. Действительно кислоты определяют с помощью специальных веществ - индикаторов, о которых вы уже слышали при изучении оснований (работа с таблицей индикаторов). 8. У вас на столах находится раствор соляной кислоты и два индикатора: лакмус и метиловый оранжевый. Налейте в две пробирки раствора соляной кислоты и в одну добавьте несколько капель лакмуса, а в другую - метилового оранжевого. !!! Сделайте вывод по увиденному и запишите его.
Вывод: присутствие кислоты легко определить с помощью индикаторов. Лакмус и метиловый оранжевый в кислой среде имеют красную окраску.
!!! На основании проведенных опытов сделаем выводы: Таким образом, поставленные учебные задачи мы выполнили. |
Работайте устно, с классом.
Работайте с учебником. Выписать названия и формулы кислот в тетрадь
Ответьте на вопросы Запишите определение кислоты в технологической карте. ПРИЛОЖЕНИЕ №2
Работа с технологической картой
Работа с личной технологической картой Записать вывод.
Внимательно рассмотрите выданные вещества
Наблюдение демонстрационного опыта.
При выполнении опытов работайте в паре. Начинайте исследование по команде учителя.
Запишите вывод в технологическую карту
Обсуждение результатов и формулирование выводов.
|
||||||||||||||||
|
УЭ-3 1-2 мин. (12 слайд) |
Динамическая пауза (физкультминутка)
|
Смотрим на экран. |
||||||||||||||||
|
УЭ – 4 10 мин.
(13 слайд)
(14 слайд) |
Цель: обобщить знания, полученные на уроке (выходной контроль) 1. Выполнение проверочной работы, состоящей из трех зданий.
Задание № 1 Вам хорошо известна игра “Крестики-нолики”. В данной таблице определите выигрышный путь «Кислоты».
Таблица № 1
Задание № 2 Зачеркните лишнюю формулу в каждом ряду: а) NaCl, HNO3, H2SO4, H2SiO3 б) HCl, H2S, CuO, HBr
Составьте классификацию данных кислот по основности:
КИСЛОТЫ
____________________ ___________________
Задание № 3 Найдите в таблице задания № 1 кислоты и классифицируйте их по содержанию кислорода: КИСЛОТЫ
______________________ ______________________
2. Самопроверка. Учащиеся проверяют свои ответы по 12 слайду презентации, к данному модульному уроку. За правильно выполненное
|
Работа самостоятельная.
Внимательно прочтите задания. Четко сформулируйте и запишите ответ (ПРИЛОЖЕНИЕ №3)
По слайду «Ответы» проверьте правильность выполнения своих заданий и оцените их. |
||||||||||||||||
|
УЭ – 5 2 мин. |
Цель: подведение итогов урока, выяснение усвоения учебных элементов модульного урока. Беседа с учениками о выполнении учебных элементов урока, т.е сколько учеников считает, что справились с задачами урока. ПРИЛОЖЕНИЕ № 4 |
Работайте все вместе с учителем Подсчитайте количество баллов. Поставьте оценку в дневник.
|
||||||||||||||||
|
УЭ – 6 2 мин. (15 слайд) |
Цель: определить для себя домашнее задание.
|
Работая с оценочным листом определите для себя домашнее задание и запишите его в дневник
Если вы затрудняетесь в выборе домашнего задания, обратитесь к учителю. |
||||||||||||||||
|
УЭ – 7 1-2 мин. (16 слайд) |
Рефлексия Цель: Проанализировать учащимся свою удовлетворенность уроком. Обратитесь к целям, которые поставлены перед вами на данном уроке, оцените, насколько вы смогли их достичь? В какой степени? С каким настроением вы уходите с урока? Нарисуйте. (Дети рисуют смайлы на оценочном листе, характеризуя свое настроение). |
Работайте индивидуально |
ПРИЛОЖЕНИЕ № 1
|
Проверочная работа по теме “Оксиды. Основания” Вариант 1. Вам даны для выполнения два задания, но каждое из них имеет два варианта. Самостоятельно выберите себе по силам и выполните один из вариантов задания. При правильном выполнении заданий варианта № 1 вы получите оценку – четыре; варианта № 2 – пять. Выполнять можно только один вариант из предложенных. 1. Запишите формулы оснований: вариант № 1: гидроксид натрия, гидроксид лития, гидроксид цинка. вариант № 2: гидроксид магния, гидроксид меди (II), гидроксид алюминия. 2. Составьте формулы оксидов, соответствующих гидроксидам: вариант № 1: гидроксид натрия, гидроксид цинка. вариант № 2: гидроксид магния, гидроксид алюминия. |
Проверочная работа по теме “Оксиды. Основания” Вариант 2. Вам даны для выполнения два задания, но каждое из них имеет два варианта. Самостоятельно выберите себе по силам и выполните один из вариантов задания. При правильном выполнении заданий варианта № 1 вы получите оценку – четыре; варианта № 2 – пять. Выполнять можно только один вариант из предложенных. 1. Запишите формулы оснований: вариант № 1: гидроксид калия, гидроксид рубидия, гидроксид бария. вариант № 2: гидроксид железа (III), гидроксид кальция, гидроксид стронция. 2. Составьте формулы оксидов, соответствующих гидроксидам: вариант № 1: гидроксид калия, гидроксид бария. вариант № 2: гидроксид железа (III), гидроксид кальция. |
ПРИЛОЖЕНИЕ №2
Технологическая карта ученика(цы)________________________________
Тема «Кислоты»
I. Определение, состав и классификация.
Вывод. Кислоты – это _________________________________________________________
_____________________________________________________________________________
а) HNO3, H2SO4, H2SiO3
б) HCl, H2S, HBr
Вывод. Кислоты делятся на ________________ и __________________ по наличию _________________; на __________________, __________________ и ____________________ по количеству атомов ____________________.
II. Физические свойства.
Запишите
физические свойства кислот: __________________________________________
__________________________________________________________________________________________________________________________________________________________
Вывод. Присутствие кислоты можно определить с помощью _____________.
Лакмус и метиловый оранжевый в кислой среде имеют _______________ окраску.
ПРИЛОЖЕНИЕ № 3
|
Задание № 1 Вам хорошо известна игра “Крестики-нолики”. В данной таблице определите выигрышный путь «Кислоты». Таблица № 1
Задание № 2 Зачеркните лишнюю формулу в каждом ряду . а) NaCl, HNO3, H2SO4, H2SiO3 б) HCl, H2S, CuO, HBr Составьте классификацию данных кислот по основности:
КИСЛОТЫ
____________________ ___________________
Задание № 3 Найдите в таблице задания № 1 кислоты и классифицируйте их по содержанию кислорода: КИСЛОТЫ
______________________ ______________________
2. Самопроверка. Учащиеся проверяют свои ответы по слайду «Ответы и решения», к данному модульному уроку. За правильно выполненное
|
||||||||||||||||
|
|
ПРИЛОЖЕНИЕ № 4
ОЦЕНОЧНЫЙ ЛИСТ
________________________________________
1. Выполнение учебных элементов
|
УЭ – 1
|
УЭ - 2 |
УЭ - 4 |
Средний балл |
|
|
|
|
|
2. Оцениваю собственные знания и умения
Я ставлю себе оценку ____________________
Моя итоговая оценка _____________________
Мое настроение после урока ______________________
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.