
ПЛАН-КОНСПЕКТ УЧЕБНОГО ЗАНЯТИЯ
Наименование учебной дисциплины:
ОП.04 Основы материаловедения (15.01.30 Слесарь)
ОП.03 Основы материаловедения (15.01.05 Сварщик (ручной и частично механизированной сварки (наплавки)*
Наименование темы учебного занятия: Коррозия металлов, причины, типы, способы защиты
Коррозионная стойкость.*
Обучающая цель учебного занятия:
- имеет общее представление о коррозии металлов;
- понимает принципы классификации и основные параметрические характеристики коррозии;
- анализирует причинно-следственные связипричины возникновения коррозионных процессов.
Развивающая цель учебного занятия:
- на уровне зрительного восприятия выделяет роль коррозии на эксплуатационные характеристики деталей, конструкций и машин;
- на уровне внимания способен сосредоточиться на работе, требующей систематизации и структуризации информации;
- на уровне мышления способен выстраивать причинно-следственные связи между причинами возникновения коррозионных процессов и методами борьбы с коррозией металлов.
Воспитывающие цели учебного занятия:
осознавая сущность и социальную значимость будущей профессии, способен анализировать сущность коррозионных процессов и решать ситуационные задачи.
Ведущая педагогическая технология:учебно-исследовательская деятельность.
Тип учебного занятия: учебное занятие по формированию новых знаний.
Вид учебного занятия: учебное занятие мини- исследование.
Форма организации учебного занятия:интерактивная форма проведения учебного занятия.
Методы, применяемые на учебном занятии:
1. по принципу расчленения или соединения знаний – синтетический, обобщающий, сравнительный;
2. по уровню познавательной активности – проблемный.
3. наглядно-демонстрационные методы (применение мультимедийных презентаций).
Приемы, применяемые на учебном занятии:
1. инструментарий ТРИЗ – АРИЗ;
2. метод проектов
3. по источнику знаний – словесные, практические и наглядные.
Оборудование для учебного занятия:
1. Мультимедийное оборудование для визуализации презентации;
2. Электронная презентация «Коррозия металлов» (фоновая);
3. Комплект раздаточного материала для обучающихся:
- бланки для решения ситуационных задач;
- бланки рефлексии для студентов;
- бланки рефлексии для слушателей курсов.
4. Лабораторное оборудование: колбы и пробирки (5 шт.), 5 гвоздей, вода проточная, соль поваренная, кусок медной проволоки, кусок алюминиевой проволоки, раствор гидроксида натрия, емкость для воды, демонстрационный стол, перчатки, халат, шапочка.
Продолжительность учебного занятия: 45 минут.
План учебного занятия
|
Этапы учебного занятия |
Время отводимое на этап |
|
1.Организационно-мотивационный момент, опережающее домашнее задание, актуализация опорных знаний |
5 минуты |
|
2. Операционно-исполнительный этап: 2.1. Историческая страница (сообщение обучающегося) 2.2. Информационная страница (сообщение обучающегося) |
10 минут |
|
3. Экспериментальная страница технология проектной деятельности по учебно-исследовательской работе «Коррозия металлов») |
6 минут |
|
4. Практическая страница Решение ситуационной задачи с помощью Алгоритма решения изобретательских задач на тему «Коррозия металла» |
17 |
|
5. Оценочно-рефлексивный этап |
4 минуты |
|
6. Выдача домашнего задания – подготовка докладов и электронных презентаций |
2 минуты |
|
Итого: |
45 минут |
ХОД УЧЕБНОГО ЗАНЯТИЯ
Здравствуйте, уважаемые студенты!
I. Организационно-мотивационный момент, актуализация знаний обучающихся (5 минут):
1. Проверить явку обучающихся по журналу.
2. Проверить готовность к учебному занятию (состояние здоровья, самочувствия обучающихся).
3. Сообщить наименование темы учебного занятия.
4. Сообщить цель и задачи учебного занятия.
5. Ознакомить с планом учебного занятия.
6. Актуализировать опорные знания обучающихся
Сегодня нам предстоит провести необычное учебное занятие-исследование. Для этого нам придётся перелистать страницы удивительной книги «КОРРОЗИЯ МЕТАЛЛОВ». Кроме того, у вас есть опережающее домашнее задание – выполнить сообщения по данной теме.
Слайды электронной презентации на время станут исследовательским дневником. На слайдах мы будем отображать промежуточные и итоговые результаты исследования. А ваши тетради станут личными дневниками, не забывайте вести записи.
Уважаемые обучающиеся, прежде чем говорить о текущей теме учебного занятия, нам необходимо вспомнить основные критерии работоспособности деталей и узлов машин из курса учебной дисциплины «Техническая механика», который мы освоили в прошлом семестре. И дать определение термину «Работоспособность деталей и узлов машин», так как они тесно связаны с объектом нашего исследования – коррозия металла.
Ежегодно из-за коррозии теряется около четверти всего произведенного в мире железа. Однако не только потеря металлов, но и порча изготовленных из них изделий обходится очень дорого. Затраты на ремонт или на замену деталей судов, автомобилей, аппаратуры химических производств, приборов и коммуникаций во много раз превышают стоимость металла, из которого они изготовлены.
Коррозия вызывает серьезные экологические последствия. Утечка газа, нефти и других опасных химических продуктов из разрушенных коррозией трубопроводов приводит к загрязнению окружающей среды, что отрицательно воздействует на здоровье и жизнь людей.
Выполним промежуточные выводы о том, что КОРРОЗИЯ – ЭТО РАЗРУШАЮЩИЙ ФАКТОР ДЛЯ МЕТАЛИЧЕСКИХ ДЕТАЛЕЙ, КОНСТРУКЦИЙ И МАШИН. И, КАК СЛЕДСТВИЕ, НЕ ВЫПОЛНЕНИЕ
КРИТЕРИЕВ РАБОТОСПОСОБНОСТИ. Записываем эти выводы в рабочую тетрадь.
II. Операционно-исполнительный этап (10 минут):
Уважаемые студенты, нашу интерактивную книгу «КОРРОЗИЯ МЕТАЛЛОВ» листаем дальше…Переходим к исторической странице, которая подразумевает выполнение опережающего домашнего задания. Слово представляется Недоросткову Александру.
2.1. Историческая страница (выступление студента) – 5 минут
Коррозией металлических материалов наука занимается уже достаточно давно и этому свидетельствуют следующие исторические факты. Например, в рукописях древности были обнаружены первые попытки применения олова для защиты железа от ржавчины. Авторами этого научного факта являются древнегреческий историк Геродот, живший в V в. до н. э. и древнеримский ученый Плиний старший, живший в I в. н.э.
Далее обратимся к научным достижениям нашей эры. И мысленно переместимся уже на начало 19 века. Когда английский химик Гемфри Деви в 1813году открыл электрохимическую коррозию металлов, английский физик Майкл Фарадей её подробно исследовал и описал. Затем в 1830 году швейцарский ученый Огюст де ла Рив сформулировал первую теорию коррозии. А вначале 30-х годов ХХ века Александр Наумович Фрумкин изучал амальгамы металлов. Кроме того, он считается основоположником современной теоретической электрохимии.
Кроме того, необходимо назвать основоположника теории коррозии металлов - это Алексей Иванович Шултин, который в 1935 году объяснил коррозию как металлов, так и сплавов. Он рассмотрел механизм протекания процесса коррозии и факторы, влияющие на его скорость.
В том же 1935 году Ярослав Васильевич Дурдин выдвинул мысль о растворении металлов в кислотах без наличия инородных включений в них. Таким образом, советские ученые, в первую очередь Шултин и Дурдин, сформулировали теорию электрохимической коррозии металлических материалов.
Спасибо за внимание! Готов ответить на вопросы.
Обучающиеся, не забываем делать промежуточные выводы. В ваших дневниках-рабочих тетрадях должна появится запись:
СОВРЕМЕННОЕ НАУЧНОЕ ПРЕДСТАВЛЕНИЕ О КОРРОЗИИ МЕТАЛЛИЧЕСКИХ МАТЕРИАЛОВ ОСНОВЫВАЕТСЯ НА ФУНДАМЕНТАЛЬНЫХ ИССЛЕДОВАНИЯХ ГЕРОДОТА, ПЛИНИЯ, ДЕВИ, ФАРАДЕЯ, ФРУМКИНА, ШУЛТИНА И ДУРДИНА.
Уважаемые студенты, листаем дальше интерактивную книгу «КОРРОЗИЯ МЕТАЛЛОВ» …Переходим к информационной странице, которая снова подразумевает выполнение опережающего домашнего задания. Слово представляется Гусеву Дмитрию.
2.2. Информационная страница (студент) – 5 минут:
Коррозионные процессы классифицируют по нескольким параметрам, а конкретные типы коррозии различают по некоторым признакам. Например, рассмотрим классификацию основных видов коррозии по механизму протекания процессов. Здесь необходимо назвать химическую и электрохимическую коррозию, кислородную и водородную коррозию.
Таким образом, под электрохимической коррозией будем понимать механизм реакционного соприкосновения раствора электролита с металлом, скорость реакций обусловлена электродным потенциалом.
Если происходит восстановление ионов H3O+ или молекул воды H2O, говорят о водородной коррозии. А если водород не выделяется, что часто происходит в нейтральной или сильно щелочной среде, происходит восстановление кислорода и здесь говорят о кислородной коррозии. Коррозионный элемент может образовываться не только при соприкосновении двух различных металлов.
Химическая коррозия представляет собой процесс контакта элемента металла со средой, способствующий развитию коррозии, во время которого реакция окисления металлического элемента и восстановления самой окислительной среды происходит одновременно.
Теории коррозии металлических материалов так же принято рассматривать классификацию типов коррозии по виду коррозионной среды и условиям. Здесь можно назвать:
· газовая коррозия;
• атмосферная коррозия;
• коррозия при переменном, неполном и полном погружении;
• коррозия по ватерлинии;
• биокоррозия;
• коррозия внешним и блуждающим током;
• контактная коррозия, коррозия при трении;
• сплошная, равномерная и неравномерная коррозия;
• поверхностная, точечная, структурная, межкристаллическая коррозия.
Таким образом, коррозия металлов наносит большой экономический вред. Человечество несет огромные материальные потери в результате коррозии трубопроводов, деталей машин, судов, мостов, морских конструкций и технологического оборудования.
Спасибо за внимание! Готов ответить на вопросы.
Обучающиеся, не забываем делать промежуточные выводы. В ваших дневниках-рабочих тетрадях должна появится запись:
КОРРОЗИЯ МЕТАЛЛИЧСКИХ МАТЕРИАЛОВ ПО ВИДУ КОРРОЗИОННОЙ СРЕДЫ БЫВАЕТ: ГАЗОВАЯ, ЖИДСКОСТНАЯ, АТМОСФЕРНАЯ, ПОЧВЕННАЯ И КОРООЗИЯ БЛУЖДАЮЩИХ ТОКОВ. ПО ХАРАКТЕРУ РАЗРУШЕНИЯ РАЗЛИЧАЮТ: СПЛОШНУЮ, МЕСТНУЮ, МЕЖКРИСТАЛЛИЧЕСКУЮ. ПО МЕХАНИЗМУ КОРРОЗИОННЫХ ПРОЦЕССОВ ВЫДЕЛЯЮТ: ХИМИЧЕСКУЮ И ЭЛЕКТРОХИМИЧЕСКУЮ.
Уважаемые студенты, мы продолжаем наше исследование и листаем познавательную книгу «КОРРОЗИЯ МЕТАЛЛОВ» дальше и обращаем внимание на экспериментальную страницу.
3. Экспериментальная страница (технология проектной деятельности
Как мы с Вами знаем, уважаемые студенты, согласно учебного плана по специальности Технология машиностроения предусмотрена для изучения общеобразовательная дисциплина Технология проектной деятельности, в рамках которой мы разрабатывали проекты и занимались исследовательской деятельностью. И мне хотелось бы представить пример лучшей учебно-исследовательской работы. Таким примером может послужить работа Чернова Максима студента группы 3ТМ15-1, занимающийся уже три года по теме «Коррозия металла». Слово представляется Чернову Максиму.
Отчет студента по учебно-исследовательской работе «Коррозия металлов» – 7 минут:
Резюмируя результаты исследования по теоретическим аспектам природы возникновения коррозии металлов, необходимо вернуться к научному описанию термина «коррозия металлов». Обратимся к российской системе стандартизации, где коррозия металлов определена как разрушение металлов вследствие химического и электрохимического взаимодействия их с коррозионной средой.
Для исследования коррозии металлов в современной науке применяется качественная и количественная оценка коррозионной стойкости металлов и средств защиты. Например, десятибалльная шкала коррозионной стойкости металлов. Затем, для оценки глубины коррозионного разрушения так же используются качественные и количественные методы. К качественным методам исследования коррозии относят визуальный, индикаторный, микроскопический методы. А к количественным методам исследования коррозии – весовой и объемный. Кроме того, в научной практике выполняются лабораторные методы исследования коррозии в форме опытов (испытаний) и экспериментов. При этом, результаты практических исследований коррозии металлов должны характеризовать такие параметры коррозии металлов, как показатель изменения массы, объемный показатель коррозии, показатель сопротивления, механический показатель коррозии, глубинный показатель коррозии.
В виду того, что в данный момент времени у нас здесь нет специальных лабораторных условий, поэтому выполним простой опыт на исследование скорости коррозии и химической коррозии металлов.Для проведения опыта мы приготовили 5 колб и 5 железных гвоздей:
1-й колба – заполнили обычной проточной водой и опустили в неё гвоздь.
2-й колба – заполнили проточной водой, добавили поваренной соли и опустили в неё гвоздь.
3-й колба – заполнили проточной водой с поваренной солью, к гвоздю прикрепили медную проволоку и опустили в колбу.
4-й колба - заполнили проточной водой с поваренной солью, к гвоздю прикрепили предварительно зачищенную наждачной бумагой алюминиевую проволоку и опустили в колбу.
5-й колба - заполнили проточной водой с поваренной солью, добавили в раствор гидроксид натрия и опустили в него железный гвоздь.
Проанализируем результаты эксперимента.
1-я колба - железо слабо прокорродировало, так как в чистой воде коррозия идет медленнее, потому что вода слабый электролит. Наблюдается химическая коррозия.
2-я колба - скорость коррозии гораздо выше, чем в первом случае, следовательно, поваренная соль (хлорид натрия) увеличивает скорость коррозии. Наблюдается химическая коррозия.
3-я колба - железный гвоздь в контакте с медной проволокой, опущенный в раствор хлорида натрия увеличивает коррозии. Следовательно, хлорид натрия – это сильная коррозионная среда для железа, особенно в случае контакта с менее активным металлом – медью.
4-я колба - так же наблюдается коррозия железного гвоздя, алюминиевая проволока остается без изменений, хотя её перед началом опыта очистили от оксидной пленки наждачной бумагой, вероятно, оксидная пленка образовалась снова.
5-я колба - железный гвоздь, размещенный в раствор хлорида натрия, к которому добавили гидроксид натрия, демонстрирует отсутствие коррозии железа (металла).
Следовательно, коррозией металлов можно управлять, зная современные защитные средства. Поэтому современные технологии защиты металлов от коррозии ориентируются на следующие методы:
• повышение химического сопротивления конструкционных материалов;
• изоляция поверхности металла от агрессивной среды;
• понижение агрессивности производственной среды;
• снижение коррозии наложением внешнего тока (электрохимическая коррозия).
Спасибо за внимание! Готов ответить на ваши вопросы.
Обучающиеся, не забываем делать промежуточные выводы. В ваших дневниках-рабочих тетрадях должна появится запись:
УПРАВЛЯЕМОСТЬ КОРРОЗИОННЫХ ПРОЦЕССОВ ОРИЕНТИРОВАНА НА ИСПОЛЬЗОВАНИЕ ЗАМЕДЛИТЕЛЕЙ КОРРОЗИИ, НАПРИМЕР, ГИДРОКСИД НАТРИЯ. АЛЮМИНИЕВЫЕ ПОКРЫТИЯ ДЛЯ КОНСТРУКЦИОННЫХ ДЕТАЛЕЙ МАШИН И МЕХАНИЗОВ ИСПОЛЬЗОВАТЬ НЕЛЬЗЯ, ТАК КАК ОНИ НЕ ВЫПОЛНЯЮТ ЗАЩИТНУЮ ФУНКЦИЮ.
Уважаемые студенты, мы наконец дошли до практических страниц интересной книги «КОРРОЗИЯ МЕТАЛЛОВ». Обращаем внимание на практическую страницу.
4. Практическая страница (17 минут):
4.1. Вводный инструктаж по ТРИЗ И АРИЗ (2 минут):
Рассмотрим и проанализируем понятий аппарат и структуру АРИЗ.
Таким образом, АРИЗ – это алгоритмичная программа для детального анализа задачи с пошаговым продвижением к ответу. В теории и практики ТРИЗ существует много вариантов структуры АРИЗ. Мы воспользуемся упрощенным вариантом АРИЗ-85, предложенный Г.С. Альтшуллером в 1985 году.

ТЕХНИЧЕСКАЯ СИСТЕМА – это некоторая совокупность взаимосвязанных элементов, обладающая свойствами, не сводящимися к свойствам отдельных элементов.
ПОЛЕЗНОЕ ДЕЙСТВИЕ ТС- компонент ТС, который помогает найти решение.
ВРЕДНОЕ ДЕЙСТВИЕ ТС-компонент ТС, который затрудняет найти решение.
КОНФЛИКРУЮЩАЯ ПАРА- компоненты ТС, которые противодействуют друг другу.
АДМИНИСТРАТИВНОЕ ПРОТИВОРЕЧИЕ – противоречие, решающее административные вопросы.
ТЕХНИЧЕСКОЕ ПРОИВОРЕЧИЕ-противоречие, описывающее суть противостояния компонентов внутри системы.
ФИЗИЧЕСКОЙ ПРОТИВОРЕЧИЕ - противоречия описывающие законы физики внутри ТС.
ХИМИЧЕСКОЕ ПРОТИВОРЕЧИЕ –противоречия описывающие законы химии внутри ТС.
ИКР – Элемент самвыполняет требуемое действие (вместо иного элемента)продолжая выполнять функцию, ради которой он был первоначально создан.
4.2. Решение ситуационной задачи с помощью Алгоритма решения изобретательских задач на тему «Коррозия металла» (15 минут)
УСЛОВИЯ СИТУАЦИОННОЙ ЗАДАЧИ:
В декабре 1967 года произошло крупномасштабное происшествие в следствие электрохимической коррозии с норвежским рудовозом «Анатина», который следовал из Кипра в Осаку (Япония). Налетевший в Тихом океане тайфун привёл к попаданию в трюмы солёной воды. Вскоре морская вода размягчила корпус судна и оно подало сигнал бедствия. Экипаж был спасён подоспевшим немецким судном, а сама «Анатина» еле-еле добралась до порта. Почему так произошло? Что не предусмотрели инженеры-конструкторы?
АЛГОРИТМ РЕШЕНИЯ СИТУАЦИОННОЙ ЗАДАЧИ:
1. Описываем техническую систему: Морская вода Тихого океана (химический состав); Тайфун (сила действия природного явления), высокие штормовые волны; Люди (экипаж), Конструктивное строение рудовоза (судна): стальной корпус, медные конструкции во внутренней отделке трюмов; Время пребывания в пути.
2. Описываем полезное и вредное действие элементов технической системы:
ПД: Тихий океан помогает рудовозу транспортировать сырье из Кипра в Осаку (Японию).
ВД1: природная стихия (Тайфун) и высокие штормовые волны могут привести к бедствию судна.
ВД2: морская (солёная) вода – отличный электролит, а медный концентрат + стальной корпус судна – это гальваническая пара. Следовательно, размягчение корпуса судна.
3. Определяем конфликтующую пару (КП): морская (солёная) вода (её химический состав) и медно-стальной корпус судна.
4. Определяем противоречия:
4.1. Административное противоречие (АП)– если бы экипаж судна своевременно узнал о надвигающемся тайфуне,то смог поменять путь следования и не натолкнуться на природную стихию, но встреча с природной стихией неизбежна рано или поздно.
4.2. Техническое противоречие(ТП) – если бы инженеры-судостроители учли бы научные знания о рядах химической активности металлов при выбореконструктивных материалов для судна и химическом составе солёной морской воды, то смогли бы предусмотреть появление коррозионных процессов электрохимической коррозии металлических материалов,но существуют безопасные технологии покрытий конструктивных деталей.
4.3. Химическое противоречие (ХП)– если использовать безопасные покрытия (например, цинкование или оцинковку)корпусных деталей, то не образуется гальваническая пара (стальной корпус + медные концентрат), но покрытия должны сохранять эксплуатационную герметичность.
5. Идеально конечный результат (ИКР)- корпус судна должен сам противостоять коррозионным процессам электрохимической коррозии металлических материалов.
6. РЕШЕНИЕ:
Решение 1: технология цинкования
Решение 2: технология газотермического напыления, образующая сверхтонкие защитные покрытия.
Решение 3: технология термодиффузионных покрытий, создающая прочную поверхностную защиту.
Решение 4: технология кадмирования, обеспечивающая защиту конструкционной стали в морской воде.
5. Оценочно-рефлексивный этап – 4 минуты:
Уважаемые студенты, вот почти наша исследовательская книга «КОРРОЗИЯ МЕТАЛЛА» подошла к концу. И мы переходим к рефлексивной страницы. У каждого из вас есть бланк индивидуальной графической рефлексии. Ваша задача в течение 1 минуты заполнить бланк, отвечая на вопросы:
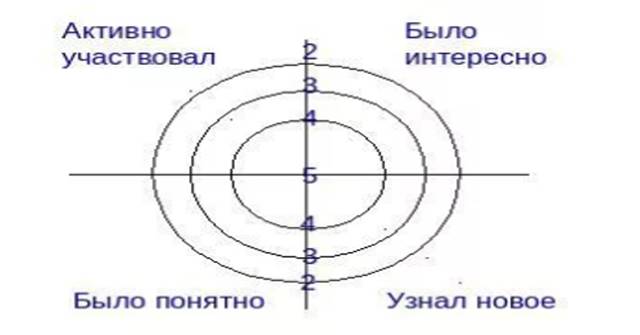
- АКТИВНО участвовал
- БЫЛО интересно
- БЫЛО понятно
- УЗНАЛ новое.
Студенты заполняют бланк индивидуальной графической рефлексии
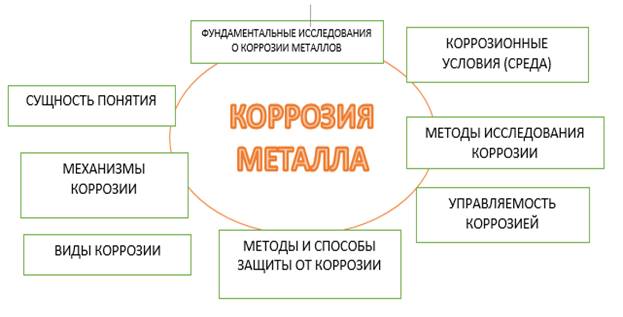
Теперь мы с Вами разделим на микрогруппы из 2 человек и заполним бланк групповой рефлексии, который предусматривает описание опорных ваших знаний по теме учебного занятия «КОРРОЗИЯ МЕТАЛЛА». В кластере можно обозначить основные объекты, явления, процессы и механизмы текущей темы. Время выполнения задания – 1 минута
ЭТАЛОН ВЫПОЛНЕННОГО ЗАДАНИЯ
Сейчас мы переходим на предпоследнюю страницу интерактивной книги «КОРРОЗИЯ МЕТАЛЛА», которая называется страница «УСПЕХОВ И НЕУДАЧ». Вашему вниманию предлагаются критерии оценки деятельности на текущем учебном занятии.
Оценка 5 баллов ставится студенту, который выполнил опережающее домашнее задание, вел текущие записи в рабочей тетради-дневнике исследования, активно задавал вопросы, участвовал в дискуссии, предлагал решения к ситуационной задаче и в групповой рефлексии обозначил опорные понятия по теме коррозия металла.
Оценка 4 балластавится студенту, который выполнил опережающее домашнее задание, вел текущие записи в рабочей тетради-дневнике исследования, пассивно задавал вопросы, но не участвовал в дискуссии, не предлагал решения к ситуационной задаче, но в групповой рефлексии обозначил опорные понятия по теме коррозия металла.
Оценка 3 балла ставится студенту, который не выполнил опережающее домашнее задание, но вел текущие записи в рабочей тетради-дневнике исследования, не предлагал решения к ситуационной задаче, но в групповой рефлексии обозначил опорные понятия по теме коррозия металла.
6. Выдача домашнего задания – подготовка докладов и электронных презентаций – 2 минуты:
Подготовить доклад объемом 3-5 страниц (форматом А4) и электронную презентацию (10-15 слайдов) на следующие темы:
Газовая коррозия
Атмосферная коррозия
Сплошная коррозия
Местная коррозия
Поверхностная коррозия
Язвенная коррозия
Методы борьбы с коррозией металлических материалов
Спасибо за активную работу! Можете быть свободны! До свидания!
ПРИЛОЖЕНИЯ
Приложение 1
БЛАНК ИНДИВИДУАЛЬНОЙ ГРАФИЧЕСКОЙ РЕФЛЕКСИИ
ФИО студента: __________________________________________
Приложение 2
БЛАНК ГРУППОВОЙ РЕФЛЕКСИИ:
ФИО студентов:____________________________________________________
Приложение 3
СИТУАЦИОННАЯ ЗАДАЧА

РЕШЕНИЕ:
Приложение 4

Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.