
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ «БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
БИРСКИЙ ФИЛИАЛ
ФАКУЛЬТЕТ БИОЛОГИИ И ХИМИИ
КАФЕДРА БИОЛОГИИ, ЭКОЛОГИИ И ХИМИИ
НАУЧНО-ИССЛЕДОВАТЕЛЬСКАЯ РАБОТА
ЛЫГИН СЕРГЕЙ АЛЕКСАНДРОВИЧ
НАУМОВА ДАРЬЯ СЕРГЕЕВНА
МОНИТОРИНГ ОРГАНИЧЕСКИХ СОСТАВЛЯЮЩИХ ВОДЫ
Р. БЕЛАЯ БЛАГОВЕЩЕНСКОГО РАЙОНА ТФК,
УКСУСНАЯ КИСЛОТА, НЕФТЕПРОДУКТЫ
БИРСК – 2018
Оглавление.
|
ВВЕДЕНИЕ |
3 |
|
ГЛАВА 1. ЛИТЕРТУРНЫЙ ОБЗОР |
5 |
|
1.1Вода и её свойства |
5 |
|
1.2 Основные источники загрязнения гидросферы |
8 |
|
1.3 Загрязняющие вещества |
10 |
|
Выводы по главе 1 |
16 |
|
ГЛАВА 2.ЭКСПЕРЕМЕНТАЛЬНАЯ ЧАСТЬ |
18 |
|
2.1 Характеристика водного объекта |
18 |
|
2.3 Отбор проб поверхностной воды |
22 |
|
2.4 Определение взвешенных веществ |
27 |
|
2.5 Определение ХПК |
29 |
|
2.6 Определение БПК |
31 |
|
2.7 Определение нефтепродуктов |
33 |
|
2.8 Определение уксусной кислоты методом капиллярного электрофореза |
34 |
|
2.9 Определение терефталевой кислоты ТФК |
37 |
|
Выводы по главе 2 |
38 |
|
ГЛАВА 3 РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ |
39 |
|
3.1 Результаты эксперимента |
39 |
|
3.2 Лекционное занятие по курсу современные методы химического анализа |
53 |
|
Выводы по главе 3 |
73 |
|
ЗАКЛЮЧЕНИЕ |
77 |
|
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ И ЛИТЕРАТУРЫ |
78 |
ВВЕДЕНИЕ
Большое значение в современном мире уделяется экологии. На смену позиции взять от природы все, пришло понимание необходимости сохранить ее для будущих поколений. В мегаполисах проблема загрязнения окружающей среды стоит наиболее остро. Воздух, вода, почва, загрязнены отходами и выбросами промышленных предприятий, выхлопными газами от транспорта, бытовым мусором.
Вода это уникальная стихия. Без воды не возможно существование жизни.
Вода играет огромную роль в биологических, и климатических процессах. Она является универсальным растворителем химических веществ, роль воды на планете обусловлена ее физическими свойствами.
Разработанность проблемы Проблема загрязнения воды реки Белой на территории Республики Башкортостан стоит особенно остро. Попадая в воду вредные вещества способны накапливаться и длительное время не изменять ее органолептические показатели. Например, при содержании нефтепродуктов в воде более чем 0,05мг/дм3 невозможно увидеть на поверхности нефтяные пленки или пятна, запах и цвет воды при этом тоже не изменятся.
Объектом исследования является вода реки Белая на территории Благовещенского района Республики Башкортостан.
Гипотеза исследования Общее загрязнение по ХПК зависит от содержания в воде органических загрязняющих веществ.
Предмет исследования органические загрязнители: Терефталевая кислота, уксусная кислота, нефтепродукты
Актуальность - изучить экологическое состояние реки Белой на территории Благовещенского района Республики Башкортостан.
Цель работы: - определить количественно суммарное загрязнение по ХПК, содержание нефтепродуктов и уксусной кислоты и ТФК в воде реки Белой в течении года.
Задача: - выявить зависимость общего загрязнения по химическому потреблению кислорода ХПК от содержания в воде терефталевой кислоты, нефтепродуктов и уксусной кислоты.
Методическая основа исследования. Эксперимент проводился на базе лаборатории Бирского филиала БашГУ. Были использованы фотометрический, флуориметрический, хроматографический методы анализа, а так же метод капиллярного электрофореза.
Теоретическая значимость исследования. Мониторинг воды р. Белая в течении года позволяет объективно оценить состояние исследуемого объекта. Установить основные источники негативного воздействия на объект окружающей среды.
Научная новизна исследования воды реки Белая на данном участке происходит впервые. Годовой мониторинг ранее не проводился.
Практическая значимость исследования состоит в получении объективных данных о содержании загрязняющих веществ в воде на участке реки Белой в Благовещенском районе.
Структура работы – научно-исследовательская работа состоит из введения, 3 основных глав, а также заключения и списка используемых источников и литературы, состоящей из 51наименования. Работа изложена на 82 страницах, включая 52 рисунка.
ГЛАВА 1. ЛИТЕРАТУРНЫЙ ОЗОР
1.1Вода и её свойства
Вода – одно из наиболее важных веществ на Земле, от которого зависит состояние растительного и животного мира. Это самая распространенная неорганическая составляющая живой материи. У человека вода составляет около 80% массы тела, у медуз ~ 98%, у грибов ~ 80%, а в растениях содержится до 95% воды. В семенах растений содержится около 10% воды, они представляют собой формы замедленной жизни. Такое же явление – ангидробиоз наблюдается у некоторых видов беспозвоночных (простейших), которые при неблагоприятных внешних условиях могут потерять большую часть воды из своих тканей и сохранить жизнеспособность [Артамонов, 2013].
Вода в природе находится в непрерывном круговороте – все время расходуется и возобновляется.
Вода играет существенную роль, как в биологических процессах, так и в климатических, являясь универсальным растворителем химических веществ. Значительная роль воды на планете обусловлена ее физическими и химическими свойствами. Данные свойства воды рассматриваются в курсе химии, поэтому рассмотрим только имеющие наиболее важное значение для природных явлений. Весовой состав чистой воды 88,8% кислорода и 11,2% водорода. Оба атома водорода смещены в одну сторону от атома кислорода, вследствие этого молекула воды характеризуется значительной полярностью. Все полярные молекулы способны к ассоциации. При нагревании воды степень ее ассоциации уменьшается. Если определить молекулярный вес по плотности пара, то мы получим величину равную 18, что указывает на полное отсутствие ассоциации [Вольф, 2012].
Теория ассоциации молекул воды объясняет причину одного из важнейших ее свойств – плотностную аномалию.
Плотность воды максимальна при 3,98°C и составляет 1,0 г/см3. Она уменьшается как при повышении, так и при понижении температуры. Эта аномалия обусловливает возможность жизни в водоемах, замерзающих в зимнее время. Так как лед легче воды - его плотность ниже, он располагается на поверхности и защищает лежащие ниже слои воды от промерзания. При дальнейшем понижении температуры увеличивается толщина слоя льда, но температура воды подо льдом остается на уровне ~4°C, что позволяет водным организмам сохранять жизнь. Плотностная аномалия воды сыграла важную роль в формировании окружающего нас мира [Masakazu Matsumoto, 2009].
Вследствие плотностной аномалии воды в глубоких водоемах наблюдается температурная слоистость. Зимой поверхностные слои имеют температуру, близкую к нулю, а нижние слои около +40С – это явление называют обратной температурной слоистостью.
В начале весны прогревающаяся до +40С вода верхних слоев опускается вниз и наслаивается на глубинную воду с той же температурой, в результате частичной циркуляции происходит выравнивание температур воды – весенняя гомотермия.
Летом по мере дальнейшего прогрева воды устанавливается прямая температурная слоистость, то есть температура воды непрерывно повышается от дна к поверхности.
Осенью охлаждающие слои воды опускаются на дно, тем самым вытесняя на поверхность более теплую воду, происходит циркуляция воды, в результате чего устанавливается осенняя гомотермия.
В процессе таких вертикальных перемещений слоев воды происходит перенос растворенного кислорода в направлении от поверхности ко дну водоема, а в обратном направлении продуктов распада донных отложений, содержащих биогенные элементы и углекислый газ.
За счет вертикального перемещения слоев воды – вертикальной стратификации создаются условия развития в водоемах растительной и животной жизни [Березина, 2014].
Вода обладает большой теплоемкостью 4,18 Дж/г*К (теплоемкость воздуха 1,009 Дж/г*К). В природных условиях вода медленно остывает и медленно нагревается, являясь регулятором температуры на Земле.
Огромную роль в формировании климата на Земле играет криосфера – то есть вода, которая находится в твёрдом состоянии в ледниках, в виде снега и в вечной мерзлоте [Конкина, 2012].
Масару Эмото, изучая воду в твердом состоянии в виде кристаллов, в своих трудах пишет: изучение кристаллов льда — многообещающее научное направление. Со временем мы сможем распознавать элементы кристаллов, которые сигнализируют о надвигающихся стихийных бедствиях. Медицинские перспективы изучения воды также многообразны. Возможно, скоро мы научимся существенно улучшать свое психологическое и физическое состояние, не прибегая к помощи врачей. Если мы осознаем, насколько важна вода, лично для нас и для всей планеты, то только силой мысли и слова мы сможем улучшить экологию Земли и собственное самочувствие. Мы можем окутать планету любовью и признательностью, не выходя из дома, благодаря удивительной энергии воды [Эмото, 2016].
Переходы воды из одних частей гидросферы в другие составляют сложный круговорот воды на Земле.
Дождевые и талые снеговые воды являются основным питанием рек и озер.
Вдали от промышленных предприятий солевой состав атмосферных осадков определяется природными условиями.
С дождевыми водами в водоем поступают органические и минеральные вещества, а так же частички пыли и сажи, содержащиеся в воздухе загрязненном выбросами промышленных предприятий [Назаренко, 2007].
Расход воды в реках подвержен сезонным изменениям, которые определяются физико-географическими факторами и деятельностью человека. Таким образом, еще одним этапом формирования химического состава природных вод является взаимодействие осадков с почвенным покровом.
Значительную роль в формирование состава природных вод играет деятельность человека. Сточные воды населенных пунктов и промышленных предприятий вносят различные загрязнения в водоемы, тем самым влияя, на его химический состав [Возня, 2015].
Загрязнение – это привнесение в среду или возникновение в ней новых не характерных для нее биологических, химических или физических факторов, приводящих к негативным воздействиям на окружающую среду или на человека [Водный кодекс, 2016].
1.2 Основные источники загрязнения гидросферы
Загрязнение вод проявляется в изменении физических и органолептических свойств, увеличении содержания сульфатов, хлоридов, нитратов, токсичных тяжелых металлов, сокращении растворенного в воде кислорода, появлении радиоактивных элементов, болезнетворных бактерий и других загрязнителей. Подсчитано, что ежегодно в мире сбрасывается более 420 км3сточных вод. Основными источниками загрязнения гидросферы являются: промышленные сточные воды, хозяйственно-бытовые сточные воды, дренажные воды с орошаемых земель, сельскохозяйственные поля и крупные животноводческие комплексы, водный транспорт. Все загрязнители сточных вод подразделяются на три группы:
1. биологические загрязнители: микроорганизмы – вирусы, бактерии; растения – водоросли; дрожжи, плесневые грибки;
2. химические загрязнители: наиболее распространенными загрязнителями являются нефть и нефтепродукты, СПАВ, пестициды, тяжелые металлы, диоксины, фенолы, аммонийный и нитритный азот;
3. физические загрязнители: радиоактивные элементы, взвешенные твердые частицы, шлам, песок, ил, тепло [Комментарий к Водному кодексу]. Загрязняющее воду вещество – это вещество вызывающее нарушение норм качества воды.
Химические вещества, загрязняющие воду: фенолы, пестициды, различные соли, кислоты, щелочи, а так же ртуть, мышьяк, кадмий, свинец и некоторые нетоксичные загрязнители.
Эвтрофикация – процесс поступления в воду большого количества биогенных элементов, содержащих азот и фосфор в виде удобрений, различных моющих веществ, отходов животноводства и т.д. [Алимов, 2011]. В России превышают предельно допустимые концентрации (ПДК) многие водные объекты. Осаждающиеся на дно водоемов загрязнители сорбируются, окисляются или восстанавливаются и выпадают в осадок. Полное самоочищение, как правило, не происходит [СанПиН 2.1.5.980-001].
Появлении в воде патогенных бактерий, вирусов, простейших, грибов и т.д. указывает на бактериальное загрязнение водоема.
Очень опасно содержание в воде радиоактивных веществ даже в малых концентрациях. Радиоактивные элементы попадают в поверхностные водоемы при сбрасывании и захоронении в них радиоактивных отходов и т.д.
Миграция химических элементов позволяет говорить о возможности попадания их в подземные воды, а также в результате их выпадения с осадками на поверхность и последующего просачивания вглубь земли.
Значительное ухудшение органолептических показателей связано с попаданием в воду различных загрязнителей в виде: шлама, песка, ила, которые получили название как механические загрязнители.
Тепловое загрязнение связано с повышением температуры природных вод в результате их смешивания с технологическими водами. Температура сточных вод ТЭС, АЭС выше температуры окружающих водоемов на 10ºC. При повышении температуры происходит изменение газового и химического состава в водах, что ведет к размножению анаэробных бактерий, выделению ядовитых газов – Н2S, СН4. Происходит цветение воды, ускоренное развитие микрофлоры и микрофауны [Федеральный закон №7-ФЗ].
Эвтрофикация – явление, связанное с поступлением в водоемы большого количества биогенных элементов соединений азота и фосфора в виде удобрений, моющих веществ, отходов животноводства [Алимов, 2011].
1.3 Загрязняющие вещества
Для эффективного снижения нагрузки от загрязнений поверхностных водоемов важно не только определить источники загрязнений, но и идентифицировать сами загрязняющие вещества. В данной работе мы рассмотрим суммарное загрязнение органическими веществами воды реки Белой в Благовещенском районе Республики Башкортостан, а так же выделим как загрязняющие вещества уксусную кислоту и нефтепродукты.
Основным показателем общего загрязнения является ХПК – химическое потребление кислорода. В природной воде присутствуют органические вещества, в родниковых и талых водах их концентрации могут быть очень малы. Естественными источниками органических веществ являются останки организмов растительного и животного происхождения. Техногенными источниками органических веществ являются промышленные предприятия и их сбросы в виде нефтепродуктов, лигнинов, белковых соединений. В качестве источников органических загрязнений могут выступать сельскохозяйственные и фекальные стоки [Никаноров, 2011].
ХПК – это количественный показатель, он является наиболее информативным. Это прежде всего общепринятый, и достаточно быстро определяемый показатель для характеристики общего загрязнения природных и сточных вод органическими соединениями. Величина ХПК или бихроматной окисляемости поверхностных вод зависит от общей биологической продуктивности водного объекта, содержания в нем органических веществ естественного происхождения и степени его загрязнения. Для различных водоемов она может быть от сотых долей до десятков миллиграммов в кубическом дециметре. Различают ХПК фильтрованных проб, свидетельствующее о содержании растворенных органических веществ и нефильтрованных проб, указывающих на общее содержание органических веществ.
Величина ХПК подвержена довольно значительным и закономерным сезонным колебаниям. Она определяется, с одной стороны, гидрологическим режимом и зависящим от него поступлением органических веществ аллохтонного происхождения с поверхности водосбора, с другой стороны - гидробиологической активностью, обусловливающей процессы продуцирования, трансформации и минерализации органических веществ в водном объекте. В водных объектах, подверженных сильному антропогенному воздействию, на изменения величины ХПК значительное влияние оказывает объем и режим поступления загрязнений со сточными водами [Иванов, 2013].
Биохимическое потребление кислорода (БПК) - это количество кислорода которое требуется для окисления органических веществ, находящихся в 1 дм3 воды в аэробных условиях при 200С, без доступа света, за определённый период в результате протекающих в воде биохимических процессов. В естественных условиях органические вещества, которые попадают в воду, разрушаются различными видами бактерий, с помощью которых происходит процесс аэробного биохимического окисления с образованием двуокиси углерода. При этом потребляется растворенный в воде кислород. В водоемы, в которые попадает большое количество органических веществ, большая часть кислорода содержащегося в воде потребляется на биохимическое окисление, лишая тем самым кислорода другие организмы. При этом увеличивается количество организмов, устойчивых к низкому содержанию растворенного кислорода. То есть в процессе биохимического окисления органических веществ в воде уменьшается содержание растворенного кислорода, и таким образом можно судить о содержании вводе органических веществ [Готовцев 2013].
Взвешенные вещества - это вещества, которые находятся в воде в твёрдом состоянии, и имеют естественную природу. Они могут включать в себя следующие компоненты: песок, ил, глиняные частички, суспендированные частицы, имеющие органическое и неорганическое происхождение, планктон и прочие микроорганизмы.
На количество взвешенных веществ, влияют факторы смены сезонов и режим поступления сточных вод с поверхности, процесс таяния снега и факторы, имеющих антропогенное происхождение – проведение сельскохозяйственных работ, горнодобывающие работы, сточные воды различного происхождения. Они влияют на прозрачность воды, её светопроницаемость, и на температурный режим. Нерастворимые в воде частицы делятся на взвеси и коллоиды.
Взвеси – это вещества или частицы, размер и масса, которых позволяет им оседать в результате воздействия силы тяжести. Размер коллоидов находится в коридоре от нанометров до долей микрометров. Такие взвешенных веществ невозможно удалить с помощью механической очистки. Крайне важно производить контроль уровня скопления взвешенных частиц во время проверки биологической и физико-химической обработки сточных вод и в процессе оценке качества природной воды [Технологический регламент, 2012].
Терефталевая (1,4 – бензолдикарбоновая) кислота, представляет собой белое кристаллическое вещество, не имеющее запаха. ТФК – не растворима, в воде, растворяется в щелочах и пиридине [Зефиров, 2004].
Процесс получения ТФК основан на реакции жидкофазного окисления параксилола (ПК) кислородом воздуха в среде растворителя уксусной кислоты (УК). В качестве катализатора используются соли Co и Mn с добавкой тетрабромэтана, который является инициатором процесса (промотором) [Никитина, 2016]. Брутто-реакция образования ТФК описывается схемой (1):
|
|
(1)
|
Тепловой эффект реакции Qp = (-∆Hр) = 326 ккал/г-моль.
Процесс проводят при температуре 180¸200°С под давлением 8¸14 атм. Теплосъем – за счет испарения растворителя (уксусной кислоты) и реакционной воды, то есть процесс осуществляется «на кипу» при температуре, определяемой давлением.
Механизм реакции – радикально–цепной с короткой цепью. Упрощенно реакцию можно рассматривать как последовательно–параллельную (2):
|
|
(2)
|
Из данной схемы видно, что из ПК – это параксилола, С6Н4 (СН3)2, с преобразованием в п-ТА – пара-толуиловый альдегид п-С6Н4(CH3)СНО, затем в п-ТК – пара-толуиловую кислоту, п-С6Н4(CH3)СООН и п-КБА – пара-карбоксибензальдегид, п-С6Н4(СНО)СООН получается ТФК – терефталевая кислота п-С6Н4(СООН)2, с побочным продуктом БК – бензойная кислота, С6Н5СООН;
Кроме образования бензойной кислоты и продуктов конденсации, основной побочной реакцией является деструктивное окисление уксусной кислоты и образование метилацетата (МА):
|
СН3СООН + 2О2 |
® |
2СО2 + 2Н2O |
(3) |
|
2СН3СООН+ 3О2 |
® |
2СО2 + 2СО + 4Н2O |
(4) |
|
2СН3СООН+ 1/2О2 |
® |
СН3СООСН3 + Н2O +СО2 |
(5) |
|
2Со(СН3СОО)3 |
® |
2Со(СН3СОО)2+ СН3СООСН3 + СО2 |
(6) |
Значение констант скоростей последовательных реакций по реакции (2), при равных значениях концентраций реагирующих компонентов, располагаются в следующей последовательности:
К2>К4>>K1>>К3 , (7)
Как видно из зависимости (7), лимитирующей стадией реакции является окисление п-ТК в п-КБА, поэтому процедура оптимизации процесса окисления, в конечном итоге, должна быть направлена на обеспечение благоприятных условий для увеличения скорости реакции [Технологический регламент, 2005].
Нефтепродукты – это продукты добычи, транспортировки и переработки нефти, являются типичными загрязнителями окружающей среды. В системах контроля качества природных вод, почв, воздуха их относят к обязательно нормируемым компонентам. Это вещества, имеющие 3 класс опасности [Приказ Росрыболовства №20, 2010]. Для различных категорий водных объектов установлены различные нормативы ПДК. Для объектов питьевого водоснабжения ПДК составляет 0,1мг/дм3 [СанПиН 2.1.4.1074-01], Для водоемов рыбохозяйственного значения ПДК, установлено на уровне 0,05 мг/дм3 [Приказ Росрыболовства №20, 2010]. Для водных объектов хозяйственно-бытового назначения ПДК установлено - 0,3мг/дм3 [ГН 2.1.5.1315-03].
Источники поступления нефтепродуктов в окружающую среду разнообразны: аварийные разливы нефти при нефтедобыче, хранение и транспортировка топлива, прорывы нефтепроводов и нефтехранилищ; нарушения технологических процессов и процессов очистки сточных вод нефтеперерабатывающих предприятий, автомобильный транспорт, в том числе и при выбросе в воздух несгоревших компонентов топлива от двигателей внутреннего сгорания, водный транспорт.
Нефтепродукты способны накапливаться в воде и донных отложениях, что может оказаться губительным для водоемов с низким водообменом. Крупные реки от накапливания нефтепродуктов спасает текучесть, а так же саморазбавление и способность к самоочищению.
Примером масштабного загрязнения нефтепродуктами может служить катастрофа на озере Ачикуль в Благовещенском районе в апреле 2011 года. Розлив нефтепродуктов привел к массовой гибели рыбы. Концентрация растворенных в воде нефтепродуктов достигала 10мг/дм3. Ущерб, составил около 4 миллионов рублей (рис.1.1) [Причина массовой гибели карася в озере Ачикуль].

Рисунок 1.1 Озеро Ачикуль. Гибель рыбы
Уксусная кислота – слабая, предельная одноосновная карбоновая кислота с характерным резким запахом и кислым вкусом. Применяется в пищевой промышленности как пищевая добавка, в бытовой кулинарии, а также в консервировании. В качестве растворителя для получения лекарственных и душистых веществ, в книгопечатании и крашении; в медицине.
Уксусная кислота используется как реакционная среда для проведения окисления различных органических веществ. В лабораторных условиях это, например, окисление органических сульфидов пероксидом водорода, в промышленности – окисление пара-ксилола кислородом воздуха в терефталевую кислоту [Лазарева, 2016].
В природе уксусная кислота распространена в свободном виде, а так же виде солей и эфиров в зеленых листьях растениях, в выделениях животных в моче и желчи, образуется при гниении и процессе брожения в кислом молоке, сыре, вине. Процесс брожения происходит под влиянием специфических бактерий "уксусного грибка".
Источниками поступления уксусной кислоты в реку являются предприятия органического синтеза, производящие уксусную кислоту, а так же использующие ее в качестве сырья.
Уксусная кислота это вещество, которое трудно окисляется растворенным в воде кислородом. В отличии от нефтепродуктов она хорошо растворима в воде, что позволяет обнаруживать ее в течении длительного времени по всему объему водотока. Однако она менее токсична для микроорганизмов водоема, так как для простейших микроорганизмов и бактерий она является питательным веществом.
Выводы по главе 1
1. Вода обладает уникальными свойствами. Без воды не возможно существование жизни на земле.
2. В воду попадают различные виды загрязнений: химические, физические, биологические.
3. Загрязняющие вещества несут опасность для водоема и могут оказаться губительными для экосистемы водоема в целом.
4. Загрязняющие органические вещества трудно окисляются и способны накапливаться в воде водоема.
5. Антропогенное воздействие на водоемы это наиболее острая проблема мирового масштаба.
ГЛАВА 2.ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1 Характеристика водного объекта
Республика Башкортостан - это, прежде всего промышленный регион. Здесь сосредоточены предприятия нефтеперерабатывающей, химической и горно-обогатительной отросли. Работа всех этих предприятий так или иначе связана с образованием выбросов, сбросов и отходов оказывающих влияние на окружающую среду [Отчет о темпах развития промышленности].
Река Белая самая крупная водная артерия Башкортостана, поэтому сохранить ее экологическое состояние является важной задачей Республики.
Река Бе́лая — река Южного Урала и Предуралья; левый и самый крупный приток реки Кама. Протекает по территории Башкортостана, являясь самой длинной рекой Башкортостана (рис.2.1).
![]()
![]()
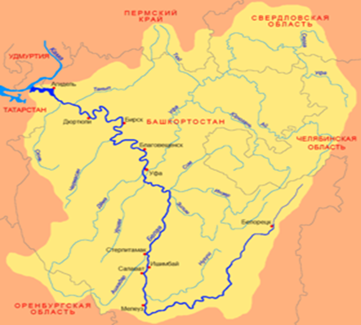
Рисунок 2.1Акватория реки Белая республики Башкортостан
Длина реки (Т1 ÷ Т2): 1430км, площадь бассейна: 142 тыс. км².
Исток (Т1 рис.2.2), в болотах недалеко от горы Иремель, на высоте 744 метров, близ деревни Новохусаиново Учалинского района.
Верховья р. Белая заболочены. Ниже Тирлянский долина сужается, на образуя крутые, обрывистые, покрытые лесом склоны. Ниже впадения притока р. Нугуш, по выходу на равнину, долина расширяется и после впадения р. Уфа Белая становится типично равнинной рекой.
Река подпитывается в основном талыми снеговыми водами. В среднем годовой расход воды у г. Бирск 858 м³/с. Река находится под ледовым покрытием со второй половины ноября до середины апреля. Примерно 60 % годового стока проходит на время весеннего таяния снега и грунтовых вод (в среднем 75 дней). Вскрывается река примерно: 10 апреля и встает в берега в конце июня: (после 20 числа). Во время половодья мутность достигает 900 мг/л (в остальное время около 50 мг/л).
![]()
![]()
![]()
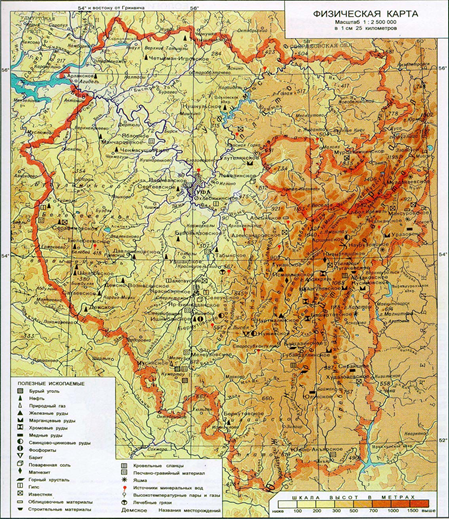
Рисунок 2.2 Географическое расположение р. Белая Республики
Башкортостан
Являясь важной водной магистралью Республики Башкортостан, река доступна для судоходства от Табынского (656 км) (Т3 рис.2.2).
Протекая по обширной пойме, изобилующей старицами, река образует много излучин и разбивается на рукава. Правый берег обычно более возвышен, чем левый.
Важная водная магистраль Республики Башкортостан. Река доступна для судоходства от Табынского (656 км) (Т3 рис.2.2).
Регулярное сообщение осуществляется от Уфы. Белая является составной частью водного пути Москва - Уфа, по которому организованы туристические рейсы [Все реки России. Река Белая].
По берегу реки Белой находится множество населенных пунктов, в том числе города, являющиеся промышленными центрами, расположенными в: Белорецке, Мелеузе, Салавате, Ишимбае, Стерлитамаке, Уфе, Благовещенске (Башкортостан), Бирске, Дюртюлях, Агидели.
Река имеет множество притоков. В Благовещенском районе в нее впадает 2 притока: в 408 километрах от устья впадает ручей Семёновка (правый приток), а в 416 километрах река Потеха (правый приток).
Через реку перекинуты многочисленные мосты, крупнейшими из которых являются автомобильные и железнодорожные мосты в Уфе.
Водоем имеет рыбохозяйственное назначение, что подразумевает соответствующие нормативы качества воды [Река Белая (Агидель)].
Муниципальный район Благовещенский Республики Башкортостан образован 20 августа 1930 года. Административным центром является город Благовещенск (рис.2.3).
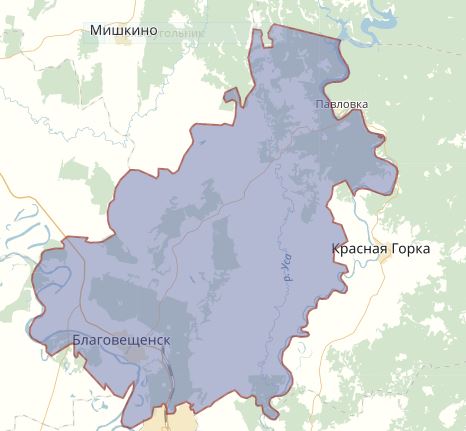
Рисунок 2.3 Карта Благовещенского района Республики Башкортостан
Территория района составляет 2324 кв.км, в том числе г.Благовещенск занимает территорию 65 кв.км. Муниципальный район Благовещенский район расположен в центральной части Республики Башкортостан на берегу реки Белой в 42 км к северу от г. Уфы и 14 км к северо-западу от железнодорожной станции Загородная.
Район имеет компактную конфигурацию. Максимальная протяженность с запада на восток 55 км., с севера на юг 73 км.
На юге он граничит с Уфимским и Иглинским районами, на западе – Кушнаренковским и Бирским, на севере – Мишкинским и Караидельским и на востоке Нуримановским районами. По территории проходят автомобильные трассы Уфа-Бирск-Янаул, Благовещенск-Павловка-Красная Горка, Авдон-Подымалово-Николаевка. Судоходные участки на р. Белая, р. Уфа определяются частью территории, лежащей в пределах Прибельской увалисто-холмистой равнины, где некоторая часть относится к Уфимскому плато. Юго-западную часть района огибает р. Белая, восточную – р. Уфа с притоками Уса и Изяк. Леса занимают 21,2% территории района, остальное пойменные луга, озера. Распространены светло-серые лесные почвы, по долинам Белой и Уфы — почвы речных пойм. Выявлены месторождения нефти, песчано-гравийной смеси, щебня, известняка, керамзитовой глины. Город Благовещенск расположен на территории Прибельской равнины на правом берегу р. Белая в 42 км к северу от г. Уфа и 27 км к северо-западу от ж/д станции «Загородная» [Администрация муниципального района Благовещенский район].
В районе города Благовещенск вода в реке Белой характеризуется, как очень загрязненная и относится к водоемам 3 класса.
2.2 Отбор проб поверхностной воды
Отбор проб воды в реке осуществляется по ГОСТ 31861-2012 Вода. Общие требования к отбору проб [ГОСТ 31861-2012]. Глубина отбора проб воды составляет 0,5 метра с середины водотока (рис. 2.4).

Рисунок 2.4 Отбор проб воды реки Белой
На общие химические анализы пробы воды отбирают пробоотборником типа ПЭ – 1650 – батометром (рис. 2.5).

Рисунок 2.5 Пробоотборник для отбора проб воды типа ПЭ 1650
Воду для анализа нефтепродуктов растворенных в воде отбирают пробоотборником ПЭ-2 (рис. 2.6).
Непосредственно после отбора проб измеряется рН и температура воды, оцениваются органолептические показатели: цвет и прозрачность воды, наличие мути или взвеси, запах воды.

Рисунок 2.6 Пробоотборник типа ПЭ – 2 для отбора проб воды для анализа нефтепродуктов
Пробы на тяжелые металлы и сульфид-ион фильтруются и консервируются на месте обора.
Для исследований по определению загрязнения р. Белая на территории Благовещенского района были выбраны две точки для отбора проб воды в районе Большого Благовещенского острова и на трассе Авдон-Подымалово-Николаевка. На данных участках водоем представляет собой типичную равнинную реку, судоходную на всем протяжении. В период навигации по реке двигаются маломерные, туристические суда, а так же нефтеналивные танкеры и баржи.
Т2 Т1
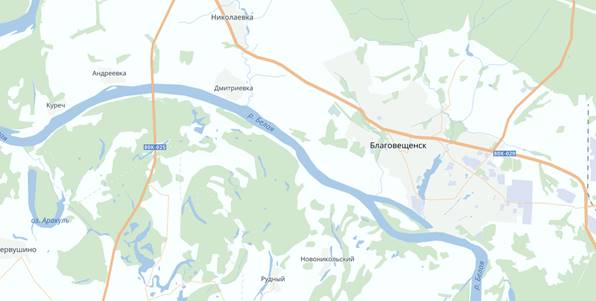
Рисунок 2.7 Пробоотборные точки на участке карты Благовещенского района
Т1 (рис.2.7) в районе Большого Благовещенского острова. Данный участок реки является местом отдыха жителей города. В период с мая по сентябрь к кромке воды подъезжают автомобили. Почва в прибрежной зоне песчаная. Растительность в основном представлена редким ивовым кустарником и незначительным количеством трав. Дно реки песчаное, твердое. Берег низкий, отлогий. С берега в реку попадают ливневые и талые воды с ближайших городских улиц (рис.2.8).
Т2 (рис.1.8) был выбран участок в районе моста через р. Белая на автодороге Авдон-Подымалово-Николаевка (рис.2.9).

Рисунок 2.8 Участок реки в районе Большого Благовещенского острова
Данный участок автодороги имеет постоянный автомобильный поток, состоящий в основном из грузового автотранспорта. Почва в районе берега имеет легкую суглинистую структуру. Дно илистое мягкое с чередованием крупных камней известковой породы. Растительность представлена так же ивовым кустарником, шиповником, разнотравьем, выше хвойными и смешенными лесами. Берег высокий под мостом укреплен бетонными плитами. Вдоль автомобильной дороги сооружены бетонные водоотводы (1 рис.1.10), по которым ливневые и талые воды с автодороги попадают непосредственно в реку [Лыгин С.А., Наумова Д.С., 2018].
![]()
![]()

Рисунок 2.9 Мост через реку Белая на трассе Авдон-Подымалово-Николаевка
2.3 Определение взвешенных веществ
Анализ содержания взвешенных веществ, в воде реки Белая мы проводили фотометрическим методом по ФР.1.31.2004.00976, прямым измерением на оптическом анализаторе взвешенных веществ ДИВ, предназначенном для определения массовой концентрации взвешенных веществ различного дисперсного состава в пробах поверхностных природных и сточных вод (рис.2.10).

Рисунок 2.10 Оптический анализатор взвешенных веществ ДИВ
Принцип действия анализаторов основан на измерении ослабления светового потока анализируемой средой с помощью фотоэлектрического преобразователя. В анализаторе однозначно обеспечивается обратная логарифмическая зависимость между коэффициентом светопропускания и массовой концентрацией взвешенных веществ [Описание типа средства измерений, 2015].
Непосредственно перед анализом проводят контроль стабильности показаний прибора по градуировочным растворам. Растворы с концентрацией 10мг/дм3 и 400мг/дм3 готовят из государственного стандартного образца нерастворимых частиц каолина, согласно инструкции по применению.
Анализ проводят в день отбора пробы.
Прибор устанавливают на ноль по дистиллированной воде, для этого в стеклянный химический стакан наливают дистиллированную воду и помещают в нее датчик прибора, включают прибор в сеть и оставляют на 30 минут. По истечении времени при помощи регулятора устанавливают стрелку на ноль.
Пробу воды хорошо перемешивают в течении 10 минут, помещают в стеклянный химический стакан объемом не менее 400см3, заполняя стакан не более чем на 2/3 объема. Опускают в него датчик прибора и фиксируют показания при постоянном перемешивании пробы стеклянной палочкой. Процедуру повторяют два раза, за результат принимают среднее значение двух параллельных определений [ФР.1.31.2004.00976].
2.4 Определение ХПК
Анализ ХПК это наиболее информативный и экспрессивный метод показывающий объем кислорода необходимый для окисления всех органических веществ находящихся в воде. Таким образом, ХПК характеризует суммарное загрязнение водоема органическими веществами.
Метод определения ХПК основан на окислении органических веществ бихромат-ионом в кислой среде при нагревании в присутствии сернокислого серебра с последующим фотометрическим определением.
Определение проводят по следующей схеме: в виалу вносят приблизительно 0,3г сухого порошка сернокислой ртути, для устранения влияния хлорид-ионов находящихся в пробе, затем добавляют 0,5 см3 0,1Н раствора бихромата калия и 3см3 раствора сульфата серебра в серной кислоте. Пробу воды тщательно перемешивают, отбирают 2 см3 и вносят в подготовленную виалу, закрывают крышкой и ставят в предварительно нагретый до 1400С термореактор на 2 часа (рис.2.11) [ПНД Ф 14.1:2:4.210-05].

Рисунок 2.11. Термореактор
Виалы охлаждают в термореакторе в течении 20 минут, аккуратно вынимают и оставляют при комнатной температуре еще на 1 час (рис.2.12).

Рисунок 2.12 Виалы перед фотометрированием
Затем проводят фотометрирование при длине волны 450нм по градуировочному графику, заложенному в памяти спектрофотометра (рис.2.13). Параллельно проводят холостое определение – анализ дистиллированной воды.

Рисунок 2.13 Спектрофотометр
2.5 Определение БПК
Определение БПК основано на измерении концентрации растворенного кислорода в воде непосредственно после отбора, и после инкубации пробы. Инкубацию пробы проводят без доступа воздуха в кислородной склянке (рис.2.14) в течение времени 5 суток (для анализа БПК5) или 25 суток (БПКполное). Инкубацию проводят в режиме постоянной температуры (20±1)0С, без доступа света [ПНД Ф 14.1:2:3:4.123-97]. При необходимости пробу разбавляют специально подготовленной дистиллированной водой. Процессу мешает нитрит-ион поэтому при содержании в исходной воде нитритов более 0,1 их нейтрализуют согласно методике. Определяют БПК после 2,5,7,10,15,20 дней инкубации. О процессе судят по изменению концентрации нитрит-иона в пробе. Для этого после определения содержания кислорода из склянки проводят анализ нитрит-ионов. При содержании нитритов более 0,2мг/дм3 процесс инкубации считается завершенным.

Рисунок 2.14 Кислородная склянка
Мы определяли БПК амперометрическим методом с использованием анализатора «АНИОН 4100» (рис.2.15), и получили следующие результаты:

Рисунок 2.15 Анализатор «АНИОН 4100»
2.6 Определение нефтепродуктов
Анализ нефтепродуктов проводился флуориметрическим методом согласно ПНД Ф 14.1:2:4.128-98 с применением анализатора жидкости «Флюорат-02».
Флуориметрический метод измерений массовой концентрации нефтепродуктов основан на их экстракции из пробы гексаном и измерении интенсивности флуоресценции полученного экстракта на анализаторе жидкости «ФЛЮОРАТ - 02» с последующим автоматическим вычислением концентрации нефтепродуктов при помощи градуировочной зависимости, заложенной в память анализатора (рис.2.16) [ПНДФ 14.1:2:4.128-98].

Рисунок 2.16 Анализатор жидкости «Флюорат-02»
В делительную воронку помещают весь объем, приблизительно 150 см3 пробы. Пипеткой отмеряют 5-10см3 гексана, ополаскивают им склянку после пробы и переносят в ту же воронку. Проводят экстракцию в течении 1 мин. Отстаивают пробу до прозрачности верхнего слоя, а затем нижний слой сливают в мерный цилиндр и точно фиксируют объем. Верхний слой через горловину сливают в кювету, проводят флоуресценцию и фиксируют результат.
Для расчета концентрации показания прибора умножают на объем гексана и делят на объем пробы.
2.7 Определение уксусной кислоты методом капиллярного
электрофореза
Движение заряженных коллоидных частиц под действием электрического поля называется электрофорез. Электрофорез как метод был обнаружен, в XX веке Тизелиусом. Он поместил смесь белков сыворотки крови в буферный раствор и наложил электрическое поле. Наблюдая явление их движения со скоростью, определяемой их размером, формой и электрическим зарядом он открыл явление электрофореза. За это в 1948 г. его работа была удостоена Нобелевской премии по химии [Л.А. Карцова, 2016].
Общее устройство систем КЭ
На (рис.2.17) представленна принципиальная схема каппилярного электрофореза.
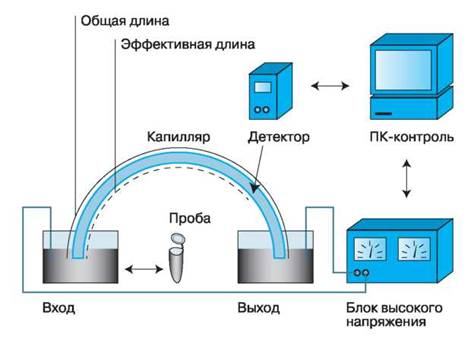
Рисунок 2.17 Принципиальная схема капиллярного электрофореза
Самым простой вариант капиллярного электрофореза является капиллярный зонный электрофорез. Компоненты сложной смеси движутся в среде электролита с разными скоростями, детектируются и выводятся на контроллер.
Для определения уксусной кислоты мы использовали систему капиллярного электрофореза «КАПЕЛЬ 105М» (рис.2.18)

Рисунок 2.18 Система капиллярного электрофореза «КАПЕЛЬ 105М»
Установка «КАПЕЛЬ 105М» готовится к работе согласно штатного расписания и инструкции подготовки к работе. Все соответствующие действия и манипуляции проводятся с соблюдением ПТБ и всех надлежащих требований, указанных в нормативных документах. Рабочие растворы готовятся согласно методики указанной в ПНД Ф с применением и соблюдением всех требований. [ПНД Ф 14.1:2.226-2006]. Приготовление раствора соляной кислоты 0,5 моль/дм3. В мерную колбу вместимостью 100 см3, заполненную дистиллированной водой на 1/2, приливают 4 см3 соляной кислоты, охлаждают и доводят раствор до метки дистиллированной водой. Срок хранения раствора 1 год. Раствор диэтаноламина 0,05 моль/дм3.
Навеску 0,525 г диэтаноламина, помещают в мерную колбу вместимостью 100 см3, в дистиллированной воде и доводят объем раствора до метки дистиллированной водой. Хранят в полимерной посуде в холодильнике не более 1 месяца.
Раствор цетилтриметиламмония бромида (ЦТАБ), массовая концентрация 3 мг/см3. В мерную колбу вместимостью 100см3 помещают навеску 0,300 г ЦТАБ и 20см3 дистиллированной воды, выдерживают на водяной бане при температуре 40°С до полного растворения, и добавляют 50 см3 дистиллированной воды, перемешивают и доводят объем раствора до метки дистиллированной водой. Срок хранения раствора 3 месяца.
Рабочий буферный раствор в сухой стакан вместимостью 50 см3 помещают 1 см3, добавляют 4 см3 раствора диэтаноламина и 3 см3 дистиллированной воды, тщательно перемешивают, затем добавляют 2 см3 раствора ЦТАБ. Общий объем рабочего буферного раствора 10 см3. Раствор используют в течение 1 недели. Перед анализом буферный раствор фильтрую через фильтр с диаметром пор 0,45нм и дегазируют центрифугированием.
Приготовление градуировочных растворов уксусной кислоты. Градуировочный раствор готовят из государственного стандартного образца (ГСО) согласно инструкции по применению. Шкалу рабочих градуировочных растворов с концентрацией уксусной кислоты 5, 10, 25 и 50 мг/дм3 готовят последовательным разбавлением основного градуировочного раствора дистиллированной водой в соответствии с табл.1. Растворы готовят непосредственно перед установлением градуировочной характеристики. Отобранную пробу анализируют в течение суток. Если такой возможности нет, то пробу фильтруют через мембранный фильтр с диаметром пор 0,45 мкм. Пробу можно хранить после фильтрования не более 7 суток при температуре (2 - 10)°С.
Если анализ проводят в день отбора, то предварительно хорошо перемешенную пробу, доведённую до комнатной температуры, фильтруют через мембранный фильтр с диаметром пор 0,45 мкм. Дозатором отбирают 250мкл пробы, помещают ее в пробирку типа эппендорф, и проводят дегазацию пробы методом центрифугирования. Дегазированные пробы помещают во входную карусель прибора и проводят анализ в автоматическом режиме. Расчет концентрации уксусной кислоты проводят на электрофореграмме (рис.2.19) по градуировочному графику в памяти прибора. Результат выдают с учетом разбавления [ПНД Ф 14.1:2.226-2006]. Приготовление градуировочных растворов уксусной кислоты.
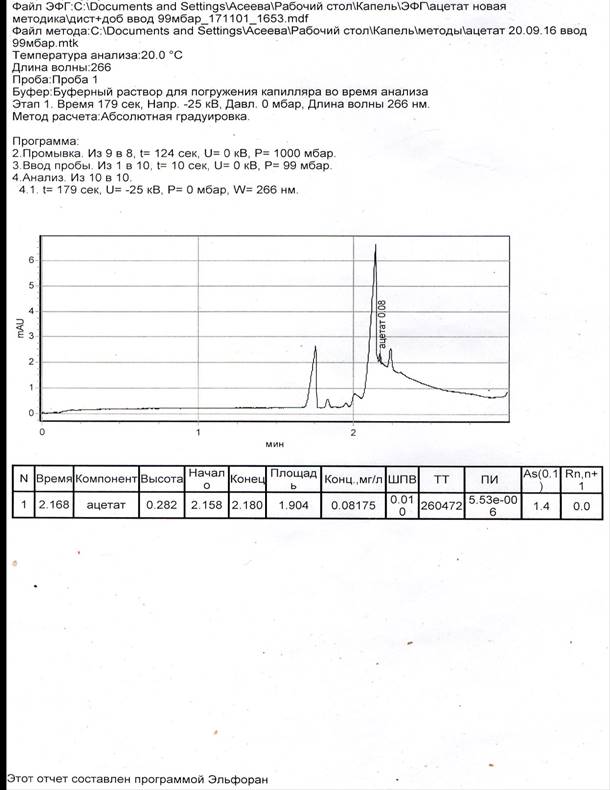
Рисунок 2.19. Электрофореграмма
2.8 Определение терефталевой кислоты ТФК
Анализ терефталевой кислоты проводили хроматографическим методом с использованием жидкостного хроматографа (рис.2.20).
Рисунок 2.20 Жидкостной хроматограф
Отобранную пробу предварительно отфильтровывают через мембранный фильтр с диаметром пор 0,45нм. Микрошприцем вводят 1мкл пробы. Анализ рассчитывают согласно [МВИ-КЛЭК-1-2008]. Подвижной фазой в данном анализе является раствор ацетонитрила с фосфорной кислотой (1:5).
Выводы по главе 2
1. Отбор проб проводился в соответствии с ГОСТ 31861-2012.
2. Методы физико-химического анализа наиболее эффективны для определения загрязняющих веществ в воде водоема.
3. Данные методы обладают большой экспрессивностью, наглядностью.
4. Точность анализа определяется в соответствии с методикой измерений.
ГЛАВА 3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
3.1 Результаты эксперимента
Результаты определения взвешенных веществ в течении года в точке 1 можно увидеть на диаграмме (рис.3.1).
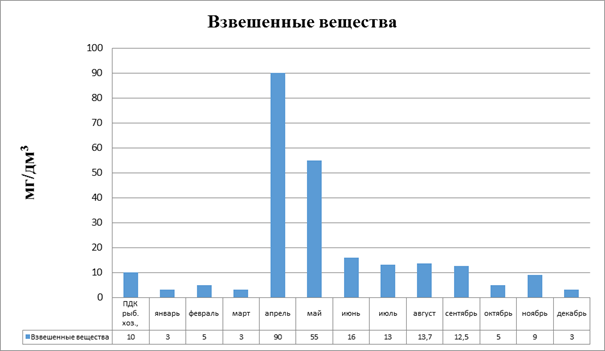
Рисунок 3.1 Диаграмма. Взвешенные вещества в точке 1
В первой точке мы можем наблюдать, что превышения ПДК зафиксированы с апреля по сентябрь. Максимум зафиксирован в паводковый период.
При наблюдении в течение года в точке 2 максимум зафиксирован в апреле и был связан с паводком(рис.3.2). Минимум в декабре и январе то есть в период покоя реки.
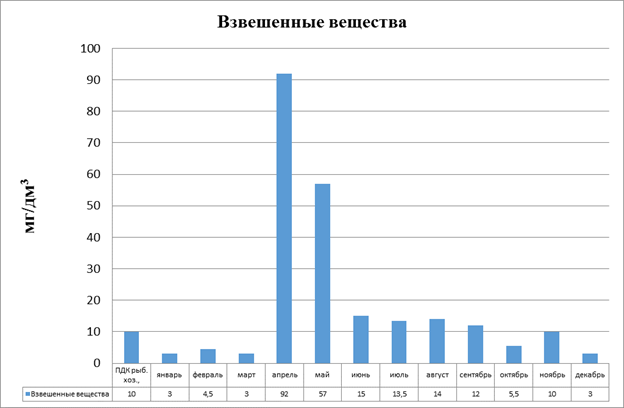
Рисунок 3.2 Диаграмма. Взвешенные вещества в точке 2
Проводя сравнительный анализ в двух точка мы наблюдаем следующее: (рис3.3
-максимальное повышение количества взвешенных веществ наблюдается в двух точках в паводковый период
-превышение ПДК наблюдалось в двух точках в один и то же время – с апреля по сентябрь – это связано, скорее всего с тем, что река в этот период судоходна, увеличен водосток с прибрежной части во время осадков, а также с активностью живых организмов;
-в точке 2 в паводковый период значения выше это связано с тем, что берег реки в точке отбора имеет глинистую структуру, частички глины с током воды с автодороги выносятся в реку.
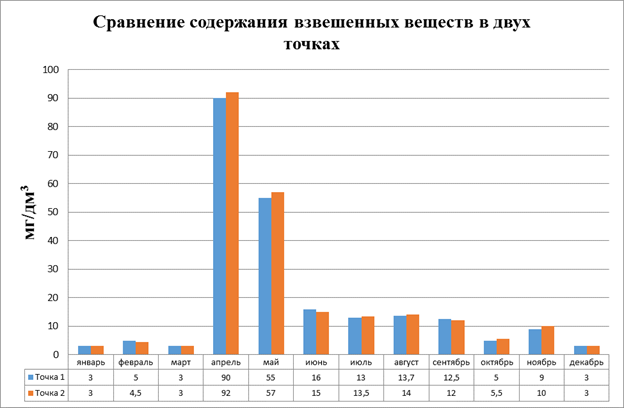
Рисунок 3.3 Диаграмма. Сравнение содержания взвешенных веществ в двух точках.
Наблюдения за ХПК проводились в течение года с периодичностью 1 раз в месяц. Были зафиксированы следующие результаты (рис.3.4).
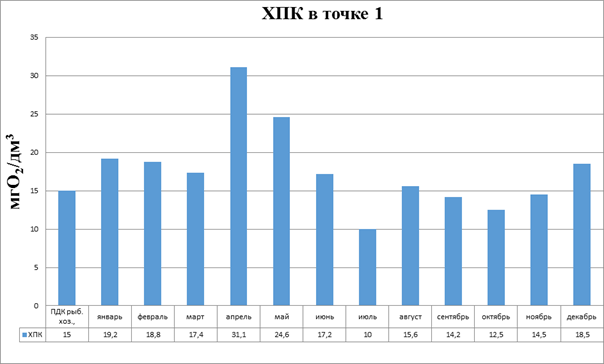
Рисунок 3.4 Диаграмма. ХПК в точке1
Из диаграммы видно, что отсутствие превышений ПДК наблюдаются только в июле, а также с сентября по ноябрь. В остальные месяцы года наблюдались превышения ПДК. Максимальные значения зафиксированы в апреле 31,1мгО2/дм3 и мае 24,6мгО2/дм3, что соответствует паводковому периоду на реке Белой.
Это связано, вероятно, с попаданием в реку загрязнений от городских улиц с талыми водами.
В точке 2 (рис.3.5) превышения ПДК наблюдалось в тот же период, однако результаты были значительно выше.
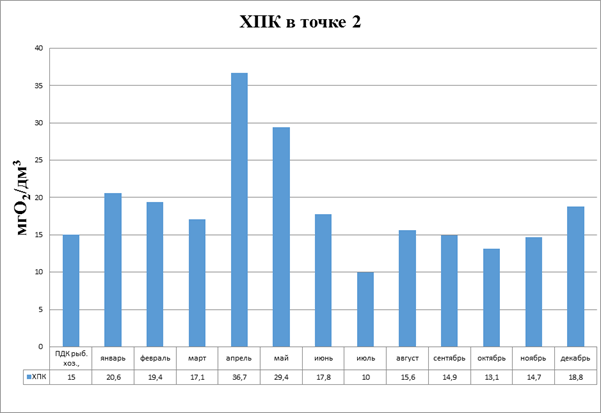
Рисунок 3.5 Диаграмма. ХПК в точке 2
Мы провели сравнение результатов ХПК в двух точках и отобразили их на диаграмме (рис.3.6).
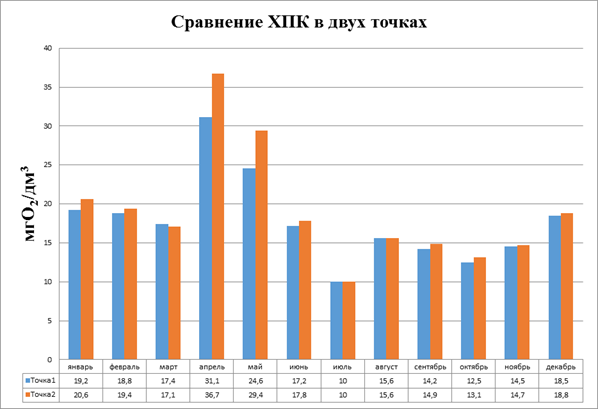
Рисунок 3.6 Диаграмма. Сравнение ХПК в двух пробоотборных точках
Сравнивая показания в двух точках, мы можем видеть, что в точке 2 ХПК не значительно выше, чем в точке 1. Это обусловлено, скорее всего тем, что значительная часть загрязнений с автодороги поступает в реку по имеющимся водостокам и не проходит процесс даже естественной фильтрации. Прибрежная почва в точке 2 в основном представлена суглинками, а в точке 1 это песок, который является природным фильтром.
Значительные превышения ПДК в двух точках наблюдаются в один и тот же период, и совпадает с паводком на реке Белой.
Результаты годового мониторинга по БПК приведены в диаграммах на рисунках 3.7, 3.8
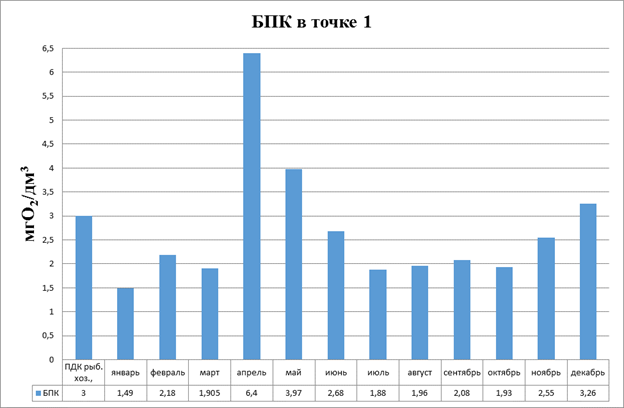
Рисунок 3.7 Диаграмма. БПКполное в точке 1
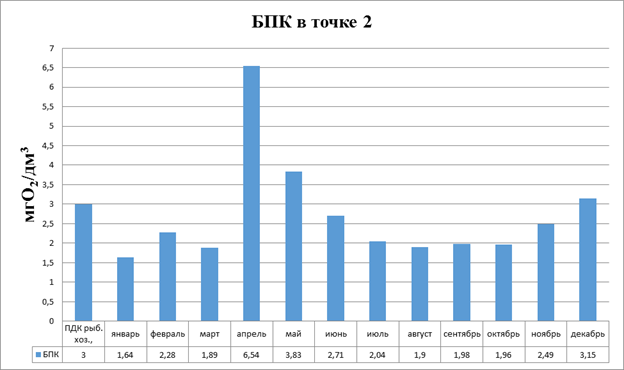
Рисунок 3.8 Диаграмма. БПКполное в точке 2
Из диаграммы на рисунке 3.8 видно, что превышения ПДК наблюдалось в тот же период, что и в точке 1.
Проводя сравнительную оценку в двух точках (рис.3.9) мы можем сделать следующие выводы:
-повышение БПК наблюдается в обоих точках в один и тот же период и совпадает с паводком;
-в точке 2 показатели не значительно выше, чем в точке 1 предположительно причиной этого может быть сток с автодороги попадающий в реку.
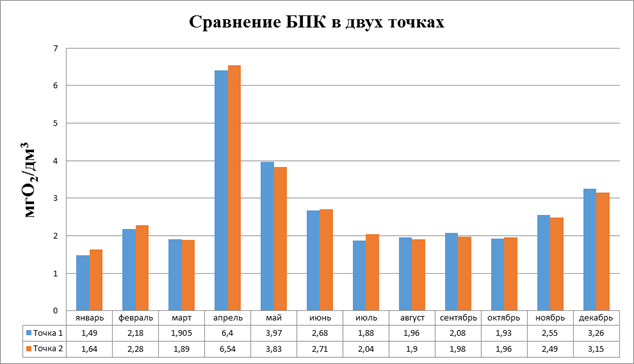
Рисунок 3.9Сравнение БПК в двух точках
Результаты наблюдений за содержанием нефтепродуктов течении года в точке 1 приведены в графике на рисунке 3.10.
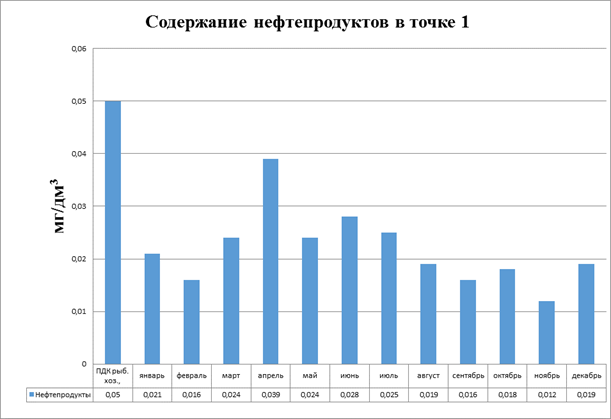
Рисунок 3.10. Диаграмма. Содержание нефтепродуктов в точке 1
В течении года превышений ПДК по нефтепродуктам выявлено не было, однако в паводковый период и в период летнего отдыха горожан концентрация их незначительно увеличивается. Это можно объяснить следующим. В период интенсивного снеготаяния талые воды с ближайших городских улиц стекают в реку, принося с собой значительное количество нефтепродуктов. Так данный участок водоема законодательно является местом отдыха жителей. В период летнего отдыха горожан большое количество автомобилей подъезжает к водоему. Местные жители зачастую оставляют после себя мусор в виде полиэтиленовых пакетов, пластиковых бутылок (рис.3.11).Так как берег имеет песчаную структуру проницаемость его для воды и растворенных в ней веществ очень высока. Являясь природным сорбентом песок способен частично задерживать загрязнения, что значительно снижает риск попадания их в водоем.

Рисунок 3.11 Мусор у кромки воды в районе Большого Благовещенского острова
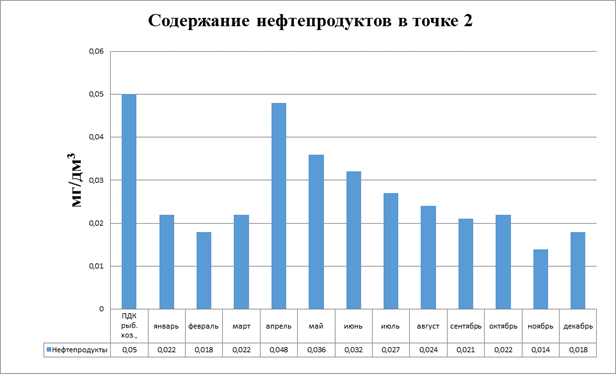
Рисунок 3.12. Диаграмма. Содержание нефтепродуктов в точке 2
Из полученных данных видно, что ПДК не превышено, но увеличение концентрации нефтепродуктов происходит в те же сроки (рис.3.12). Как и в точке 1 максимальное значение мы наблюдаем в паводковый период (апрель-май). Это то же связно с тем, что талые воды с автодороги стекают непосредственно в реку.
Сделав сравнительную оценку в двух точках исследования (рис.3.13), мы пришли к следующим выводам.
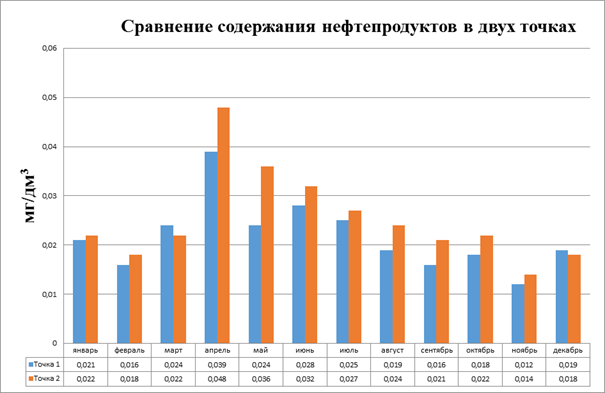
Рисунок 3.13. Сравнение содержания нефтепродуктов в двух точках
Превышений предельно допустимых концентраций в воде реки Белой по показателю нефтепродукты в течении календарного года не наблюдалось. Увеличение концентрации в двух точках происходит приблизительно в одни и те же сроки. В точке 2 концентрация нефтепродуктов выше, чем в точке 1. В связи с полученными данными можно предположить, что на оживленной автодороге выброс нефтепродуктов гораздо выше, чем в городе. Так же повышение концентрации наблюдается гораздо более продолжительный период это скорее всего связано с тем, что поток отдыхающих в районе Большого Благовещенского острова в августе, сентябре постепенно снижается, уменьшается количество водного транспорта прежде всего маломерных и туристических судов, а поток автомобильного транспорта на автодороге Авдон-Подымалово-Николаевка остается постоянным в течении всего года. В зимний период мы наблюдаем снижение концентрации нефтепродуктов в обеих точках, возможно из-за установления на реке ледяного покрова и окончания навигации. Толщина льда составляет от 40 до 70 сантиметров. Нефтепродукты с автодороги не поступают в реку.
Из рисунка 3.13 можно увидеть, что отсутствие нефтепродуктов в течении календарного года не наблюдалось. Это связано, скорее всего с тем, что в районе города Уфа множество нефтеперерабатывающих предприятий, сбрасывающих нормативно очищенные стоки в реку.
Таким образом мы определили источники попадания нефтепродуктов в воду реки Белой Благовещенского района Республики Башкортостан.
Проводя наблюдения, содержания уксусной кислоты в течение года в точке 1 мы получили, следующие результаты (рис.3.14)
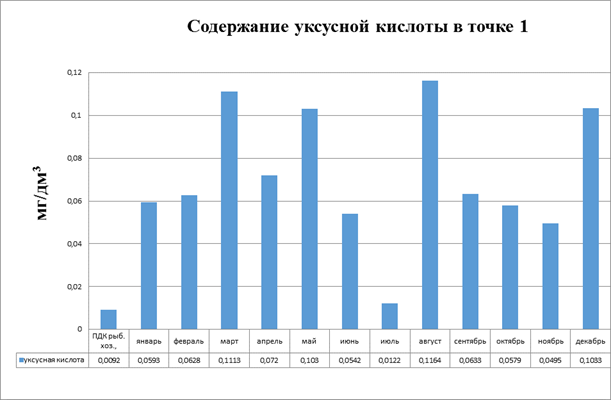
Рисунок 3.14. Диаграмма. Содержание уксусной кислоты в точке 1
Из рисунка видно, что в течение года наблюдалось значительное превышение ПДК. Это связано, скорее всего с тем, что уксусная кислота вещество трудно окисляемое кислородом, находящимся в воде. Так же она является продуктом окисления и может являться естественным загрязнителем.
В точке 2 при наложении значений на диаграмму мы видим, что превышения ПДК то же значительны (рис.3.15.).
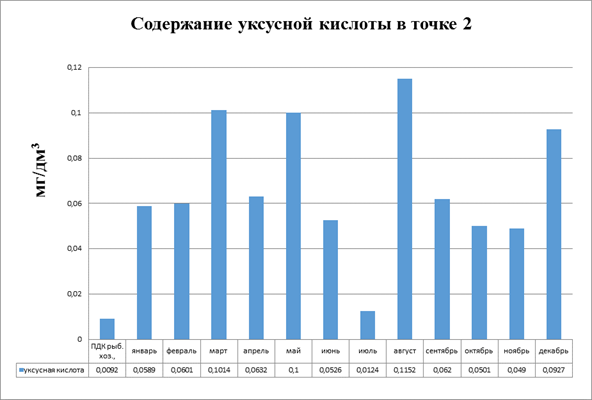
Рисунок 3.15. Диаграмма. Содержание уксусной кислоты в точке 2
Для сравнения результатов в двух точках мы наложили их на диаграмму (рис.3.16) и сделали выводы.
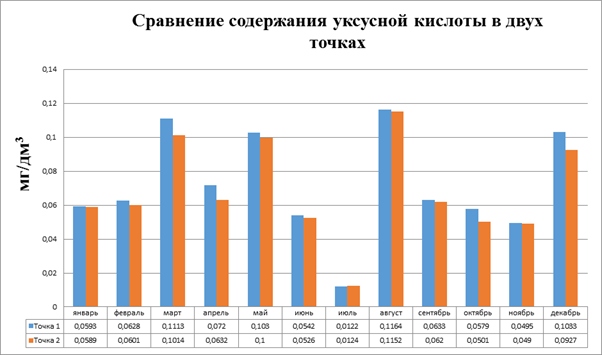
Рисунок 3.16. Диаграмма. Сравнение содержания уксусной кислоты в двух точках.
Максимальное превышение ПДК наблюдается в марте, августе и декабре, что соответствует вертикальной стратификации. Это еще раз служит доказательством, что загрязнение уксусной кислоты водоема может иметь, как антропогенную, так и естественную природу.
Уксусная кислота является источником питания для бактерий, скорее всего с этим связано незначительное понижение ее концентрации в точке 2, то есть водоем способен к самоочищению.
Для стоков с автодороги уксусная кислота не является специфичной, поэтому повышения концентрации в данной точке мы не наблюдаем.
По содержанию ТФК в точках определения были получены значения в 20-100 раз менее предела определения прибора, то есть значение содержание ТФК в воде можно принять равную нулю (рис.3.17, 3.18)
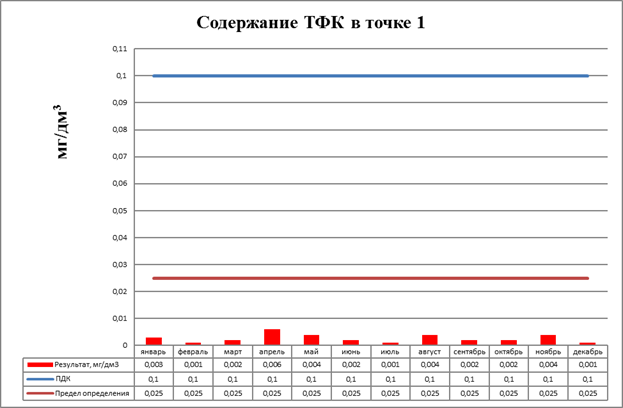
Рисунок 3.17 Содержание ТФК в точке 1
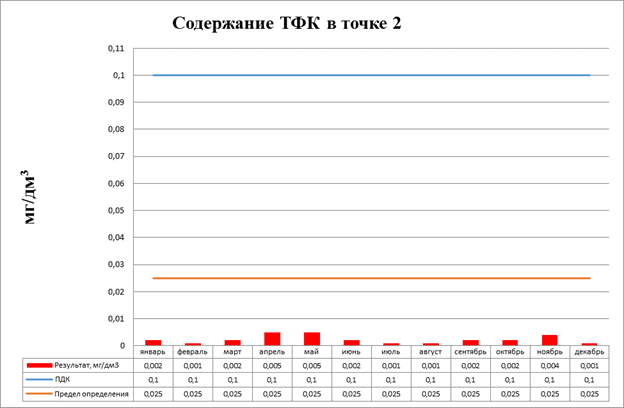
Рисунок 3.18 Содержание ТФК в точке 2
Дальнейшее сравнение нецелесообразно, так как данные результаты согласно, методики [МВИ-КЛЭК-1-2008] считаются недостоверными и находятся в пределах шумов хроматографа.
3.2 Лекционное занятие по курсу современные методы химического анализа
На сегодняшний день с ростом промышленности люди все больше стали обращать внимание и на экологическую ситуацию. Качество поверхностной воды и атмосферного воздуха интересуют современного человека не меньше.
Задача современных лабораторий точно определить качественные и количественные показатели. Современное оборудование, методы анализа и реактивы дают максимально точные результаты за минимальное время, благодаря чему и создается возможность быстрого влияния на качество окружающих нас предметов и состояния окружающей среды.
Методика количественного химического анализа; методика анализа: совокупность операций, выполнение которых обеспечивает получение результатов количественного химического анализа (результатов анализа) с установленными показателями точности (неопределенностью или характеристикой погрешности).
Значение неопределенности или характеристики погрешности, установленное для любого результата анализа, полученного при соблюдении требований и правил данной методики.
Систематическая погрешность методики анализа - разность между математическим ожиданием результатов анализа, полученных во всех лабораториях, применяющих данную методику, и истинным (действительным) значением измеряемой характеристики [РМГ 61-2010].
Физико-химические методы анализа, основаны на зависимости физических свойств вещества от его природы, аналитический сигнал представляет собой величину физического свойства, связанную функционально с концентрацией или массой определяемого компонента.
Важное практическое значение имеют методы, основанные на исследовании испускания и поглощения электромагнитного излучения в различных областях спектра, к ним относятся, например спектральный анализ, люминесцентный анализ, нефелометрия или турбидиметрия [Алемасова А.С., Енальева Л.Я., 2017].
К важным физико-химическим методам анализа принадлежат, электрохимические методы, использующие измерение электрического сигнала, исходящего от вещества – это кондуктометрия, кулонометрия, потенциометрия капиллярный электрофорез, а также хроматография.
Как и любой другой физико-химический метод, потенциометрия бывает прямой и косвенной. В обоих случаях анализ проводят в потенциометрической ячейке, состоящей из двух электродов – электрода сравнения и индикаторного электрода, помещенных в исследуемый раствор.
Во внешней электрической цепи электроды подключены к измерительному прибору – потенциометру, измеряющему разность потенциалов электродов ячейки. Либо потенциал индикаторного электрода относительно потенциала электрода сравнения, который в данных условиях является величиной постоянной, тогда как потенциал индикаторного электрода таковой величиной не является постоянной величиной, разность потенциалов называется электродвижущей силой или ЭДС [Нечипоренко А.П.].
При выполнении физико-химических методов анализа используют специальную, иногда довольно сложную, измерительную аппаратуру, в связи с чем эти методы часто называют инструментальными. Многие современные приборы оснащены встроенными ЭВМ, которые позволяют задать оптимальные условия анализа длину волны, калибровочную кривую. Почти во всех физико-химических методах анализа применяют два основных приема: методы прямых измерений и метод титрования. В прямых методах используют зависимость аналитического сигнала от концентрации анализируемого вещества.
Зависимость сигнала от природы вещества – основа качественного анализа. В некоторых методах связь аналитического сигнала с природой вещества установлена теоретически. Спектр атома может быть рассчитан по теоретически выведенным формулам. В количественном анализе используют зависимость интенсивности сигнала от концентрации вещества. Например, зависимость оптической плотности от концентрации при фотометрии. Чаще всего она имеет вид I = a + bс (уравнение связи), где I – интенсивность сигнала (оптическая плотность в спектрофотометрии сила диффузионного тока в полярографии,) с – концентрация, а и b – постоянные, причем во многих случаях а = 0
Измеряют интенсивность аналитического сигнала у нескольких стандартных образцов или стандартных растворов и строят градуировочный график в координатах I=f(с) или I=f(lgc), где с – концентрация компонента в стандартном растворе или стандартном образце. В тех же условиях измеряют интенсивность сигнала у анализируемой пробы и по градуировочному графику находят концентрацию [Чакчир Б. А., Алексеева Г. М.,2012].
Флоуриметрические методы анализа основаны на флуоресценции веществ, возникающей при облучении их ультрафиолетовыми лучами. Для проведения анализа используют флуориметрические анализаторы различных типов. Для выделения компонентов из пробы используют органические растворители в различных соотношениях и в чистом виде.
Принцип работы анализатора иллюстрируется оптической и структурной схемами (рис.3.19).
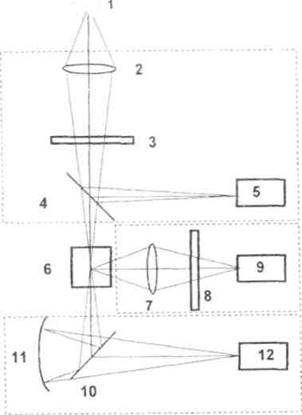
Рисунок 3.19 Оптическая схема анализатора
Оптическая схема анализатора может быть условно разбита на три канала: опорный (возбуждения); регистрации люминесценции и пропускания (фотометрический).
В опорном канале излучение ксеноновой лампы (1), работающей в импульсном режиме, проходит через собирающую линзу (2), светофильтр (3), выделяющий спектральную область возбуждения, отображается от светоделительной пластины (4) и попадает на приемник излучения (5) опорного канала. Электрический сигнал от этого приемника называется сигналом сравнения и служит для учета нестабильности работы лампы от импульса к импульсу, а также для запуска импульсной электронной схемы регистрации и обработки сигналов.
В канале пропускания излучение ксеноновой лампы (1), проходит через собирающую линзу (2), светофильтр канала возбуждения (3), светоделительную пластину(4), кварцевую кювету с образцом (6) и, отражаясь от поворотной пластины (10) и зеркала (11), попадает на приемник излучения (12) канала пропускания. Электрический сигнал от этого приемника зависит от оптической плотности образца и называется сигналом пропускания.
Под действием излучения ксеноновой лампы в кювете с образцом происходит возбуждение люминесценции растворенных веществ.
В канале регистрации излучение люминесцирующих компонентов пробы из кварцевой кюветы (6) проходит через собирающую линзу (7), светофильтр (8), выделяющий спектральную область регистрации, и попадает на приемник излучения канала регистрации люминесценции(9). Электрический сигнал этого приемника зависит от концентрации и состава определяемых веществ в растворе и называется сигналом люминесценции.
Результаты измерений по всем трем каналам связаны между собой следующими соотношениями.
Для методов «люминесценция»
![]()
Для метода «фотометрия» и «фосфоресценция»
![]() ,
,
где J – итоговый результат измерений в условных (приборных) единицах;
Jл – результат измерений по каналу регистрации люминесценции;
Jп – результат измерений по опорному каналу;
Jф – результат измерений по фотометрическому каналу;
n – число усредняемых измерений;
К - приборная константа.
Структурная схема анализатора состоит из низковольтного блока питания, импульсного источника света, измерительного блока, включающего в себя фотоприемники всех трех каналов, микропроцессорного контроллера и пульта управления с жидкокристаллическим графическим дисплеем (далее ЖК-дисплей) и клавиатурой.
Низковольтный блок питания преобразует переменное напряжение сети в нестабилизированное постоянное напряжение 12 В (при питании от сети переменного тока 220; при питании от источника постоянного тока 12 В в преобразовании нет необходимости), а затем в постоянное стабилизированное напряжение (+5 В, +15 В, -15 В), необходимое для питания измерительного блока и контролера.
Импульсный источник света вырабатывает световые импульсы длительности 100 мкс с частотой, определяемой микропроцессорным контролером (5 Гц).
Измерительный блок содержит приемники излучения, служащие для преобразования световых сигналов в электрические сигналы пропускания, сравнения и люминесценции и осуществляет регистрацию сигналов, поступающих от приемника.
Панель управления служит для выбора режимов работы прибора, ввода и вывода значений исходных параметров и результатов измерения на ЖК-дисплей.
Микропроцессорный контроллер обеспечивает выполнение команд, поступающих с клавиатуры, хранение в оперативной памяти значений исходных параметров, контролирует работу всех систем, управляет запуском импульсного источника света, обменом данными по RS-232, выводом данных и сообщений об ошибках на ЖК-дисплей.
Одним из самых распространенных методов количественного химического анализа является хроматография. На сегодняшний день большое количество вариантов хроматографического анализа позволяет решать самые различные задачи.
Одним из вариантов является жидкостная хроматография. Метод высокоэффективной жидкостной хроматографии, основан на различном перемещении компонентов, между неподвижной и подвижной фазами. Процесс хроматографии представлен на рисунке 3.20.
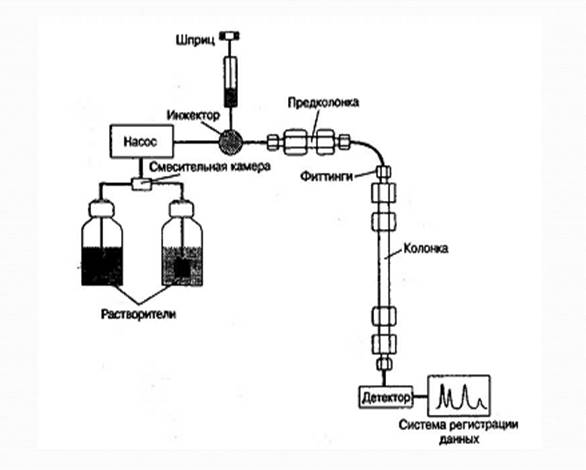
Рисунок 3.20 Схема системы ВЭЖХ
Разделение компонентов пробы осуществляется в хроматографических колонках. Перед колонкой устанавливается предколонка.
Ее функция заключается в следующем: накапливание сильно удерживаемых примесей на сорбенте колонки может сократить срок ее службы. Сокращая активную площадь поверхности неподвижной фазы, эти примеси вызывают смещение времен удерживания, ухудшение разрешения и формы пиков [Н.С.Зефиров,2008].
Таким образом, способом защиты аналитической колонки от подобного рода загрязнений является установка предколонки в линию между инжектором и аналитической колонкой (рис.3.21).

Рисунок 3.21 Хроматографическая колонка Waters Spherisorb S5 AX.
Задачи разделения разных классов веществ решаются благодаря использованию разнличных хроматографических колонок. При принятии решения какую использовать колонку, исходят из характеристик анализируемых веществ и подходящей подвижной фазы [К.И. Сакодынский, С.А. Волков].
Подвижная фаза представляет собой водный раствор органических и неорганических веществ, например аммония фосфорнокислого однозамещенного с добавлением ацетонитрила. После прохождения через колонку подвижная фаза сливается в отдельную емкость (рис.3.22).

Рисунок 3.22 Установка емкостей с подвижной фазой и сливом подвижной фазы
Раствор подвижной фазы должен быть тщательно очищен и освобожден от взвешенных частиц. Простейший способ очистки – пропускание его через мембранный фильтр с размером пор 0,5 мкм под вакуумом (рис.3.23).

Рисунок 3.23 Фильтрация подвижной фазы
Перед началом работы подготовленную подвижную фазу необходимо дегазировать – освободить от растворенных пузырьков воздуха, которые нарушают работу детектора, вызывают дрейф нулевой линии, снижают разрешение компонентов. Дегазацию осуществляют методом барботации. При барботировании через слой растворителя продувочный газ захватывает и уносит из системы растворенный воздух. Этот способ особенно предпочтителен при использовании легко окисляющихся растворителей (рис.3.24).

Рисунок 3.24 Дегазация подвижной фазы
Проводят предварительную подготовку пробы согласно методике анализа. В колонку вводят 20 мкл раствора пробы. Процесс разделения пробы на компоненты представлен в виде хроматограммы (рис.3.25). Результат анализа расчитывают по градуировочному графику по площади пиков и времени выхода компонентов.
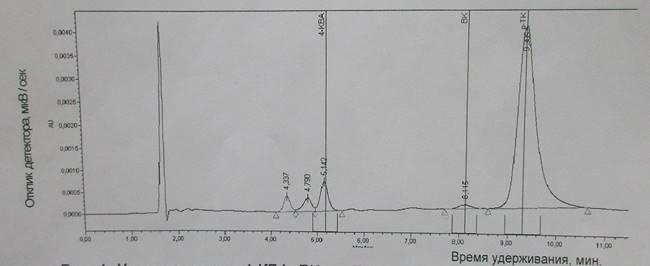
Рисунок 3.25 Хроматограмма
Газовая хроматография – это разновидность хроматографии для разделения летучих компонентов, при этом подвижной фазой служит газ-носитель в основном это инертный газ азот или гелий, протекающий через неподвижную фазу с большой поверхностью.
Различают газо-твёрдофазную и газо-жидкостную хроматографию. В первом случае неподвижной фазой является твёрдый носитель это силикагель, активированный уголь, оксид алюминия, во втором — жидкость, нанесённая на поверхность инертного носителя [Н.А. Коваленко, Г. Н. Супиченко, 2007].
Современные газовые хроматографы – это полностью автоматизированные програмно-аппаратные комплексы (рис.3.26).

Рисунок 3.26 Газовый хроматограф «Shimadzu» с автосемплером.
Источником газа-носителя чаще всего служит баллон со сжатым или сжиженным газом, который обычно находится под большим давлением, также часто используют сетевые газы от компрессорных установок и генераторов газов. Посредством редуктора давление на выходе снижают до 4 - 10 атмосфер то есть до рабочего давления хроматографа. Чаще всего при хроматографии использую азот или гелий.
Регулятор расхода газа – это модуль контроля потока, предназначенный, для контроль расхода газа в системе, а также поддержки необходимого давления газа на входе в хроматограф.
Устройство для ввода пробы, предназначено для подачи пробы анализируемой смеси в хроматографическую колонку.
Если хроматограф предназначен для анализа жидких проб, устройство ввода проб совмещают с испарителем. Пробы вводят микрошприцом в испаритель, путём прокалывания эластичной прокладки. Испаритель обычно имеет температуру, превышающую температуру самой колонки на 500C.
Принципиальная схема газового хроматографа представлена на рисунке 3.27.
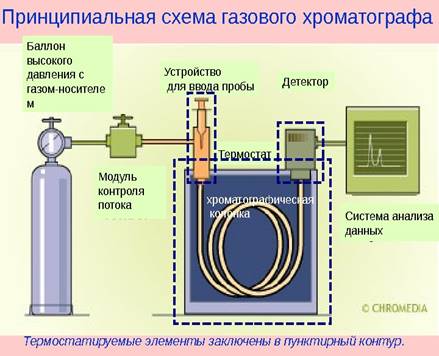
Рисунок 3.27 Схема газового хроматографа
В случае газообразных образцов, проба может вводиться 2 способами:
-включение в газовую схему «газового крана» перед испарителем. Газовый кран имеет 2 положения: «отбор пробы» и «анализ». В положении «отбор пробы» газ-носитель поступает напрямую в колонку, в это же время петля подключена одним концом к штуцеру отбора пробы, а вторым соединена со штуцером сброса пробы (атмосферой). При повороте газового крана в режим «анализ» происходит переключение потоков газов: теперь газ-носитель идет в колонку через пробоотборную петлю (обычно используют петли объёмом 1 или 2 мл) осуществляя таким образом ввод пробы в колонку, в это же время штуцер отбора пробы соединяется с атмосферой минуя пробоотборную петлю.
-проба вводится в испаритель путём прокалывания эластичной прокладки при помощи микрошприца.
Для анализа проб методом газовой хроматографии используют кварцевые или металлические капиллярные колонки (рис.3.28), а также насадочные колонки изготовленные из стекла или металла (рис.3.29).

Рисунок 3.28 Кварцевые и металлические капиллярные колонки

Рисунок 3.29 Стеклянные и металлические насадочные колонки
Основным этапом хроматорафии является детектирование. Детекторы предназначены для непрерывного измерения концентрации веществ на выходе из хроматографической колонки. Принцип действия детектора должен быть основан на измерении такого свойства аналитического компонента, которым не обладает подвижная фаза.
Существуют хроматографы с пламенно-ионизационным, фотометрическим и кондуктометрическим детектором [В.В. Бражников, 2012].
Современные методы количественного и не только анализа включают в себя несколько различных методик. Одной из таких методик является методика количественного анализа, которую можно рассмотреть на примере практического руководства по использованию систем капилярного электрофореза «КАПЕЛЬ» под авторством Н.В. Комаровой и Я.С. Каменцева, работающих в Санкт-Петербурге.
В последние годы в мире отмечен активный интерес к новому, интенсивно развивающемуся методу разделения сложных смесей — капиллярному электрофорезу, который позволяет анализировать ионные и нейтральные компоненты различной природы с высокой скоростью и эффективностью. В основе капиллярного электрофореза лежат электромиграция ионов и других заряженных частиц и электрический осмос.
В России работы, связанные с изучением капиллярного электрофореза и его аналитических приложений, стали появляться лишь в последние годы, что в существенной степени инициировалось созданием отечественных приборов для капиллярного электрофореза [Ягов Г.В., 2013].
Капиллярный электрофорез часто сравнивают с высокоэффективной жидкостной хроматографией, поскольку в обоих методах разделение происходит в длинных тонких трубах - капилляре или колонке с участием движущейся жидкой фазы элюента или буферного раствора. Для регистрации сигналов используют схожие принципы детектирования, однако в программах обработки данных у методов есть различия, которые, безусловно, относятся к достоинствам капиллярного электрофореза. Микрообъем анализируемого раствора попадает в кварцевый капилляр, предварительно заполненный подходящим буферным раствором электролита. После подачи высокого напряжения к концам капилляра компоненты смеси начинают двигаться с разной скоростью, которая зависит, в первую очередь, от заряда и массы или от величины ионного радиуса и, соответственно, в разное время достигают зоны детектирования. Полученная последовательность пиков называется электрофореграммой. Качественной характеристикой вещества является время миграции, а количественной — высота или площадь пика, пропорциональная концентрации вещества.
Высокая эффективность разделения то есть сотни тысяч теоретических тарелок, недоступная ВЭЖХ и связанная с плоским профилем электроосмотический поток, малый объем анализируемой пробы и буферов не более 1–2 мл в день, при этом практически не требуется применение высокочистых, дорогостоящих органических растворителей, отсутствие колонки, сорбента, проблем с его старением и, значит, заменой колонки, простая и недорогая аппаратура, быстрота и низкая себестоимость единичного анализа.
Из ограничений электрофореза следует отметить невысокую, по сравнению с ВЭЖХ, концентрационную чувствительность и требование к анализируемым соединениям растворяться в воде и разбавленных водно-органических смесях. Эти ограничения не являются непреодолимыми. Недостаточную чувствительность определения при использовании УФ-детектирования из-за малой длины оптического пути, равного внутреннему диаметру капилляра можно скомпенсировать использование таких видов детектирования, как лазерно-индуцированное, флуориметрическое или масс-спектрометрическое. А анализировать сильно гидрофобные, нерастворимые в водных растворах компоненты пробы возможно при варианте неводного капиллярного электрофореза успешно позволяющего разделять их.
Системы капиллярного электрофореза «Капель», разработанные и выпускаемые фирмой «Люмэкс», являются первым в России и СНГ серийным семейством приборов, они внесенны в Госреестр средств измерений и предназначенных для реализации метода капиллярного электрофореза. В состав семейства на сегодняшний день входят следующие модификации «Капель-103Р», «Капель-103РТ», «Капель-104Т», «Капель-104М», «Капель-105» и «Капель-105М», аттестованные как средства измерения: Фирма выпускает также электроинжекционные анализаторы «Капель-РЕ». Разрабатываются модели с встроенным блоком измерения потенциала течения «Капель-ПТ».
Системы капиллярного электрофореза «Капель» предназначены для качественного и количественного определения состава проб веществ в водных и водно-органических растворах методом капиллярного электрофореза. На приборах любой из модификаций без ограничений могут быть реализованы основные варианты капиллярного электрофореза — капиллярный зонный электрофорез и мицеллярная электрокинетическая хроматография.
Для того чтобы получить более подробное представление о методе, необходимо рассмотреть ряд процессов, происходящих в капилляре,который заполненен электролитом и помещен в продольное электрическое поле. Находящиеся на поверхности плавленного кварца силоксановые группы при контакте с водой или водными растворами гидролизуются и образуют удвоенного количества силанольных групп, которые затем гидратируются.
Самым простым вариантом является капиллярный зонный электрофорез. Компоненты сложной смеси движутся в среде электролита с разными скоростями, и образуют дискретные зоны. Отличительная особенность КЗЭ состоит в том, что он пригоден для разделения только ионогенных компонентов, в свою очередь как нейтральные соединения, не обладающие собственной электрофоретической подвижностью, будут двигаться со скоростью электроосмотического потока и выходить в зоне нейтральных компонентов.
Скорость и степень гидролиза зависят от температуры и рН, концентрации солевого фона раствора.
Несмотря на то, что в последнее время вернулось предложенное Хиртеном более корректное название электрофорез в свободном растворе, большая часть публикаций в этой области продолжает использовать традиционное название — «капиллярный зонный электрофорез». Основным достоинством его является высокая эффективность то есть сотни тысяч теоретических тарелок, при этом избирательность, определяемая механизмом разделения внутри одной фазы, в электрофорезе недостаточна. Повышение селективности может быть получено за счет изменения кислотности среды ведущего электролита, введения в состав буфера различных добавок в виде поверхностно-активных веществ, макроциклов, органических растворителей многих других.
Для определения методом капиллярного зонного электрофореза анионных компонентов проб в основном, неорганического происхождения, необходимо поменять полярность прикладываемого напряжения. В этом случае изменится не только направление миграции анионов, но и направление ЭОП.
В приборах капиллярного электрофореза, полярность входного конца чаще всего положительная (анод), и ЭОП переносит зону пробы к катоду.
Вблизи катодного выхода установлен детектор. При этих условиях катионные компоненты анализируемой пробы, тоже мигрирют к катоду, обгоняя ЭОП, они первыми достигают детектора в виде отдельных зон, которые на электрофореграмме выходят индивидуальными пиками. Через некоторое время детектора достигает и зона исходного раствора. В зависимости от того, поглощают они или нет, на электрофореграмме фиксируется прямой или обратный пик, который обычно называют системным. Иногда для идентификации системного пика в пробу добавляют специальные маркеры ЭОП, например, бензиловый спирт. Поведение анионных компонентов пробы зависит от соотношения скоростей ЭОП и электромиграции анионов. Если скорость миграции аниона выше скорости ЭОП, то такой анион выйдет из капилляра в прианодное пространство. Если же скорость электромиграции аниона меньше скорости ЭОП, то он может быть зарегистрирован на той же электрофореграмме, но после выхода системного пика. В таком варианте КЗЭ с положительной полярностью обычно определяются катионные компоненты проб и большинство органических анионов.
В результате первый слой двойного электрического слоя становится положительным, а второй отрицательным, и ЭОП будет двигаться от входного конца к детектору, немного отставая от мигрирующих быстрее анионов.
Мицеллярная электрокинетическая хроматография объединяет электрофорез и хроматографию. Она была введена в 1984 г. японским ученым Терабе.
Каждая мицелла окружена собственным двойным электрическим слоем, внешнюю диффузную часть слоя формируют катионы, присутствующие в растворе ведущего электролита. Число мономеров, образующих мицеллу, колеблется от 60 до 100 молекул, но при этом общий заряд мицеллы меньше из-за наличия в неподвижной части второго слоя ДЭС гидратированных катионов. Ни мицеллярная, ни мономерная форма АПАВ не реагируют со стенкой кварцевого капилляра, но при подаче на капилляр высокого напряжения обе формы мигрируют к аноду, в то время как ЭОП направлен к катоду.
Среди многообразия методов, основные преимущества капиллярного электрофореза, реализованные в системах капиллярного электрофореза:
-за один анализ может определятся несколько компонентов пробы, в кварцевом капилляре;
-достигаются эффективности разделения сотни тысяч теоретических тарелок;
-дозируется минимальный объем анализируемого образца, достигаются высокие скорости анализа;
-для большинства объектов используется в основном фильтрование и дегазирование \
-благодаря многообразию вариантов метода электрофореза разделяются гидрофобные и гидрофильные, ионные, нейтральные и хиральные компоненты;
Основными областями применения метода КЭ и некоторыми решаемыми задачами являются:
-анализ объектов окружающей среды:
-природные, питьевые, сточные воды;
-для определения в них анионов:
-катионов: аммония, калия, натрия, лития, магния, стронция, бария, кальция и других неорганических и органических анионов и катионов;
-хлоридов, сульфатов, нитратов, и др;
-анализ гербицидов классов феноксикарбоновых кислот, симметричных триазинов;
-почвы содержащие подвижные, водорастворимые формы анионов и катионов Co, Cu, Ni, Zn;
-анализ кормов, комбикормов и сырья для их производства на содержание в них аминокислот, белков витаминов;
-контроль качества пищевых продуктов и продовольственного сырья таких как минеральная и бутилированная вода, безалкогольные напитки и соки, спиртосодержащие напитки: вина, коньяки и коньячные спирты, водки;
-анализ лекарственных форм в фармакологии [Комарова Н.В., Каменцев Я.С.,].
Выводы по главе
1.Рассматривая зависимость показателя ХПК, как показателя общего органического загрязнения и сравнивая его повышения с повышением концентрации нефтепродуктов и уксусной кислоты, как органических загрязнителей мы наблюдаем следующее (рис.3.30, 3.31):
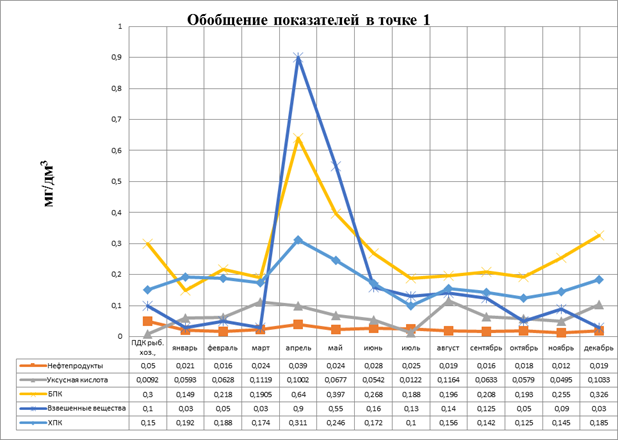
Рисунок 3.30. Диаграмма. Обобщение показателей в точке 1
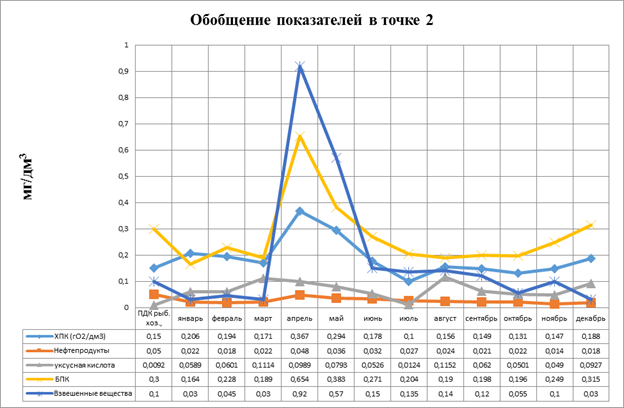
Рисунок 3.31. Диаграмма. Обобщение показателей в точке 2
2.Такие изменения могут быть связаны в данном случае с наступлением паводка, подъемом грунтовых и увеличением объема талых вод в весенний период по сравнения в летне –осенний (дождевой) период.
3.Максимальное повышение ХПК, концентрации уксусной кислоты и нефтепродуктов приходится на паводковый период.
4.Минимальное количество загрязнений зарегистрировано в июле, это связано скорее всего с летней гомотермией и активным размножением микроорганизмов в теплое время года, для которых загрязняющие вещества могут служить питанием - хемоавтотрофные организмы.
5.Отсутствие же загрязнений нефтепродуктами в течении всего календарного года не наблюдалось. Это связано, скорее всего, с тем, что в районе города Уфа множество нефтеперерабатывающих предприятий, которые сбрасывают нормативно очищенные стоки в реку.
6.По берегам реки находится множество населенных пунктов имеющих локальные очистные сооружения и сброс в реку Белая. Бытовые сточные воды имеют неоднородную структуру и большое количество органических загрязнений. С этим скорее всего связано постоянное превышение ПДК уксусной кислоты. Так как она может не только поступать в водоем, но и являться продуктом разложения и окисления органических веществ.
7.Суммарное же повышение ХПК может быть связано не только с данными веществами, но и с другими органическими загрязнителями не определенными в данной работе.
Таким образом мы определили источники попадания нефтепродуктов и уксусной кислоты в воду реки Белой Благовещенского района Республики Башкортостан.
Из всего сказанного можно сделать вывод:
1. поступление нефтепродуктов с ливневыми и талыми водами с автодороги Авдон-Подымалово-Николаевка выше, чем от городских улиц;
2. песчаный берег является естественным фильтром от загрязнения вод нефтепродуктами;
3. уксусная кислота загрязнитель не специфичный и может попадать как со сточными водами предприятий, так с городскими стоками и являться продуктом разложения органических веществ непосредственно в водоеме;
4. разложение прибрежного мусора – органических пищевых отходов, пластиковых бутылок может тоже быть источником поступления в воду уксусной кислоты [Д. С. Наумова, 2016].
5. ТФК в водном объекте не обнаружена.
ЗАКЛЮЧЕНИЕ
После проведения исследований мы выяснили, что исключить загрязнения водоемов не возможно, но можно максимально снизить количество поступающих в водоем загрязнений проводя ряд мероприятий по защите окружающей среды. Развитие безотходных производств, внедрение систем оборотного водоснабжения – создание замкнутого цикла использования производственных и бытовых сточных вод, то есть сточные воды все время находятся в обороте, и попадание их в поверхностные водоемы практически исключено. Очистка сточных вод.
Главный загрязнитель поверхностных вод – сточные воды, поэтому разработка и внедрение эффективных методов очистки сточных вод является важной экологической задачей. Очистка и обеззараживание поверхностных вод, используемых для водоснабжения и других целей.
Очистка ливневых и талых вод в том числе и от автодорог, применяя естественные методы фильтрации.
Современные методы очистки промышленных, бытовых ливневых и талых сточных вод может решить ряд проблем, возникающих в экологии: - механическая очистка, используемая с целью очистки сточных вод от различных механических загрязнений (взвешенные вещества, песок, глинистые частицы и волокна).
Основой механической очистки является четыре процесса: процеживание, отстаивание, центрифугирование, фильтрование; - физико-химические методы очистки – это флотация, коагуляция, реагентный метод, нейтрализация, экстракция.
Более эффективными методами очистки сточных вод в последние годы являюстся: озонирование, биологическая очистка В сооружениях для очистки ливневых и талых вод применяются естественные песчаные фильтры и отстойники [О.Г. Никитина, 2010].
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ И ЛИТЕРАТУРЫ
1. Артамонов, А. А. Параметрические характеристики водной среды, подвергшейся внешнему радиационному воздействию. Технологии живых систем / Федотова, И. В., Цетлин, В. В., Носовский, А. М.,2013г. - 29-34с [Электронный ресурс] http://h2o-institute.com/vsyo-o-vode/nauka-o-vode/voda-i-zhizn-kak-rabotaet-voda- v-nashem-tele-97/ (дата обращения 17.02.2016)
2. Вольф, И.В.Химия и микробиология природных и сточных вод. / Ткаченко, Н.И. СПбГУ, 2012-239с.
3. Новая теория, температурного сжатия и расширения воды. Источник Masakazu Matsumoto. Why Does Water Expand When It Cools, Phys. Rev. Lett.103. 2009 [Электронный ресурс] http://www.dinos.ru/sci/20090809232.html (дата обращения 24.02.2016).
4. Березина, Н.А. Гидробиология М, «Наука», 2014 -176с.
5.Конкина, Н. Г., Общая гидрология М., 2012 -427с.
6. Масару Эмото The Message from Water, 2016 [Электронный ресурс] http://www.litres.ru/po-bronson-2/mify-vospitaniya-nauka-protiv-intuicii/?lfrom=3785270 (дата обращения 12.08.2017)
7.Назаренко, О.Б. Экология: учебное пособие – Томск, 2007 – 100 с.
8. Возня, Н.Ф.Химия воды и микробиология. М., «Высшая школа» 2015 - 268с.
9. Российская Федерация. Водный кодекс. (с изменениями на 28 ноября 2015 года) (редакция, действующая с 1 января 2016 года) [Электронный ресурс] http://техэксперт.рус/
10. Комментарий к Водному кодексу Российской Федерации. [Электронный ресурс] http://техэксперт.рус/
11. Алимов, А. Ф. Эвтрофирование водоемов и структура сообщества гидробионтов. / Голубков, М. С. 2011 – 330с. [Электронный ресурс] http://naukarus.com/evtrofirovanie-vodoemov-i-struktura-soobschestva-gidrobiontov (дата обращения 3.06.2017г.)
12.Санитарные правила и нормы 2.1.5. Водоотведение населенных мест, санитарная охрана водных объектов гигиенические требования к охране поверхностных вод. СанПиН 2.1.5.980-00. [Электронный ресурс] http://техэксперт.рус/ (дата обращения 3.10.2016г.)
13. Российская федерация. Федеральный закон №7-ФЗ Об охране окружающей среды (с изменениями на 3 июля 2016 года) [Электронный ресурс] http://техэксперт.рус/ (дата обращения 10.01.2017г.)
14. Никаноров, И.Н. Качество поверхностных вод Российской Федерации за 2010 год. Ростов-на-Ддону 2011 – 475с.
15.Иванов, М.И. Химическое потребление кислорода как критерий чистоты воды 2013 – 224с. [Электронный ресурс] https://aqua-therm.ru/articles/articles_385.html (дата обращения 07.06.2017г.)
16.Готовцев, А.В. Вычисление биохимической потребности в кислороде и скорости биохимического окисления. Вода: химия и экология Всероссийский научно-практический журнал №8 2013 [Электронный ресурс] http://watchemec.ru/article/25910/ (дата обращения 29.09.2017)
17.Технологический регламент цеха нейтрализации и очистки сточных вод. Часть 4 Описание технологического процесса и технологической схемы очистки промышленных и хозяйственно-бытовых сточных вод. - Благовещенск, 2012 - 265с.
18.Зефиров, Н.С. Химическая энциклопедия. Том 4, 2004 -641с.
19.Никитина, А.П. Основы химической технологии. УГНТУ Уфа 2016 - 410с
20.Технологический регламент производства получения технической терефталевой кислоты. – Благовещенск, 2005. – 849 с.
21. Приказ Росрыболовства №20 от 18.01.2010. ПДК водных объектов рыбохозяйственного значения. [Электронный ресурс] http://техэксперт.рус/ (дата обращения 3.10.2016г.)
22.Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества. Гигиенические требования к обеспечению безопасности систем горячего водоснабжения. СанПиН 2.1.4.1074-01 [Электронный ресурс] http://техэксперт.рус/ (дата обращения 5.12.2017г.)
23. ГН 2.1.5.1315-03 с изменениями ГН 2.1.5.2280-07 и СанПиН 2.1.5.980-00. ПДК водных объектов питьевого, хозяйственно-бытового и рекреационного водопользования. [Электронный ресурс] http://техэксперт.рус/ (дата обращения 4.11.2016г.)
24 Причина массовой гибели карася в озере Ачикуль - повторное загрязнение водоема. [Электронный ресурс] URL:https://www.vesti.ru/doc.html?id=485112# (дата обращения 12.09.2016).
25. Лазарева, Н.В. Вредные вещества в промышленности. / Левиной, Э.Н СПб., «Химия», 2016г.
26. Отчет о темпах развития промышленности Республики Башкортостан [Электронный ресурс] https://economy.bashkortostan.ru/ (дата обращения 15.11.2017г.)
27. Все реки России. Река Белая [Электронный ресурс] http://vsereki.ru/ (дата обращения 6.12.2017)
28. Река Белая (Агидель) [Электронный ресурс] http://rekiurala.ru/reka-belaya (дата обращения 6.02.2017)
29. Администрация муниципального района Благовещенский район Республики Башкортостан [Электронный ресурс] URL: http://blag-gp.ru/ (дата обращения 10.03.2017).
30. ГОСТ 31861-2012 Межгосударственный стандарт. Вода. Общие требования к отбору проб. [Электронный ресурс] http://техэксперт.рус/ (дата обращения 3.05.2016г.)
31 Лыгин, С.А.Загрязнение р. Белая нефтепродуктами на территории Благовещенского района Республики Башкортостан «Вестник НИЦ МИСИ: актуальные вопросы современной науки» / Наумова, Д.С. электронный международный научный журнал. – М.: НИЦ МИСИ. – 2018. - № 7
32. Описание типа средства измерений. Приложение к свидетельству № 51881 об утверждении типа средств измерений. Анализаторы взвешенных веществ оптические ДИВ. 2015г.
33.Методика выполнения измерений на приборе. ДИВ ФР.1.31.2004.00976 [Электронный ресурс] http://техэксперт.рус/ (дата обращения 26.08.2017г.)
34.ПНД Ф 14.1:2:4.210-05 Количественный химический анализ вод. Методика измерений химического потребления кислорода (ХПК) в пробах питьевых, природных и сточных вод фотометрическим методом. [Электронный ресурс] http://техэксперт.рус/ (дата обращения 3.10.2016г.)
35.Количественный химический анализ вод. Методика выполнения измерений биохимической потребности в кислороде после n-дней инкубации (БПКполн.) в поверхностных пресных, подземных (грунтовых), питьевых, сточных и очищенных сточных водах. ПНД Ф 14.1:2:3:4.123-97 [Электронный ресурс] http://техэксперт.рус/ (дата обращения 3.10.2016г.)
36. "Методика измерений массовой концентрации нефтепродуктов в пробах природных, питьевых, сточных вод на анализаторе жидкости “Флюорат-02” ПНДФ 14.1:2:4.128-98 (Издание 2012 г.) [Электронный ресурс] http://техэксперт.рус/ (дата обращения 3.10.2016г).
37 Карцова, Л.А. Проблемы аналитической химии. Том 18. М, 2016 – 567с.
38. Количественный химический анализ вод. Методика измерений массовых концентраций уксусной кислоты в природных и сточных водах методом капиллярного электрофореза. ПНД Ф 14.1:2.226-2006. [Электронный ресурс] http://техэксперт.рус/ (дата обращения 3.10.2016г.)
39. Методика выполнения измерений терефталевой кислоты в природных водах. Благовещенск АО «ПОЛИЭФ». МВИ-КЛЭК-1-2008
40. Наумова, Д. С. Эколого-химический мониторинг природной поверхностной воды реки Белой на территории города Благовещенск. Экология России и сопредельных территорий : материалы XXI Междунар. экол. студенческой конф. / Новосиб. гос. ун-т. – Новосибирск : ИПЦ НГУ, 2016. – 342 с.
41. Рекомендации по межгосударственной стандартизации. Государственная система обеспечения единства измерений. Показатели точности, правильности, прецизионности методик количественного химического анализа. Методы оценки. РМГ 61-2010 [Электронный ресурс] http://техэксперт.рус/ (дата обращения 3.10.2016г.)
42. Алемасова, А.С. Лекции по аналитической химии. / Енальева, Л.Я. ДонНУ, Донецк 2017. – 284 с.
43. Нечипоренко, А.П. Физико-химические (инструментальные) методы анализа. Электрохимические методы. Потенциометрия и кондуктометрия: Учеб.-метод. пособие / Под ред. В.В. Кириллова. – СПб.: НИУ ИТМО; ИХиБТ, 2013. – 34 с.
44. Чакчир, Б. А. Фотометрические методы анализа. / Алексеева, Г. М. М 2012
45. Зефиров, Н.С. Химическая энциклопедия том 5. М «Большая Российская Энциклопедия»2008
46. Сакодынский, К.И.Аналитическая хроматография. / Волков, С.А. М., Химия 2013г.
47. Коваленко, Н.А.Химические методы количественного анализа. Варианты методов газовой хроматографии. / Супиченко, Г. Н. [Электронный ресурс] https://studfiles.net/preview/2524652/page:22/ (дата обращения 7.12.2017г.)
48. Бражников, В.В. Детекторы в хроматографии. М., 2012г.
49. Ягов, Г.В. Реферат: Элементы метода капиллярного электрофореза Элементы метода капиллярного электрофореза.
50. Комарова, Н.В.Практическое руководство по использованию систем капиллярного электрофореза. / Каменцев, Я.С. «КАПЕЛЬ» — СПб.: ООО «Веда», 2006. — 212 с. [Электронный ресурс] http://www.anchem.ru/literature/books/kniga_kap_forez.pdf (дата обращения 30.07.2017г.)
51. Никитина, О.Г. Биоэстимация: Контроль процесса очистки и самоочищения воды. М., 2010г.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.