
ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
«МНОГОПРОФИЛЬНЫЙ ЛИЦЕЙ
КИСЛОВОДСКОГО ГУМАНИТАРНО – ТЕХНИЧЕСКОГО
ИНСТИТУТА»
АЙСАНДЫРОВА САЛИМА АРСЕНОВНА
ПРОЕКТНАЯ РАБОТА
ПО БИОЛОГИИ
«Муковисцидоз :
продолжительность и качество жизни
в современном мире.
Научный руководитель:
Кравченко Ольга Семеновна,
преподаватель биологии
Кисловодск 2023
Содержание:
|
Глава 1. Болезнь муковисцидоз |
8-16 |
|
1.1.Понятие «Муковисцидоз» |
8-11 |
|
1.2.«Заболевание муковисцидозом в мире и России». |
11 |
|
1.3. История изучения муковисцидоза |
12-16 |
|
Глава 2.Жизнь с муковисцидозом |
17-20 |
|
2.1. Продолжительность жизни в современном мире с муковисцидозом |
17-19 |
|
2.2. Качество жизни в современном мире с муковисцидозом |
19-20 |
|
Глава 3. Диагностика и лечение муковисцидозом |
21-30 |
|
3.1. Перспективы ранней диагностике |
21-25 |
|
3.2. Перспективы лечения |
25-30 |
«Воспроизведение жизни-это и есть наследственность, в ней проявляется инвариантная сторона жизненных явлений, принцип сохранения жизни»
Н.П.Дубинин
Введение
Актуальность темы
Актуальность темы обусловлена тем, что в настоящее время в связи с внедрением неонатального скрининга на муковисцидоз и увеличения количества выявленных случаев муковисцидоза у детей существует необходимость изыскания рациональных способов оценки функционального состояния органов дыхания у больных, не способных к проведению спирометрии в силу возраста, для обьективной оценки тяжести патологического процесса.
· повышение уровня и качества медицинского, социального обслуживания больных муковисцидозом в крае.
Задачи
1. Расширить уровень социального сопровождения больных муковисцидозом и членов их семей.
2. Повысить квалификацию и уровень профессиональных знаний медицинских работников в области лечения муковисцидоза.
3. Повысить уровень знаний и умений больных муковисцидозом и членов их семей.
4. Повысить уровень информированности целевых групп проекта в теме муковисцидоза.
Наследственность человека подчиняется тем же биологическим закономерностям, что и наследственность всех живых существ. У человека, как и у других организмов, встречаются доминирующие и рецессивные признаки. В формировании каждого свойства или признака человека, разумеется, также участвует как наследственность, так и среда.
Так как наследственные заболевания — это заболевания, обусловленные генными или хромосомными мутациями. У людей от 20 000 до 25 000 генов. Генетическая мутация возникает, когда изменяется один или несколько генов. Если это генетическое изменение передается детям, то это наследственное генетическое заболевание. При совпадении у партнеров статусов носительства определенных болезней есть высокий риск рождения ребенка с наследственным заболеванием. Если у вас не проявляются симптомы заболевания, вы по-прежнему можете быть носителем и передать мутации своим детям. Многие генетически обусловленные заболевания проявляются не сразу после рождения, а спустя некоторое время. От наследственных заболеваний следует отличать врожденные заболевания, вызванные внутриутробными повреждениями, например, инфекцией или внешними воздействиями. И так как генетика- это наука, изучающая наследственность и изменчивость, то вопросами наследственных болезней занимается медицинская генетика.
С генетических позиций все болезни человека можно разделить на три класса: собственно наследственные болезни, куда входят хромосомные и генные заболевания, болезни с наследственной предрасположенностью, которые называют полигенными, комплексными или, чаще, многофакторными, и приобретенные, основной этиологический механизм которых связан с определенными неблагоприятными внешними воздействиями.
Муковисцидоз является наиболее распространенным опасным для жизни генетическим заболеванием среди белого населения. В США его выявляют примерно у 1/3 300 рожденных европеоидов, у 1/15 300 рожденных афроамериканцев и у 1/32 000 рожденных американцев азиатского происхождения. Вследствие применения усовершенствованных методов лечения продолжительность жизни больных значительно увеличилась, так, например, приблизительно 56% пациентов с муковисцидозом в США –взрослые.
Все больные муковисцидозом потенциально опасны друг для друга, так как очень подвержены инфекциям и обладают разной микрофлорой.
Кроме того, Уилл инфицирован сепацией (Burkholderia cenocepacia ST709) – для больных муковисцидозом это смертельная инфекция, еще более опасная, чем синегнойная палочка.
Заболевание оценивается как социально значимое, поскольку оказывает существенное влияние как на гуманитарную составляющую общественного здоровья, так и на ресурсы систем здравоохранения . Снижение социальных расходов обеспечивается, в первую очередь, предупреждением обострений инфекционного процесса в лёгких, лидирующих среди всех осложнений МВ .
Специалисты подчеркивают, что в последнее время наблюдается улучшение ситуации с выживаемостью больных, что достигается не только за счёт своевременной диагностики заболевания, но и во многом применением новых инновационных препаратов с учётом генотипа, обусловливающего патологический процесс .Эти препараты заставляют по-новому рассматривать проблему МВ, поскольку, воздействуя на одно из основных звеньев патогенеза заболевания, они позволяют отказаться от рассмотрения результатов лечения только через призму частоты обострений инфекционного процесса в лёгких или улучшения функции лёгких. Сейчас следует измерять эффективность терапии этого жизни угрожающего заболевания в дополнительных годах жизни, что, собственно, и лежит в основе оценки важности применения таргетной терапии, что уже стало понятным по опыту её применения в ряде стран.
Поскольку внедрение новых лекарственных и иных подходов к лечению требует определённых финансовых затрат, следует уточнить место заболевания в общей структуре заболеваемости и его экономической нагрузки на общественные ресурсы. Это в полной мере относится к рассматриваемой болезни, важность которой определяется уже тем, что в нашей стране она входит в Перечень высокозатратных заболеваний (ВЗН),
позволяющий финансировать лекарственные препараты за счёт государства. Тем не менее, с учётом перспективы разработки и постепенного внедрения в практику новых эффективных препаратов для лечения МВ, важно обратиться к изучению его социально-экономического бремени. Это должно дать понимание того, насколько заболевание ресурсоемкое, и посмотреть на проблему не только и не столько с точки зрения стоимости лекарств, но и учесть иные расходы (прямые и непрямые) для понимания приоритетности принятия финансовых решений в системе здравоохранения.
Перспективным способ неивазивной функциональной диагностике является компьютерная бронхофонография, метод, разработанный и зарегистрированный российскими учеными, основанный на регистрации звуковых феноменов, возникающих при дыхании, с последующим анализом и математической обработкой частотных и временных характеристик спектра этих шумов. Однако возможности при муковисцидозе изучены недостаточно, а имеющиеся данные противоречивы. Имеется необходимость сопоставления особенностей течения заболевания, которое приводит к изменению основных параметров компьютерной бронхофонографии, ввиду отсутствия данных по этой проблеме. Помимо этого, в предшествующих работах отмечена вариабельная информативность метода в выявлении нарушений бронхиальной проводимости у тяжелых больных.
Не установлены основные операционные характеристики компьютерной бронхофонографии (чувствительность и специфичность) примуковисцидозе, что требует сопостановления результатов исследования со стандартом функциональной дагностики в пульмонологии – спирометрией.
Ввиду отсутствия возрастных ограничений, применение компьютерной
бронхофонографии является перспективным в диагностике обструктивных нарушений вентиляции у детей, не способных к проведению спирометрии в силу возраста. Однако в настоящий момент установление степени тяжести бронхообструкции у детей с муковисцидозом невозможна, так как не разработаны критерии градации степени тяжести вентиляционных нарушений для интерпретации результатов компьютерной бронхофонографии.
Таким образом, актуальность проблемы муковисцидоза состоит в том, что болезнь требует ранней диагностики, постоянного лечения дорогостоящими препаратами, активного диспансерного наблюдения, сопровождается низкой продолжительностью жизни пациентов и всегда приводит к ранней инвалидизации пациентов.
Существует ряд болезней человека, которые при своей наследственной передаче воспроизводят тип аутосомного (НЕ СЦЕПЛЕННОГО С ПОЛОМ) доминантного и рецессивного наследования.
Глава 1. Болезнь муковисцидоз.
1.1.Понятие «Муковисцидоз».
Муковисцидоз имеет аутосомно-рецессивный тип наследования
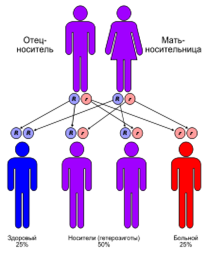
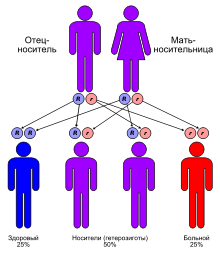
Ген, ответственный за муковисцидоз, был клонирован в 1989 году. Благодаря этому удалось выяснить природу мутации и усовершенствовать метод выявления носителей. В основе заболевания лежат мутации в гене CFTR, который локализован в середине длинного плеча 7-й хромосомы[3]. Муковисцидоз наследуется по аутосомно-рецессивному типу и регистрируется в большинстве стран Европы с частотой 1:2000-1:2500 новорождённых. В России в среднем частота болезни 1:10000 новорождённых. Если оба родителя гетерозиготные (являются носителями мутировавшего гена), то риск рождения больного муковисцидозом ребёнка составляет 25 %. Носители только одного дефектного гена (аллели) не болеют муковисцидозом. По данным исследований, частота гетерозиготного носительства патологического гена равна 2-5 %.
Идентифицировано около 2000 мутаций гена муковисцидоза. Следствием мутации гена является нарушение структуры и функции белка, получившего название муковисцидозного трансмембранного регулятора проводимости (МВТП). Следствием этого является сгущение секретов желёз внешней секреции, затруднение эвакуации секрета и изменение его физико-химических свойств, что, в свою очередь, и обусловливает клиническую картину заболевания. Изменения в поджелудочной железе, органах дыхания, желудочно-кишечном тракте регистрируются уже во внутриутробном периоде и с возрастом пациента неуклонно нарастают. Выделение вязкого секрета экзокринными железами приводит к затруднению оттока и застою с последующим расширением выводных протоков желез, атрофией железистой ткани и развитием прогрессирующего фиброза. Активность ферментов кишечника и поджелудочной железы значительно снижена. Наряду с формированием склероза в органах имеет место нарушение функций фибробластов. Установлено, что фибробласты больных муковисцидозом продуцируют цилиарный фактор, или М-фактор, который обладает антицилиарной активностью — он нарушает работу ресничек эпителия.
В настоящее время рассматривается возможное участие в развитии патологии лёгких при МВ генов, ответственных за формирование иммунного ответа (в частности, генов интерлейкина-4 (IL-4) и его рецептора), а также генов, кодирующих синтез оксида азота (NO) в организме[4].
Муковисцидоз является наследственным заболеванием желез внешней секреции, проявляется в первую очередь патологией со стороны желудочно-кишечного тракта и дыхательной системы. Повышенная вязкость секрета желез внешней секреции приводит к хроническому воспалительному процессу в легких, экзокринной недостаточности поджелудочной железы, гепатобилиарной патологии и аномально высокому содержанию электролитов в поте. Диагноз ставят на основании данных исследования пота или идентификации 2 вариантов гена, вызывающих муковисцидоз, у больных с положительным результатом неонатальных скрининг-тестов или характерных клинических признаков.
Мутации, из-за которых возникают наследственные заболевания, могут иметь доминантный или рецессивный характер наследования.
Доминантное наследование означает, что только одна копия гена - от матери или отца — должна иметь мутацию (или патогенный вариант гена) для проявления признака или заболевания. А при рецессивном типе человек наследует две измененные копии одного и того же гена. На нашем примере, муковисцидоз наследуется по аутосомно-рецессивному типу, частота выявления мутации гена CFTR – 3% среди белого населения. Ответственный ген локализован на длинном плече хромосомы 7. Он кодирует мембраноассоциированный белок, называемый муковисцидозным трансмембранным регулятором проводимости (CFTR). Наиболее распространенная вариантами гена, F508del, встречается примерно у 85% аллелей; были идентифицированы > 2000 менее распространенных вариантов CFTR. CFTR представляет собой циклический аденозиновый монофосфат (цАМФ) – управляемый канал движения хлоридов, регулирующий транспорт хлоридов, натрия и бикарбонатов через эпителиальные мембраны. Возможно, он имеет ряд дополнительных функций. Болезнь проявляется только у гомозигот. У гетерозигот могут появляться небольшие нарушения эпителиального транспорта электролитов, но клинически они чаще здоровы.
Варианты гена CFTR были поделены на шесть классов на основе воздействия варианта на функции или процессинг CFTR-белка. Считается, что пациенты с I, II или III классом вариантов, имеют более тяжелый генотип, что приводит к недостаточной или отсутствующей CFTR функции, тогда как пациенты с 1 или 2 копиями вариантов IV, V или VI класса, считаются имеющими более мягкий генотип, и, как результат, остаточную CFTR функцию. Тем не менее строгая зависимость между конкретными вариантами и проявлениями болезни отсутствует.
Патофизиология муковисцидоза.
Почти все экзокринные железы вовлечены в патологический процесс в той или иной степени. Железы могут:
1) Подвергаться обтурации вязким или твердым материалом в просвете (поджелудочная железа, кишечные железы, внутрипеченочные желчные протоки, желчный пузырь и подчелюстные железы)
2) Выявляется чрезмерная секреция при измененной гистологии экзокринных желез (трахеобронхиальные и Бруннеровы железы)
3) Чрезмерная секреция натрия и хлоридов отмечается при нормальной гистологии экзокринных желез (потовые, околоушные и малые слюнные железы)
Нарушения дыхания.
Хотя легкие гистологически при рождении чаще нормальные, у большинства пациентов патология со стороны дыхательной системы развивается в младенчестве или раннем детстве. Тампонада слизью и хроническая бактериальная инфекция сопровождаются выраженным воспалительным ответом, повреждением дыхательных путей, что в конечном счете приводит к бронхоэктазам и дыхательной недостаточности. Течение заболевания характеризуется эпизодическими обострениями бронхолегочного процесса и прогрессирующим снижением функции легких.
Повреждение легких, вероятно, инициируется диффузной обструкцией дистальных отделов дыхательных путей аномально большим выделением слизи. Бронхиолит и слизисто-гнойная закупорка дыхательных путей возникают вторично по отношению к обструкции и присоединения инфекции. Хроническое воспаление, вторичное по отношению к высвобождению протеаз и провоспалительных цитокинов клетками дыхательных путей, также способствует повреждению легких.
Изменения дыхательных путей встречаются чаще, чем изменения паренхимы легких. Около 50% пациентов имеют повышенную реактивность бронхов, которая может реагировать на применение бронходилататоров. У пациентов, с запущенными заболеваниями легких, хроническая гипоксия приводит к мышечной гипертрофии легочных артерий, легочной гипертензии и гипертрофии правого желудочка. В дыхательных путях пациентов с муковисцидозом часто присутствуют анаэробные бактерии и распространенные респираторные вирусы, но их роль в прогрессировании заболевания не установлена.
Желудочно-кишечный
При муковисцидозе в патологический процесс часто вовлекаются поджелудочная железа, кишечник.
Экзокринная функция поджелудочной железы нарушена у 85–95% больных.
Исключение составляет группа пациентов, имеющих определенные «легкие» варианты CFTR с остаточной функцией, при которых функция поджелудочной железы остается неизменной. Пациенты, с недостаточностью поджелудочной железы, имеют нарушения всасывания жиров, жирорастворимых витаминов и белка. Секрет в двенадцатиперстной кишке аномально вязкие и показывает отсутствие или уменьшение активности фермента и снижение концентрации бикарбоната; трипсин и химотрипсин в стуле отсутствуют или снижены. Эндокринная дисфункция поджелудочной железы возникает реже, но нарушение толерантности к глюкозе или сахарный диабет присутствует примерно у 2% детей, 20% подростков и до 50% взрослого населения.
1.2. «Заболевание муковисцидозом в мире и России».
На сегодняшний день, по данным национальных регистров, в мире сегодня живут приблизительно 70 000 человек с установленным диагнозом «муковисцидоз» . В России эту патологию выявляют с частотой 1:4900 новорождённых . Ежегодно в России диагностируют около 150 новых случаев муковисцидоза. Общее количество больных муковисцидозом в России по данным Росстата на 1 января 2019 г. составляло 3645 человек. Частота муковисцидоза в Российской Федерации 2,5 на 100 тыс. населения согласно данным Регистра больных муковисцидозом от 2018 г. .
В регистр больных муковисцидозом Российской Федерации вошли данные о 3142 пациентах из 81 региона Российской Федерации. ДНК-диагностика1 проведена у 94,3%, среди них у 89,3% выявлена мутация в гене CFTR, две мутации обнаружены у 82,4%. У 14% выявлена одна мутация, у 3,7% больных генетических вариантов не выявлено. При этом число взрослых больных постоянно возрастает
1.3. История изучения муковисцидоза.
Муковисцидоз известен с древности. В средние века среди европейских народов считали, что ребёнок, при поцелуе которого ощущается солёный привкус на губах, обречён на скорую смерть, но объяснить патогенез заболевания не удавалось. С развитием научных знаний развивались и представления о природе заболевания. В 1936 г. один из основоположников современной педиатрии Guido Fanconi впервые описал муковисцидоз. Он совместно с командой докторов выявил и описал первые случаи кистофиброза поджелудочной железы и бронхоэктазы у детей, указав на семейный характер заболевания. Затем в 1938 г. вышла монография американского патологоанатома D.H. Andersen «Кистофиброз поджелудочной железы и его взаимоотношение с целиакией». Таким образом, заболевание было выделено в самостоятельную нозологическую единицу, и в его терапии начали применять панкреатический фермент.

Дороти Хансин Андерсен
Считается, что МВ появился около 3000 лет до н. э. в результате миграции народов, генных мутаций и новых условий питания. Хотя весь клинический спектр муковисцидоза не был известен до 1930-х годов, некоторые аспекты болезни были выявлены гораздо раньше. Немецкие авторы 18 века предупреждали "Wehe dem Kind, das beim Kuß auf die Stirn salzig schmeckt, es ist verhext und muss bald sterben" («Горе ребенку, который на вкус соленый от поцелуя в лоб, ибо он проклят и скоро должен умереть»), что указывало на потерю соли при муковисцидозе].
В 1938 году Дороти Хансин Андерсен (на илл.) опубликовала статью «Кистозный фиброз поджелудочной железы и его связь с глютеновой болезнью: клиническое и патологическое исследование» в Американском журнале детских болезней. Она была первой, кто описал характерный кистозный фиброз поджелудочной железы и связал его с заболеванием легких и кишечника, характерным для муковисцидоза]. Она также впервые выдвинула гипотезу о том, что муковисцидоз является рецессивным заболеванием, и впервые применила замену ферментов поджелудочной железы для лечения больных детей. В 1952 году Поль ди Сант-Аньезе обнаружил отклонения в электролитах пота].
Впервые связь между муковисцидозом и другим маркером (пароксоназой) была обнаружено в 1985 г. Гансом Эйбергом. В 1988 году Фрэнсис Коллинз, Сюй Личжи и Джон Р. Риордан обнаружили первую мутацию CF, ΔF508, на седьмой хромосоме. Последующие исследования выявили более 1000 различных мутаций, вызывающих муковисцидоз].
Поскольку мутации в гене CFTR, как правило, невелики, классические методы генетики не могли точно определить мутировавший ген. Используя белковые маркеры, исследования сцепления генов позволили сопоставить мутацию с хромосомой 7]. В 1989 году Сюй Личжи возглавил группу исследователей в больнице для больных детей в Торонто, которые обнаружили ген, ответственный за муковисцидоз
Прогноз при муковисцидозе до настоящего времени остаётся неблагоприятным. Летальность составляет 50—60 %, среди детей раннего возраста — выше. При поздней диагностике и неадекватной терапии прогноз значительно менее благоприятный. Большое значение приобретает медико-генетическое консультирование семей, в которых есть больные муковисцидозом.
Критерием качества диагностики и лечения муковисцидоза является средняя продолжительность жизни больных. В европейских странах этот показатель достигает 40 лет, в Канаде и США — 48 лет, а в России — 22—30 лет.
На каждого выявленного больного обычно приходится 100 невыявленных Муковисцидозом болеют:
· Белоруссия — 150 человек
· Россия — 2 186 человек (по официальной статистике на 2010 год
В 1946 г. термин «муковисцидоз» (лат. mucus — слизь, viscus — вязкий) ввёл американский педиатр S. Farber. Он указал на вторичный характер поражения внутренних органов при этом заболевании в связи с обструкцией вязкой слизью выводных протоков желёз
Во второй половине XX века учёные J. West и Paudi Sant’Agnese впервые описали функциональное состояние и ателектазы в лёгких у детей с муковисцидозом. Изначально муковисцидоз называли «болезнью солёного поцелуя», это наблюдение позволило в 1953 г. педиатрам из США во главе с Paudi Sant’Agnese изучить симптом повышенного содержания хлоридов в поте у больных муковисцидозом, что дало возможность в 1959 г. L.E. Gibson и R.E. Cook применить пилокарпиновый тест для проведения потовой пробы, который и сегодня остаётся главным диагностическим критерием ранней диагностики муковисцидоза.
Доктора H. Shwachman и L. Kulczycki представили медицинской общественности разработанную ими систему клинической оценки тяжести заболевания, которая актуальна по настоящее время . Лёгочная инфекция бывает ведущей причиной смертности при муковисцидозе. С приходом эры применения антибиотикотерапии удалось увеличить продолжительность жизни больных. Также учёные того времени понимали важность ранней постановки диагноза, особое значение придавали ежедневной кинезитерапии
В 1949–1953 гг. H. Shwachman и N. Hoiby провели исследования эффективности антибиотикотерапии, и на основе их данных в схему лечения муковисцидоза с конца 1970-х годов были внедрены регулярные (1 раз в 3 мес) курсы внутривенной антибактериальной терапии препаратами с антисинегнойной активностью.
С 1999 г. для контроля инфекции, вызванной P. aeruginosa, начато применение ингаляционного тобрамицина — аминогликозида с антисинегнойной активностью, имеющего минимум побочных эффектов и хорошую переносимость . Исследования под руководством B. Ramsey показали достоверное улучшение объёма форсированного выдоха на 10% за 20 мес наблюдения и уменьшение количества обострений, тогда как в группе плацебо была отрицательная динамика .
В 1964 г. L. Matthews изложил универсальный комплексный подход к терапии заболевания: борьба с обструкцией дыхательных путей и вторичной инфекцией, коррекция панкреатической недостаточности и дефицита питания. Данная концепция легла в основу работы центров муковисцидоза
В 1978 г. R. Kraemer доказал, что высококалорийное питание с использованием очень высоких доз панкреатических ферментов эффективно для больных муковисцидозом, тесно коррелирует с выживаемостью, а дефицит веса существенно ухудшает прогноз .
В 1989 г. совместная работа группы учёных из Канады и США под началом доктора Lap-Сhee Tsui выявила мажорный ген, который получил название «трансмембранный регулятор проводимости муковисцидоза» (CFTR) . Началась эпоха ДНК-диагностики муковисцидоза с поиском мутаций, вовлечённых в патогенез заболевания.
В 1990 г. новым прорывом в лечении муковисцидоза стал генно-инженерный муколитик дорназа альфа. К концу года применения дорназы альфа у больных происходит увеличение объёма форсированного выдоха за 1-ю секунду на 7,3%, снижается инфицирование синегнойной палочкой дыхательных путей. Установлено, что как краткосрочное (от 1 нед до 2 мес), так и долгосрочное (от 1 до 4 лет) лечение дорназой альфа снижало частоту обострений бронхолёгочного процесса, значительно замедляло регресс объёма форсированного выдоха за 1-ю секунду, улучшало нутритивный статус, а также оказывало выраженное противовоспалительное действие .
В 1993 г. для терапии муковисцидоза начали применять инновационный препарат панкреатин (мини-микросферы в кишечнорастворимой оболочке), он улучшил нутритивный статус больных муковисцидозом . Большой вклад в изучение муковисцидоза внесли отечественные учёные.
У истоков исследования проблемы муковисцидоза в бывшем СССР стояли профессора С.В. Рачинский, В.К. Таточенко, Н.И. Капранов. Российские учёные К.К. Примбетов, М.Я. Ниязова, А.Б. Абилов, М.Г. Георгобиани, И.Е. Турина, Л.А. Петросян, Н.Ю. Каширская, О.И. Симонова, Т.Е. Гембицкая, Л.А. Желенина, А.Г. Черменский, Л. Ковалёва, В.С. Баранов, Т.Э. Иващенко, А.Г. Чучалина, Л. Кронина, Е.Л. Амелина, С.А. Красовский, В.А. Самойленко, М.В. Самсонова, А.Л. Черняев, А.В. Черняк, С.Н. Авдеев и другие проводили исследования патофизиологических и патоморфологических особенностей, микробиологического статуса у пациентов, иммунологических, микроциркуляторных, сердечно-сосудистых нарушений, поражения желудочно-кишечного тракта и гепатобилиарной системы, клинико-функциональной эффективности кинезитерапии при муковисцидозе. Они уделяли внимание совершенствованию методов лечения муковисцидоза и медико-генетического консультирования семей. Генетику муковисцидоза в нашей стране изучают учёные С.И. Куцев, Е.К. Гинтер, Е.И. Кондратьева, Н.В. Петрова, В.С. Баранов, Т.Э. Иващенко, С.А. Красовский, О.И. Голубцова, С.Л. Кожевникова, Г.В. Павлов и др. С 1990 г. в России открывается сеть центров по оказанию специализированной помощи пациентам с муковисцидозом. В настоящий момент в Российской Федерации функционирует сеть из 57 региональных центров диагностики и лечения детей и 10 центров для взрослых, больных муковисцидозом, возглавляемых научно-консультативным отделом муковисцидоза Медико-генетического научного центра Российской академии медицинских наук . Значительное улучшение ранней диагностики заболевания достигнуто в 2006 г. после внедрения программы обязательного неонатального скрининга на муковисцидоз .
Комплексный мультидисциплинарный подход к ранней диагностике и своевременной терапии заболевания способствовал увеличению продолжительности жизни больных . Были проведены глубокие исследовательские поиски, и достигнут прогресс в понимании последствий мутаций в гене для структуры и функции белка CFTR. Созданы методы лечения, специфичные для мутаций, но в настоящее время они доступны только для определённых мутаций . Продолжаются разработки ряда других соединений с иными механизмами действия. Можно предвидеть, что новые комбинации соединений улучшат коррекцию функции белка CFTR. Развитие новых стратегий, таких как создание препаратов для преждевременного считывания стоп-кодонов, антисмысловых олигонуклеотидов, которые будут исправлять основной дефект на уровне матричной рибонуклеиновой кислоты, редактирование гена для восстановления дефектного гена, генной терапии, позволит влиять на патогенез заболевания, что повысит эффективность лечения для всех пациентов с муковисцидозом .
Глава 2.Жизнь с муковисцидозом.
2.1 Продолжительность жизни в современном мире с муковисцидозом.
Однако если раньше средняя продолжительность жизни таких больных не превышала 5 лет, то сейчас заболевание диагностируется намного раньше, методы лечения стали эффективнее, что привело к увеличению средней продолжительности жизни больных муковисцидозом в развитых странах, составляя до 40 лет в США, Канаде и Великобритании, до 16 лет в целом по России (в Москве и Петербурге - свыше 23 лет).
Основываясь на статистике 2017 года, медиана прогнозируемого возраста выживаемости составляет:
|
Год рождения |
Средняя прогнозируемая продолжительность жизни |
|
1993-1997 |
31 |
|
2003-2007 |
37 |
|
2013-2017 |
44 |
Статистические данные в таблице отражают текущие показатели ожидаемой продолжительности жизни в развитых странах, таких как США и Великобритания. По данным организации Cystic Fibrosis Worldwide, в развивающихся странах, таких как Сальвадор и Индия, ожидаемая продолжительность жизни людей с муковисцидозом составляет менее 15 лет. Данные также показывают, что половина всех детей, рожденных с муковисцидозом в 2017 году, доживет до 46 лет и старше.Другие статистические данные свидетельствуют о том, что более 50% детей с муковисцидозом, рожденных в 2018 году, и 50% людей в возрасте 30 лет и старше в 2018 году, вероятно, достигнут по крайней мере своего пятидесятилетия.
Факторы, влияющие на продолжительность жизни.
На поздних стадиях муковисцидоза осложнения часто вызывают серьезные проблемы у людей. Эти осложнения обычно поражают легкие, но они также могут влиять на: эндокринную (гормональную) систему; кишечник; печень;
Возраст.
Когда люди становятся старше, возрастает риск осложнений, некоторые из которых могут иметь летальный исход. Однако другие факторы могут оказывать большее влияние на продолжительность жизни, поэтому некоторые люди с муковисцидозом доживают до возраста старше 70 лет.
Пол.
Женщины с муковисцидозом имеют худшие перспективы, чем мужчины с этим заболеванием. Некоторые исследования показывают, что это связано с повышенным риском смерти женщин с диабетом, связанным с муковисцидозом.
Состояние здоровья.
Ожидаемая продолжительность жизни людей с муковисцидозом в значительной степени зависит от осложнений, которые у них развиваются. Условия, связанные с более низкой выживаемостью, включают: некоторые инфекции, включая золотистый стафилококк; диабет у женщин; женский пол как таковой; недоедание; низкий индекс массы тела, или ИМТ; недостаточность поджелудочной железы; сниженная легочная функция; обострения легочных проявлений заболевания.
Однако другие факторы могут оказывать большее влияние на продолжительность жизни, поэтому некоторые люди с муковисцидозом доживают до возраста старше 70 лет.
2.2. Качество жизни в современном мире с муковисцидозом.
При обсуждении продолжительности жизни также важно учитывать качество жизни человека. То, как человек оценивает качество своей жизни, зависит от ряда факторов, в том числе от его возраста и общего состояния здоровья.
Хотелось бы остановиться на одном примере больного. Главная героиня романа «Голубое бистро» Элина Хилдербранда является шеф-поваром, но она больна муковисцидозом. Но несмотря на это она не сдается и показывает высокий профессиализм в своей работе.
У многих людей с муковисцидозом постепенно развиваются осложнения. Некоторые из них могут способствовать снижению качества жизни и приводить к преждевременной смерти. Потенциальные осложнения: непроходимость желчевыводящих путей или кишечные обструкции; бронхоэктазия, состояние, которое вызывает повреждение дыхательных путей; хронические инфекции, в том числе бронхит и пневмония; диабет; бесплодие, особенно у мужчин; дефицит питательных веществ; остеопороз, заболевание костей; пневмоторакс, который подразумевает скопление воздуха или газов в плевральной полости; нарушение дыхания.
Несмотря на возможность этих осложнений, некоторые исследования показывают, что восприятие качества жизни улучшается с возрастом у пациентов с муковисцидозом. Исследование основывалось на данных, собранных со слов более чем 300 взрослых пациентов.
Более конкретно, результаты показывают, что люди с муковисцидозом с возрастом воспринимают свое бремя лечения по-разному, и их «эмоциональное функционирование» возрастает. Хотя есть разница от человека к человеку. Например, люди с лучшей функцией легких постоянно оценивают качество своей жизни как более высокое по сравнению с оценками людей с более низкой функцией легких.
Поздняя стадия муковисцидоза.
На поздних стадиях муковисцидоза осложнения часто вызывают серьезные проблемы у людей. Обычно они поражают легкие, но также могут влиять на: эндокринную (гормональную) систему; кишечник; печень; поджелудочную железу.
Основными причинами смерти среди людей с муковисцидозом являются дыхательная недостаточность и хроническое прогрессирующее заболевание легких. Другие состояния, такие как острый панкреатит, могут привести к смертельным заболеваниям сердца, легких или почек.
Генная вариация.
На сегодняшний день исследователи обнаружили более 1700 мутаций в гене CFTR, которые могут вызывать муковисцидоз. Некоторые мутации вызывают более серьезные симптомы, чем другие, а некоторые могут быть связаны с более ранней смертью. Например, мутацию delta F508 ученые связывают с более короткой продолжительностью жизни. Это самая распространенная мутация, составляющая около 70% от общего числа мутаций.
Глава 3. Диагностика и лечение муковисцидозом
3.1. Перспективы ранней диагностике .
В последние десятилетия активно совершенствуются алгоритмы диагностики муковисцидоза. Понимание молекулярного механизма развития этого заболевания при различных вариантах мутаций в гене CFTR позволяет сегодня достичь высоких результатов в реализации мероприятий, способствующих восстановлению функции дефектного белка CFTR . Для дальнейшего совершенствования оказания медико-генетической помощи пациентам необходимо провести комплексные исследования и выявить все закономерности его развития, чтобы эффективно развивать патогенетическую терапию, это шанс для больных на выздоровление.
Результаты клинических исследований показали, что наибольший эффект от лечения достигается только у детей, в лёгких которых ещё не успели развиться необратимые патологические изменения. Таким образом, стало ясно, что ранняя диагностика и терапия предотвращают развитие тяжёлых проявлений заболевания . С целью раннего выявления муковисцидоза реализуется программа неонатального скрининга.
В 1979 г. команда исследователей из Новой Зеландии под руководством J. Crossley продемонстрировала повышение в плазме крови новорождённых с муковисцидозом содержания иммунореактивного трипсина . Данное открытие легло в основу современного протокола неонатального скрининга заболевания. Ранняя диагностика даёт возможность своевременно начать адекватную терапию, что ведёт к значительному улучшению качества и продолжительности жизни больных. Кроме того, проведение неонатального скрининга и идентификация CFTR-генотипа новорождённых с муковисцидозом предполагает более раннее генетическое консультирование пациентов, что может повлиять на репродуктивное поведение супругов и их родственников .
Протокол неонатального скрининга на муковисцидоз в России включает четыре этапа:
1) определение иммунореактивного трипсина в сухом пятне крови;
2) ретест — повторное определение иммунореактивного трипсина в сухом пятне крови;
3) потовый тест;
4) ДНК-диагностика.
Причём только первые три являются обязательными. ДНК-диагностика доступна не для всех пациентов по различным причинам; в первую очередь, это отсутствие государственного финансирования такого направления исследований.
По данным Европейского консенсуса, повышение показателя иммунореактивного трипсина в сухом пятне крови в неонатальном периоде встречается при перинатальном стрессе, гипербилирубинемии новорождённых, трисомиях 13-й и 18-й хромосом, у детей с врождёнными инфекциями, почечной недостаточностью и атрезией тонкой кишки, а также в случае нефрогенного несахарного диабета .
Популяционное распределение концентраций иммунореактивного трипсина в крови в период новорождённости несколько выше у детей североафриканского происхождения и афроамериканцев , чем у детей из Северной Европы, поэтому всем пациентам необходимо дополнительное обследование. В связи с этим биохимический скрининг в неонатальном периоде не является окончательным методом диагностики. Тем не менее, неонатальный скрининг на муковисцидоз оправдан, так как продолжительность жизни больных, выявленных с помощью скрининга, выше, чем у пациентов, у которых заболевание было установлено в более старшем возрасте .
Благодаря развитию технологий ДНК-диагностики достигнут значительный прогресс в реализации программ скрининга новорождённых на муковисцидоз, поэтому ДНК-диагностика становится частью всё большего количества стратегий диагностики этого заболевания в регионах Российской Федерации. Наиболее эффективный алгоритм ДНК-диагностики муковисцидоза на сегодняшний день следующий:
– первый этап — поиск вариантов наиболее частых мутаций в популяции, к которой принадлежит обследуемый;
– второй этап — расширенный поиск более редких вариантов с использованием секвенирования по Сенгеру или высокопроизводительного секвенирования генома нового поколения (MPS/NGS).
Анализ включает исследование всей кодирующей последовательности гена CFTR (27 экзонов), областей экзон-интронных соединений, 5- и 3-некодирующих областей (до 200–300 нуклеотидов), а также (желательно) глубоких интронных областей, где расположены варианты с доказанной патогенностью .
Применение данного метода необходимо при назначении CFTR-модуляторов с целью исключения комплексных аллелей, влияющих на эффективность терапии, например диагностика в генотипе варианта L467F, при котором лекарственный препарат ивакафтор + лумакафтор неэффективен Третий этап — В этом тесте локальное потоотделение стимулируется пилокарпином, измеряется количество пота и определяется концентрация хлоридов. Хотя концентрация хлоридов пота незначительно увеличивается с возрастом, исследование пота проводится в любом возрасте:
Нормальный уровень: ≤ 30 мЭкв/л (≤ 30 ммоль/л) (муковисцидоз маловероятен).
Средний: от 30 до 59 мЭкв/л (от 30 до 59 ммоль/л) (муковисцидоз возможен)
Отклонение от нормы: ≥ 60 мЭкв/л (≥ 60 ммоль/л) (этот результат соответствует наличию муковисцидоза)
Полученные результаты объективны уже после 48 часов жизни, но получить достаточный объем пробы пота (> 75 мг на фильтровальной бумаге или > 15 мкл в микроколонках) может быть трудно до 2-недельного возраста. Ложноотрицательные результаты редки, но могут возникать при наличии отеков и гипопротеинемии или недостаточного количества пота в пробе. Ложноположительные результаты, как правило, связаны с технической ошибкой. Кратковременное повышение концентрации хлоридов в поте может быть результатом психосоциальной депривации (например, жестоком обращении с детьми, пренебрежении) и может возникнуть у пациентов с нервной анорексией. Положительный результат потовой пробы должен быть подтвержден 2-й потовой пробой или идентификацией двух вызывающих муковисцидоз вариантов.
Промежуточные результаты исследования пота.
Небольшая часть пациентов имеет умеренный или частичный фенотип муковисцидоза, а значения хлоридов пота находятся в промежуточном или даже нормальном диапазоне. Кроме того, есть пациенты, которые имеют симптомы со стороны одного органа или системы, например, хронический или рекуррентный панкреатит, изолированные брохоэктазы или врожденное двустороннее отсутствие семявыносящих протоков, наряду с данными, указывающими на аномальную функцию CFTR. Их симптомы не соответствуют критериям для постановки диагноза муковисцидоза и классифицируются как симптомы расстройства, связанного с трансмембранным регулятором муковисцидоза.
У некоторых из этих пациентов диагноз муковисцидоза может быть подтвержден путем идентификации двух вариантов, вызывающих муковисцидоз, по 1 в каждой из хромосом. Если 2 муковисцидоз-вызывающие варианты не идентифицированы, могут быть полезны вспомогательные оценки, такие как исследование функции поджелудочной железы и ее визуализация, рентгенография и/или КТ органов грудной полости высокого разрешения, КТ придаточных пазух носа, определение легочных функций, исследование мочеполовой системы у мужчин, бронхоальвеолярный лаваж с оценкой микробной флоры.
3.2. Перспективы лечения
Симптомы муковисцидоза
Тяжесть заболевания во многом зависит от возраста, в котором обнаружились первые проявления. Меньше всего шансов имеют новорожденные и дети первого года жизни, даже несмотря на проводимое лечение. Для всех возрастов характерны легочные и желудочно-кишечные проявления: одышка, шумное со свистом дыхание, плохой набор веса, частые поносы.
Муковисцидоз у новорожденных проявляется мекониевой (меконий – первородный кал) непроходимостью кишечника, ребенок не выделяет кал. В первые сутки развивается обструктивная (вследствие закупорки общего желчного протока) желтуха. Бывает частая рвота желчью, на животе появляется рисунок сосудов.
Младенец страдает от малокровия или анемии. Выпячивается большой родничок, часто бывает асимметрия лица из-за паралича лицевого нерва. Младенец очень плохо набирает вес, значительно отстает от сверстников в физическом развитии. Если опустить ладошку в воду, то пальчики быстро сморщиваются – вода растворяет соли на коже. Такие дети плохо переносят смеси для искусственного вскармливания.
Муковисцидоз у детей постарше проявляется синдромом обструкции (сужения просвета) бронхиального дерева. Беспокоят удушье на вдохе, удлиненный выдох. У детей увеличиваются печень и селезенка, воспаляются придаточные пазухи носа, они не переносят жару. Нарушается углеводный обмен, формируется цирроз печени, дети пьют много воды и выделяют много мочи. Характерен симптом «барабанных палочек» – утолщение концевых фаланг стоп и кистей. Становится заметным отставание в физическом и нервно-психическом развитии.
Муковисцидоз у взрослых в полной мере проявляется кистозным фиброзом. Формируется бочкообразная форма грудной клетки, отсутствуют волосы в паху и под мышками, у мужчин видны недоразвитые половые органы, нет живых сперматозоидов. У женщин недостаточно сформированы молочные железы, отсутствует менструальный цикл. Беспокоит частое повышение температуры, вероятно развитие сахарного диабета, артритов, остеопороза (снижение минеральной плотности костной ткани).
Лечение
Применяется симптоматическая терапия, поскольку вылечить это заболевание невозможно. Лечение – пожизненное, направлено на компенсацию функций пострадавших органов.
Питание должно содержать много животного белка – мясо, рыбу, яйца, молочные продукты (если нет лактазной недостаточности). Больному требуется много жидкости, которую нужно подсаливать.
Для улучшения функции легких нужна лечебная гимнастика, используются положения тела, при котором грудная клетка растягивается. Полезно громко кричать, петь, постукивать рукой по грудной клетке. Используют особое устройство – виброжилет, имитирующий движения грудной клетки при кашле.
Лекарственные препараты при муковисцидозе используют разные: облегчающие отхождение мокроты или бронхолитики; антибиотики; ферменты для улучшения пищеварения; общеукрепляющие средства.
Сколько живут при муковисцидозе, во многом зависит от качества препаратов. В нашей стране применяются только дженерики – аналоги (копии) брендовых лекарств. Они содержат то же основное действующее вещество, что и оригинальный препарат, но отличаются вспомогательными компонентами. Производить дженерики приходится не от хорошей жизни: многие фармкомпании отказываются поставлять в Россию оригинальные препараты либо цена импортного лекарства оказывается неподъемной.
Все особенности диагностики и лечения детально изложены в Федеральных клинических рекомендациях по муковисцидозу – нормативном документе для врачей. В тяжелых случаях применяется хирургическое лечение: трансплантация легких, операции на кишечнике.
Заболевание, как и все хронические, протекает волнообразно, с периодами обострения и затишья (ремиссии).
Желательно, чтобы пациенты обращались для профилактического осмотра регулярно, вне зависимости от остроты процесса. Клинические рекомендации постоянно обновляются, появляются новые препараты и результаты научных работ.
У врача, находящегося в тесном контакте с пациентом, всегда есть возможность облегчить его состояние.
Прогноз при регулярном лечении – относительно благоприятный. Профилактика заключается в медико-генетическом обследовании родителей, особенно при наследственных болезнях у кровных родственников. Комплексную интенсивную терапию должен проводить опытный врач, работающий в многопрофильной команде, которая включает других врачей, медсестер, диетологов, физиотерапевтов, пульмонологов, специалистов в области психического здоровья, фармацевтов и социальных работников. Цель терапии состоит в поддержании нормального физического статуса, профилактике или своевременном активном лечении легочных и других осложнений, поощрении физической активности, а также предоставлении психологической поддержки. Схема лечения является комплексной и может занимать до 2 часов каждый день. При соответствующей поддержке, большинство пациентов могут проводить коррекцию соответственно возрасту дома и в школе. Несмотря на многочисленные проблемы, образовательные, профессиональные и семейные, успехи пациентов впечатляют.
Перспективы лечения
Уменьшение числа обострений и улучшение функции лёгких, как и увеличение вследствие этого продолжительности жизни больных муковисцидозом с внедрением новых технологий в здравоохранении (таргетной терапии), имеет целью снижение социальной нагрузки заболевания, что потребует расширения доступности эффективных (таргетных) средств в будущем.
Сразу после открытия факта, что муковисцидоз вызван мутациями в гене CFTR, у исследователей возникло желание синтезировать вещества, которые могли бы хоть отчасти скомпенсировать эффект данных мутаций.
Довольно быстро стало понятно, что эти вещества будут грубо делиться по своей функции на два типа — корректоры, которые будут повышать количество дефектного белка (например, с мутацией F508del) на поверхности клетки, и потенциаторы, которые будут усиливать активность белка, уже находящегося на поверхности.
Наиболее простой мишенью при этом выглядят мутации класса III: при них белок правильно свернут, находится на мембране, но преимущественно в закрытом состоянии.
Поэтому с 2000-х годов начали поиск таких соединений, которые бы повышали вероятность его пребывания в открытом состоянии
Немаловажно, что препарат оказался очень безопасным — частота побочных эффектов не превосходила плацебо. К сожалению, в России он так до сих пор и не зарегистрирован.
Хотя пока недостаточно данных для того, чтобы говорить о снижении смертности от муковисцидоза под воздействием ивакафтора, но проведенное моделирование показывает, что его влияние на FEV1 способно вылиться в увеличение продолжительности жизни в среднем на 15 лет , а также снизить потребность в трансплантации легких
Такая эффективность дала основание компании Vertex установить на свой препарат очень высокую цену: годовой курс стоит в США $310 000. Недавние исследования, проведенные в США и Великобритании, показали, что такая цена неоправданно высока .
Механизм действия «Калидеко»: пока гипотеза!
Заключение
Муковсцидоз - хроническое неизлечимое заболевание, поэтому больные нуждаются в активном диспансерном наблюдении и непрерывном лечении. Лечение больных МВ предпочтительно проводить в специализированных центрах. Терапия МВ не ограничивается рамками медикаментозного лечения: больным МВ требуется комплексная медицинская помощь при активном участии не только врачей, а также медицинских сестер, диетологов, кинезитерапевтов, психологов и социальных работников. У одних пациентов, несмотря на своевременную диагностику и адекватную терапию, поражение бронхолегочной системы быстро прогрессирует, у других динамика изменений более благоприятна. Многие пациенты доживают до взрослого и даже зрелого возраста.
Список литературы
1.Амелина Е.Л., Ефремова А.С., Мельяновская Ю.Л., Булатенко Н.В., Бухарова Т.Б., Каширская Н.Ю., Красовский С.А., Гольдштейн Д.В. Использование функциональных тестов для оценки остаточной активности канала CFTR и индивидуального подбора эффективных CFTR-модуляторов для лечения пациентов с муковисцидозом с «мягким» и «тяжёлым» генетическими вариантами. Пульмонология. 2021;31 с.
2.Амелина Е.Л., Черняк А.В., Черняев А.Л. Муковисцидоз: определение продолжительности жизни. Пульмонология. 2001;(3):61-64.
3.Воронкова А.Ю., Амелина Е.Л., Каширская Н.Ю., Кондратьева Е.И. Регистр больных муковисцидозом в Российской Федерации. 2019 год. М.: Медпрактика-М; 2021. 68 с.
4.Ефремова А.С., Мельяновская Ю.Л., Булатенко Н.В., Одинаева Н.Д., Орлов А.В., Пашкевич А.А., Адян Т.А., Кондратьева Е.И. Описание редких аллелей гена CFTR при муковисцидозе с помощью функциональных тестов и форсколинового теста на ректальных органоидах. Пульмонология. 2021;31(2):178–188.
5. Капранов Н.И. Муковисцидоз. Современное состояние проблемы. Пульмонология. 2006(приложение):5–11.
6. Капранов Н.И., Каширская Н.Ю. Актуальные проблемы муковисцидоза на современном этапе в России. Пульмонология 1997; 4: 7-17.
7. Кондратьева Е.И., Каширская Н.Ю., Капранов Н.И. Национальный консенсус «Муковисцидоз: определение, диагностические критерии, терапия». М.: Боргес; 2016. 205 с
8.Толстова В.Д., Каширская Н.Ю., Капранов Н.И. Массовый скрининг новорождённых на муковисцидоз в России. Фарматека. 2008;(1):38–44.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.