
Практическое занятие №6 Уравнение Менделеева-Клайперона. Изопроцессы.
Цель: научиться применять уравнение Менделеева-Клайперона и его частные случаи при решении экспериментальных, расчетных и графических задач.
Теоретические сведения
Уравнение состояния идеального газа:
![]()
Для одного моля любого газа это соотношение принимает вид:
pV=RT
Для смеси невзаимодействующих газов уравнение состояния принимает вид:
 pV = (ν1 + ν2 + ν3 + ...)RT,
pV = (ν1 + ν2 + ν3 + ...)RT,
где ν1, ν2, ν3 и т. д. – количество вещества каждого из газов в смеси.
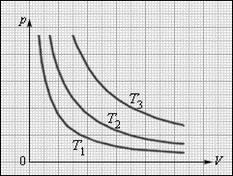
Изотермическим процессом называют процесс, протекающий при постоянной температуре T. Из уравнения состояния идеального газа следует, что при постоянной температуре T и неизменном количестве вещества ν в сосуде произведение давления p газа на его объем V должно оставаться постоянным:
pV = const.
![]()
Семейство изотерм на плоскости (p, V).T3 > T2 > T1
Изохорный процесс – это процесс нагревания или
охлаждения газа при постоянном объеме V и при условии,
что количество вещества ν в сосуде остается неизменным.
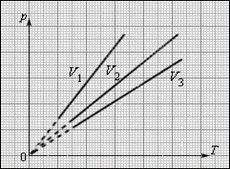
Как следует из уравнения состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p ~ T или
![]()
![]() Семейство
изохор на плоскости (p, T).V3 > V2 > V1
Семейство
изохор на плоскости (p, T).V3 > V2 > V1
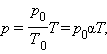
Уравнение изохорного процесса может быть записано в виде:
где p0 – давление газа при T = T0 = 273,15 К (т. е. при температуре 0 °С). Коэффициент α, равный (1/273,15) К–1, называют температурным коэффициентом давления.
 Изобарным
процессом называют процесс,
протекающий при неизменном давлении p.
Изобарным
процессом называют процесс,
протекающий при неизменном давлении p.
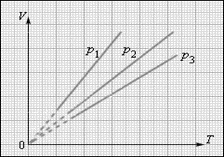
Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид:
![]()
где V0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273,15) К–1. Его называют температурным коэффициентом объемного расширения газов.
![]()
Семейство изобар на плоскости (V, T).p3 > p2 > p1
Контрольные вопросы
1. Охарактеризуйте уравнение Менделеева-Клайперона.
2. Дайте характеристику изотермическому, изобарному, изохорному процессам.
3. Изобразите эти процессы графически.
Задание 1. Оценить массу воздуха в учебном кабинете.
Цель: Ознакомиться с экспериментальным методом определения массы воздуха.
Оборудование: сантиметровая лента, барометр, термометр, таблица Менделеева.
Ход работы:
Массу воздуха
можно рассчитать по формуле ![]() , где
, где ![]() - плотность воздуха,
- плотность воздуха, ![]() - объем занимаемый воздухом.
- объем занимаемый воздухом.
Учитывая, что кабинет имеет форму прямоугольного параллелепипеда, ее объем можно рассчитать по формуле:
![]()
Определить плотность воздуха можно из уравнения Менделеева – Клапейрона:
|
|
Þ |
|
Þ |
|
Þ
|
|
где
![]() – давление воздуха,
– давление воздуха, ![]() - температура воздуха
- температура воздуха
На основании указанных формул массу воздуха в кабинете можно рассчитать по формуле
![]()
1. Измерьте длину, ширину и высоту учебного кабинета.
2. С помощью термометра измерьте температуру воздуха t°.
3. Переведите значение температуры в СИ T = t°+273.
4.
С
помощью барометра-анероида измерьте давление воздуха в учебном кабинете ![]() .
.
5. Рассчитайте примерную массу воздуха по формуле:
![]()
где M = 29×10-3кг/моль, R = 8,31 Дж/моль×К
6. Рассчитайте относительную погрешность измерения массы по формуле:
![]()
7. Рассчитайте абсолютную погрешность измерения массы по формуле:
![]()
8. Результат измерения массы представьте в виде:
![]()
9. Результаты измерений и вычислений занесите в таблицу:
|
p, Па |
T, К |
a, м |
b, м |
c, м |
Dp, Па |
DT, К |
Da, м |
m, кг |
% |
|
|
|
|
|
|
|
|
|
|
|
Задание 2. Решите задачи.
1. Вычислите массу воздуха в комнате объёмом 120 м3 при нормальных условиях. Молярная масса воздуха равна 0,029 кг/моль.
Сколько молекул воздуха выйдет из комнаты при повышении температуры в ней до 20°С? Давление и объём считать постоянными.
2. Найдите плотность кислорода при температуре 300К и давлении 1,6×105Па.
Вычислите массу кислорода при данных условиях, если он находится в баллоне объёмом 0,2 м3. Вторую часть задачи решите двумя способами.
3. Шар объёмом 2л содержит кислород при атмосферном давлении и температуре 27°С. Вычислите массу и плотность кислорода.
Какой объем займет кислород, если шар опустить в воду на глубину 10 м? Температуру воды на этой глубине примите равной 4° С. Оболочку шара считайте идеально эластичной.
4. Сколько гелия потребуется для наполнения воздушного шара емкостью 500 м3 при нормальном атмосферном давлении и температуре 300 К?
Вычислите массу груза и снаряжения, которую может поднять этот шар при данных условиях. Молярную массу воздуха примите равной 0,029 кг/моль.
Задание 3. Работа с графиками.
1. По данному графику определить:
a) протекающий изопроцесс и указать постоянный параметр;
b) известные начальные и конечные параметры.
2. Определить неизвестный параметр, используя газовый закон для данного процесса.
3. Определите молярную массу, данного газа.
4. Используя уравнение Клапейрона - Менделеева, определите третий параметр.
2. Построить график данного процесса в двух других координатах.
Графики для выполнения задания на «5»

Построить графики данного процесса в координатах РТ; VТ
Графики для выполнения задания на «4».
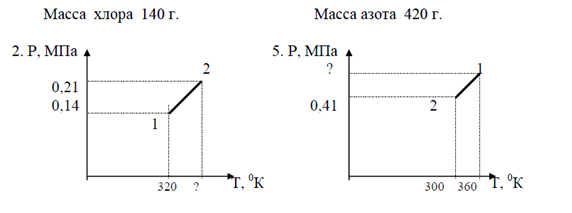
Построить графики данного процесса в координатах РV; PТ.
Графики для выполнения задания на «3».
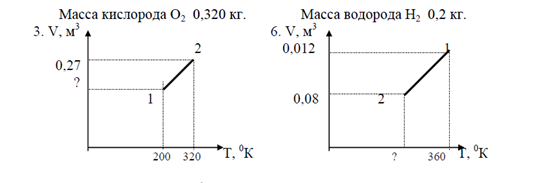
Построить графики данного процесса в координатах РV; PТ.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.