

Примерное время выполнения задания – 2 минуты
Уровень сложности задания – базовый
Максимальный балл за выполнение задания - 1
Задание № 14 направлено на проверку знаний реакций ионного обмена и условий их осуществления, а также умения составлять молекулярное уравнение реакции обмена, записывать для него полное и сокращенное ионное уравнение.
Задание содержит перечень из шести веществ. Необходимо выбрать два вещества, взаимодействию которых соответствует сокращенное ионное уравнение реакции, приведенное в условии задания. В ответе нужно записать номера выбранных вариантов.

Реакции между ионами называются ионными реакциями, а уравнения этих реакций – ионными уравнениями.
Основным из условий протекания ионных реакций является образование малодиссоциирующего вещества (слабого электролита), осадка или газа. Эти вещества записываются в молекулярном виде. Если выпадает осадок, то рядом с его формулой ставят стрелку, направленную вниз (↓), если образуется газ, то рядом с его формулой ставят стрелку, направленную вверх (↑).
Если к раствору хлорида натрия добавить раствор нитрата серебра, то образуется белый творожистый осадок хлорида серебра.
NaCl + AgNO3 = NaNO3 + AgCl↓
После записи молекулярного уравнения следует записать ионное уравнения, записав сильные электролиты в виде ионов, а образовавшийся осадок нужно записать в молекулярном виде. Две соли: хлорид натрия и нитрат серебра являются растворимыми и полностью распадаются на ионы, как и образующаяся соль – нитрат натрия, а хлорид серебра – осадок, поэтому его нужно записать в виде молекулы. Если вы забыли, как определяются заряды ионов, то нужно обратиться к таблице растворимости, в ней всегда указаны заряды ионов, а также по ней можно определить растворимо или нет вещество в воде.
Na+ + Cl- + Ag+ + NO3- = Na+ + NO3- + AgCl↓
Мы записали таким образом полное ионное уравнение. Если исключить из обеих частей равенства одинаковые ионы, т.е. ионы не участвующие в реакции – ионы натрия и нитрат-ионы в левой и правой части, то получится сокращенное ионное уравнение.
Ag+ + Cl- = AgCl↓
Это уравнение показывает, что сущность этой реакции сводится к взаимодействию ионов серебра и ионов хлора, в результате которого образуется осадок хлорида серебра.

Если мы к раствору гидроксида калия добавим несколько капель фенолфталеина, то раствор гидроксида калия окрасится в малиновый цвет. А затем сюда же прильем раствор серной кислоты, раствор станет бесцветным, следовательно, прошла химическая реакция.
2KOH + H2SO4 = K2SO4 + 2H2O
Чтобы записать полное ионное уравнение, нужно помнить, что вода – малодиссоциирующее вещество, поэтому её записываем в молекулярном виде. 2K+ + 2OH- + 2H+ + SO42- = 2K+ + SO42- + 2H2O
Т.к. ионы калия и сульфат-ионы в левой и правой части остаются неизменными, то их можно не записывать в сокращенном ионном уравнении.
2OH- + 2H+ = 2H2O
Все коэффициенты в сокращенном ионном уравнении можно сократить на два. OH- + H+ = H2O
Таким образом, взаимодействие сильной кислоты и щёлочи сводится к тому, что взаимодействуют ионы водорода и гидроксид-ионы с образованием воды – малодиссоциирующего вещества.

Если к раствору хлорида железа (III) добавить раствор щелочи, например, гидроксид натрия, то у нас образуется осадок – гидроксид железа (III). FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
Записав полное ионное уравнение, мы видим, что ионы натрия и хлорид-ионы не участвуют в реакции, значит, их можно исключить, а в сокращенном ионном уравнении записать только ионы железа и гидроксид-ионы, которые участвуют в реакции с образованием осадка.
Fe3+ + 3Cl- + 3Na+ + 3OH- = Fe(OH)3↓ + 3Na+ + 3Cl-
Fe3+ + 3OH- = Fe(OH)3↓
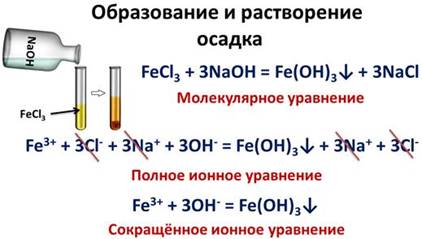
Поделим полученный осадок на три части, к одной части прильем раствор серной кислоты, ко второй – раствор соляной кислот, к третьей – раствор азотной кислоты. Осадок растворится в трёх случаях, т.е. прошла химическая реакция. Fe(OH)3 + 3H+ = Fe3+ + 3H2O
Если в раствор карбоната натрия добавить соляной кислоты, то происходит «вскипание» раствора, вследствие образования углекислого газа. В нашем случае образуется угольная кислота, которая распадается на углекислый газ и воду.
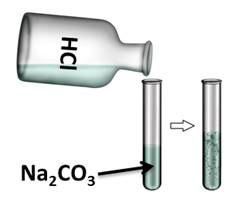
Na2CO3 + 2HCl = 2NaCl + CO2↑ + H2O
При записи полного ионного уравнения помните, что газ и вода записываются в молекулярном виде.
2Na+ + CO32- + 2H+ + 2Cl- = 2Na+ + 2Cl- + CO2↑ + H2O
Ионы натрия и хлорид-ионы не участвуют в реакции, поэтому в сокращенном ионном уравнении их можно не записывать.
CO32- + 2H+ = CO2↑ + H2O

Задание 1. Выберите два исходных вещества, при взаимодействии которых выпадает осадок?
1) хлорид алюминия
2) нитрат калия
3) фосфат натрия
4) бромид аммония
5) карбонат кальция
6) сульфат лития
Запишите номера выбранных ответов. Ответ: 13
Пояснение:
По таблице растворимости определяем растворимость указанных веществ в воде. Все вещества, кроме карбоната кальция (5), растворимы в воде. Следовательно, в растворе есть ионы алюминия, калия, натрия, аммония, лития, а также хлорид-, нитрат-, фосфат-, бромид-, сульфат – ионы. Из перечисленных ионов Al3+ и PO43- могут при взаимодействии друг с другом образовывать осадок. Поэтому для реакции возьмем хлорид алюминия (1) и фосфат натрия (3)
AlCl3 + Na3PO4 = Al PO4↓ + 3NaCl
Al3+ + 3Cl- + 3Na+ +PO43- = Al PO4↓ + 3Na+ + 3Cl-
Al3+ +PO43- = Al PO4↓
В ответе записываем цифры 1 и 3.
Задание 2. Выберите два исходных иона, при взаимодействии которых в растворе образуется газ.
1) Ba2+
2) H+
3) S2-
4) SO32-
5) PO43-
6) NO2-
Запишите номера выбранных ответов. Ответ: 23
Пояснение:
Из перечисленных ионов ионы водорода (2) и сульфид – ионы (3) могут при взаимодействии друг с другом образовывать газ – сероводород.
Составляем сокращенное ионное уравнение:
2H+ + S2- = H2S↑
В ответе записываем цифры 2 и 3.
Задания для подготовки
1. Выберите два исходных
вещества, взаимодействию которых соответствует сокращённое ионное уравнение
реакции ![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
2. Сокращённое ионное уравнение
![]() соответствует
взаимодействию веществ:
соответствует
взаимодействию веществ:
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите в поле ответа в порядке возрастания номера исходных веществ, взаимодействию которых соответствует приведённое сокращённое ионное уравнение реакции.
3. Сокращённое ионное уравнение
![]() соответствует взаимодействию веществ:
соответствует взаимодействию веществ:
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите в поле ответа в порядке возрастания номера исходных веществ, взаимодействию которых соответствует приведённое сокращённое ионное уравнение реакции.
4. Выберите два исходных
вещества, взаимодействию которых соответствует сокращённое ионное уравнение
реакции ![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
5. Выберите два исходных вещества, взаимодействию которых соответствует сокращённое ионное уравнение реакции
![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
6. Осадок не образуется при взаимодействии водных растворов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
7. Раствор хлорида меди (II) не реагирует с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
8. Осадок не образуется при взаимодействии водных растворов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
9. Раствор фосфата калия реагирует с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
10. Вода образуется в реакции ионного обмена при взаимодействии
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
11. Раствор нитрата бария реагирует с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
12. Сокращённое ионное уравнение
![]() соответствует взаимодействию
соответствует взаимодействию
1) хлорида аммония с гидроксидом цинка 2) нитрата аммония с водой
3) аммиака с водой 4) бромида аммония с гидроксидом меди (II)
5) нитрата аммония с гидроксидом натрия
6) сульфата аммония с гидроксидом калия
13. Хлорид бария не реагирует с раствором
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
14. Сокращённое ионное уравнение
![]() соответствует взаимодействию
соответствует взаимодействию
1) нитрата кальция и карбоната натрия
2) фосфата кальция и карбоната калия
3) нитрата кальция и карбоната бария
4) хлорида кальция и карбоната аммония
5) оксида кальция и оксида углерода (IV)
6) карбоната кальция и угольной кислоты
15. Для растворения гидроксида железа (II) можно использовать раствор
1) хлорида бария 2) серной кислоты 3) гидроксида натрия
4) соляной кислоты 5) нитрата натрия 6) гидроксида меди (II)
16. Сокращённое ионное
уравнение ![]() соответствует взаимодействию
соответствует взаимодействию
1) бромида железа (III) и гидроксида лития
2) нитрата железа (III) и гидроксида меди (II)
3) хлорида железа (III) и гидроксида бария
4) хлорида железа (II) и гидроксида калия
5) оксида железа (III) и гидроксида натрия
6) нитрата железа (II) и гидроксида натрия
17. Осадок образуется при взаимодействии водных растворов
1) нитрата аммония и гидроксида калия
2) фосфата аммония и гидроксидом лития
3) нитрата серебра и бромида кальция
4) азотной кислоты и карбоната натрия
5) соляной кислоты и гидроксида бария
6) хлорида аммония и гидроксида лития
18. Между какими веществами возможно взаимодействие?
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
19. Газ не выделяется в ходе реакций между
1) серной кислотой и карбонатом калия
2) серной кислотой и гидроксидом кальция
3) серной кислотой и гидроксидом бария
4) сульфатом аммония и гидроксидом натрия
5) сульфитом натрия и соляной кислотой
6) карбонатом натрия и соляной кислотой
20. В реакцию и с гидроксидом кальция, и с нитратом серебра вступает
1) карбонат магния 2) хлорид аммония 3) нитрат натрия
4) сульфат бария 5) фосфат натрия 6) гидроксид меди (II)
21. Краткое ионное уравнение
![]() отвечает взаимодействию веществ:
отвечает взаимодействию веществ:
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
22. Сульфат натрия реагирует с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
23. Сокращённому ионному
уравнению ![]()
соответствует левая часть схемы уравнения химической реакции
1) ![]() 2)
2) ![]()
3) ![]() 4)
4) ![]()
5) ![]() 6)
6) ![]()
24. Краткое ионное уравнение
![]() отвечает взаимодействию веществ
отвечает взаимодействию веществ
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
25. Практически полностью в водном растворе взаимодействуют вещества:
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
26. Практически полностью в водном растворе взаимодействуют вещества:
1) нитрат серебра и хлороводород 2) нитрат кальция и хлорид калия
3) хлороводород и нитрат натрия 4) серная кислота и хлорид бария
5) хлороводород и нитрат калия 6) фосфат калия и нитрит натрия
27. Нитрат аммония в водном растворе может прореагировать с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
28. Нитрат цинка в водном растворе реагирует с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
29. Хлорид меди (II) в водном растворе может прореагировать с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
30. Хлорид цинка в водном растворе реагирует с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
31. В водном растворе реагируют между собой
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
32. Соли, которые могут
реагировать и с хлоридом бария, и с гидроксидом калия, — 1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
33. В водном растворе реагируют между собой
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
34. Соли, которые могут реагировать и с соляной кислотой, и с нитратом кальция
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
35. В водном растворе реагируют с выделением газа
1) ![]() 2)
2) ![]() 3)
3) ![]()
4) ![]() 5)
5) ![]() 6)
6) ![]()
36. Соли, которые в водном растворе могут реагировать и с серной кислотой, и с нитратом серебра
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
37. В водном растворе реагируют с образованием осадка
1) ![]() 2)
2) ![]() 3)
3) ![]()
4) ![]() 5)
5) ![]() 6)
6) ![]()
38. Соль, которая в водном растворе может реагировать и с хлоридом бария, и с гидроксидом калия —
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
39. В реакцию с соляной кислотой вступают
1) нитрат серебра 2) нитрат бария 3) серебро 4) оксид кремния
5) карбонат натрия 6) нитрат лития
40. Газ выделяется при взаимодействии
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
41. Газ выделяется при взаимодействии соляной кислоты с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
42. Газ выделяется при взаимодействии разбавленной серной кислоты с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
43. Осадок образуется при взаимодействии хлорида аммония с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
44. Осадок образуется при взаимодействии сульфида натрия с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
45. В водном растворе одновременно могут находиться ионы
1) ![]() 2)
2) ![]()
3) ![]() 4)
4) ![]()
5) ![]() 6)
6) ![]()
46. И с ![]() и
с
и
с ![]() реагируют
растворы
реагируют
растворы
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
47. В водном растворе одновременно могут находиться ионы
1) ![]() 2)
2) ![]()
3) ![]() 4)
4) ![]()
5) ![]() 6)
6) ![]()
48. И с ![]() ,
и с
,
и с ![]() реагируют
растворы
реагируют
растворы
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
49. Вода образуется при действии азотной кислоты на
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
50. Газ выделяется при действии соляной кислоты на
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
51. В водном растворе ![]() будет
реагировать с
будет
реагировать с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
52. C раствором ![]() может
взаимодействовать каждая из двух солей:
может
взаимодействовать каждая из двух солей:
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
53. В водном растворе ![]() будет
реагировать с
будет
реагировать с
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
54. C соляной кислотой может взаимодействовать каждая из двух солей:
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
55. Газ выделяется при взаимодействии
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
56. Сульфит натрия в водном растворе может вступать в реакцию с каждым из веществ:
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
57. Бромид алюминия в водном растворе может вступать в реакцию с каждым из веществ:
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
58. Сокращённое ионное уравнение реакции
![]() соответствует взаимодействию веществ
соответствует взаимодействию веществ
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
59. Осадок не образуется при взаимодействии водных растворов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
60. Как раствор сульфата натрия, так и раствор карбоната натрия взаимодействует с
1) фосфатом алюминия 2) гидроксидом цинка 3) хлоридом бария
4) азотной кислотой 5) нитратом кальция 6) нитрата калия
61. Газ выделяется при взаимодействии
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
62. Газ не выделяется при взаимодействии
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
63. Между какими веществами возможно взаимодействие?
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
64. Сульфат алюминия вступает в реакцию с каждым из двух веществ:
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
65. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию
соответствует
взаимодействию
1) хлорида железа(II) и гидроксида калия
2) хлорида железа(III) и гидроксида бария
3) нитрата железа(III) и гидроксида меди(II)
4) оксида железа(III) и гидроксида натрия
5) сульфата железа(III) и гидроксида лития
6) сульфата железа(II) и гидроксида натрия
66. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию между
соответствует
взаимодействию между
1) нитратом железа(II) и гидроксидом калия
2) сульфатом железа(II) и гидроксидом бария
3) хлорид железа(II) и гидроксид натрия
4) оксидом железа(III) и водой
5) фосфатом железа(II) и водой
6) оксидом железа(II) и водой
67. Практически до конца протекает реакция ионного обмена между
1) гидроксидом натрия и нитратом бария
2) гидроксидом калия и сульфатом цинка
3) фосфатом калия и сульфатом натрия
4) фосфатом калия и сульфатом алюминия
5) нитратом калия и соляной кислотой
6) хлорида меди(II) и нитратом натрия
68. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию между
соответствует
взаимодействию между
1) азотной кислотой и гидроксидом натрия
2) нитратом серебра и гидроксидом калия
3) водой и оксидом натрия
4) гидроксидом бария и соляной кислотой
5) серной кислотой и хлоридом бария
6) кремниевой кислотой и гидроксидом натрия
69. Между какими веществами возможно взаимодействие?
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
70. Взаимодействие каких ионов в растворе приводит к образованию осадка?
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
71. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию
соответствует
взаимодействию
1) ![]() с
с ![]() 2)
2) ![]() с
с ![]() 3)
3) ![]() с
с ![]()
4) ![]() с
с ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
72. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию веществ
соответствует
взаимодействию веществ
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
73. В реакцию с хлороводородной кислотой вступает
1) хлорид калия 2) карбонат натрия 3) нитрат серебра
4) сульфат натрия 5) нитрат бария 6) бромид меди (II)
74. Между какими веществами возможно взаимодействие?
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
75. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию
соответствует
взаимодействию
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
76. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию веществ
соответствует
взаимодействию веществ
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
77. При нагревании выделение
газа происходит в результате взаимодействия ионов 1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
78. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию между
соответствует
взаимодействию между
1) гидроксидом бария и оксидом углерода (IV)
2) хлоридом бария и карбонатом калия
3) барием и угольной кислотой
4) нитратом бария и карбонатом натрия
5) оксидом бария и оксидом углерода (IV)
6) гидроксидом бария и угольной кислотой
79. Выпадением осадка сопровождается взаимодействие ионов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
80. C выделением осадка протекают химические реакции между
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
81. Выделением газа сопровождается взаимодействие ионов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
82. Краткому ионному
уравнению ![]() соответствует
левая часть схемы химической реакции
соответствует
левая часть схемы химической реакции
1) ![]() 2)
2) ![]()
3) ![]() 4)
4) ![]()
5) ![]() 6)
6) ![]()
83. Реакция ионного обмена идёт до конца при взаимодействии растворов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
84. Выпадением осадка сопровождается взаимодействие ионов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
85. Краткому ионному
уравнению ![]() соответствует
левая часть схемы химической реакции
соответствует
левая часть схемы химической реакции
1) ![]() 2)
2) ![]() 3)
3) ![]()
4) ![]() 5)
5) ![]() 6)
6) ![]()
86. Хлорид цинка реагирует с каждым из двух веществ:
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
87. Одновременно в водном растворе могут находиться ионы
1) ![]() 2)
2) ![]()
3) ![]() 4)
4) ![]()
5) ![]() 6)
6) ![]()
88. Необратимо происходит взаимодействие между ионами
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
89. Какие вещества реагируют между собой с образованием осадка?
1) оксид меди и серная кислота 2) гидроксид бария и серная кислота
3) гидроксид натрия и оксид серы (IV)
4) гидроксид натрия и хлорид железа (III)
5) железо и соляная кислота 6) серебро и разбавленная серная кислота
90. В реакцию с каждым из
растворов ![]() и
и ![]() вступают
вступают
1) соляная кислота 2) гидроксид натрия 3) хлорид бария
4) нитрат алюминия 5) бромид кальция 6) гидроксид меди (II)
91. Газ выделяется при взаимодействии
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]()
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
92. В водном растворе одновременно не могут находиться ионы
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
93. Выпадением осадка сопровождается взаимодействие ионов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
94. В водном растворе одновременно не могут находиться ионы
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
95. Выпадением осадка сопровождается взаимодействие ионов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
96. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию веществ
соответствует
взаимодействию веществ
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
97. Осадок образуется при взаимодействии ионов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
98. При взаимодействии каких ионов в растворе не образуется осадок?
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
99. Осадок образуется при взаимодействии водных растворов
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
100. Сокращённое ионное
уравнение ![]() соответствует
реакции между
соответствует
реакции между
1) оксидом алюминия и гидроксидом калия 2) алюминием и водой
3) сульфатом алюминия и гидроксидом меди (II)
4) фосфатом алюминия и водой
5) сульфатом алюминия и гидроксидом лития
6) хлоридом алюминия и гидроксидом натрия
101. В водном растворе одновременно могут находиться ионы
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
102. Сокращенному ионному
уравнению ![]() соответствует
взаимодействие веществ
соответствует
взаимодействие веществ
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
103. Сокращённое ионное
уравнение ![]() соответствует
реакции между
соответствует
реакции между
1) нитратом бария и сульфатом цинка
2) оксидом бария и серной кислотой
3) карбонатом бария и серной кислотой
4) гидроксидом бария и сульфатом цинка
5) хлоридом бария и сульфатом натрия
6) оксидом бария и сульфатом натрия
104. Сокращенному ионному
уравнению ![]() соответствует
взаимодействие веществ
соответствует
взаимодействие веществ
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
105. В реакцию с гидроксидом железа(III) вступает
1) нитрат натрия 2) сульфат бария 3) гидроксид алюминия
4) соляная кислота 5) кремниевая кислота 6) азотная кислота
106. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию
соответствует
взаимодействию
1) ![]() с
с ![]() 2)
2) ![]() с
с ![]() 3)
3) ![]() с
с ![]()
4) ![]() с
с ![]() 5)
5) ![]() с
с ![]() 6)
6) ![]() с
с ![]()
107. Газ выделяется при взаимодействии
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]()
3) ![]() и
и ![]() 4)
4) ![]() и
и ![]()
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
108. Между какими веществами возможно взаимодействие?
1) сульфатом калия и карбонатом кальция
2) сульфатом бария и хлоридом натрия
3) сульфатом железа(III) и фосфатом калия
4) сульфатом аммония и нитратом алюминия
5) карбонатом аммония и нитратом натрия
6) карбонатом кальция с соляной кислотой
109. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию сульфида железа и
соответствует
взаимодействию сульфида железа и
1) фосфорной кислоты 2) соляной кислоты 3) кремниевой кислоты
4) сернистой кислоты 5) угольной кислотой 6) бромоводорода
110. Сокращённое ионное
уравнение ![]() соответствует
взаимодействию веществ
соответствует
взаимодействию веществ
1) ![]() и
и ![]() 2)
2) ![]() и
и ![]() 3)
3) ![]() и
и ![]()
4) ![]() и
и ![]() 5)
5) ![]() и
и ![]() 6)
6) ![]() и
и ![]()
111. Выберите два исходных
вещества, взаимодействию которых соответствует сокращённое ионное уравнение
реакции ![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
112. Выберите два исходных вещества, взаимодействию которых соответствует сокращённое ионное уравнение реакции
![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
113. Выберите два исходных вещества, взаимодействию которых соответствует сокращённое ионное уравнение реакции
![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
114. Выберите два исходных вещества, взаимодействию которых соответствует сокращённое ионное уравнение реакции
![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
115. Выберите два исходных
вещества, взаимодействию которых соот-ветствует сокращённое ионное уравнение
реакции ![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
116. Выберите два исходных вещества, взаимодействию которых соответствует сокращённое ионное уравнение реакции
![]()
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]() 6)
6) ![]()
Запишите номера выбранных ответов.
Ответы:
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
34 |
15 |
34 |
34 |
16 |
23 |
26 |
14 |
16 |
12 |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
13 |
56 |
35 |
14 |
24 |
13 |
23 |
34 |
23 |
25 |
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
|
35 |
24 |
14 |
23 |
12 |
14 |
34 |
24 |
13 |
35 |
|
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
39 |
40 |
|
45 |
25 |
14 |
45 |
14 |
34 |
45 |
34 |
15 |
13 |
|
41 |
42 |
43 |
44 |
45 |
46 |
47 |
48 |
49 |
50 |
|
25 |
45 |
14 |
34 |
25 |
23 |
12 |
15 |
13 |
25 |
|
51 |
52 |
53 |
54 |
55 |
56 |
57 |
58 |
59 |
60 |
|
24 |
12 |
35 |
14 |
23 |
35 |
45 |
25 |
34 |
35 |
|
61 |
62 |
63 |
64 |
65 |
66 |
67 |
68 |
69 |
70 |
|
23 |
15 |
12 |
13 |
25 |
13 |
24 |
14 |
34 |
13 |
|
71 |
72 |
73 |
74 |
75 |
76 |
77 |
78 |
79 |
80 |
|
35 |
25 |
23 |
34 |
35 |
12 |
34 |
24 |
15 |
16 |
|
81 |
82 |
83 |
84 |
85 |
86 |
87 |
88 |
89 |
90 |
|
25 |
15 |
36 |
15 |
35 |
45 |
13 |
45 |
24 |
35 |
|
91 |
92 |
93 |
94 |
95 |
96 |
97 |
98 |
99 |
100 |
|
25 |
24 |
25 |
36 |
25 |
56 |
34 |
46 |
26 |
56 |
|
101 |
102 |
103 |
104 |
105 |
106 |
107 |
108 |
109 |
110 |
|
14 |
36 |
15 |
35 |
46 |
23 |
35 |
36 |
26 |
12 |
|
111 |
112 |
113 |
114 |
115 |
116 |
|
|||
|
15 |
32 |
36 |
15 |
36 |
24 |
|
|||
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.