
Реферат по фармацевтической химии на тему «Ключевые методы анализа ФФА в исследовании лекарственных средств, производных пурина (природные и синтетические аналоги)»
Содержание:
1. Введение………………………………………………………………………...1
2. Производные ксантина....……………………………………………………....1
3. Производные гуанина………………………………..……………………...….8
4. Синтетические замещенные пурина………………………………………..….8
5. Заключение…………………………………………………………………….13
6. Литература……………………………………………………………………..14
ПРОИЗВОДНЫЕ ПУРИНА
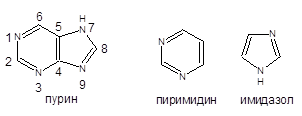
Пурин – конденсированная гетероциклическая система, состоящая из двух циклов: пиримидина и имидазола.
ПРОИЗВОДНЫЕ КСАНТИНА
COFFEINUM ГФ ХII

1,3,7-триметилксантин моногидрат
Белые шелковистые игольчатые кристаллы или белый кристаллический порошок, без запаха. На воздухе выветривается, при нагревании возгоняется.
Легко растворим в горячей воде и хлороформе, медленно растворим в воде, мало растворим в спирте.
КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
Основные свойства связаны с наличием неподеленной пары электронов у атома азота в положении 9.
Кофеин кислотными свойствами не обладает.
ИДЕНТИФИКАЦИЯ
1. ГФ ХII. Общей реакцией, рекомендуемой для испытания подлинности производных ксантина, является мурексидная проба.
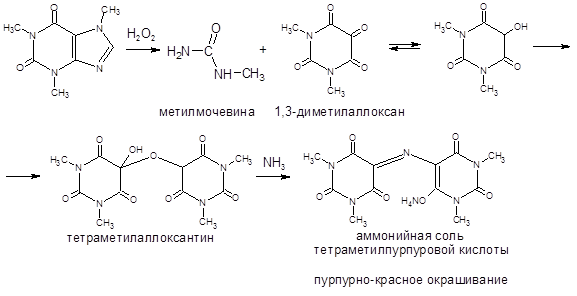
2. ГФ ХII. ИК-спектр субстанции по положению полос поглощения должен соответствовать рисунку спектра кофеина моногидрата, представленному в ФС.
3. ГФ ХII. УФ-спектр раствора в кислой среде должен иметь максимум поглощения при 273 нм.
4. Как третичное основание взаимодействует с осадительными (общеалкалоидными) реактивами:
а) кофеин с 0,01% раствором танина образует белый осадок таната, растворимый в избытке реактива.
б) ГФ ХII. К раствору кофеина в горячей воде после охлаждения добавляют 0,1М раствор йода; не должно быть ни осадка, ни помутнения. При добавлении нескольких капель хлористоводородной кислоты разведенной образуется бурый осадок, растворимый в избытке раствора натрия гидроксида.
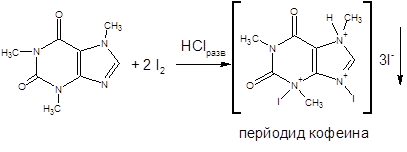
COFFEINUM-NATRII BENZOAS
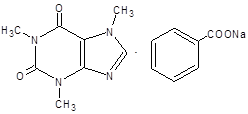
Белый порошок без запаха, слабо горького вкуса.
Легко растворим в воде, трудно растворим в спирте, практически нерастворимы в эфире и хлороформе.
ИДЕНТИФИКАЦИЯ
1. Дает все реакции, характерный для кофеина, после его извлечения из подщелоченного водного раствора хлороформом.
2. Дает характерную реакцию на бензоат: при добавлении к нейтральному раствору раствора хлорида железа (III) образуется розово-желтый (телесный) осадок.

3. Дает характерную реакцию на натрий: препарат, внесенный в бесцветное пламя, окрашивает его в желтый цвет.
THEOBROMINUM
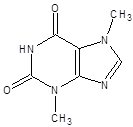
3,7-диметилксантин
Белый кристаллический порошок без запаха, горького вкуса.
Очень мало растворим в воде, мало растворим в горячей воде, очень мало растворим в спирте, эфире и хлороформе, легко растворим в разведенных щелочах и кислотах.
КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
Теобромин и теофиллин являются амфотерными соединениями.
Их основные свойства обусловлены наличием неподеленной пары электронов атома азота в положении 9.
Кислотные свойства теобромина) связаны с подвижностью атома водорода имидной группы, а теофиллина – с подвижностью атома водорода при азоте в положении 7.
Кислотные свойства у теофиллина выражены сильнее, чем у теобромина.
ИДЕНТИФИКАЦИЯ
1. Мурексидная проба.
2. Наличие NH-кислотного центра обуславливает способность взаимодействия с солями тяжелых металлов.
а) При взаимодействии с солями кобальта появляется быстроисчезающее фиолетовое окрашивание и почти сразу же образуется осадок серовато-голубого цвета (отличие от теофиллина и кофеина):
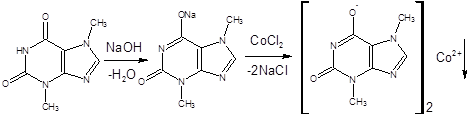
б) При взаимодействии с раствором нитрата серебра в среде аммиака при встряхивании образуется густая желатинообразная масса, которая разжижается при нагревании до 80°С и снова застывает при охлаждении:
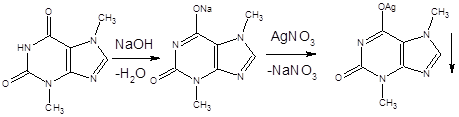
THEOPHYLLINUM ГФ ХII
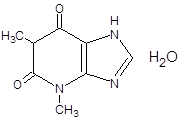
1,3-диметилксантина моногидрат
Белый или почти белый кристаллический порошок без запаха.
Мало растворим в воде, 96% спирте, эфире и хлороформе. Легко растворим в горячей воде и горячем спирте, растворим в кислотах и растворах щелочей.
ИДЕНТИФИКАЦИЯ
1. ГФ ХII. ИК-спектр субстанции по положению полос поглощения должен соответствовать рисунку спектра теофиллина, представленному в ФС.
2. ГФ ХII. Мурексидная проба.
3. ГФ ХII. За счет кислотных свойств взаимодействует с раствором хлорида кобальта после растворения в растворе натрия гидроксида. Образуется белый с розовым оттенком осадок (отличие от теобромина и кофеина).
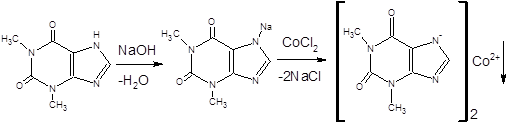
4. ГФ ХII. Температура плавления: от 270 до 274°С.
5. Теофиллин после щелочного гидролиза (в 30%-ном растворе гидроксида натрия при нагревании) превращается в теофиллидин, который вступает во взаимодействие с солью диазония, образуя азокраситель красного цвета:
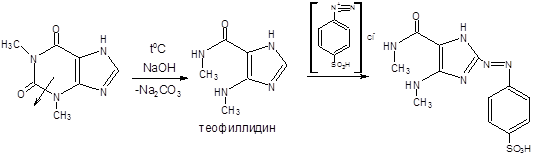
EUPHYLLINUM (AMINOPHYLLINE)
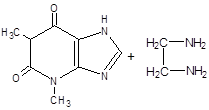
Теофиллин с 1,2-этилендиамином
Белый или белый с желтоватым оттенком кристаллический порошок со слабым аммиачным запахом.
Растворим в воде. Очень мало растворим в этаноле.
ИДЕНТИФИКАЦИЯ
1. Дает все реакции, характерный для теофиллина, после его осаждения из водного раствора (полученного при нагревании) с помощью хлористоводородной кислоты. Осадок отфильтровывают, сушат и используют для идентификации.
2. Дает характерную реакцию на 1,2-этилендиамин: при добавлении раствора сульфата меди появляется ярко-фиолетовое окрашивание:
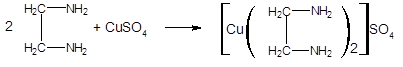
DIPROPHYLLINUM
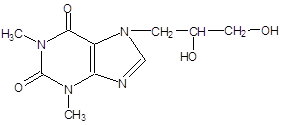
Белый мелкокристаллический порошок горького вкуса.
Медленно растворим в воде, растворим при кипячении в метаноле и этаноле 95%, практически нерастворим в ацетоне, хлороформе и эфире.
ИДЕНТИФИКАЦИЯ
1. Мурексидная проба.
2. После кипячения с раствором гидроксида натрия выделяется аммиак, обнаруживаемый по запаху и по посинению влажной красной лакмусовой бумаги.
3. К препарату добавляют гидросульфат калия, пробирку накрывают фильтровальной бумагой, смоченной свежеприготовленным раствором нитропруссида натрия и каплей пиперидина и нагревают. Появляется синее пятно, переходящее в розовое, при добавлении 2-3 капель 1М раствора гидроксида натрия.
ПРОИЗВОДНЫЕ ГУАНИНА (2-АМИНО-6-ОКСИПУРИНА)
ACICLOVIR (ЗОВИРАКС) ГФ ХII
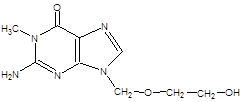
Белый или почти белый кристаллический порошок.
Мало растворим в воде, очень мало растворим в спирте, практически нерастворим в хлороформе и эфире. Растворим в растворах кислот и щелочей.
ИДЕНТИФИКАЦИЯ
1. ГФ ХII. ИК-спектр субстанции по положению полос поглощения должен соответствовать спектру стандартного образца ацикловира.
2. ТСХ. Пятно основного вещества на хроматограмме должно быть на уровне пятна стандартного образца.
3. ВЭЖХ по времени удерживания основных компонентов с использованием гуанина в качестве внутреннего стандарта. Подвижная фаза: ледяная уксусная кислота – вода (1:1000).
СИТЕТИЧЕСКИЕ 6,9-ЗАМЕЩЕНЫЕ ПУРИНА
RIBOXINUM (INOSINЕ) ГФ ХII

Белый или почти белый кристаллический порошок.
Медленно растворим в воде, очень мало растворим в этаноле практически нерастворим в хлороформе и эфире.
ИДЕНТИФИКАЦИЯ
1. ГФ ХII. ИК-спектр субстанции по положению полос поглощения должен соответствовать рисунку спектра рибоксина, представленному в ФС.
2. ГФ ХII. ВЭЖХ. Время удерживания основного пика на хроматограмме испытуемого раствора должно соответствовать времени удерживания основного пика на хроматограмме стандартного раствора.
3. ГФ ХII. При добавлении к водному раствору рибоксина 0,1% раствора хлорида железа (III) в хлористоводородной кислоте концентрированной и 10% спиртового раствора орцина и нагревании в течение 20 минут в кипящей водяной бане появляется зеленое окрашивание.
MERCAPTOPURINUM (MERCAPTOPURINЕ)
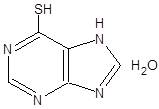
Желтый кристаллический порошок без запаха или почти без запаха.
Практически нерастворим в воде и спирте, растворим в горячей воде, в растворах щелочей, мало растворим в разведенных кислотах.
ИДЕНТИФИКАЦИЯ
1. УФ-спектр раствора в кислой среде должен иметь максимум поглощения при 325 нм, а в щелочной – при 231 и 310 нм.
2. При добавлении раствора нитропруссида натрия в щелочной среде образуется желтовато-зеленое окрашивание, переходящее при подкислении в темно-зеленое.
3. После растворения в аммиаке добавляют хлорид меди (II) и гидроксиламина гидрохлорид; наблюдается выпадение белого осадка.
4. Из растворов в этаноле при добавлении насыщенного спиртового раствора ацетата ртути (II) выпадает белый осадок, а под действием спиртового раствора ацетата свинца – желтый осадок.
5. Проводят реакции с селенистой кислотой (красный осадок), концентрированной азотной кислотой (желтое окрашивание), концентрированной серной кислотой в присутствии этанола и сахарозы (коричневое окрашивание).
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
1. За счет основных свойств атомов азота в положении 9 в пурине возможно кислотно-основное титрование в среде неводного растворителя.
Растворитель: ледяная уксусная кислота;
Кофеин в неводной среде проявляет наиболее сильные основные свойства, чем другие производные ксантина. Кофеин титруют в среде уксусного ангидрида и хлороформа до желтого окрашивания.
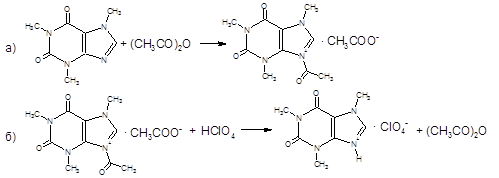
Титрант: титрованный раствор хлорной кислоты (HClO4);
Индикатор: кристаллический фиолетовый;
Конечную точку титрования ацикловира определяют потенциометрически.
При титровании теобромина в качестве растворителя используют муравьиную кислоту и уксусный ангидрид (1:10), индикатором служит Судан III.
fэкв = 1.
2. Обратная йодометрия основана на способности образовывать периодиды. Этот метод используют при определении кофеина в кофеин-бензоате натрия, которого должно быть в пересчете на сухое вещество не менее 38% и не более 40%.
Добавляют избыток титрованного раствора йода и разведенную серную кислоту. Образовавшийся осадок периодида отфильтровывают. В фильтрате титруют йод, не вступивший в реакцию.
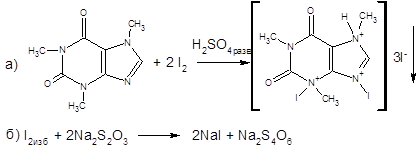
Титрант: титрованный раствор натрия тиосульфата (Na2S2O3);
Индикатор: крахмал. Добавляют в конце титрования и титруют до исчезновения синего окрашивания.
fэкв = ¼ - для кофеина и теобромина.
3. Для определения бензоата натрия в кофеин бензоате натрия используют ацидиметрию в присутствии эфира для извлечения выделяющейся бензойной кислоты.

Титрант: титрованный раствор кислоты хлористоводородной (HCl);
Индикатор: смешанный – метиловый оранжевый и метиленовый синий (1:1);
Титруют до появления сиреневой окраски в водном слое.
fэкв = 1.
Бензоата натрия в кофеин бензоате натрия в пересчете на сухое вещество должно быть не менее 58% и не более 62%. Поэтому при определении кофеина бензоата натрия в лекарственных формах по бензоату натрия рассчитывают условный титр:
М.м. бензоата натрия = 144,1
0,1 * 144,1
Т = -------------- = 0,01441 (г/мл) - количество бензоата натрия, соответствующее
1000 1 мл 0,1М HCl
0,01441 *100
Тусл = ------------------ = 0,0232 (г/мл)
62
Ацидиметрически титруют также этилендиамин в эуфиллине, которого в пересчете на сухое вещество должно быть не менее 14% и не более 18% (в растворе для инъекций 18-22%).
![]()
Титрант: титрованный раствор кислоты хлористоводородной (HCl);
Индикатор: метиловый оранжевый (в точке эквивалентности оранжево-розовое окрашивание);
fэкв = ½.
4. Для количественного определения теофиллина, теобромина и теофиллина в эуфиллине (80-85% в пересчете на сухое вещество) используют метод косвенной нейтрализации. Метод основан на образовании солей серебра и выделения эквивалентного количества азотной кислоты, которую оттитровывают щелочью.
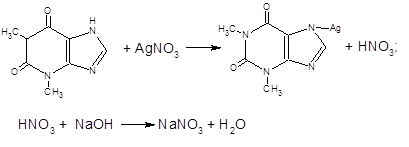
Титрант: титрованный раствор натрия гидроксида (NаОН);
Индикатор: феноловый красный (в точке эквивалентности фиолетово-красное окрашивание);
fэкв = 1.
Количественное определение теофиллина в эуфиллине выполняют после нагревания (для удаления этилендиамина) в течение 2,5 часов при 125-130°С.
5. Как слабые кислоты (теобромин, теофиллин) титруют методом кислотно-основного титрования в протофильном растворителе.
Растворитель: диметилформамид, диметилсульфоксид или бутиламин.
Титрант: титрованный раствор метилата лития или натрия.
Индикатор: тимоловый синий.
6. Образование серебряных солей для теофиллина, теобромина или меркаптопурина лежит в основе обратной аргентометрии.
К раствору препарата добавляют аммиак и фиксированный избыток титрованного раствора нитрата серебра. Образовавшийся осадок серебряной соли отфильтровывают. В фильтрате определяют избыток нитрата серебра.
Титрант: титрованный раствор роданида аммония (NH4SCN);
Индикатор: железоаммониевые квасцы (в точке эквивалентности красное окрашивание);
fэкв = 1.
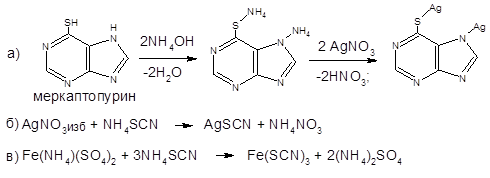
7. Спектрофотомерия возможна так как все препараты имеют максимумы поглощения в УФ-области спектра.
8. Фотоэлектроколориметрия возможна так как все препараты образуют окрашенные соединения.
9. Метод Къельдаля.
ГФ Х для дипрофиллина.
10. ВЭЖХ.
Для рибоксина и ацикловира по ГФ ХII.
ХРАНЕНИЕ
Кофеин, кофеин-бензоат натрия, теобромин, дипрофиллин,– список Б. В хорошо укупоренной таре, в сухом месте.
Теофиллин, ацикловир – список Б. В сухом, защищенном от света месте.
Эуфиллин – список Б. В хорошо укупоренной, заполненной доверху таре, предохраняющей от действия света.
Рибоксин – список Б. В сухом, защищенном от света месте.
Меркаптопурин – список А. В хорошо укупоренной таре. При работе соблюдать осторожность, избегая попадания на кожу и в дыхательные пути.
ПРИМЕНЕНИЕ
Кофеин, кофеин-бензоат натрия – стимулятор центральной нервной системы, кардиотоническое средство.
Формы выпуска: раствор для инъекций 10% и 20%, таблетки 0,1 и 0,2.
Теобромин, теофиллин – спазмолитическое (сосудорасширяющее, бронхорасширяющее) и диуретическое средство.
Форма выпуска: таблетки по 0,25 (теобромин).
Эуфиллин – спазмолитическое (сосудорасширяющее, бронхорасширяющее) средство.
Форма выпуска: раствор для инъекций 2,4% и 12%, таблетки 0,15.
Дипрофиллин – спазмолитическое (сосудорасширяющее, бронхорасширяющее) средство.
Форма выпуска: таблетки по 0,2, раствор для инъекций, суппозитории.
Ацикловир – противовирусное средство.
Форма выпуска: раствор для инъекций, таблетки по 0,2 и 0,4, мазь 3% и крем 5% (ацикловир).
Рибоксин – средство метаболической терапии в кардиологии.
Форма выпуска: таблетки покрытые оболочкой 0,2, раствор для инъекций.
Меркаптопурин – антилейкемическое средство.
Форма выпуска: таблетки 0,05.
ЗАКЛЮЧЕНИЕ
Применение в медицине алкалоидов пуринового ряда основано на их стимулирующем действии на центральную нервную систему. Особенно сильно это действие выражено у кофеина (тонизирующее средство).
Теобромин и теофиллин обладают диуретическим действием, кроме того, они расширяют коронарные сосуды.
Природными источниками алкалоидов пуринового ряда являются: листья чая (кофеин, теофиллин), зерна кофе (теофиллин), шелуха бобов какао (теобромин), откуда путем экстракции органическими растворителями и получали эти алкалоиды.
Кроме алкалоидов, листья чая содержат много сопутствующих веществ (дубильные вещества, белки, углеводы, смолы, нуклеопротеиды, ферменты и др.), поэтому требовалась тщательная очистка экстрактов от этих примесей.
В настоящее время препараты пуриновых алкалоидов получают синтетически из веществ, представляющих уже готовый иуриновый цикл, например мочевая кислота (I), или из веществ, не являющихся пуринами, но путем ряда преобразований приходящих к пуриновому циклу. В первом случае метод называется полусинтетическим; во втором случае имеет место полный синтез.
Литература:
1. Методы анализа лекарственных препаратов. Фармацевтическая химия: учебник для студентов. Глущенко Н.Н. – Москва, 1998
2. Фармацевтическая химия. Беликов В.Г. – Москва, 2008
3. ФАРМАЦЕВТИЧЕСКАЯ ХИМИЯ. Учебное пособие. Арзамасцев А.А. – Москва, 2005
4 . Введение в фармацевтическую химию. Учебное пособие. Логинова Н.В., Полозов Г.И. – Волгоград, 2003
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.