
ПОУРОЧНЫЙ ПЛАН
ЗАНЯТИЯ № 16
Тема занятия: Уравнение Менделеева—Клапейрона. Газовые законы.
Цели занятия:
Образовательная:
- вывести уравнение Клапейрона-Менделеева и научить решать задачи по этой формуле.
- установить зависимость между двумя макропараметрами газа при неизменном третьего.
Развивающая:
– развивать логическое мышление при постановке и решении учебных проблем, формировать навыки и умения при планировании ответов, постановки целей на урок, рефлексии, при работе по алгоритму решения задач.
Воспитывающая:
- побуждать обучающихся к преодолению трудностей в процессе умственной деятельности, воспитать интерес к физике.
Формируемые компетенции:
ОК 2. Организовывать собственную деятельность, выбирать типовые методы и способы выполнения профессиональных задач, оценивать их эффективность и качество.
ОК 3. Принимать решения в стандартных и нестандартных ситуациях и нести за них ответственность.
ОК 4. Осуществлять поиск и использование информации, необходимой для эффективного выполнения профессиональных задач, профессионального и личностного развития.
Тип занятия: урок изучения и первичного закрепления нового материала
Вид занятия: практико-ориентированное занятие.
Методы обучения: словесные методы, наглядные методы, практические метод, объяснительно-иллюстративный метод.
Методы контроля: фронтальный опрос, решение задач.
Техническое оснащение:
Комплексно-методическое оснащение: РП, КТП, поурочный план, раздаточный материал.
Межпредметные и внутрипредметные связи. Республиканский компонент:
ОДП.08 Химия
Используемая литература:
Основная
|
№ п/п |
Наименование |
Автор |
Издательство, год издания |
|
1 |
Физика//Учебник для 10 класса общеобразовательных учреждений, |
Мякишев Г.Я., Буховцев Б.Б., Сотский Н.Н. |
М.: Просвещение, 2005 |
Дополнительная
|
№ п/п |
Наименование |
Автор |
Издательство, год издания |
|
2 |
Физика // Учебник для средних специальных учебных заведений. |
Дмитриева В.Ф. |
М.: Академия, 2002.
|
Структура и ход урока:
I. Организационный этап.
II. Актуализация опорных знаний.
Решение задач у доски.
- Гелий находится в закрытом сосуде под нормальным давлением и имеет плотность 0,16 кг/м3. Определите температуру газа.
-
При какой температуре средняя кинетическая энергия
поступательного движения молекул газа равна ![]() Дж?
Дж?
- Найдите среднюю квадратичную скорость молекул азота при температуре 270С.
III. Постановка цели и задач урока.
Мотивация учебной деятельности учащихся.
IV. Первичное усвоение новых знаний.
- Уравнение состояния системы.
- Вывод уравнения Клапейрона-Менделеева для произвольной массы идеального газа.
- Универсальная газовая постоянная.
- Запись уравнения состояния для одного моля.
- Физический смысл универсальной газовой постоянной.
- Изопроцессы.
Для решения задач можно рекомендовать такую последовательность:
- внимательно проанализировать условие задачи, установить, какой газ участвует в процессе, какие параметры меняются, какие - остаются постоянными;
- сделать, если возможно, схематический чертеж, указав при этом, какие параметры характеризуют каждое состояние;
- особое внимание уделить параметрам, заданным неявно; иногда для нахождения объема газа нужно использовать формулы геометрии, для нахождения давления газа на жидкость- закон Паскаля или соотношение p = p0+Pgh
- для каждого состояния записать нужные соотношения и решить полученную систему уравнений относительно искомой величины.
V. Первичная проверка понимания.
- Вычислите массу воздуха в комнате объёмом 120 м3 при нормальных условиях. Молярная масса воздуха равна 0,029 кг/моль.
- Сколько молекул воздуха выйдет из комнаты при повышении температуры в ней до 20°С? Давление и объём считать постоянными.
- 2. Найдите плотность кислорода при температуре 300К и давлении 1,6×105Па.
- Вычислите массу кислорода при данных условиях, если он находится в баллоне объёмом 0,2 м3.
- Дан график изменения состояния идеального газа. Прочитать его и построить график этого процесса на диаграмме P,Т; V,T.

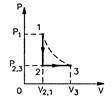
- На рисунке изображены процессы изменения состояния некоторой массы газа. Назовите эти процессы. Изобразите графики процессов в системе координат P,T и V,T.
VI. Первичное закрепление.
Самостоятельная работа.
Вариант №1
1. Газ изотермически сжат от объема 6 л до объема 3 л. Найти конечное давление, если первоначальное равно 250 кПа.
2. В помещении объемом 20 м3 температура воздуха понизилась от 20 0С до 0 0С при давлении 101 кПа. На сколько увеличилась масса газа? Молярная масса воздуха 0,029 кг/моль.
Вариант №2
1. Газ при 300 К занимал объем 250 м3. Какой объем займет тот же газ, если его температура повысится до 324 К? Давление газа неизменно.
2. В баллоне содержится 2 кг газа при 270 К. Какую массу газа нужно удалить из баллона, чтобы при нагревании до 300 К давление осталось прежним?
Вариант №3
1. Давление в рентгеновской трубке при 15 0С равно 1,2 мПа. Каково будет давление в работающей трубке при 150 0С?
2. В закрытом сосуде находится газ под давлением 500 кПа. Какое давление установится в этом сосуде, если после открытия крана 4/5 массы газа выйдет наружу? Процесс изотермический.
Вариант №4
1. Какое количество идеального газа находится в объеме 36 л под давлением 2,5 МПа при температуре 27 0С?
2. Сколько молей вещества содержится в газе, если при давлении 200 кПа и температуре 240 К его объем равен 40 л?
VII. Информация о домашнем задании, инструктаж по его выполнению.
|
[1], §70-71, |
Рабочая тетрадь по физике: стр. 20-22, в. 1-9, задач 1.
VIII. Рефлексия.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.