
Уравнение теплового баланса.
Первое начало термодинамики. Адиабатный процесс.
Для механических явлений при определённых условиях выполняется закон сохранения механической энергии: полная механическая энергия системы тел сохраняется, если они взаимодействуют силами тяготения или упругости. Если действуют силы трения, то полная механическая энергия тел не сохраняется, часть её (или вся) превращается в их внутреннюю энергию.
При изменении состояния тела (системы) меняется его внутренняя энергия. Состояние тела и соответственно его внутреннюю энергию можно изменить двумя способами: в процессе теплопередачи или путём совершения внешними силами работы над телом (работа, например, силы трения). Мерой изменения внутренней энергии тела в процессе теплообмена выступает количество теплоты (Q).
Уравнение теплового баланса
В изолированной системе при смешивании горячей и холодной воды, количество теплоты Q1, отданное горячей водой, равно количеству теплоты Q2, полученному холодной водой, т.е.:
|Q1|= |Q2|. Q1 (выделенное) < 0, Q2 (полученное) > 0.
Qотданное + Qполученное = 0
Записанное равенство называется уравнением теплового баланса (эта формула и уравнение, используемое в 8 классе!).
Определение: суммарное количества теплоты, которое выделяется в теплоизолированной системе равно суммарному количеству теплоты, которое в этой системе поглощается.
Уравнение теплового баланса связывает количество теплоты, полученное одним телом, и количество теплоты, отданное другим телом при теплообмене. При этом в теплообмене могут участвовать не два тела, а три и более: Q1 + Q2 + Q3 + … = 0

Уравнение теплового баланса – это закон сохранения энергии для процессов теплообмена в термоизолированных системах. Оно даёт возможность определить те или иные величины. В частности, значения удельной теплоёмкости веществ определяют из уравнения теплового баланса.
Количественное соотношение между изменением внутренней энергии, теплотой и работой устанавливает первый закон термодинамики:
Q = ΔU + А.
Если к системе подводится теплота Q, то она расходуется на изменение внутренней энергии системы ΔU и на совершение системой работы А над окружающей средой.
Теплоту и работу можно измерить, отсюда,
ΔU = Q – А
Первый закон термодинамики является формой выражения закона сохранения энергии. Согласно этому закону, энергия не может ни создаваться, ни исчезать, но может превращаться из одной формы в другую. Его справедливость доказана многовековым опытом человечества.
Если система осуществляет переход из одного состояния в другое при постоянном объеме (реакция протекает в автоклаве), то работа расширения системы
А = рΔV = 0 и Qv = ΔU = U2 – U1,
т.е. если реакция протекает при постоянном объеме, то выделение или поглощение теплоты Q связано с изменением внутренней энергии системы.
Если на систему не действуют ни какие другие силы, кроме постоянного давления, т.е. химический процесс осуществляется в изобарных условиях, и единственным видом работы является работа расширения, то первый закон термодинамики запишется:
Qp = ΔU + pΔV.
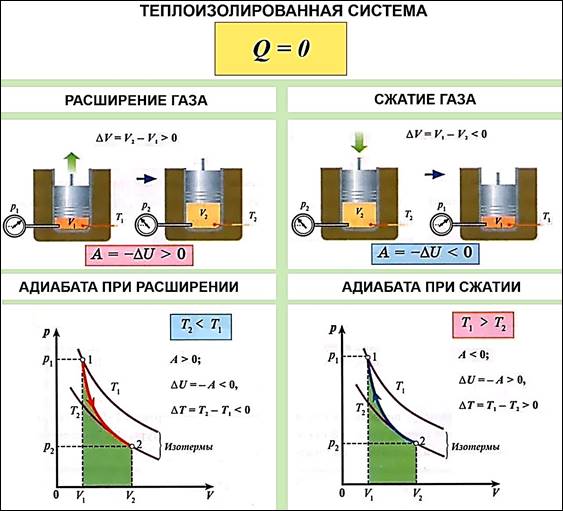
Адиабатный (адиабатический) процесс медленный процесс без теплообмена с окружающей средой.
В этом процессе Q = 0,
поэтому A = ∆U, то есть работа
газа равна убыли внутренней энергии газа.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.