
Лабораторная работа
ИССЛЕДОВАНИЕ ИЗОТЕРМИЧЕСКОГО ПРОЦЕССА
Цель. Экспериментально проверить зависимость изменения объема газа данной массы и изменение его давления при постоянной температуре (проверить закон Бойля-Мариотта).
Теоретическое обоснование
|
|
Изопроцессы — равновесные процессы, в которых один из основных параметров сохраняется.
Процесс изменения давления и объема газа при постоянной температуре называется изотермическим процессом.
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС (T=const)
Изотермический процесс в идеальном газе подчиняется закону Бойля - Мариотта: для данной массы газа при неизменной температуре произведение значений давления и объема есть величина постоянная: pV=const или p1V1=p2V2
|
|
График зависимости давления газа от его объема при изотермическом процессе называется изотермой.
p1 и V1 – давление и объем воздуха в одном состоянии
p2 и V2 - давление и объем воздуха в другом состоянии
Оборудование: стеклянная трубка 10-12 мм и длиной 60 см, запаянная с одного конца, мензурка (250 мл) с водой комнатной температурой, измерительная лента (линейка), барометр.
Ескерту: Шыны түтікшенің диаметрі 10-12 мм және ұзындығы 60 см шыны түтікше болмаса, онда диаметрі және ұзындығы басқа шыны түтікше қолдануға болады. Ондай жағдайда шыны түтікшенің диаметрі 10-12 см-ден аспау керек, ал ұзындық қалауыңызша.
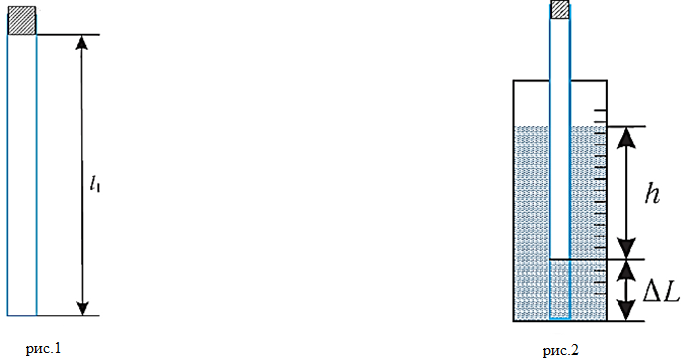
Исследуемым газом в выполняемой работе является воздух, находящийся внутри прозрачной стеклянной трубки с пробкой на конце. (рис.1)
Поскольку внутренняя полость трубки имеет форму цлиндра и площадь S ее поперечного сечения одинакова по всей длине трубки, то
V1=Sl1 и V2=Sl2

Ход работы
|
l1, м |
p1, Па |
∆L, м |
h, м |
l2, м |
pc, Па |
p2, Па |
(p1∙l1 / p2∙l2) |
ε, % |
|
|
|
|
|
|
|
|
|
|
1. Измерте линейкой длину l1, столба воздуха в трубке начальном состояний.
2. Измерте давление p1 воздуха в начальном состояний, используя барометр (или посмотрите атмосферное давление на данный момент p1 в интернете).
3. Заполните мензурку водой комнотной температуры.
4. Погрузите в мензурку с водой трубку так, чтобы ее открытый конец оказался у дна мензурки. (см.рис.2)
5.Наблюдайте за поступлением воды трубку. Когда оно прекратится, измерте длину ∆L столба воды, вошедший трубку.
6. Измерте разность уровней h воды в мензурке и трубке.
7. Вычислите длину l2 столба воздуха в трубке в конечном состояний: l2 = l1 - ∆L
8. Вычислите давление воды pв столба воды по формуле pв= ρgh. Где ρ-плотность воды (ρ=1000 кг/м3 ). Ускорение свободного падения g=9,8 м/с2.
9. Вычислите давления p2 водуха в трубке конечном состояний: p2= p1+ pc
10. Вычислите отношение p1∙l1 / p2∙l2 . Результат вычисление запишите в таблицу.
11. Различие между теоретичиским ожидаемым
![]() и
экспериментально полученным
(
и
экспериментально полученным
(![]() ) результатами
позволяет
оценит относительную погрешенность экспериментального потверждения закона
Бойля-Мариота.
) результатами
позволяет
оценит относительную погрешенность экспериментального потверждения закона
Бойля-Мариота.
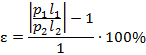
12. Сделайте вывод о выполнений или невыполнении (или выполнение с небольшой погрешенностью) изотермического закона Бойля – Мариотта полученным в ходе работы результатам.
(P.S. Для того, чтобы утверждать о выполнений закона нужно этот закон сначала сформулировать, а затем показать конкретный результат, найденный в работе, который его подверждает.)
Контрольные вопросы
1. При каких условиях для определения параметров состояния газа можно использовать уравнение PV=const?
2. Почему при выполнении данной работы процесс изменения обьема воздуха можно считать практически изотермическим?
3. Что влияет на точность полученных результатов?
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.