
МЕТОДИЧЕСКИЕ УКАЗАНИЯ ДЛЯ ОБУЧАЮЩИХСЯ ПО ВЫПОЛНЕНИЮ ПРАКТИЧЕСКИХ РАБОТ
Основы материаловедения
15.01.05. Сварщик (ручной и частично механизированной сварки (наплавки)
Разработал: преподаватель Трегуб Т.А.
ОБЩИЕ УКАЗАНИЯ
Практические занятия - форма учебного занятия, на котором преподаватель организует детальное рассмотрение обучающимися отдельных теоретических положений учебной дисциплины и формирует умения и навыки их практического применения путем выполнения соответствии поставленных задач. Целью практических занятий по учебной дисциплине Основы материаловедения является закрепление обучающимися теоретического материала и выработка практических навыков для применения знаний в будущей профессиональной деятельности.
Практические занятия по учебной дисциплине реализуют дидактический принцип связи теории с практикой и ориентированы на решение следующих задач:
- углубление, закрепление и конкретизацию знаний, полученных на лекциях и в процессе самостоятельной работы;
- формирование практических умений и навыков, необходимых в будущей профессиональной деятельности выпускников согласно ФГОС СПО по профессии.
Освоение дисциплины направлено на развитие общих и профессиональных компетенций, предусмотренных ФГОС СПО по профессии 15.01.05. Сварщик (ручной и частично механизированной сварки (наплавки)
ОК 4. Осуществлять поиск информации, необходимой для эффективного выполнения профессиональных задач.
ОК 5. Использовать информационно-коммуникационные технологии профессиональной деятельности
ОК 6. Работать в команде, эффективно общаться с коллегами, руководством.
В результате освоения учебной дисциплины обучающийся должен уметь:
- пользоваться справочными таблицами для определения свойств материалов;
- выбирать материалы для осуществления профессиональной деятельности;
В результате освоения учебной дисциплины обучающийся должен знать:
- наименование, маркировку, основные свойства и классификацию углеродистых и конструкционных сталей, цветных металлов и сплавов, а также полимерных материалов (в том числе пластмасс, полиэтилена, полипропилена);
- правила применения охлаждающих и смазывающих материалов;
- механические испытания образцов материалов
Рабочей программой предусмотрено выполнение 6 практических работ. Каждая практическая и лабораторная работа содержит сведения о цели ее проведения и практическом использовании результатов исследования, о необходимых для работы материалах, инструментах; включает описание работы.
Основные требования к подготовке и выполнению практических работ
Для оформления отчетов по практическим работам каждый обучающийся должен иметь рабочую тетрадь. Начинать работу на занятии рекомендуется с изучения и анализа краткого теоретического материала, касающегося темы практического занятия. Предлагаемые контрольные вопросы должны способствовать более глубокому изучению теоретического курса, связанного с темой практического занятия. Также контрольные вопросы должны помочь в решении поставленных перед обучающимися задач и подготовке к защите практической работы. Выполнять практическую работу нужно в порядке, изложенном в данных указаниях.
ПРАКТИЧЕСКАЯ РАБОТА
ИЗУЧЕНИЕ ТИПОВ КРИСТАЛЛИЧЕСКИХ РЕШЕТОК И ИХ ВЛИЯНИЕ НА СТРУКТУРУ И СВОЙСТВА МЕТАЛЛОВ И ИХ СПЛАВОВ
Цель работы: Ознакомиться с видами и характеристикой кристаллических решеток металлов. Изучить влияния кристаллических решеток на структуру и свойства металлов.
Основные теоретические положения
1. АТОМНО-КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ.
Металлические материалы. 83 из известных 112 химических элементов таблицы Менделеева Д. И. являются металлами. Они обладают рядом характерных свойств:
- высокой тепло- и электропроводностью;
- положительным коэффициентом электросопротивления (с повышением температуры электросопротивление растет);
- термоэлектронной эмиссией (испусканием электронов при нагреве);
- хорошей отражательной способностью (блеском);
- способностью к пластической деформации;
- полиморфизмом.
Наличие перечисленных свойств обусловлено металлическим состоянием вещества, главным из которых является наличие легкоподвижных коллективизированных электронов проводимости.
Металлическое состояние возникает в совокупности атомов, когда при их сближении внешние (валентные) электроны теряют связь с отдельными атомами, становятся общими и свободно перемещаются между положительно заряженными, периодически расположенными ионами. Силы притяжения (силы связи) в твердых телах существенно отличаются по своей природе. Обычно рассматривают четыре основных типа связей в твердых телах: ван-дер-ваальсовые, ковалентные, металлические, ионную.
Под атомно-кристаллической структурой понимают взаимное расположение атомов в кристалле. Кристалл состоит из атомов (ионов), расположенных в определенном порядке, который периодически повторяется в трех измерениях.
Наименьший комплекс атомов, который при многократном повторении в пространстве позволяет воспроизвести пространственную кристаллическую решётку, называют элементарной ячейкой.
Для характеристики элементарной ячейки используют параметры кристаллической решётки:
• три ребра а, в, с, измеряемых в ангстремах (1Å = 1* 10-8см) или в килоиксах – kX (1kX = 1,00202 Å) и три угла , , ,;
• компактность структуры h - отношение объема, занимаемого атомами, к объёму ячейки ( для решётки ОЦК h = 64 %, для решётки ГЦК h = 74 %);
• координационное число К - число ближайших соседей данного атома: для решётки ОЦК это число равно 8, т.е. атомы, находящиеся в вершине, принадлежат восьми элементарным ячейкам (рис.1.а), для решётки ГЦК это число равно 12, т.е. атомы, находящиеся в вершине, принадлежат двенадцати элементарным ячейкам (рис. 1.б).
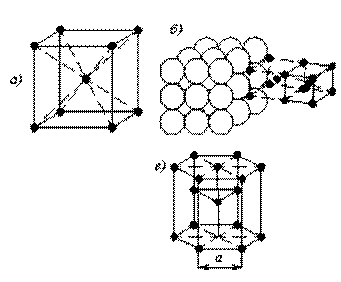
Рисунок 1. Схема определения координационного числа кристаллической решётки: а – ГЦК; б – ОЦК; в – ГПУ
Простейшим типом кристаллической ячейки является кубическая решётка. В простой кубической решётке атомы расположены (упакованы) недостаточно плотно.
Стремление атомов металла занять места, наиболее близкие друг к другу, приводит к образованию решеток других типов (рис. 2.):
- объёмноцентрированной кубической решётки (ОЦК) (рис.2.а) с параметром
а = 0,28 – 0,6мм = 2,8 – 6,0 Å
- гранецентрированной кубической решётки (ГЦК) (рис.2.б) с параметром
а = 0,25мм
- гексагональной плотно упакованной решётки (ГПУ) (рис.2.в) с параметром
с / а » 1,633
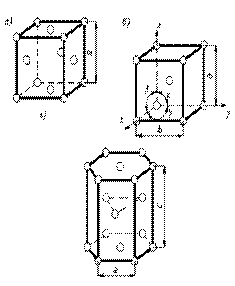
Рисунок 2. Кристаллические решётки: а – гранецентрированный куб (ОЦК); б – объемноцентрированный куб (ГЦК); в- гексагональная плотно упакованная (ГПУ)
Узлы (положения атомов), направления в плоскости и в пространстве обозначаются с помощью так называемых индексов Миллера (рис.3).
Индексы узла записываются – (mnp),
Индексы направления записываются – mnp,
Индекс плоскости записываются – (hk1).

Рисунок 3. Символы некоторых важнейших узлов, направлений и плоскостей в кубической решётке.
Вследствие неодинаковой плотности атомов в различных плоскостях и направлениях решётки многие свойства отдельно взятого кристалла (химические, физические, механические) по данному направлению отличаются от свойств в другом направлении и, естественно, зависят от того, сколько атомов встречается в этом направлении.
Различие свойств в зависимости от направления испытания носит название анизотропии.
Все кристаллы анизотропны.
Анизотропия – особенность любого кристалла, характерная для кристаллического строения.
Технические металлы являются поликристаллами, т.е. состоят из совокупности кристаллитов с различной ориентацией. При этом свойства во всех направлениях усредняются.
Атомы данного элемента могут образовать, если исходить только из геометрических соображений, любую кристаллическую решетку. Однако устойчивым, а следовательно, реально существующим типом является решетка, обладающая наиболее низким запасом свободной энергии.
Так, разные металлы образуют разные виды кристаллической решетки:
- Li, Na, K, Mo, W – ОЦК;
- Al, Ca, Cu, Au, Pt – ГЦК;
- Mg, Zr, Hf – ГПУ.
Однако в ряде случаев при изменении температуры или давления может оказаться, что для одного и того же металла более устойчивой будет другая решетка, чем та, которая существует при данной температуре или давлении. Так, например, существует железо с решетками объемно-центрированного и гранецентрированного кубов, обнаружен кобальт с гранецентрированной и с гексагональной решетками (рис.4).
Существование одного и того же металла (вещества) в нескольких кристаллических формах носит название полиморфизма или аллотропии.
Различные кристаллические формы одного вещества называются полиморфными или аллотропическими модификациями (таблица 1).
Аллотропические формы обозначаются греческими буквами a, b, g и т.д., которые в виде индексов добавляют к символу, обозначающему элемент. Аллотропическая форма при самой низкой температуре, обозначается буквой a, следующая - b и т. д.
Явление полиморфизма основано на едином законе об устойчивости состояния с наименьшим запасом энергии. Запас свободной энергии зависит от температуры. Поэтому в одном интервале температур более устойчивой является одна модификация, а в другом – другая.
Температура, при которой осуществляется переход из одной модификации в другую, носит название температуры полиморфного (аллотропического) превращения.
Механизм роста кристаллов новой фазы может быть нормальным кристаллизационным и мартенситным.
Нормальный механизм роста – это зарождение новой фазы на границах зерен, блоков, фрагментов при малых степенях переохлаждения (Sna « Snb).
Мартенситный механизм реализуется при низких температурах и большой степени переохлаждения, при малой диффузионной подвижности атомов путем их сдвига (смещения) по определенным кристаллографическим плоскостям и направлениям. Новая фаза имеет форму игл и растет очень быстро (Coa « Cob).
Аллотропическое превращение сопровождается изменением свойств, объема и появлением внутренних напряжений.
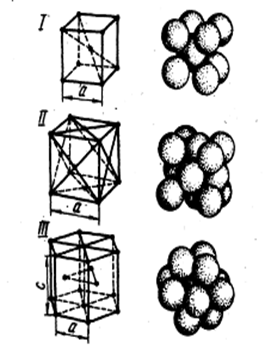
Рисунок 4. Элементарные ячейки кристаллических решеток:
I — кубическая объемно-центрированная ( α-железо),
II — кубическая гранецентрированная (медь),
III - гексагональная плотноупакованная;
а и с — параметры решеток.
Таблица 1. Аллотропические модификации металлов.
|
Металл |
Группа |
Модификация |
Кристаллическая решетка |
|||
|
Кальций |
II-A |
Сaa до 450 Caab 450-851 |
Кубическая гранецентрированная Гексагональная плотноупакованная |
|||
|
Галлий |
III-B |
Gaa Gab |
Ромбическая Тетрагональная |
|||
|
Таллий |
III-B |
Tla до 262 Tlb 262-304 |
Гексагональная плотноупакованная Кубическая объемноцентрированная |
|||
|
Титан |
IV-A |
Tia до 882 Tib 882-1725 |
Гексагональная плотноупакованная Кубическая объемноцентрированная |
|||
|
Цирконий |
IV-A |
Zra до 862 Zrb 862-1830 |
Гексагональная плотноупакованная Кубическая объемноцентрированная |
|||
|
Гафний |
IV-A |
Hfa до 1610 Hfb 1610-1952 |
Гексагональная Кубическая объемноцентрированная |
|||
|
Олово |
IV-B |
Sna до 18` Snb 18-232 |
Алмазная Тетрагональная объемноцентрированная |
|||
|
Вольфрам |
VI-A |
Wa до 650 Wb 650-3400 |
Кубическая объемноцентрированная Сложная (нерасшифрованная) |
|||
|
Уран |
VI-A |
Ua до 660 Ub 660-770 Ug 770- 1133 |
Ромбоэдрическая Тетрагональная Кубическая объемноцентрированная |
|||
|
Марганец |
VII-A |
Mna до 742 Mnb 742-1080 Mng 1080-1180 Mnd 1180-1242 |
Кубическая сложная Тетрагональная гранецентрированная |
|||
|
Железо |
VIII |
Fea до 910 1401-1539 Feg 910-1401 |
Кубическая объемноцентрированная
Кубическая гранецентрированная |
|||
|
Кобальт |
VIII |
Coa до 477 Cob 477-1490 |
Гексагональная плотноупакованная Кубическая гранецентрированная |
|||
Изучить виды кристаллических решеток.
Изучить и зарисовать схему определения координационного числа кристаллической решетки.
Изучить и зарисовать элементарные ячейки кристаллических решеток.
Отчет по практической работе должен содержать следующий материал:
Наименование и цель работы.
Виды кристаллических решеток.
Описание аллотропических модификаций металлов.
ПЕРЕЧЕНЬ КОНТРОЛЬНЫХ ВОПРОСОВ;
1. Виды кристаллических решеток.
2. Анизотропия кристаллов.
3. Характеристика кристаллических структур.
4. Полиморфизм (аллотропия).
ПРАКТИЧЕСКАЯ РАБОТА
Построение кривых охлаждения для сплавов диаграммы «Ғе -Ғе3С»
1.Освоить умения построения кривых охлаждения для сплавов
диаграммы «Ғе - Ғе3С»
2.Освоить умения практического применения диаграммы «Ғе- Ғе3С»
Оборудование:
диаграмма «Ғе - Ғе3С»
чертёжные инструменты
Общие положения
Первое представление о диаграмме «Fe – C» дал Д.К. Чернов, который в 1868 году указал на существование стали критических точек и их зависимость от содержания в ней углерода, т.е. фактически впервые указал на полиморфизм железа. Обычно диаграмму «Fe-C» изображают только до 6,67% С, когда образуется химическое соединение карбид железа Fe-C, т.к. практическое значение имеет лишь эта часть диаграммы «Fe-C». (Сплавы, содержащие больше углерода, очень хрупкие). Этот участок диаграммы называют диаграммой состояния «Fe-FeC»
Основные структуры в сплавах системы «Fe-FeC»:
Феррит - твердый раствор внедрения углерода в Fea. Максимальная растворимость углерода достигает 0,02% при Т=727С. При комнатной температуре растворяется меньше 0,006% С. Твердость и механические свойства феррита близки к свойствам чистого железа (НВ=80).
Аустенит - твердый раствор внедрения углерода в Fey. При Т=1147 С аустенит содержит 2,14% С, а при Т=727 С – 0,8%. Аустенит пластичен, немагнитен, имеет твердость НВ=170-220.
Цементит- карбид железа Fe3C, образующийся при содержании углерода = 6,67 % С. Цементит имеет сложную орторомбическую решетку и очень высокую твердость (НВ=800), хрупкий.
Ледебурит- эвтектика системы «Fe – FeC», представляют механическую смесь цементита и аустенита, содержащая 4,3 % С.
Перлит- механическая смесь (эвтектоид), состоящая из мелких различных размеров пластинок цементита в ферритной основе, содержание углерода составляет 0,8%.
Алгоритм выполнения:
1. Внимательно ознакомиться с заданием.
2. Определить к какой группе сплавов относится заданный сплав.
3. Построить диаграмму состояния сплавов «Ғе-Ғе3С (Размером не менее 150×150 мм)
4. Обозначить все точки и структуры на диаграмме «Ғе-Ғе3С».
5. Провести на диаграмме «Ғе-Ғе3С» заданный сплав (вертикальную линию соответствующую по концентрации заданному сплаву).
6. Обозначить точки пересечения сплава с линиями диаграммы.
7. Рядом с построенной диаграммой «Ғе-Ғе3С» построить новую систему координат «Температура – время охлаждения» (Масштаб температур на диаграмме «Ғе - Ғе3С» и на вновь построенной системе координат должен совпадать).
8. Спроектировать точки пересечения заданного сплава с линиями диаграммы «Ғе- Ғе3С» на вновь построенную систему координат «Температура – время охлаждения».
9. Построить кривую охлаждения заданного сплава, соединив спроектированные точки отрезками линий с учётом тепловых эффектов, которые наблюдаются при превращениях в структуре сплавов (скорость охлаждения сплава, которая определяет наклон отрезков кривой охлаждения сплава, рекомендуется выбирать произвольно).
10. Охарактеризуйте превращения в структуре заданного сплава при медленном охлаждении.
Пример построения кривой охлаждения для сплава с содержанием углерода С=3,8%.
Заданный сплав с содержанием углерода - С =3,8% - это доэвтектический чугун.
1. Построение кривой охлаждения сплава
|
|
2. Превращения в сплаве при медленном охлаждении
Доэвтектический чугун (3,8 % углерода) охлаждается до температуры линии ликвидус в жидком состоянии. Первичная кристаллизация начинается на ликвидусе (точка-1) с выделения из жидкости аустенита. При охлаждении в интервале температур точек 1-2 количество аустенита увеличивается и соответствует при температуре точки 2 отрезку 2-С, а концентрация углерода в нем, изменяясь по линии солидус - JE, достигает предельной растворимости, равной 2,14 % (проекция точки Е). Одновременно к концу кристаллизации сохраняется некоторое количество жидкости (отрезок Е-2), концентрация углерода в которой, изменяясь по линии ликвидус ВС, соответствует эвтектическому составу (4,3 % углерода). В результате первичная кристаллизация завершается при температуре точки 2 (1147 °С) эвтектическим превращением; оставшаяся жидкость затвердевает в ледебурит на аустенитной основе (аустенитно-цементитная смесь). После кристаллизации сплав имеет структуру: аустенит и ледебурит на аустенитной основе (А + ЛА). При дальнейшем охлаждении в интервале точек 2-3, вследствие уменьшения растворимости углерода в аустените по линии ES, из аустенита выделяется цементит вторичный; аустенит при этом обедняется углеродом до 0,8 %. При температуре точки 4 (727 °С) аустенит, получивший эвтектоидный химический состав, превращается в перлит. Поскольку это превращение претерпевает и аустенит, входящий в состав ледебурита, то ледебурит на аустенитной основе становится ледебуритом на перлитной основе (перлитно-цементитная смесь). Окончательная структура сплава после охлаждения — перлит, ледебурит на перлитной основе и цементит вторичный (П + Лп + Ц2).
Варианты заданий
|
№ варианта |
Содержание углерода в сплаве, С % |
№ варианта |
Содержание углерода в сплаве, С % |
|
1. |
С = 0,3% |
9. |
С = 0,45% |
|
2. |
С = 3,5% |
10. |
С = 5,5% |
|
3. |
С = 1,2% |
11. |
С = 2,5% |
|
4. |
С = 0,8% |
12. |
С = 4% |
|
5. |
С = 6% |
13. |
С = 0,65% |
|
6. |
С = 4,3% |
14. |
С = 4,5% |
|
7. |
С = 0,9% |
15. |
С = 1,8% |
|
8. |
С = 0,55% |
16. |
С = 0,3% |
1. Какие линии на диаграмме «Ғе -Ғе3С» называются……..:?
солидус_______________________________________________________________________________________________________________________________________________
ликвидус______________________________________________________________________________________________________________________________________________
эвтектического превращения__________________________________________________
эвтектоидного превращения___________________________________________________
2. Что такое……?
феррит_____________________________________________________________________
аустенит____________________________________________________________________
перлит_____________________________________________________________________
цементит___________________________________________________________________
ледебурит__________________________________________________________________
3. В каких условиях выделяется первичный, вторичный цементит?
_____________________________________________________________________________________________________________________________________________________________
4. Каково строение ледебурита при комнатной температуре и немного ниже эвтектической температуры 1147°С?
________________________________________________________________________________________________________________________________________________________________
5. Что из себя представляют структуры: перлит, ледебурит?
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
6. Как содержание цементита в структуре Ғе–С-х сплавов влияет на свойства сплавов?
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() Диаграмма «Fe – Fe3C»
Кривая охлаждения
Диаграмма «Fe – Fe3C»
Кривая охлаждения
Т,С0 Т,С0 сплав ________
Анализ структурных составляющих:
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
ПРАКТИЧЕСКАЯ РАБОТА
ОЦЕНКА СВАРИВАЕМОСТИ СТАЛЕЙ
Цель работы: Приобретение навыков в расчете эквивалента углерода для различных марок сталей при определении свариваемости.
Методическое обеспечение:
- Методические указания при проведении практической работы
- Справочная литература
Последовательность выполнения практической работы:
1. Изучить методику расчета эквивалента углерода для различных марок сталей при определении свариваемости.
2. Выписать химический состав данной стали.
3. Рассчитать Сэкв для каждой марки стали и дать заключение о свариваемости.
4. Составить отчет.
5. Сделать выводы о работе.
6. Ответить на контрольные вопросы.
Основные теоретические положения:
Свариваемость сталей оценивается по четырехклассной системе:
ХС – хорошая свариваемость;
УС – удовлетворительная свариваемость;
ОС – ограниченная свариваемость;
ПС – плохая свариваемость.
Существует целый ряд методик оценки свариваемости. Одна из них: оценка свариваемости по эквиваленту углерода.
Определение свариваемости стали с учетом ее химического состава определяется по формуле:
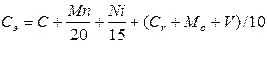 ,
(1)
,
(1)
где C, Mn, Ni, Cr, Mo, V - %-ое содержание компонентов в стали.
С учетом толщины металла поправка к эквиваленту углерода рассчитывается по формуле:
N = 0,005· S· Сэ, (2)
где N – поправка к эквиваленту углерода;
S – толщина свариваемого металла;
Сэ – эквивалент углерода;
0,005 – коэффициент толщины.
Полный эквивалент углерода рассчитывается по формуле:
Сэкв = Сэ(1 + 0,005·S), (3)
Стали, у которых Сэ = 0,2...0,45%, хорошо свариваются, не требуют предварительного подогрева и последующей термообработки.
Предварительный подогрев в случае необходимости может определяться по формуле:
![]() ,
(4)
,
(4)
Таблица 1 – Химический состав сталей
|
Марка стали |
ГОСТ |
Содержание элементов, % |
||||||
|
C |
Si |
Mn |
Cr |
Ni |
Cu |
Другие элементы |
||
|
Cт3пс |
380-94 |
0,14-0,22 |
0,05-0,17 |
0,40-0,85 |
<0.3 |
<0.3 |
<0.3 |
|
|
09Г2 |
19281-89 |
<0.12 |
0,17-0,38 |
1,40-1,80 |
<0.3 |
<0.3 |
<0.3 |
|
|
14Г2 |
19281-89 |
0,12-0,18 |
0,17-0,37 |
1,20-1,60 |
<0.3 |
<0.3 |
<0.3 |
|
|
17ГС |
19281-89 |
0,14-0,20 |
0,40-0,60 |
1,0-1,40 |
<0.3 |
<0.3 |
<0.3 |
|
|
09Г2С |
19281-89 |
<0,12 |
0,50-0,80 |
1,30-1,70 |
<0.3 |
<0.3 |
<0.3 |
|
|
10ХСНД |
19281-89 |
<0,12 |
0,80-1,10 |
0,50-0,80 |
0,6-0,9 |
0,5-0,8 |
0,4-0,6 |
|
|
10ХНДП |
19281-89 |
<0,12 |
0,17-0,37 |
0,30-0,60 |
0,5-0,8 |
0,3-0,6 |
0,3-0,5 |
Фосфор 0,070-0,012 |
Контрольные вопросы:
Содержание отчета:
Список литературы:
1.Куркин С. А., Николаев Г. А. Сварные конструкции. – М.: Высшая школа, 1991. – 398с.
2.Белоконь В.М. Производство сварных конструкций. – Могилев, 1998. – 139с.
3.Блинов А.Н., Лялин К.В.Сварные конструкции – М.: - «Стройиздат», 1990. – 352с.
Цель работы: расшифровать буквы и цифры в названии марок цветных металлов и сплавов
Оборудование: мультимедийный проектор
Основные теоретические сведения.
Классификация цветных сплавов.
2.1 Алюминий и алюминиевые сплавы
Деформируемые алюминиевые сплавы
Литейные алюминиевые сплавы
2.2 Медь и медные сплавы
Бронзы
Латуни
Сплавы меди с никелем
Титан, магний и их сплавы
Титан
Магний
Олово, свинец, цинк и их сплавы
Припои
Антифрикционные сплавы
2.1 Алюминий и его сплавы
Алюминий - легкий металл, обладающий высокими тепло- и электропроводностью, стойкий к коррозии. В зависимости от степени частоты первичный алюминий согласно ГОСТ 11069-74 бывает особой (А999), высокой (А995, А95) и технической чистоты (А85, А7Е, АО и др.). Алюминий маркируют буквой А и цифрами, обозначающими доли процента свыше 99,0% Al; буква "Е" обозначает повышенное содержание железа и пониженное кремния.
А999 - алюминий особой чистоты, в котором содержится не менее 99,999% Al;
А5 - алюминий технической чистоты в котором 99,5% алюминия. Алюминиевые сплавы разделяют на деформируемые и литейные. Те и другие могут быть не упрочняемые и упрочняемые термической обработкой.
Деформируемые алюминиевые сплавы хорошо обрабатываются прокаткой, ковкой, штамповкой. Их марки приведены в ГОСТ4784-74. К деформируемым алюминиевым сплавам не упрочняемым термообработкой, относятся сплавы системы Al-Mn и AL-Mg:Aмц; АмцС; Амг1; АМг4,5; Амг6. Аббревиатура включает в себя начальные буквы, входящие в состав сплава компонентов и цифры, указывающие содержание легирующего элемента в процентах. К деформируемым алюминиевым сплавам, упрочняемым термической обработкой, относятся сплавы системы Al-Cu-Mg с добавками некоторых элементов (дуралюны, ковочные сплавы), а также высокопрочные и жаропрочные сплавы сложного хим.состава. Дуралюмины маркируются буквой "Д" и порядковым номером, например: Д1, Д12, Д18, АК4, АК8.
Чистый деформируемый алюминий обозначается буквами "АД" и условным обозначением степени его чистоты: АДоч (>=99,98% Al), АД000(>=99,80% Аl), АД0(99,5% Аl), АД1 (99,30% Al), АД(>=98,80% Аl).
Литейные алюминиевые сплавы (ГОСТ 2685-75) обладает хорошей жидко-текучестью, имеет сравнительно не большую усадку и предназначены в основном для фасонного литья. Эти сплавы маркируются буквами "АЛ" с последующим порядковым номером: АЛ2, АЛ9, АЛ13, АЛ22, АЛЗО.
Иногда маркируют по составу: АК7М2; АК21М2, 5Н2,5; АК4МЦ6. В этом случае "М" обозначает медь. "К" - кремний, "Ц" - цинк, "Н" - никель; цифра - среднее % содержание элемента.
Из алюминиевых антифрикционных сплавов (ГОСТ 14113-78) изготовляют подшипники и вкладыши как литьем так и обработкой давлением. Такие сплавы маркируют буквой "А" и начальными буквами входящих в них элементов: А09-2, А06-1, АН-2,5, АСМТ. В первые два сплава входят в указанное количество олова и меди (первая цифра-олово, вторая-медь в %), в третий 2,7-3,3% Ni и в четвертый медь сурьма и теллур.
2.2 Медь и её сплавы
Технически чистая медь обладает высокими пластичностью и коррозийной стойкостью, малым удельным электросопротивлением и высокой теплопроводностью. По чистоте медь подразделяют на марки (ГОСТ 859-78).
После обозначения марки указывают способ изготовления меди: к - катодная, б - бес кислородная, р - раскисленная. Медь огневого рафинирования не обозначается.
МООк - технически чистая катодная медь, содержащая не менее 99,99% меди и серебра.
МЗ - технически чистая медь огневого рафинирования, содержит не менее 99,5%меди и серебра.
Медные сплавы разделяют на бронзы и латуни. Бронзы- это сплавы меди с оловом (4 - 33% Sn хотя бывают без оловянные бронзы), свинцом (до 30% Pb), алюминием (5-11% AL), кремнием (4-5% Si), сурьмой и фосфором (ГОСТ 493-79 , ГОСТ 613-79, ГОСТ 5017-74, ГОСТ 18175-78).
Латуни - сплавы меди с цинком (до 50% Zn) и небольшими добавками алюминия, кремния, свинца, никеля, марганца (ГОСТ 15527-70, ГОСТ 17711-80). Медные сплавы предназначены для изготовления деталей методами литья, называют литейными, а сплавы, предназначенные для изготовления деталей пластическим деформированием - сплавами, обрабатываемыми давлением.
|
А - алюминий |
Су - сурьма |
|
Мц - марганец |
К - кремний |
|
С - свинец |
Н - никель |
|
Б - бериллий |
Т - титан |
|
Мг - магний |
Кд - кадмий |
|
Ср - серебро |
О - олово |
|
Ж - железо |
Ф - фосфор |
|
Мш - мышьяк |
Х - хром |
|
|
Ц - цинк |
Медные сплавы обозначают начальными буквами их названия (Бр или Л), после чего следуют первые буквы названий основных элементов, образующих сплав, и цифры, указывающие кол-во элемента в процентах. Приняты следующие обозначения компонентов сплавов
:
Примеры: БрА9Мц2Л - бронза, содержащая 9% алюминия, 2% Mn, остальное Cu ("Л"' указывает, что сплав литейный);
ЛЦ40Мц3Ж - латунь, содержащая 40% Zn, 3% Mn, ~l% Fe, остальное Cu;
Бр0Ф8,0-0,3 - бронза на ряду с медью содержащая 8% олова и 0,3% фосфора;
ЛАМш77-2-0,05 - латунь содержащая 77% Cu, 2% Al, 0,055 мышьяка, остальное Zn (в обозначении латуни, предназначенной для обработки давлением, первое число указывает на содержание меди).
В несложных по составу латунях указывают только содержание в сплаве меди:Л96 - латунь содержащая 96% Cu и ~4% Zn (томпак);
Лб3 - латунь содержащая 63% Cu и -37% Zn.
Марки меди и её применение

Порядок выполнения работы
1. Изучить характеристики и расшифровку марок алюминия и его сплавов, меди и её сплавов, изложенных в теоретической части работы.
2. Произвести расшифровку предложенных марок материалов таблицы 1, полученные результаты записать в таблицу 2.
Таблица 1
|
1) БСт3кп |
9) БрАЖНЮ-4-4 |
|
2) АЛ9 |
10) БрА7Мц15ЖЗН2Ц2 |
|
3) БрОФ4-0 |
11) ЛЦ23АбЖЗМц2 |
|
4) БрСуЗНЗЦЗС20Ф |
12) БрКМцЗ-1 |
|
5) ЛЦ40МцЗА |
13) Бр06Ц6СЗ |
|
6) ЛЖМц59-1-1 |
14) ЛАНКМц75-2-2 |
|
7) ЛС59-1 |
15) АК4М4.ВТ22 |
|
8) Л68 |
16) АК9 |
Таблица 2
|
№ |
Марка |
Химические элементы и их содержание
|
|
1 |
Пример ЦАМ10-5Л |
содержит 9,0-12,4%Al, 4,0-5,5% Cu, 0,03-0,06% Mg, временное сопротивление не менее 250 МПа, пластичность не менее 0,4%, твердость -не менее 100HB. Из сплава изготавливают подшипники и втулки металлообрабатывающих станаков, прессов, работающих под давлением до200-10000 Па. |
|
2 |
|
|
|
3 |
|
|
|
4 |
|
|
3. Оформить отчёт работы
4.Ответить на контрольные вопросы
Контрольные вопросы
1. Опишите основные свойства меди.
2. Какие примеси меди значительно снижают пластичность и электропроводность?
3. Как влияет кислород, висмут, сера на структуру и свойства меди?
4. Опишите влияние цинка на свойства латуней.
5. Опишите влияние легирующих элементов на свойства бронз.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.