
Дата:
Класс: 10
Учитель:
Предмет: Химия
Тема: «Амины: метиламин и анилин»
Контролируемые элементы содержания
Применение изученных органических веществ
Контролируемые умения
Характеризовать строение и химические свойства изученных органических соединений
Проверяемые элементы содержания
Вредные привычки и факторы, разрушающие здоровье (курение, наркомания)
Предметные умения
Использовать знания о составе, строении и химических свойствах веществ для безопасного применения в практической деятельности
Личностные результаты
Сформированность основ экологической культуры, соответствующей современному уровню экологического мышления
Функциональная грамотность
Оценивать научные аргументы и доказательства из различных источников (например, газета, интернет, журналы)
Тип урока: Комбинированный урок
Библиотека ЦОК: https://lesson.edu.ru/lesson/0c608a59-4c69-4481-839e-9205f201b73e?backUrl=%2F04%2F10%3Fterm%3D%25D0%25B0%25D0%25BC%25D0%25B8%25D0%25BD%25D1%258B
БЛОЧНО-МОДУЛЬНОЕ ОПИСАНИЕ УРОКА:
1. Вхождение в тему урока и создание условий для осознанного восприятия нового материала
1.1 Мотивация на учебную деятельность
Здравствуйте, садитесь!
Сегодня мы продолжаем изучение органических соединений и рассмотрим тему «Амины» и разберемся, какие химические элементы входят в состав аминов.
1.2 Актуализация опорных знаний
Какие классы органических соединений мы изучали?
Что такое углеводы? Общ формула ?
1.3 Целеполагание
Сформулируйте цели урока вместе с детьми:
Цели урока:
· образовательные: рассмотреть строение, классификацию и свойства класса аминов; закрепить знания учащихся о причинах многообразия аминов; познакомить с областями применения аминов;
· развивающие: сформировать у учащихся логическое мышление, умение самостоятельно мыслить, передавать информацию;
· воспитательные: сформировать положительное отношение к изучению предмета, умение выслушивать своих товарищей, воспитывать творчески мыслящую личность.
План урока.
1. Понятие об аминах.
2. Номенклатура.
3. Классификация.
4. Изомерия.
5. Физические свойства.
6. Химические свойства.
7. Применение.
2 Освоение нового материала
2.1 Осуществление учебных действий по освоению нового материала
Мы с вами рассматривали кислородсодержащие органические соединения. В органической химии есть соединения, которые кроме углерода, водорода, кислорода содержат элемент азот. К ним относятся амины, аминокислоты, белки, нуклеиновые кислоты, азотсодержащие гетероциклические соединения. Эти соединения играют важную роль в повседневной жизни. Мы начинаем изучать азотсодержащие органические соединений. Тема нашего урока сегодня – амины
Амины в природе образуются при гниении живых организмов. Амины – это производные аммиака, в молекулах которого один, два или три атома водорода замещены на углеводородные радикалы .Общая формула – R-NH2.
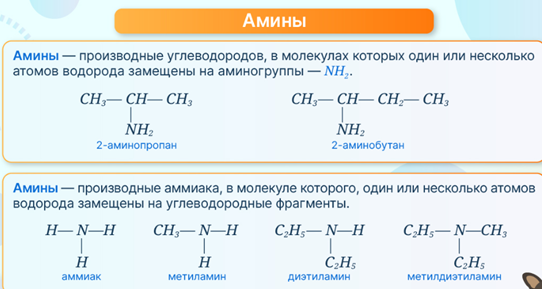
Ø Номенклатура
Названия даются путем перечисления радикалов с добавлением слова амин.
Например:
СН3 – NН2 метиламин;
СН3 – NН–С2Н5 метилэтиламин;
СН3 – N(СН3)–СН3 триметиламин;
С6 Н5 – NН2 фениламин.
Различные радикалы перечисляются в алфавитном порядке.
Например: CH3-CH2-NH-CH3 метилэтиламин.
При наличии одинаковых радикалов используют приставки ди и три.
Например: (CH3)2NH диметиламин.
Первичные амины часто называют как производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на аминогруппы -NH2. В таком случае аминогруппа указывается в названии суффиксами амин (одна группа -NH2), диамин (две группы -NH2) с добавлением цифр, отражающих положение этих групп в углеродной цепи.
v Классификация аминов.
В зависимости от радикала, амины бывают (Слайд ):
– предельные (см. ниже);
– непредельные СН2 = СН–NН2;
– ароматические С6Н5–NН2.
· В зависимости от строения аминогруппы, бывают
– первичные R-NH2. Например: СН3–NН2, СН3–СН2–СН2–СН2 –NН2
– вторичные R-NH-R1. Например: СН3–NН–С2Н5
– третичные RN(R1)R2. Например: СН3–N(СН3)–СН3
v Химические свойства
Взаимодействие с водой:
Водные растворы аминов имеют щелочную реакцию (амины реагируют с водой по донорно-акцепторному механизму)
CH3 – NH2 + HOH = CH3 – NH3OH (CH3 – NH3 + + OH-)
(гидроксид метиламмония)
Взаимодействие с кислотами
CH3 – NH2 + HCl = CH3 – NH3 Cl
(хлорид метиламмония)
Реакция горение
4CH3 – NH2 +9O2 =2N2 +10H2O +4СО2.
v Физические свойства
С1– С3 газы, с запахом аммиака.
С4– С9 жидкости с запахом тухлой рыбы, хорошо растворяются в воде.
С10 твердые, нерастворимые вещества в воде, не имеющие запаха.
v  Изомерия
Изомерия
![]()
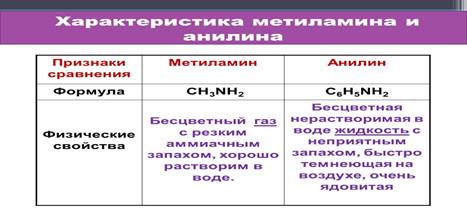
v 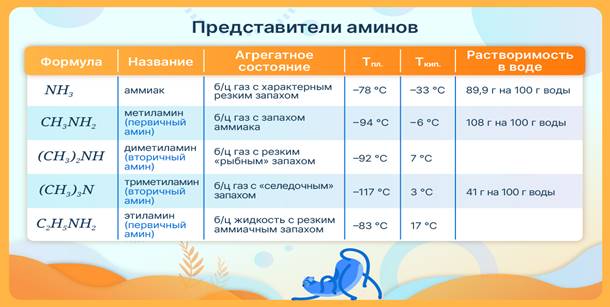 Анилин (фениламин)
С6H5NH2 – ароматический амин. Анилин это
бесцветная маслянистая жидкость с характерным запахом (т. кип. 184 °С, т. пл. –
6 °С). На воздухе окисляется и приобретает красно-бурую окраску. Ядовит. Анилин
широко применяется в производстве красителей, взрывчатых веществ и
лекарственных средств (сульфаниламидные препараты).
Анилин (фениламин)
С6H5NH2 – ароматический амин. Анилин это
бесцветная маслянистая жидкость с характерным запахом (т. кип. 184 °С, т. пл. –
6 °С). На воздухе окисляется и приобретает красно-бурую окраску. Ядовит. Анилин
широко применяется в производстве красителей, взрывчатых веществ и
лекарственных средств (сульфаниламидные препараты).
История открытия анилина. Унфердорбен, химик в Даме (Саксония) нашел в 1826 г. между продуктами сухой перегонки индиго маслообразное вещество, названное им кристалином .Несколько лет спустя Рунге в Берлине открыл в каменноугольном дегте соединение, дающее с хлорной известью фиолетовое окрашивание, дал ему название цианода (голубого масла).
Поздние, академик Фрицше в Петербурге, изучал соединения, нашел маслообразное вещество которое назвал анилином, (от португальского названия индиго – “Anil”).
В 1842 г. знаменитому русскому химику Н. Н. Зинину удалось из бензола, заключающегося в каменноугольном дегте, получить восстановлением нитробензола маслообразное тело, названное им бензидамом.
В 1843 г. Гофман показал, что четыре тела: кристалин, цианол, анилин и бензидам тождественны между собою и дал название – анилин.
Получение анилина (реакция Зинина) .
С6Н5–NО2+6Н![]() С6Н5–NН2 +
2Н2О (Уравнение написано схематично.)
С6Н5–NН2 +
2Н2О (Уравнение написано схематично.)
v Метиламин представляет собой органическое соединение с формулой CH3NH2. Этот бесцветный газ является производным аммиака, но с одним атомом водорода, замененным метильной группой. Это простейший первичный амин.
Ø
 |
Основные свойства аминов предельного
ряда выражены сильнее. Слабые основные свойства ароматических аминов
объясняется влиянием групп атомов в органических веществах, например,
бензольного кольца на аминогруппу. Бензольное кольцо притягивает к себе
электроны атома азота, уменьшая электронную плотность на атоме азота,
следовательно, уменьшается способность присоединения протона (катиона) водорода
и основные свойства уменьшаются СН3NH2![]() NH3
NH3![]() C6H5NH2
C6H5NH2
2.2. Проверка первичного усвоения
Задание. Попробуйте составить по 2 возможные формулы аминов и назвать полученные вещества, если молекулярная формула аминаC4H11N.
Решение : ?
Задание: Составьте структурные формулы первичного, вторичного и третичного аминов, имеющих состав C4H11N. Назовите все вещества.
Решение:
H3C-CH2-CH2-CH2-NH2___1-аминобутан
H3C-CH2-CH(NH2)-CH3___2-аминобутан___втор-бутиламин
H3C-CH(CH3)-CH2-NH2___1-амино-2-метилпропан___изо-бутиламин
H3C-C(СH3)2-NH2___2-амино-2-метилпропан___трет-бутиламин
H3C-NH-CH2-CH2-CH3___1-(N-метил) аминопропан___метилпропиламин
H3C-CH2-NH-CH2-CH3___N-этиламиноэтан___диэтиламин
H3C-CH(CH3)-NH-CH3___2-(N-метил) аминопропан___изо-пропилметиламин
H3C-N(CH3)-CH2-CH3___N,N-диметиламиноэтан___диметилэтиламин

3 Применение изученного материала.
3.1 Применение знаний, в том числе в новых ситуациях


3.2  Систематизация
знаний и умений
Систематизация
знаний и умений
4.

 Проверка
приобретенных знаний, умений и навыков
Проверка
приобретенных знаний, умений и навыков
 4.1 Диагностика/самодиагностика
4.1 Диагностика/самодиагностика
5. Подведение итогов, домашнее задание
5.1 Рефлексия
![]()

5.2 Домашнее задание.
Информация по теме : «Применение анилина и метиламина».
– Написать реакцию взаимодействия метиламина с серной кислотой.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.