
Атомные спектры. Закон Мозели . Принцип Паули.
С увеличением атомного номера элемента его характеристический спектр смещается в сторону более коротких волн, то есть в ультрафиолетовую, а затем в рентгеновскую область. Частоты характеристических рентгеновских лучей могут быть сгруппированы в 3 серии: К, L, М(РИС.11.12). Лучи серии К наиболее, а серии М-наименее жесткие. Первые возникают у элементов с меньшими атомными массами, а точнее с меньшим порядковым номером атома Z в системе Д. И. Менделеева. Закон Мозели был описан уравнением
![]() , из которого следует, что квадратные корни частот
характеристического рентгеновского излучения атомов элементов линейно зависят
от атомных номеров Z. Здесь р-константа, неизменная для данной серии; S- поправка на экранирование заряда ядра электронами,
близкая к 1 и ослабляющая силовое поле ядра. Закон Мозели раскрывает смысл
периодического закона Менделеева : свойства элементов зависят от атомного
номера. С количественной стороны выражение 11.3 можно для Кα –серии
переписать в форме ν= 2,47
, из которого следует, что квадратные корни частот
характеристического рентгеновского излучения атомов элементов линейно зависят
от атомных номеров Z. Здесь р-константа, неизменная для данной серии; S- поправка на экранирование заряда ядра электронами,
близкая к 1 и ослабляющая силовое поле ядра. Закон Мозели раскрывает смысл
периодического закона Менделеева : свойства элементов зависят от атомного
номера. С количественной стороны выражение 11.3 можно для Кα –серии
переписать в форме ν= 2,47![]() 10 15 (Z-s)2 =
10 15 (Z-s)2 = ![]() R(Z-s)2
R(Z-s)2 ![]() R(1/12-1/22) · (Z-s)2, где 22 есть n
R(1/12-1/22) · (Z-s)2, где 22 есть n![]() . Eсли n2=2, находим частоты серии Кα, если n 2 =3 – серии Кβ , если n2=4- серии Кγ. Уровни,
различающие главными квантовыми числами , обозначаются следующим образом:
. Eсли n2=2, находим частоты серии Кα, если n 2 =3 – серии Кβ , если n2=4- серии Кγ. Уровни,
различающие главными квантовыми числами , обозначаются следующим образом:
Главное квантовое число 1 2 3 4 5 6
Обозначение уровня К L М N O P
Уровни, различающиеся побочными квантовыми числами, обозначаются так: побочное квантовое число 0 1 2 3 4
Обозначение подуровня s р d f g
Принцип Паули- в атоме не может быть двух электронов со всеми четырьмя одинаковыми квантовыми числами.
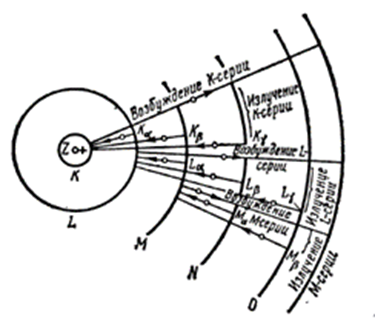
Рис.11.12 Происхождение К-,L-,и М-серий (схема).
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.