
Тема: «Физическая химия и кристаллохимия полупроводников».
1.Фазовый анализ – это комплексное изучение вещества.
Осуществляется множеством разных методов: физико – химическим, рентгеновским, электроно- и нейтронографическим, оптическим, электрофизическим, гальваномагнитным.
2.Содержание физико-химического анализа включает много ветвей:
термографический анализ, металлографический, рентгенографический,
нейтронографический . Диаграммы состав-свойство , диаграммы состояния являются важным обьектом этого анализа.
3.Метод термографического анализа и диаграммы плавкости:
изучается процесс нагревания или охлаждения вещества во времени.
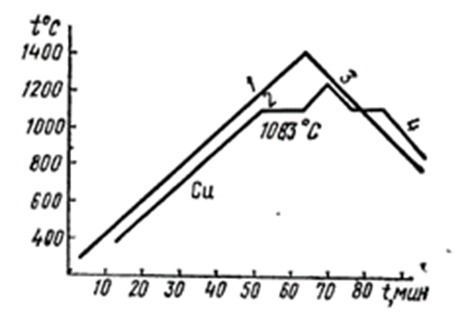
Рис.11.1«Кривые нагревания и охлаждения однокомпонентных систем (медь)»:
1 и 3 - нагревателя; 2 и 4 – образца
При равномерном повышении температуры нагревателя на кривой нагревания образца Т=f(t) где t-время (кривая 1), при T=1083°C(точка плавления меди)появляется горизонтальная площадка, которая сохраняется до тех пор, пока меди не будет сообщена вся необходимая скрытая теплота плавления и вся медь не расплавится. Затем температура образца снова растет . При равномерном охлаждении нагревателя (кривая 3)около той же точки на кривой T=T плавления образца (кривая 4)также наблюдается горизонтальная площадка, вызванная выделением скрытой теплоты плавления. Химические соединения постоянного состава ,например NаCl , ведут себя аналогично.
При исследовании бинарных систем (состоящих из компонентов A и В) строятся диаграммы состояния , по оси абсцисс откладывается содержание В в массовых долях либо атомных долях в процентах, по оси ординат –величина некоторого свойства :либо точки плавления (ось температур), либо значения других свойств, например электрической проводимости , твердости.
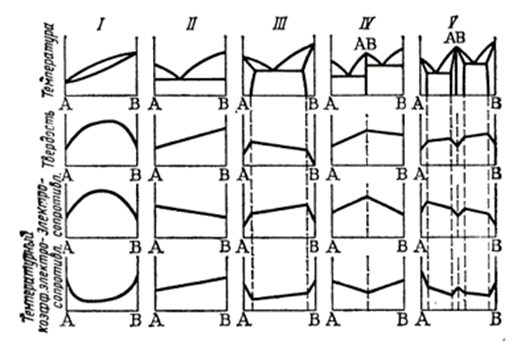
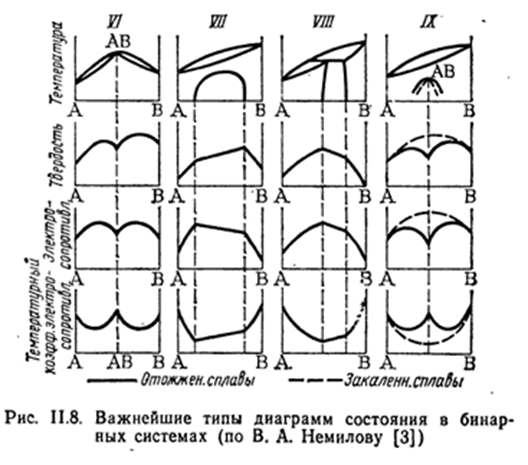
4. Бинарные системы (типы диаграмм)
Эвтектическая диаграмма состояния без областей твердых растворов
Эвтектическая диаграмма состояния без твердых растворов (построение ее на рис.11.2 а, вид диаграммы-рис.11.2 b)имеет два максимума, отвечающие чистым компонентам А и В, и четкий минимум, отвечающий эвтектической точке Е. Кривые охлаждения составов А, В,Е показывают горизонтальные площадки(см.рис.2.1,кривая 4),отвечающие температуре кристаллизации расплава. Эти точки (ТА, Тв,ТE)наносятся на диаграмму состояния. На рис.11.2.b видно ,как диаграмма распадается на три поля: верхнее поле расплава L,снизу ограниченное кривой ликвидуса l, нижнее поле твердых фаз S, ограниченное сверху кривой солидуса s, и между кривыми l и s-область кристаллизации (О.К.). Кривые ликвидуса и солидуса соприкасаются в эвтектической точке E. Точка на диаграмме состояния , отвечающая составу образца и отражающая условия существования системы, называется фигуративной. Составы, отвечающие фигуративным точкам на диаграмме Ф1 и Ф2, остывают с постоянной скоростью до точек l´A, l´в (на кривой ликвидуса), и кривые охлаждения испытывают в этих точках перелом(уголγ на рис.11.2,а). По температурам таких точек на кривой охлаждения находится кривая ликвидуса диаграммы плавкости. Проследим на примере состава Ф2 ход охлаждения. В точке l´в, отвечающей температуре Т´В, начинается область кристаллизации. Дальнейшее охлаждение сопровождается выпадением кристаллов состава В, причем состав расплава смещается в сторону эвтектики. Так в точке К´В при Т´В состав расплава l´в; в точке К″В при Т″ В состав расплава l″В; В точке К‴ В при ТЕ состав расплава отвечает эвтектике; кристаллизуется эвтектический состав, представляющий в фазовом отношении механическую мелкодисперсную смесь обеих фаз А+В.
Так как кристаллизация происходит уже не в одной температурной точке(как в случае чистых веществ или эвтектики), а в интервале температур Т′в-ТЕ, то на кривой охлаждения вместо горизонтальной площадки появляется ветвь с менее крутым спадом температур , чем на предыдущем участке кривой: охлаждение тормозится выделением скрытой теплоты кристаллизации. По достижении точки солидуса К‴В кристаллизуется эвтектическая смесь; на кривой охлаждения –горизонтальная площадка. При температуре солидуса ТЕ кристаллизация закончена и наблюдается новый перелом кривой охлаждения: начинается более быстрый спад температуры( рис.11.2,а, кривая Ф2). По таким точкам перелома определяется ход кривой солидуса.
При застывании состава Ф1 обнаруживается такая же картина с той разницей, что выделяется твердая фаза А , а не В, а состав расплава приближается к составу эвтектики, пока при температуре ТE не закристаллизуется эвтектическая смесь Е(30 ат. долей ,%В).
Форма эвтектической диаграммы зависит от разности температур плавления A и В. Если температуры плавления близки, точка Е лежит примерно посередине диаграммы. Если температуры плавления сильно отличаются, точка Е смещается к точке плавления низкоплавкого компонента и в пределе сливается или почти сливается с ней(см.рис.11.2,c).
Результаты микроскопического изучения шлифов (рис.11.2.е). Наша диаграмма состояния (рис.11.2.b) содержит два компонента А и В, фазовая картина которых бывает различна. На рис.11.2,е А-светлые гексагональные призмы, В- темные кубы. В шлифах чистых исходных веществ кристаллы занимают все поле шлифа (А, В). В шлифах состава , отвечающего точке эвтектики Е, происходит очень быстрая (ширина области кристаллизации практически равна нулю) кристаллизация обеих твердых фаз. В микроскоп видна механическая смесь мельчайших кристаллов фаз А и В, тесно переплетенных друг с другом. Она очень прочная. Соотношение обеих фаз в шлифе зависит от содержания компонента В в точке Е. В этом примере(Е)его всего 30 ат. долей % ,то есть в шлифе преобладает фаза А. Еще меньше компонента В в сплаве состава Ф1-20 атом.долей, %. Поэтому на шлифе Ф1 заметно очень сильное преобладание фазы А. Но не только это. На шлифе Ф1 имеются только мелкие кристаллы В, входящие в состав эвтектики; кристаллы же А двух типов : мелкие , тоже эвтектического в основном происхождения , и крупные. Крупные кристаллы выросли на тех немногочисленных зародышах фазы А, которые выделились около точки l′A и медленно росли , пока система охлаждалась от температуры ликвидуса до температуры солидуса. По отношению размеров полей крупных кристаллов А к размерам полей эвтектики можно оценить положение точки Ф1 на диаграмме. Составу Ф2 отвечает свыше 85 ат. долей ,%,В. Поле этой фазы (шлиф Ф2) уже значительно превалирует .Имеются не только мелкие, но и крупные кристаллы В.
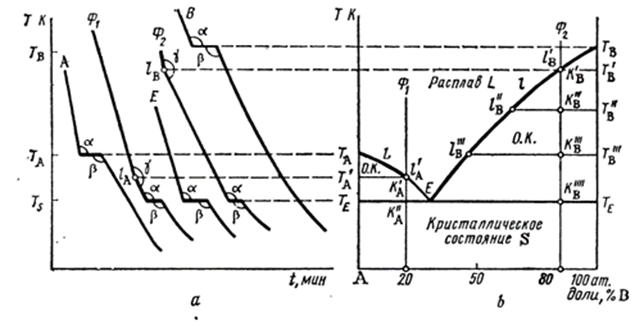
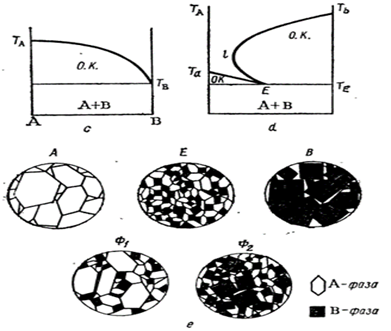
Рис.11.2 Эвтектическая диаграмма состояния : а-кривые охлаждения, отвечающие разным фигуративным точкам; b,с,d-вид диаграммы состояния ;e-микроскопическая картина шлифов составов, отвечающих фигуративным точкам на рис. а и b
5. Дистектическая диаграмма состояния без областей твердых растворов.
В системе А-В образовалось химическое соединение, например АВ, тогда на диаграмме состояния возникает дистектическая точка D, разделяющая диаграмму на две эвтектические диаграммы с эвтектическими точками Е1 и Е2 (рис.11.3,а). Заслуживает внимания острота пика дистектики. Если пик острый, то плавление не сопровождается заметной диссоциацией соединения АВ в расплаве ; если пик пологий , то плавление АВ сопровождается диссоциацией на компоненты А и В в расплаве. Однако в обоих случаях состав расплава тождествен составу твердого АВ , то есть плавление является конгруэнтным . Если соединение АВ плавится с разложением на твердую фазу и расплав (по реакции АВТВ→AТВ+L, то такое плавление является инконгруэнтным.
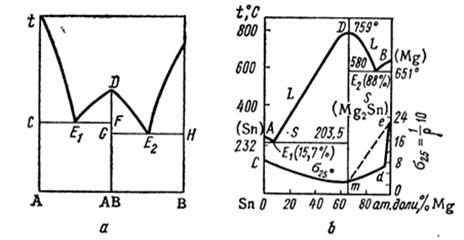
Рис.11.3.Дистектическая диаграмма состояния :
а-общий вид диаграммы с дистектической точкой; b-диаграмма состояния системы Mg2-Sn.
6.Эвтектическая диаграмма состояния с областями твердых растворов:
На самом деле на практике почти всегда обнаруживается хотя бы ничтожная , но все же растворимость, и вместо диаграммы рис.11.2.,b наблюдается образование диаграммы с областями твердых растворов β и α , о которых подробно указано например в главе 8 учебника Б.Ф.Ормонт «Введения в физическую химию и кристаллохимию полупроводников».
Рассмотрим диаграмму на рис.11.4,а, которая указывает на то, что есть отличие от диаграммы 11.2,b: при охлаждении расплава , отвечающего фигуративной точке Ф1(рис.11.4.a), до температур на бесконечно малую величину ниже температур кривой ликвидуса выпадают кристаллы не чистой фазы A, а твердого раствора В в А и притом состава , отвечающего точке кривой солидуса , в которую упирается горизонтальный «рычаг». Так , расплаву состава l´ отвечает состав кристаллов s´, расплаву состава l″-расплав кристаллов s″. Наконец , при температуре ТЕ из расплава , отвечающего эвтектической точке Е, выпадает механическая смесь кристаллов α-фазы (являющихся твердым раствором 10 ат.долей,% В в А) и кристаллов β-фазы (являющихся твердым раствором 21 ат.доли, %A в В), что отвечает диаграмме рис.11.4,а.
Если охлаждение происходит очень медленно, то ранее выпавшие кристаллы одной фазы обмениваются веществом с кристаллами другой фазы и состав обеих фаз все время приближается к равновесному , то есть обедняется примесью второго компонента. На рис.11.4.b видно, при кристаллизации составов, лежащих влево от эвтектической точки выпадает твердый раствор меди в серебре(фаза α), при кристаллизации составов лежащих вправо от эвтектической точки –твердый раствор серебра в меди(фаза β).При температуре ТЕ=779°С состав этих твердых растворов равен 8,8, соответственно 8,0 масс.доли, %растворенного компонента. Из диаграммы рис.11.4.b видно, что при охлаждении от 779°С до комнатной температуры состав кристаллов становится близким к 100%-ным серебру и меди. Если же охлаждение от 779°С осуществить быстро, возникнут закаленные твердые растворы с примерно 8% примеси второго компонента. На этом рис.11.4.b внизу на оси абсцисс (х )дан масштаб в массовых долях в %, вверху -масштаб дан в атомных долях в % и видно, что различия очень значительны.
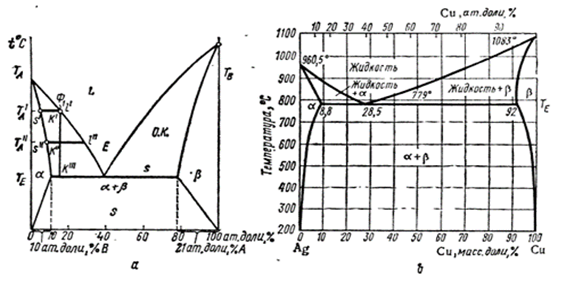
Рис.11.4.Эвтектическая диаграмма состояния с твердыми растворами:а-общий вид диаграммы;b-диаграмма системы Ag-Cu
7.Дистектическая диаграмма состояния с областями твердых растворов:
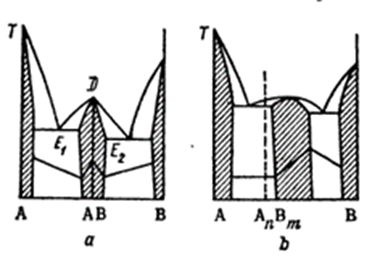
Рис.11.5 Дистектические диаграммы состояния с твердыми растворами :а-c дальтонидной фазой;b-c бертоллидной фазой. Пологий пик на кривой не только ликвидуса, но и солидуса, то есть фаза диссоциирует и в жидком и в твердом состояниях.
Диаграмма состоит из двух эвтектических диаграмм с областями твердых растворов при наличии одной дистектической точки D, разделяющей диаграмму. Так как дистектической точке часто отвечает стехиометрический состав, например АВ, то Н.С.Курнаков предложил называть такие точки дальтоновскими . К каждой из этих частей диаграммы полностью относится сказанное выше об эвтектической диаграмме с твердыми растворами. Фаза переменного состава , в пределах области гомогенности которой находится дальтоновская точка, называется дальтонидом или дальтонидной фазой. Причем на кривых состав –свойство этой точке соответствует максимум (например точка плавления на рис.11.5,а) или минимум (например точка на кривой электросопротивления, см.рис.11.8,V). В случае дальтоновской точки (рис.11.5,a) можно сделать вывод о присутствии в системе соединения переменного состава . Существует еще одна диаграмма (на рис.11.5,b) указывающая на отсутствие максимумов или минимумов на кривых свойств в пределах твердого раствора . Н. С. Курнаков обьяснил это так «если соединение, на котором основана фаза , лежит за пределами области гомогенности, такая фаза называется бертоллидной или бертоллидом».(Бертоллиды Курнакова).
8.Диаграммы состояния непрерывных твердых растворов. Типы диаграмм в бинарных системах.
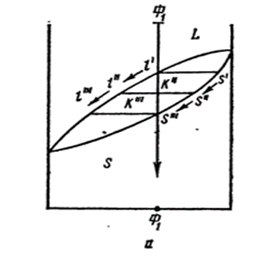
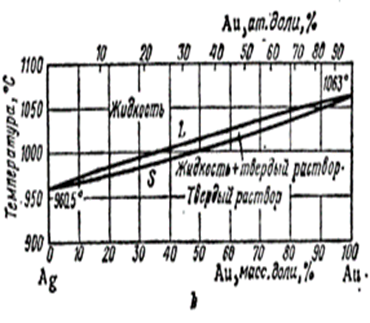
Рис.11.6 а-ход кристаллизации в таких системах, b-диаграмма состояния в системе Ag-Au.

Если А и В по строению электронных оболочек атомов , по их радиусам и энергиям химических связей достаточно близки друг другу и их замена друг другом не связана с затруднениями структурного и энергетического характера, то обычно возникают непрерывные твердые растворы(рис.11.6,а). Над кривой ликвидуса Ɩ лежит область расплава L, под кривой солидуса s-область твердого раствора S, между ними –область кристаллизации (об этом подробно рассказывает в учебнике «Введение в физическую химию и кристаллохимию полупроводников « Б.Ф.Ормонт гл.4). Рассмотрим особенности кристаллизации систем этого типа (рис.11.6.,а). Исходя из состава,отвечающего фигуративной точке Ф1, охлаждаем расплав до точки Ɩ′.
Начинают выпадать кристаллы состава S′. При охлаждении до точки К″выпадают кристаллы S″,состав расплава отвечает точке Ɩ″. По мере охлаждения состав кристаллов изменяется по кривой S′-S″-S‴,состав расплава –по кривой Ɩ′-Ɩ″-Ɩ‴. В точке S‴расплав окончательно застынет. Соотношение количеств выпавших кристаллов и расплава равно отношению КƖ :KS рычага Ɩ S. Если охлаждение проводить очень медленно , кристаллы все время обмениваются веществом с расплавом , становясь все ближе к составу S″, отвечающему фигуративной точке Ф1. Ecли охлаждение протекает быстро, то образуется механическая смесь кристаллов разных составов .Если вычерпывать выкристаллизовавшиеся первыми порции, более богатые тугоплавким компонентом, что неоднократным повторением процесса можно создать фракции , сильно обогащенные как А, так и В.
9.Диаграммы состояния тройных систем :
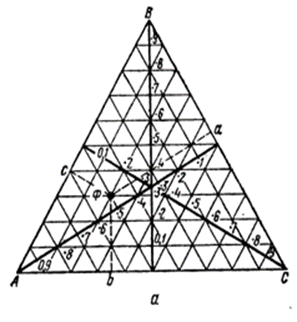
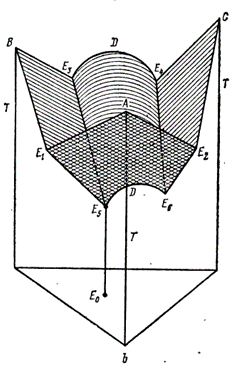
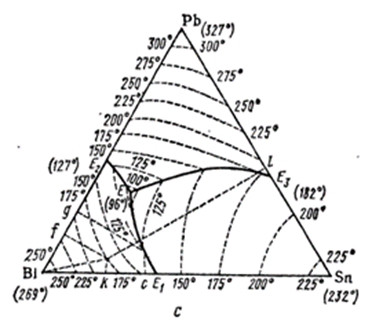

Тройная система A-B-C построена в виде треугольной диаграммы Гиббса (симметричная) или несимметричными диаграммами Ормонта. В первом случае чтобы определить состав фигуративной точки Ф опущены перпендикуляры к сторонам диаграммы(рис.1.9,a).Высота таких перпендикуляров в долях высоты треугольника показывает концентрацию компонента , символ которого помещен в противоположной вершине треугольника. Значение свойства задается двумя способами: высотой перпендикуляра (например Е0 Е5 на рис.11.9 b)к данной точке; совокупность вершин перпендикуляров образует поверхность представляющую зависимость состав – свойство в данной тройной системе или , 2)кривыми , отражающими на диаграмме геометрические места точек с равными свойствами . На рис.11.9, с показана диаграмма плавкости системы Вi-Рb-Sn, построенная по способу 2.
На рис.11.9, b компоненты В и С образуют дистектическую диаграмму с эвтектиками Е3 и Е4. Компоненты А и В, а также A и С образуют эвтектические диаграммы с эвтектиками Е 1 и Е 2 и, наконец , возникают тройные эвтектики Е 5 и Е 6 . Если соединения являются сложными (что часто имеет место при синтезе диэлектриков), то введение несимметричной диаграммы дает существенные преимущества .
Концентрация любого простого оксида может быть представлена эквипотенциальными прямыми, которые для каждого оксида проходят под определенными углами к сторонам диаграммы (рис.11.10,b). Отложив на сторонах последней концентрационный масштаб и используя шаблоны, стороны которых направлены под углами, отвечающими эквипотенциальным линиям(рис.11.11, а), можно без всякого расчета найти по положению точки ее состав в простых оксидах . По химическому составу же можно найти сразу фигуративную точку(рис.11.11, б). Для этой цели нужно знать содержание некоторых (например двух или трех) простых оксидов , ибо в идеальном случае все прямые должны пересечься в одной точке S .Можно непосредственно связать химический и фазовый состав с ходом температур плавления, механических, оптических, электрических, и магнитных свойств фигуративных точек , значительно сократить количество аналитических определений.
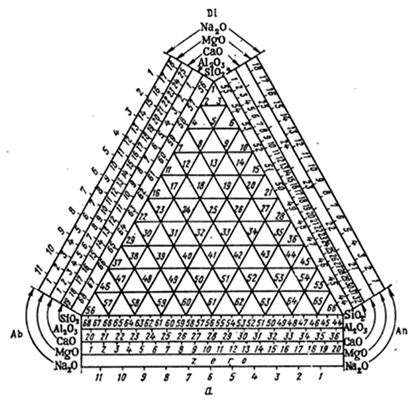
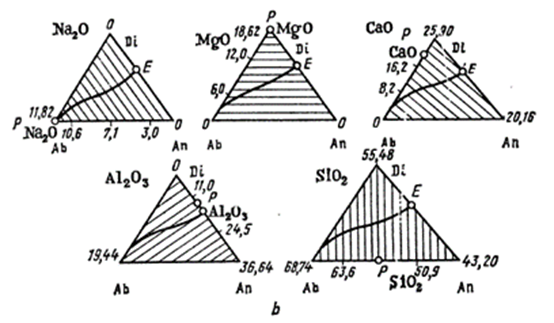
Рис.11.10 несимметричная тройная диаграмма состояния по Ормонту для системы альбит-анорит-диопсид. На сторонах диаграммы отложено содержание каждого простого оксида в процентах :a-общий вид диаграммы,b-эквиконцентрационные линии для пяти простых оксидов.На одной из сторон треугольника показан ход изменения концентрации даного оксида( рис.а). Cоединяя точку р для данного оксида, например Аl 2 O 3 ( если она лежит на стороне треугольника ), с противоположной вершиной , находим направление эквиконцентрационных линий, AbE-эвтектическая линия.
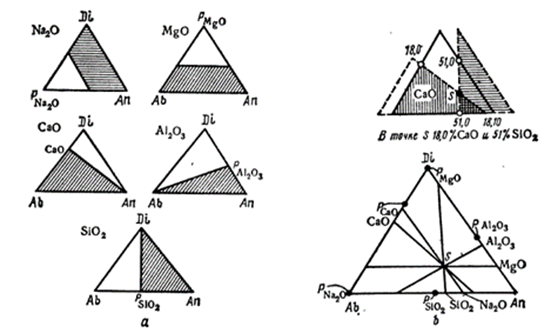
Рис.11.11 Построение и применение шаблонов для нахождения фигуративной точки по содержанию простых веществ и определение содержания простых веществ по положению фигуративной точки:a- построение шаблонов;b-применение шаблонов для расчетных целей.
10.Об атомных спектрах . Закон Мозели . Принцип Паули.
С увеличением атомного номера элемента его характеристический спектр смещается в сторону более коротких волн, то есть в ультрафиолетовую, а затем в рентгеновскую область. Частоты характеристических рентгеновских лучей могут быть сгруппированы в 3 серии: К, L, М(РИС.11.12). Лучи серии К наиболее, а серии М-наименее жесткие. Первые возникают у элементов с меньшими атомными массами, а точнее с меньшим порядковым номером атома Z в системе Д. И. Менделеева. Закон Мозели был описан уравнением
![]() , из которого следует, что квадратные корни частот
характеристического рентгеновского излучения атомов элементов линейно зависят
от атомных номеров Z. Здесь р-константа, неизменная для данной серии; S- поправка на экранирование заряда ядра электронами,
близкая к 1 и ослабляющая силовое поле ядра. Закон Мозели раскрывает смысл
периодического закона Менделеева : свойства элементов зависят от атомного
номера. С количественной стороны выражение 11.3 можно для Кα –серии
переписать в форме ν= 2,47
, из которого следует, что квадратные корни частот
характеристического рентгеновского излучения атомов элементов линейно зависят
от атомных номеров Z. Здесь р-константа, неизменная для данной серии; S- поправка на экранирование заряда ядра электронами,
близкая к 1 и ослабляющая силовое поле ядра. Закон Мозели раскрывает смысл
периодического закона Менделеева : свойства элементов зависят от атомного
номера. С количественной стороны выражение 11.3 можно для Кα –серии
переписать в форме ν= 2,47![]() 10 15 (Z-s)2 =
10 15 (Z-s)2 = ![]() R(Z-s)2
R(Z-s)2 ![]() R(1/12-1/22) · (Z-s)2, где 22 есть n
R(1/12-1/22) · (Z-s)2, где 22 есть n![]() . Eсли n2=2, находим частоты серии Кα, если n 2 =3 – серии Кβ , если n2=4- серии Кγ. Уровни,
различающие главными квантовыми числами , обозначаются следующим образом:
. Eсли n2=2, находим частоты серии Кα, если n 2 =3 – серии Кβ , если n2=4- серии Кγ. Уровни,
различающие главными квантовыми числами , обозначаются следующим образом:
Главное квантовое число 1 2 3 4 5 6
Обозначение уровня К L М N O P
Уровни, различающиеся побочными квантовыми числами, обозначаются так: побочное квантовое число 0 1 2 3 4
Обозначение подуровня s р d f g
Принцип Паули- в атоме не может быть двух электронов со всеми четырьмя одинаковыми квантовыми числами.
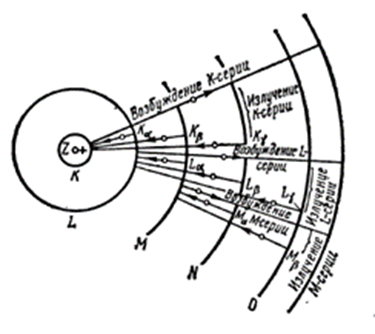
Рис.11.12 Происхождение К-,L-,и М-серий (схема).
11. Метод рентгеновского фазового анализа порошков. Уравнение Вульфа –Брэгга:
При исследовании полупроводников нужно устанавливать количество фаз в системе, сингонию, вид симметрии, строение элементарных ячеек фаз, периоды идентичности, химический состав фаз, тип реальной структуры кристалла, является ли фаза фазой постоянного или переменного состава,
в последнем случае –область гомогенности фазы; степень упорядоченности структуры, величину кристаллитов в полукристаллическом материале; магнитную структуру полупроводников и др. Одним из методов, позволяющих решить эти задачи, является рентгенографический метод.
Уравнение Вульфа-Брэгга: nλ=2 x=2d h R L ![]() .
.
Рис.11.3 К выводу уравнения Вульфа –Брэгга:
Направление рентгенографического анализа : задачей рентгеновского структурного анализа является нахождение точных позиций атомов в элементарной ячейке , установление пространственной группы структуры, распределения электронной плотности. Он характеризует конкретную выделенную фазу ; осуществляется главным образом на монокристаллах.
В подавляющем большинстве случаев инженер радиоэлектронной промышленности может использовать литературу по рентгеноструктурному анализу данной фазы или поручить такой анализ специализированным лабораториям институтов.
Рассеяние рентгеновских лучей веществом : должно наблюдаться два вида рассеяния – когерентное без изменения длины волны и комптоновское некогерентное с изменением длины волны. Рассеяние рентгеновских лучей осуществляют только электроны. Свободный электрон вызывает в основном некогерентное комптоновское рассеяние. Квант рассеянных лучей меньше, а длина волн больше, чем первичных.
· квантомеханических моделях строения атома :не допустимо распространять на явления микромира законы макромира из классической физики. Согласно квантово механическим представлениям электроны в атоме и молекуле движутся по «размазанным» орбитам, чем то напоминающим «электронное облако». Каждой «орбите» соответствуют строго определенные квантовые состояния. Последним отвечают точно рассчитанные и экспериментально найденные энергетические уровни(термы). Квантовая механика описывает атом как систему стоячих волн вокруг ядра, как струна с закрепленными концами , которая может колебаться с определенными , характерными для нее частотами. Система стоячих волн , характеризующая атом, отличается тем, что на определенном очень малом расстоянии от ядра амплитуды этих волн становятся незначительными , как бы ограничивая тем самым размер атома. Пространственное распределение амплитуд волн вокруг ядра может быть найдено с помощью уравнения Шредингера, известного из курсов физики и квантовой механики;
· Важным выводом волновой механики является установление симметрии распределения вокруг атомного ядра валентных орбит-облаков:s орбита образует вокруг ядра электронное облако шаровой симметрии.Три р – орбиты распределены вокруг осей X,Y,Zдекартовых координат так, что обычно различают Px , Pу , Pz орбиты.
· Называются орбиталями.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.