
Для нормальной жизнедеятельности клеток и организма необходима непрерывная выработка и постоянное потребление энергии. Источником легко усваиваемой с помощью АТФаз является энергия фосфатных связей макроэргических соединений, главным из которых является АТФ. АТФ образуется в процессе окислительно-восстановительных реакций, в которых участвуют углеводы, жиры, белки, являющиеся главными субстратами окисления. Процесс окислительно-восстановительных превращений питательных веществ называется биологическим окислением. Большая часть всей вырабатываемой АТФ образуется в митохондриях, в которых осуществляется сопряженное с фосфорилированием окисление субстратов с участием кислорода. Поэтому нормальное функционирование клеток возможно только при условии:
- непрерывного образования достаточного количества АТФ;
- хорошего усвоения поступающих в митохондрии питательных субстратов и кислорода.
Нарушение этих условий приводит к развитию гипоксии, которая сопровождается энергетическим дефицитом.
Гипоксия (кислородное голодание тканей) – типовой патологический процесс, развивающийся в результате недостаточности или неэффективности биологического окисления, сопровождающийся энергетическим дефицитом и развитием деструктивных изменений в тканях.
В доставке кислорода тканям принимают участие: легкие, кровь, сердечно-сосудистая система (транспортные системы). Дефицит кислорода может возникнуть на различных этапах его поступления и использования, а также при уменьшении его содержания в окружающем воздухе.
Гипоксию можно условно разделить на две группы:
- гипоксию из-за недостатка кислорода во вдыхаемом воздухе;
- гипоксию при патологических процессах.
Гипоксия может быть физиологической и патологической.
Физиологическая гипоксия наблюдается после тяжелой физической работы, больших физических нагрузок у спортсменов, гипоксия матери и плода, гипоксия у пожилых людей.
При старении наблюдается неадекватное кислородное снабжение тканей. Даже небольшая степень гипоксии в пожилом возрасте вызывает включение компенсаторных механизмов, но они оказываются мало эффективными для поддержания кислородного снабжения тканей. При работе даже небольшой интенсивности у пожилых людей величина кислородного долга втрое выше, чем у молодых людей.
Физиологическая гипоксия имеет адаптивное значение для организма, так как является важной причиной ограничения интенсивности двигательной активности или полностью прекращает ее. Искусственное подавление гипоксии, например, с помощью допинга у спортсменов, может привести к летальному исходу. Физиологическая гипоксия повышает устойчивость организма, подготавливая его к качественно новому этапу существования.
Гипоксия может быть острой, развивающейся в течение нескольких минут или даже секунд (молниеносной), и хронической, продолжающейся месяцами и годами. Острая гипоксия наблюдается при массивной кровопотере, инфаркте миокарда, а также при отравлении угарным газом, в результате чего нарушается способность крови переносить к тканям кислород. Хроническая гипоксия может наблюдаться при патологии легких (эмфизема легких) и сердца (пороки, кардиосклероз). Особое место занимает гипоксия, вызванная отравлением цианидами. Эти вещества блокируют дыхательные ферменты клеток и тканей, которые утрачивают способность усваивать кислород. Наиболее страдает нервная система. Так, при полном прекращении снабжения кислородом серьезные нарушения в коре больших полушарий отмечаются уже через 2,5-3 минуты.
Гипоксия возникает или за счет нарушения доставки кислорода тканям или в результате нарушения его утилизации дыхательными системами клеток.
В крови кислород растворен в плазме и входит в состав оксигемоглобина. Чем выше в крови напряжение свободного кислорода, тем больше химически он связывается с гемоглобином. При оптимальных условиях ph, температуры, электролитного баланса, давления углекислого газа, достаточного содержания витамина С 1 грамм гемоглобина связывает 1,34-1,36 мл. О2. Количество миллилитров кислорода, способное связаться с гемоглобином в 100 мл крови, называется кислородной емкостью крови.
В нормальных условиях эффективное биологическое окисление является основным источником богатых энергией фосфатных соединений, необходимых для жизнедеятельности органов и тканей.
Всякое изменение парциального давления кислорода в плазме изменяет насыщение гемоглобина кислородом и изменяет способность гемоглобина отдавать кислород тканям. Жизнедеятельность клеток может осуществляться при снижении парциального давления в окружающей среде только до определенного предела, при котором еще сохраняется тканевое дыхание. Эта величина называется критическим парциальным давлением кислорода внутри клеток.
Для артериальной крови критическая концентрация кислорода составляет 27-33 мм.рт.ст.; для венозной крови – 19 мм.рт.ст.; для митохондрий – 1,5-2,0 мм.рт.ст. Для клеток головного мозга критическая концентрация кислорода равна 2-6 мм.рт.ст.
При уменьшении содержания кислорода ниже этого критического уровня возникает состояние энергетического дефицита, приводящее к разнообразным морфологическим и функциональным нарушениям, вплоть до гибели клетки.
С гипоксией (дефицитом кислородоснабжения) человек встречается еще в утробе матери. В повседневной жизни умеренная гипоксия может быть во сне, при интенсивной работе, гипоксия может возникать в работающем органе или ткани. Умирание организма всегда сопровождается тяжелой гипоксией.
Периодически возникающий дефицит кислорода – это эволюционно древний фактор, к которому у человека выработалась многогранная адаптивная реакция, которая направлена на повышение мощности систем транспорта и утилизации кислорода.
Следовательно, умеренная гипоксия стимулирует нормальную адаптивную физиологическую реакцию организма и является одним из важных стимулов его развития. При тяжелой гипоксии адаптивные реакции выражены слабо, поэтому преобладают деструктивные изменения. Гипоксия встречается при многих заболеваниях и служит патогенетической основой их развития.
Гипоксии объединены в две группы: экзогенные и эндогенные.
Проявления гипоксии зависят от: индивидуальной реактивности организма, степени скорости развития, продолжительности гипоксического состояния и его этиологии.
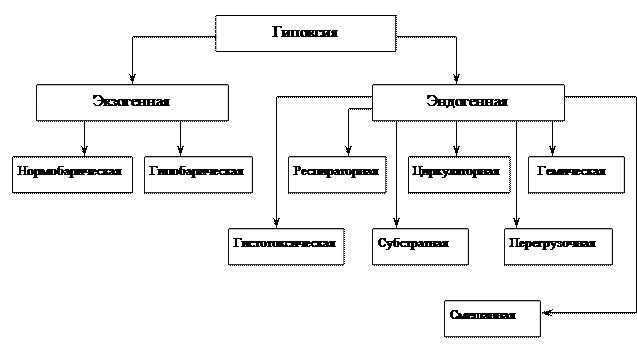
Классификация гипоксий по этиологии.
По распространенности гипоксического состояния различают местную и общую гипоксию. По скорости развития и длительности различают молниеносную, острую, подострую и хроническую гипоксию. По степени тяжести: легкую, умеренную, тяжелую, критическую (смертельную) гипоксию.
Экзогенная гипоксия возникает при снижении содержания кислорода во вдыхаемом воздухе. Выделяют две формы экзогенной гипоксии: нормобарическую и гипобарическую.
Нормобарическая гипоксия возникает при нормальном атмосферном давлении, но сниженном парциальном давлении кислорода во вдыхаемом воздухе. Такая ситуация складывается при длительном пребывании в замкнутых невентилируемых помещениях малого объема, работах в шахтах, нарушениях регенерации воздуха или подачи кислородной смеси для дыхания в летательных и глубинных аппаратах, автономных костюмах (космонавты, летчики, водолазы, спасатели, пожарники), несоблюдении техники искусственной вентиляции легких. При этом уменьшение содержания кислорода во вдыхаемом воздухе приводит к недостаточному насыщению гемоглобина кислородом, т.е. к развитию артериальной гипоксемии.
Гипобарическая гипоксия развивается при снижении атмосферного давления. Чаще всего наблюдается при восхождениях в горы или в барокамерах. В этих условиях возможно развитие горной, высотной или декомпрессионной болезни.
Ведущим патогенетическим фактором развития экзогенных гипоксий является гипоксемия (снижение насыщения крови кислородом), дополнительным отрицательным фактором является гипокапния (низкое содержание углекислого газа в крови). Гипокапния и газовый алкалоз возникают в результате компенсаторного рефлекторного увеличения гипервентиляции легких, то есть усиления дыхания.
Гипокапния и увеличение pН крови (алкалоз) повышают сродство гемоглобина к кислороду. Этот эффект, с одной стороны, улучшает насыщение гемоглобина кислородом в легочных капиллярах, а с другой стороны, ухудшает отдачу кислорода тканям при низких значениях его парциального давления. Это приводит к нарушению газообмена и метаболизма в тканях.
Газовый алкалоз является результатом гипокапнии. Однако, при высоком содержании углекислого газа во вдыхаемом воздухе (при дыхании в замкнутом пространстве) экзогенная гипоксемия может сочетаться с гиперкапнией и ацидозом. Умеренная гиперкапния способствует увеличению кровообращения в сосудах мозга и сердце. Выраженная гиперкапния приводит к развитию ацидоза, снижению сродства Hb к кислороду, дисбалансу ионов в биологических жидкостях и клетках.
Следствием гипокапнии является снижение системного артериального давления. СО2 – один из основных факторов регуляции тонуса сосудов мозга, поэтому значительное снижение парциального давления углекислого газа является сигналом сужения сосудов мозга, сердца и уменьшения их кровоснабжения. Это приводит к обморокам, коронарной недостаточности, проявляющейся стенокардией или даже инфарктом. Параллельно с этими изменениями развивается гипернатриемия, гипокалиемия, гипокальциемия в клетках и биологических жидкостях.
Респираторная (дыхательная) гипоксия возникает из-за нарушения функции внешнего дыхания. Этот вид гипоксии наблюдается при: недостаточности альвеолярной вентиляции, нарушениях диффузионной способности легких, нарушении кровоснабжения легких.
Альвеолярная гиповентиляция наблюдается при рестриктивных и обструктивных формах нарушения дыхания, центральных расстройствах ритма дыхания.
Рестриктивные заболевания легких – это заболевания при которых ограничена подвижность легких, то есть способность их расправляться при вдохе. Возникают такие заболевания при врожденных или приобретенных нарушениях строения грудной клетки, воспалительных процессах в дыхательных мышцах, нарушениях нервно-мышечной передачи разного происхождения. Например, при полиомиелите, столбняке, ботулизме. При этих заболеваниях поражаются мотонейроны, иннервирующие наружные межреберные мышцы и диафрагму в результате ограничивается расширение грудной клетки при вдохе, уменьшается отрицательное давление в плевральной полости, в результате чего снижается присасывающая функция легких и в альвеолы поступает меньше воздуха. Рестриктивные расстройства дыхания и респираторная гипоксия возникает при пневмотораксе, ожирении. При ожирении уменьшается альвеолярная вентиляция, что приводит к гипоксемии, полицитемии и легочной гипертензии.
Обструктивные нарушения альвеолярной вентиляции обусловлены возрастанием сопротивления воздухоносных путей потоку воздуха. Они отмечаются при хроническом бронхите, эмфиземе легких, бронхиальной астме. Расстройства дыхательного ритма могут возникать в результате прямого действия токсичных веществ на нейроны дыхательного центра, например, при диабетической и печеночной коме, при нарушении кровоснабжения мозга при ишемических и геморрагических инсультах, шоковых состояниях, при повышении внутричерепного давления.
Нарушение диффузионной способности легких возможно из-за уменьшения диффузионной поверхности или утолщения альвеолярных перегородок. Диффузионная поверхность уменьшается при сдавлении альвеол или их спадении при ателектазе.
Толщина альвеолярных перегородок (толщина аэрогематического барьера), то есть расстояние, которое должны преодолеть молекулы кислорода, чтобы попасть из альвеол в легочные капилляры, в норме не превышают 1 мкм. Этот диффузионный путь увеличивается при воспалительном отеке, фиброзе легочной паренхимы.
Изменение вентиляционно-перфузионного отношения может быть одной из причин респираторной гипоксии.
Отношение минутного объема альвеолярной вентиляции к объему крови протекающей через легкие за 1 минуту в норме колеблется в диапазоне 0,8-1,2. Снижение этого показателя отражает уменьшение альвеолярной вентиляции.
При респираторной гипоксии артериальная гипоксемия сочетается с гиперкапнией. Содержание кислорода уменьшается как в артериальной, так и в венозной крови.
Циркуляторная гипоксия развивается при нарушении в системе кровообращения, что приводит к недостаточному крово- и кислородоснабжению органов и тканей. Снижение системного артериального давления приводит к уменьшению кровоснабжения большинства органов, в результате чего развивается общая циркуляторная гипоксия. Уменьшение количества крови, протекающей через капилляры в единицу времени может быть обусловлено общим уменьшением объема крови (гиповолемией), например, при кровопотере, обезвоживании организма и нарушениями функций сердца и сосудов.
Общая циркуляторная гипоксия может возникать как вследствие уменьшения производительности сердца (при кардиомиопатиях), так и в результате снижения тонуса сосудов (при ортостатическом или панкреатическом коллапсе). Циркуляторная гипоксия является центральным звеном патогенеза таких экстремальных состояний как кома и шок.
При нарушении кровоснабжения какого-нибудь органа может возникать местная циркуляторная гипоксия. Чаще всего местная циркуляторная гипоксия возникает в результате атеросклеротического поражения стенок артериальных сосудов и сужения их просвета. В зависимости от локализации возможны разные клинические проявления: ишемическая болезнь сердца, ишемический инсульт.
Для циркуляторной гипоксии характерно нормальное содержание кислорода в артериальной крови и снижение этого показателя в венозной крови – увеличение артериовенозной разницы по кислороду.
Гемическая (кровяная) гипоксия развивается при уменьшении кислородной емкости крови. Различают две ее формы: анемическую, связанную с уменьшением содержания эритроцитов в крови и гипоксию, связанную с нарушением способности гемоглобина связывать, транспортировать и отдавать тканям кислород.
Эритропении (снижение количества эритроцитов в единице объема крови) могут быть обусловлены: подавлением кроветворной функции костного мозга, гемолизом эритроцитов, уменьшением выброса эритропоэтина из-за недостаточности функции почек. Эритропении обычно сопровождаются снижением содержания гемоглобина в крови.
Гемическая гипоксия может возникать не только при уменьшении количества гемоглобина, но и при его качественных изменениях, например, при серповидноклеточной анемии, когда в молекуле гемоглобина глутамин заменяется на валин и образуется HbS, у которого снижено сродство к кислороду.
В патологических условиях возможно образование таких соединений гемоглобина, которые не могут выполнять дыхательную функцию. Таким соединением является карбоксигемоглобин-соединение гемоглобина с угарным газом (СО). Сродство гемоглобина к угарному газу в 300 раз выше, чем к кислороду, что обусловливает высокую ядовитость угарного газа, отравление наступает при очень низкой концентрации угарного газа в воздухе. Карбоксигемоглобин не способен транспортировать кислород. При отравлении нитратами, анилином, производными бензола, при воздействии некоторых лекарственных препаратов (амидопирин, сульфаниламиды, фенацетин) образуется метгемоглобин, в котором трехвалентное железо не присоединяет кислород.
Значительное ухудшение переноса и отдачи кровью кислорода (О2) наступает при изменении физических свойств эритроцитов, их значительной агрегации и образовании «сладжей».
Для гемической гипоксии характерно значительное снижение объемного содержания кислорода в артериальной крови.
Первично-тканевая (гистотоксическая) гипоксия связана с нарушениями утилизации кислорода. При этом виде гипоксии страдает биологическое окисление на фоне достаточного снабжения тканей кислородом.
Причинами тканевой гипоксии является снижение количества или активности дыхательных ферментов, разобщение окисления и фосфорилирования. Классическим примером тканевой гипоксии, при которой происходит инактивация дыхательных ферментов, в частности цитохромоксидазы – конечного фермента дыхательной цепи, является отравление цианидами, монойодацетатом. Алкоголь, некоторые наркотики в больших дозах угнетают дегидрогеназы, что сопровождается развитием гистотоксической гипоксии.
Снижение синтеза дыхательных ферментов, вызывающее развитие гистотоксической гипоксии, наблюдается при недостаточности витаминов В1, В2, РР (никотиновая кислота), так как они необходимы для их образования, а также при кахексии и нарушениях белкового обмена.
В возникновении тканевой гипоксии может иметь значение разобщение окисления и фосфорилирования, так как при этом развивается энергетическое голодание тканей.
Газовый состав крови при гистотоксической гипоксии характеризуется нормальным содержанием кислорода в артериальной крови и значительным его повышением в венозной крови (уменьшение артериовенозной разницы по кислороду).
В возникновении этого вида гипоксии может иметь значение активация перекисного свободнорадикального окисления, при котором органические соединения подвергаются неферментативному окислению молекулярным кислородом. Перекиси липидов вызывают дестабилизацию мембран митохондрий и лизосом. Активация свободнорадикального окисления наблюдается при дефиците его естественных ингибиторов (подавителей), особенно витамина Е (токоферола), серотонина и др.
Перегрузочная гипоксия развивается на фоне достаточного или даже повышенного снабжения тканей кислородом. Однако, повышенное функционирование органа и значительно возросшая потребность в кислороде могут привести к неадекватному кислородному снабжению тканей даже в условиях полной мобилизации функциональных резервов системы транспорта и утилизации кислорода. Примером могут служить чрезмерные нагрузки в спорте, интенсивная мышечная работа.
Субстратная гипоксия возникает при нарушении доставки или утилизации основных субстратов биологического окисления при нормальной доставке кислорода. В норме запас субстратов достаточно велик, но иногда при нормальном метаболизме кислорода, нормальных мембранах и ненарушенных ферментативных системах возникает первичный дефицит субстратов, что приводит к нарушению биологического окисления. Чаще всего этот вид гипоксии развивается при недостаточном поступлении в клетки глюкозы. Ткань головного мозга наиболее чувствительна к таким нарушениям. Прекращение поступления глюкозы в мозг уже через 5-8 мин приводит к гибели нервных клеток. Субстратная гипоксия может развиваться при сахарном диабете, общем голодании.
Перечисленные виды гипоксии в чистом виде встречаются редко, чаще наблюдается их комбинация. Это дало основание выделить смешанную форму гипоксии. Например, при травматическом шоке наряду с циркуляторной гипоксией развивается и дыхательная гипоксия из-за нарушения микроциркуляции в легких. При тяжелой анемии, массивном образовании карбоксигемоглобина развивается гипоксия миокарда, что приводит к снижению функций сердца, падению кровяного давления – в результате на анемическую гипоксию накладывается циркуляторная гипоксия.
Смешанные формы гипоксии оказывают более выраженное повреждающее действие, так как приводят к срыву ряда коменсаторно-приспособительных реакций.
Развитию гипоксии способствуют состояния, при которых возрастает потребность в кислороде – лихорадка, стресс, высокая физическая нагрузка.
При гипоксии организм реагирует включением сформировавшегося в эволюции комплекса защитно-приспособительных реакций, с помощью которых осуществляется адаптация к этому патогенному возбудителю.
В адаптации к гипоксии участвуют следующие функциональные системы:
- система внешнего дыхания;
- система транспорта О2;
- система утилизации кислорода и образования АТФ.
Выделяют срочные и долговременные приспособительные реакции организма к гипоксии.
Срочные реакции (при острой гипоксии) включаются немедленно при развитии гипоксии. В их основе лежит рефлекторный механизм, активирующий системы кровообращения, внешнего дыхания и крови, обеспечивающие кислородное снабжение организма. В процессе восстановления кислородного баланса организма участвуют следующие механизмы.
1. Механизмы, мобилизация которых увеличивает поступление кислорода в организм, даже при его дефиците в среде:
- гипервентиляция легких (усиление дыхания);
- увеличение ударного и минутного объемов сердца;
- увеличение количества эритроцитов (из депо);
- увеличение кислородной емкости крови за счет увеличения количества эритроцитов (выброс из депо);
- облегчение диссоциации оксигемоглобина в тканях.
2. Механизмы, делающие возможным достаточное поступление кислорода к мозгу, сердцу и другим жизненно важным органам, несмотря на гипоксемию (недостаток кислорода в крови):
- феномен централизации кровообращения, проявляющийся преимущественным кровоснабжением сердца, головного мозга, легких за счет уменьшения кровоснабжения кожи, скелетных мышц, желудочно-кишечного тракта;
- расширение артерий и капилляров мозга, сердца, легких;
- открытие нефункционирующих в норме капилляров;
- изменение способности клеток утилизировать кислород за счет увеличения концентрации миоглобина.
3. Увеличение способности клеток и тканей утилизировать кислород из крови и образовывать АТФ, несмотря на гипоксемию за счет:
- увеличения сродства дыхательного фермента – цитохромоксидазы к кислороду путем изменения качества митохондрий;
- увеличения степени сопряжения окисления и фосфорилирования.
4. Увеличение ресинтеза АТФ за счет активации гликолиза.
Такое аварийное увеличение внешнего дыхания и системы кровообращения не может обеспечить стойкого и длительного приспособления к гипоксии, так как требует для своего осуществления повышенного потребления кислорода.
Возникает парадоксальная ситуация, состоящая в том, что в период экстренной адаптации к экзогенной гипоксии потребление кислорода не только не снижается, но даже, наоборот, возрастает.
Поэтому постепенно формируется качественно иной тип приспособления к дефициту кислорода – долговременная адаптация.
Долговременные приспособительные реакции развиваются (при хронической гипоксии) постепенно при длительном действии на организм гипоксии. Они сохраняются все время пока есть гипоксия и даже некоторое время после ее ликвидации. Такие реакции в физиологических условиях наблюдаются у жителей высокогорья, тренированных альпинистов. В условиях патологии возникают при хронической сердечно-сосудистой недостаточности, при хронических заболеваниях легких, при анемиях.
Характерным для долговременных приспособительных процессов является гипертрофия и гиперплазия клеток и органов, принимающих участие в приспособлении к гипоксии.
Механизмы долгосрочной адаптации:
- снижение основного обмена и потребности организма в кислороде;
- усиление газообменной функции легких (увеличение числа функционирующих альвеол и капилляров, увеличение мощности дыхательных мышц);
- развитие умеренной гипертрофии миокарда (повышение сердечного выброса);
- увеличение кислородной емкости крови (активация эритропоэза, повышение сродства Hb к кислороду в легких, ускорение диссоциации оксигемоглобина в тканях);
- повышение экономичности функционирования (переход на оптимальный уровень функционирования, повышение эффективности метаболизма);
- повышение эффективности и надежности механизмов регуляции (повышение резистентности нейронов к гипоксии, снижение степени активации симпатико-адреналовой и гипаталамо-гипофизарно-надпочечниковой систем);
- усиление способности тканевых ферментов утилизировать кислород, поддерживать высокий уровень окислительных процессов и осуществлять синтез АТФ;
- эффективность использования энергии окислительных процессов.
Другой механизм адаптации заключается в увеличении количества дыхательных ферментов и мощности системы митохондрий путем увеличения их количества.
Таким путем восстанавливается или увеличивается способность клетки вырабатывать энергию, несмотря на недостаток кислорода в притекающей крови.
Такие процессы происходят, главным образом, в органах ответственных за транспорт кислорода (легкие, сердце, дыхательные мышцы, эритробластический росток костного мозга) и в органах, наиболее страдающих от недостатка кислорода (кора больших полушарий мозга, нейроны дыхательного центра). В этих органах увеличивается синтез структурных белков, приводящий к явлениям гиперплазии и гиперфункции. Эти фундаментальные перемены на клеточном уровне меняют характер адаптационного процесса при гипоксии.
Расточительная и не экономная гиперфункция дыхания и сердца становится не нужной. Развивается стойкая и экономная адаптация.
При разных видах гипоксии эффективность компенсаторно-приспособительных реакций различна.
При респираторной и циркуляторной гипоксии ограничены возможности адаптивных реакций в системе внешнего дыхания и кровообращения. При тканевой гипоксии неэффективны приспособительные реакции в системе транспорта кислорода.
Возникающие в организме нарушения при гипоксии можно условно разделить на:
1. Нарушения метаболических процессов в клетках.
2. Нарушения функций отдельных органов и систем.
При снижении парциального давления кислорода ниже критических величин наступают изменения в обмене веществ.
Нарушения метаболических процессов в клетках начинается в митохондриях – энергетических станциях клетки.
Длительное отсутствие кислорода нарушает работу митохондрий, в которых снижается скорость аэробного окисления и окислительного фосфорилирования. Это ведет к понижению количества АТФ и возрастанию содержания аденозиндифосфата и аденозинмонофосфата. При этом снижаются функциональные возможности клетки, например, сократимость кардиомиоцитов, но для клетки это еще не смертельно. Дефицит АТФ и увеличение АДФ активируют гликолиз. Клетки расходуют гликоген, обеспечивая себя энергией за счет анаэробного распада глюкозы. Происходит адаптация к гипоксии, и доставка энергии стабилизируется. Однако, это сопровождается истощением запасов гликогена. Конечным продуктом гликолиза является молочная кислота. Это вызывает в клетке ацидоз.
Прогрессирующий ацидоз внутриклеточной среды вызывает денатурацию белков и формирование в цитоплазме зерен, «зернистая дистрофия» проявляется помутнением цитоплазмы – «мутное набухание», – термины, применяемые в патологической анатомии для обозначения начальной степени острой гипоксии органа.
Ацидоз подавляет некоторые ферменты. Это приводит к тому, что усиливается гликолиз, который усиливает ацидоз, ацидоз тормозит гликолиз. Так в клетке формируется настоящий дефицит АТФ, так как аэробный механизм не работает из-за кислородного дефицита, а анаэробный из-за ацидоза.
В незрелых клетках ферменты менее чувствительны к ацидозу. Это лежит в основе повышенной устойчивости эмбриональных клеток к острой гипоксии и обусловливает большую выносливость маленьких детей к кислородному голоданию. В акушерской практике известны случаи, когда роженица погибает от гипоксии, а плод остается жив. Известно, что срок клинической смерти у детей больше, чем у взрослых.
Дефицит кислорода в тканях вызывает нарушение всех видов обмена. В результате нарушения белкового и жирового обмена в крови нарастает содержание аминокислот, b-оксимасляной, ацетоуксусной кислот, то есть развивается метаболический ацидоз.
Повышается проницаемость биологических мембран, что вызывает нарушение баланса ионов. Внутрь клетки поступают Na+ и вода, а из клетки выходит К+. В результате этого положительный поверхностный заряд клеток уменьшается или даже меняется на отрицательный. Это облегчает агрегацию клеток крови и их адгезию, что способствует развитию сладжа эритроцитов, формированию белых тромбов. Клетки становятся менее возбудимыми. В нейронах мозга развивается глубокое торможение, что проявляется развитием комы с потерей сознания и утратой рефлексов.
Сдвиг pН в кислую сторону повреждает мембраны лизосом, что приводит к выходу активных протеолитических ферментов, которые оказывают повреждающее действие на митохондрии, выражающееся в набухании и деградации митохондрий, отеке, гиперхроматозе и распаде ядра.
При гипоксии наблюдается увеличение продукции оксида азота (NO). Умеренная его продукция имеет положительное значение, так как сопровождается расширением прекапиллярных сосудов, снижением адгезии и агрегации тромбоцитов, активацией белков острой фазы, защищающих клетку от повреждения. Однако, гиперпродукция оксида азота оказывает повреждающее действие, особенно на нервные клетки.
Изменения энергетического, углеводного, белкового, жирового и электролитного обменов в клетках, возникающий при этом ацидоз являются главной причиной нарушения функций отдельных тканей, органов и систем с развитием в них дистрофических и склеротических процессов.
Чувствительность различных органов и тканей к гипоксии неодинакова и зависит от:
- интенсивности обмена;
- мощности гликолитических систем;
- запасов энергии в виде макроэргов;
- возможности генетического аппарата обеспечить гиперфункцию.
Нервная система. В первую очередь при гипоксии страдает нервная система. Еще до появления грозных симптомов гипоксии возникает эйфория, характеризующаяся эмоциональным и двигательным возбуждением, так как нарушаются процессы внутреннего торможения.
Затем угнетаются функции коры больших полушарий: появляется вялость, заторможенность, сонливость, головная боль, головокружение, оглушенность, клонические и тонические судороги. В последующем возникает потеря сознания, может развиться кома.
Дыхательная система. Сначала возникает активация дыхания, которая ограничивается развивающейся гипокапнией. Ухудшается кровоснабжение мозга и сердца; развивается алкалоз, нарушается электролитный обмен, повышается потребление кислорода.
Развивается угнетение дыхания, что приводит к гиперкапнии, алкалоз сменяется ацидозом, ухудшается насыщение крови кислородом.
Затем нарушается глубина и ритм дыхания, потом появляется периодическое дыхание Чейн-Стокса, наконец, развивается агональное дыхание и его остановка.
Сердечно-сосудистая система. Развивается тахикардия, сменяющаяся брадикардией. Это сопровождается нарушением ритма вплоть до развития фибрилляции. Системное артериальное давление сначала повышается, затем падает. Гипоксия повреждает микрососуды, вызывая нарушения микроциркуляции и ухудшая диффузию кислорода.
Почки. Первоначальная полиурия сменяется нарушением фильтрационной способности почек. Развивается острая почечная недостаточность вплоть до анурии и уремии.
В тяжелых случаях гипоксии снижается температура тела, что объясняется снижением обмена веществ и нарушением терморегуляции.
Переносимость гипоксии зависит от многих причин, в том числе от возраста.
Новорожденные легче переносят гипоксию, так как автоматическая деятельность дыхательного центра новорожденных при гипоксии может поддерживаться более старой и примитивной формой обмена – анаэробным (бескислородным) расщеплением углеводов. Кроме этого новорожденный обладает некоторым запасом фетального гемоглобина, который способен выполнять дыхательную функцию при пониженном парциальном давлении кислорода в крови. Однако, решающее значение в высокой устойчивости новорожденных к гипоксии имеет менее высокий уровень развития центральной нервной системы.
При некоторых состояниях, характеризующихся глубоким торможением центральной нервной системы и снижением обмена веществ (сон, наркоз, гипотермия, зимняя спячка животных) понижена чувствительность организма к недостатку кислорода.
Переносимость гипоксии можно повысить искусственно. Например, снижением реактивности организма и его потребности в кислороде (наркоз, гипотермия). Второй способ – тренировка в условиях барокамеры или высокогорья. Заслуга разработки метода ступенчатой акклиматизации к высокогорному климату принадлежит Н.Н. Сиротинину.
Роль белка HIF-1α — фактора, индуцированного гипоксией
Кислород составляет около 20% атмосферы Земли. Он необходим для жизни животных: его используют митохондрии, присутствующие практически во всех клетках животных, для преобразования пищи в полезную энергию. Отто Варбург (Otto Warburg), лауреат Нобелевской премии по физиологии и медицине 1931 года, показал, что это преобразование является ферментативным процессом. Ключевым физиологическим ответом на гипоксию является повышение уровня гормона эритропоэтина, что приводит к увеличению выработки эритроцитов (эритропоэзу). Важность гормонального контроля эритропоэза была известна уже в начале XX века, но каким образом этот процесс контролировался кислородом, оставалось загадкой.
Нобелевскую премию по физиологии или медицине в этом году присудили за открытие белка HIF-1α — фактора, индуцированного гипоксией, — и его роли в защитных и других реакциях организма на недостаток кислорода. Главная функция HIF-белков — обеспечить выживание в узком диапазоне концентрации кислорода. Если кислорода слишком мало, в организме не будут протекать обменные процессы, и человек погибнет. Слишком большая концентрация кислорода также губительна: это очень сильный окислитель. Чем больше кислорода, тем больше его активных форм вырабатывают митохондрии. Это может привести к окислительному стрессу. Поэтому необходимо поддерживать баланс. Белок HIF-1α находится в центре системы, отвечающей за адаптацию организма к различным концентрациям кислорода.
Группа Грега Семенцы выяснила, что существует специальный транскрипционный фактор HIF-1α, который чувствует активные формы кислорода и при его недостатке включает целый набор разных генов, в том числе ген эритропоэтина. Если много клеток в ткани активируют HIF-1α, это сигнализирует о том, что они нуждаются в кислороде и организм стремится улучшить его доставку. Его активация в клетках сосудов увеличивала синтез эритропоэтина. Но HIF-1α постоянно окисляется и модифицируется — и в конце концов разрушается протеосомой, то есть клетка его все время подъедает. Для его удаления необходим кислород. Если кислорода становится мало, уровень HIF-1α увеличивается, и он успевает пролезть в ядро и активировать нужные гены. Это очень изящный и редкий механизм регуляции, основанный на стабильности белка. Питер Ратклифф также изучал регуляцию гена эритропоэтина, зависимую от кислорода, и обе исследовательские группы обнаружили, что механизм определения кислорода присутствует практически во всех тканях, а не только в клетках почек, где обычно производится эритропоэтин. Эти важные выводы свидетельствуют о том, что механизм является общим и функциональным для различных типов клеток.
Когда уровень кислорода высокий, клетки содержат мало HIF-1α. Однако при низком уровне кислорода количество HIF-1α возрастает, что позволяет ему связываться с геном эритропоэтина и другими генами (из сегмента фактора, индуцируемого гипоксией), и регулировать их. Несколько исследовательских групп показали, что HIF-1α, обычно разлагающийся достаточно быстро, защищён от разложения при гипоксии. При нормальном уровне кислорода HIF-1α разрушается клеточным комплексом под названием протеасома (открытие которого было отмечено Нобелевской премией по химии в 2004 году — премию вручили Аарону Чехановеру (Aaron Ciechanover), Авраму Гершко (Avram Hershko) и Ирвину Роузу (Irwin Rose)). В этих условиях к белку HIF-1α добавляется небольшой пептид, убиквитин. Убиквитин функционирует как метка для белков, предназначенных для разложения протеасомы. Показано, что функция активации генов HIF-1α регулируется кислород-зависимым гидроксилированием.
Кислородное зондирование позволяет клеткам адаптировать свой метаболизм к низкому уровню кислорода, например, в мышцах во время интенсивных тренировок. Другие примеры адаптивных процессов, контролируемые с помощью кислородного зондирования, — образование новых кровеносных сосудов и эритроцитов. Наша иммунная система и многие другие физиологические функции так же точно настроены с помощью механизмов, ощущающих кислород. Было доказано, что во время развития плод ощущает уровень кислорода, что контролирует нормальное образование кровеносных сосудов и плаценты.
Зондирование уровня кислорода играет центральную роль в огромном количестве заболеваний. Например, пациенты с хронической почечной недостаточностью часто страдают от тяжёлой анемии, вызванной снижением экспрессии эритропоэтина. Кроме того, механизм кислородной регуляции играет важную роль в развитии рака. В опухолях данный механизм используется для стимулирования образования кровеносных сосудов и изменения метаболизма для эффективной пролиферации раковых клеток.
Лечение гипоксии проводится с учетом основных патогенетических механизмов этого процесса и его тяжести. Согласно классификации В.М. Виноградова и соавторов, выделяют следующие противогипоксические средства.
Улучшающие доставку кислорода к тканям и его утилизацию за счет стимуляции дыхания и кровообращения (аналептики и кардиотонические средства), повышающие диссоциацию оксигемоглобина (углекислота, молочная кислота), усиливающие эритропоэз.
Стимулирующие средства наиболее эффективны при нетяжелых формах кислородного голодания. При тяжелой гипоксии возбуждение дыхания и сердца усиливают потребление кислорода и утяжеляют гипоксию. Кроме того, при сильном возбуждении дыхания развивается алкалоз, при котором ухудшается диссоциация оксигемоглобина.
Вещества, повышающие устойчивость организма к гипоксии за счет снижения потребления кислорода (наркотические, снотворные, транквилизаторы и др.).
Угнетение функции симпатоадреналовой системы введением резерпина уменьшает кислородный запрос тканей и повышает устойчивость организма к гипоксии.
Наркотики, снотворные, транквилизаторы, снижая функцию симпатического отдела нервной системы, способствуют снижению обменных процессов, что уменьшает потребность организма в кислороде.
Средства, способствующие сохранению и образованию макроэргов: цитохром С, аскорбиновая кислота, глютамин, АТФ, метионин, кокарбоксилаза, никотинамид, пентоксил, метацил и др.
Средства, нормализирующие мембраны клеток, pH, электролитный обмен. Учитывая, что при гипоксии развивается ацидоз назначают ощелачивающие вещества и хлористый калий. Стабилизация мембран достигается назначением глюкокортикоидов и хлористого магния.
В настоящее время важным фактором профилактики и лечения гипоксии является гипербарическая оксигенация – вдыхание кислорода под повышенным давлением, что повышает кислородную емкость крови, так как при этом увеличивается растворимая фракция кислорода в крови. Надо помнить, однако, что избыток кислорода в тканях (гипероксия) оказывает благоприятное действие только при вдыхании кислорода под давлением 3 атм. Повышение давления вдыхаемого кислорода до 8-10 атм вызывает явления тяжелой интоксикации, так как образуются свободные радикалы и перекисные соединения.
Гипербарическая оксигенация применяется при отравлении угарным газом и барбитуратами, при врожденных пороках сердца, а также во время операций на сухом сердце, то есть в условиях временной остановки кровообращения и дыхания.
Нельзя забывать, что кислород является мощным окислителем, его избыток токсичен для организма. Поэтому в случаях умеренной гипоксии прибегают к периодическому вдыханию газовых смесей с содержанием 10-12% кислорода.
Кислородная терапия неэффективна при гистотоксической форме гипоксии, а также при гипоксии, обусловленной веноартериальным шунтированием (некоторые врожденные пороки сердца и сосудов). Противопоказаний к применению кислородной терапии нет. И все-таки надо помнить, что применение кислородной терапии до некоторой степени опасно при снижении чувствительности дыхательного центра к повышенному содержанию СО2 в крови, что имеет место у лиц пожилого и старческого возраста с наличием церебрального атеросклероза, при органических поражениях центральной нервной системы. У таких людей регуляция дыхания происходит с участием каротидных хеморецепторов, чувствительных к гипоксемии. Устранение гипоксемии может привести к остановке дыхания.
Используется и метод гипокситерапии, основанный на повышении компенсаторных возможностей организма, мощности собственных систем транспорта и утилизации кислорода. Этот метод оказался эффективным при гемической гипоксии (гипопластическая и железодефицитная анемии, пострадиационные нарушения кроветворения), хронических неспецифических заболеваниях легких, гипоксии нагрузки.
Проводится большая работа по изысканию специфических противогипоксических препаратов, корригирующих нарушения на тканевом и клеточном уровнях. Разрабатываются искусственные переносчики электронов в цепи дыхательных ферментов (препараты, подобные цитохрому С, гидрохинону).
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.