
ТЕМА 1. Биохимия – как наука, цели и задачи.
Научные и практические достижения в области биохимии.
Роль российских ученных в развитии биохимии.
Обмен веществ и энергии.
1. Определение биохимии, цели, задачи, структура, связь с другими науками.
Биологическая химия – наука о химическом составе живых организмов и химических процессах, лежащих в основе их жизнедеятельности.
Задача биохимии - идентификация биохимических процессов, выяснение взаимосвязи между структурой и функциями биомолекул, участвующих в реакциях метаболизма.
Объект изучения - химический состав живых организмов и химические процессы, обеспечивающие их существование.
Общая биохимия рассматривает закономерности, общие для всех живых систем.
Частная биохимия рассматривает биохимические особенности отдельных систем, органов, тканей, клеток.
2. Химический состав живых организмов.
Биологически важные химические элементы
Макроэлементы: -Н, О, С, N, P, S – входят в состав всех живых организмов. На 99% живые организмы состоят из Н, О, С, N, из них
- 60-70% - Н и О
-металлы – Na, K, Mg, Ca
-неметаллы – Cl,
Микроэлементы: -Mn,Co,Zn,Cu,B,I,F
Ультрамикроэлементы -Se, U, Hg, Ra, Au, Ag
Белки́ (протеи́ны, полипепти́ды)— высокомолекулярные органические вещества, состоящие из альфа-аминокислот, соединѐнных в цепочку пептидной связью . В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот. Множество их комбинаций создают молекулы белков с большим разнообразием свойств.
Углево́ды (сахара́ , сахариды) — органические вещества, содержащие карбонильную группу и несколько гидроксильных групп.
Липи́ды (от греч. λίπος, lípos — жир) — обширная группа природных органических соединений, включающая жиры и жироподобные вещества. Молекулы простых липидов состоят из спирта и жирных кислот, сложных — из спирта, высокомолекулярных жирных кислот и других компонентов. Содержатся во всех живых клетках. Будучи одним из основных компонентов биологических мембран, липиды влияют на проницаемость клеток и активность многих ферментов, участвуют в передаче нервного импульса, в
мышечном сокращении, создании межклеточных контактов, в
иммунохимических процессах
3. Аминокислоты. Строение и классификация. α-аминокислоты - производные карбоновых кислот, у которых один
или несколько водородных атомов замещены на аминогруппу.
Протеиногенными называются 20 аминокислот, которые кодируются генетическим кодом и включаются в белки в процессе трансляции.
Протеиногенные аминокислоты α-аминокислоты производные
карбоновых кислот, у которых один водородный атом, у αуглерода, замещен а на аминогруппу Протеиногенными называются 20 аминокислот, которые кодируются генетическим кодом и включаются в белки в процессе трансляции.
Классификация аминокислот
• По радикалу Неполярные:аланин, валин, изолейцин, лейцин, пролин, метионин, фенилаланин, триптофан Полярные незаряженные (заряды скомпенсированы) при pH=7: глицин, серин, треонин, цистеин, аспарагин, глутамин, тирозин Полярные заряженные отрицательно при pH=7: аспарагиновая кислота, глутаминовая кислота Полярные заряженные положительно при pH=7: лизин, аргинин, гистидин
• По функциональным группам Алифатические
• Моноаминомонокарбоновые: глицин, аланин, валин, изолейцин, лейцин
• Оксимоноаминокарбоновые: серин, треонин
• Моноаминодикарбоновые: аспарагиновая кислота, глутаминовая кислота
• Амиды моноаминодикарбоновых: аспарагин, глутамин
• Диаминомонокарбоновые: лизин, аргинин
• Серосодержащие: цистеин, метионин
Ароматические: фенилаланин, тирозин, триптофан, гистидин
Гетероциклические: триптофан, гистидин, пролин
Иминокислоты: пролин.
Тема 2. Белки: строение, классификация, биологическое значение.
1.Определение, состав
Белки являются основными биополимерами клеток, за счет которых осуществляются прак-тически все функции организма. Термин «белок» происходит от немецкого слова "Eiweiss", что означает яичный белок или вообще белок. Другое название - протеины, происходит от греческого слова «протос» - первичный.
Белки - линейные неразветвленные полимеры, построенные из аминокислот.
Белки относятся к высокомолекулярным соединениям, в составе которых сотни и тысячи аминокислотных остатков: 2-10 - олигопептиды, 1030 - полипептиды, 30 и более - белки.
Массы атомов и молекул сравнивают с атомной массой углерода 12С, равной 12 дальтон (Да), и выражают в Да или кДа. Масса 1 Да равна 1,661 x 10-24 г. Молекулярная масса пеп-тидов - до 6000 Да, белков от 6000 до 1 000 000 Да и выше.
Информация о структуре белка закодирована в ДНК. Все живые организмы используют 20 идентичных аминокислот и, за некоторым исключением, имеют одинаковый генетический код.
Краткая историческая справка. Начало XIX века - открытие азота в белках (Мульдер); 1820 г. - выделение первой аминокислоты - глицина - из кислотного гидролизата желатина (Браконно); 1871 г. - установление факта расщепления белков до аминокислот пищевари-тельными соками (П. Н. Любавин); 1902 г. - открытие пептидной связи (Фишер); 20-е годы XX века - определение молекулярной массы белков ультрацентрифугированием (Сведберг); 20- е годы XX века - доказательство положения о том, что ферменты являются белками (Самнер, Нортроп, Кунитц); 1955 г. - описание первичной структуры инсулина (Сэнджер); 30-50-е годы - описание пространственной структуры белков с помощью рент-гено-структурного анализа (Перутц, Кендрю). Настоящее время - расшифровка первичной структуры и создание трехмерных моделей нескольких тысяч белков.
Элементный состав белков
Белки преимущественно состоят из 5 главных элементов: С - 50-55 %, Н - 6 - 7,3 %, О - 19-24 %, N - 13-19 %, S - 0-4 %. Кроме вышеперечисленных, белки могут содержать также другие элементы, такие как Р, Fe, Сu, I, Hg, Zn и др. В большинстве белков имеется посто-янное содержание азота, равное 16 %. Поэтому количество белков иногда выражают через азот:
количество белка = содержание азота х 6,25.
Различные ткани отличаются по содержанию белков. В пересчете на сухую массу в селе-зенке 84%, в легких 82%, в мышцах 80%, в костях 2428% белков.
Различают несколько способов классификации белков: 1) по функции, 2) по химической структуре и растворимости и 3) по биологической (пищевой) ценности.
Ферменты или катализаторы, активаторы и ингибиторы ферментов
Для белков-ферментов характерна высокая степень структурирования молекулы, благодаря чему возможен катализ химической реакции в области активного центра и регуляция ак-тивности фермента через взаимодействие эффекторов с аплостерическим центром. Из-вестны белки-активаторы (апопротеин Al, СМ) и ингибиторы (ингибиторы трипсина из поджелудочной железы, соевых бобов; ингибиторы протеиназ из яда гадюки, ингибитор химотрипсина из картофеля).
Гормоны
Как правило, белки (м.м. 20-30 кДа), которые содержат небольшие фрагменты, определяю-щие гормональную активность; относятся к группе непроникающих в клетку гормонов, на поверхности клеток взаимодействуют с рецепторами, гормональный эффект реализуется через внутриклеточные посредники (гормоны гипоталамуса, гипофиза, поджелудочной железы, паращитовидных желез, кальцитонин).
Регуляторные белки
Гистоны стабилизируют структуру ДНК и регулируют функционирование генома (прояв-ление матричной активности ДНК при ослаблении связей с гистонами); гетерогенная группа негистоновых белков (м.м. 5-200 кДа) участвует в формировании нуклеосом и взаи-модействии с хроматином гормон-рецепторных комплексов, в регуляции процессов репликации, транскрипции и трансляции; белки теплового шока (стрессовые белки); G-белки, ре-гулирующие синтез циклических нуклеотидов; онкобелки и антионкобелки, определяющие малигнизацию клетки. Защитные белки
Антитела (иммуноглобулины) вырабатываются в ответ на введение антигенов; белки си-стемы свертывания крови, белки системы комплемента; ферменты обезвреживания ксе-нобиотиков; интерфероны, интерлейкины, лизоцим; белки-антифризы рыб; антивирусные белки растений; антибактериальные белки насекомых.
Транспортные белки
Альбумины и глобулины - переносчики различных веществ в плазме крови. Порины - обра-зуют поры для переноса веществ через клеточные мембраны. Транслоказы - обеспечивают обмен компонентами различных компартментов клеток.
Токсические белки
Высокомолекулярные белковые токсины микроорганизмов и растений представлены тремя типами белков. Мультимерные дифтерийный и холерный токсины, токсин шигеллы (АВ5 протеины) построены из одной субъединицы типа А (20, 28 и 32 кДа, соответственно) и пяти субъединиц типа В (25,12 и 7,7 кДа, соответственно); субъединицы В связываются с клеточной поверхностью, а субъединица А проникает внутрь клетки, где блокирует синтез белков на рибосомах. Аналогично действуют растительные токсины - рицин, абрин, моде-цин, лектин. Энтеротоксин стафилококка или гемолизин кишечной папочки встраивается в плазматическую мембрану, образуют в ней поры, через которые теряются важные компо-ненты цитоплазмы клеток. Токсины ядов змей представлены малыми белками (м.м. 6,7-7 кДа, примерно 60 аминокислотных остатков). Токсические пептиды ядов скорпиона, пчелы и осы состоят в среднем из 45 аминокислотных остатков. Эти токсины связываются с хо-линергическими белками и оказывают нейротоксическое действие.
Структурные белки
Структурные белки являются структурными компонентами мембран, склонны к агрегации и специфическим взаимодействиям (процессы самосборки), содержат в своем составе до 20% гидрофобных аминокислотных остатков, до 40% приходится на α-спиральные участки. Эти белки легко взаимодействуют с фосфолипидами мембран. Структурные функции вы-полняют также белки межклеточного матрикса (коллаген, ретикулин, кератин, кристал-лины, белки ядерного матрикса, белки цитоплазматического скелета.
Сократительные
Участвуют в механическом сокращении для осуществления движения, обладают, как пра-вило, аденозинтрифосфатазной активностью: актин и миозин мышц, белки центральных и периферических фибрилл жгутиков и ресничек простейших, жгутиков сперматозоидов, ту-булин аппарата движения хромосом в процессе митоза, миксомиозин - нитевидный белок из плазмодия гриба фузариума и др.
Рецепторные белки
Во внутренней среде организма служат для взаимодействия с молекулами-биорегулято-рами (сигнальными молекулами). Локализуются в мембранных структурах клеток или мо-гут быть в растворенном состоянии. Клетка, содержащая рецептор, является клеткой-ми-шенью для управляющего химического сигнала, а также для взаимодействия с липопроте-инами или вирусами. Для восприятия сигналов внешней среды известны фоторецепторные белки (опсин), для оценки вкуса - сладкочувствительный белок, для восприятия запаха - обонятельный белок, для восприятия звука - холинорецепторные белки, в жизнедеятельно-сти живых организмов важное место занимает рецепция ферромонов, аттрактантов, репел-лентов, стрессогенных веществ ран.
Эта классификация наиболее распространенная. Она основана на аминокислотном составе, структуре, размере и растворимости. Различают 2 группы белков: простые и сложные (конъюгированные).
1. Простые белки (альбумин, кератин и др.) состоят только из аминокислот и делятся на:
![]() а) фибриллярные белки имеют
палочкообразную вытянутую форму (отношение длины молекулы к диаметру больше
10), нерастворимы в воде, физически прочные; выпол-няют структурные и защитные
функции;
а) фибриллярные белки имеют
палочкообразную вытянутую форму (отношение длины молекулы к диаметру больше
10), нерастворимы в воде, физически прочные; выпол-няют структурные и защитные
функции;
![]() б) глобулярные белки представляют
собой компактные сферические молекулы (отношение длины молекулы к диаметру не
превышает 4), водорастворимы. Глобулярные белки выполняют динамические функции
(ферменты, иммуноглобулины и транспортные белки гемоглобин и альбумины).
б) глобулярные белки представляют
собой компактные сферические молекулы (отношение длины молекулы к диаметру не
превышает 4), водорастворимы. Глобулярные белки выполняют динамические функции
(ферменты, иммуноглобулины и транспортные белки гемоглобин и альбумины).
2. Сложные (конъюгированные) белки состоят из простого белка, комбинированного с небелковым компонентом. Небелковая часть называется простетической группой (или конъюгированной группой). Белок без простетической группы называется апопротеином. Белковая часть с простетической группой называется хололротеином. Простатическая группа играет ключевую роль в функционировании белка. Простые белки (деление по растворимости белков) Альбумины.
Водорастворимые белки, осаждаются сульфатом аммония при 100 % насыщении. В плазме крови человека и животных альбумины составляет 50 % от всех белков; в белке яиц оваль-бумина - до 50 %; в молоке - лактальбумин; апьбумино-подобными белками богаты расте-ния. Поддерживают осмотическое давление и осуществляют транспорт многих веществ, включая ксенобиотики.
Глобулины.
Растворимы в слабых растворах нейтральных солей; осаждаются сульфатом аммония при 50 % насыщении. В воде нерастворимы, поэтому выпадают в осадок при очистке от солей диализом. Глобулины составляют большую часть белков семян многих растений, особенно бобовых и масляничных, например, легумин в семенах гороха, фазеолин - фасоли, эдестин - конопли. Отдельные фракции являются специфическими транспортерами веществ (транскортин - переносит глюкокортикоидные гормоны). Концентрация увеличивается при воспалении - белки острой фазы, участвуют в гуморальном иммунитете - иммуногло-булины. Проламины
Хорошо растворимы в 60-80 % этиловом спирте, в их составе много глу и про и мало лиз, арг и илей. Являются запасными белками злаков: глиадин - зерна пшеницы и ржи, гордеин - зерна ячменя, зеин - зерна кукурузы. Глютелины
Хорошо растворимы в 0,2-2 % растворах щелочей. Содержатся в семенах злаков и зеленых частях растений. Комплекс щелочерастворимых белков семян пшеницы - глютенин, риса - оризенин. Глиадин и глютенин образуют клейковину, которая определяет качество муки и теста. Гистоны
Щелочные белки (12-30 кДа) содержат 20-30 % щелочных аминокислот. Растворимы в сла-бых кислотах (0,2 нормальные растворы), осаждаются аммиаком, спиртом. Не содержат триптофана, а также цистеина и цистина. Входят в состав хроматина, поэтому имеются во всех ядросодержащих клетках. В процессе эволюции - консервативные белки.
Протамины
Щелочные белки (12 кДа) содержат 80 % щелочных аминокислот; отсутствуют или содер-жатся в малом количестве цис, три, асп, тир, фен. Являясь поливалентным органическим катионом, легко образуют комплексы с нуклеиновыми кислотами. Образуют хроматин, в связи с чем представлены во всех ядросодержащих клетках. В большом количестве встре-чаются в сперме рыб - сальмин у лососевых и клупеин у сельди.
Протеиноиды
Труднорастворимые белки, содержат много серы. Фибриллярные белки: фиброин шелка, кератины волос, рогов, копыт, коллагены - белки соединительной ткани, спонгин - белок морских губок и др.
Гликопротеины
Содержат в своем составе гликозидные компоненты различной структуры. Гпикопротеинами являются многие структурные белки, ферменты, рецепторы и т. д. Большинство бел-ков, расположенных на внешней поверхности животных клеток, являются гликопротеи-нами. На долю углеводного компонента приходится от 1-3 % (овальбумин) до 80-90 %
(груп-повые вещества крови). В составе гликопротеинов обнаружено 10 различных моносахари-дов: D-галактоза, D-манноза, D-глюкоза, Nацетилглюкозамин, N- ацетилгалактозамин, дезоксисахара (L-фукоза, Lрамноза), D-ксилоза, L-арабиноза, Типичным компонентом гликопротеинов является нейраминовая кислота (чаще в форме сиаловых кислот). Протеогликаны состоят из небольшой белковой части, к которой ковалентно присоединяется несколько десятков гетерополисахаридных цепей, содержащих в своих молекулах остатки аминосахаров и уроновых кислот. Углеводные компоненты - глюкозамингликаны- пред-ставлены гиалуроновой кислотой, хондроитинсульфатами, гепарансульфатом, кератан-сульфатами.
Липопротеины
В качестве небелковой части содержат молекулы липидов. Эти макромолекулы в значи-тельных количествах находятся в митохондриях, из них в основном состоит эндоплазмати-ческий ретикулум, их обнаруживают в плазме крови и молоке. Инозитолдифосфат-содер-жащий липопротеин выделен из белого вещества мозга, в состав липопротеинов серого ве-щества мозга входят сфинголипиды. У растений значительная часть фосфолипидов в про-топлазме находится в форме липопротеинов. Протеолипиды - комплексы липидов и белков, белковая часть которых содержит преимущественно гидрофобные аминокислоты.
Нуклеопротеины
Содержат нуклеиновые кислоты - РНК и ДНК - в качестве простетических групп.
Металлопротеины
Содержат ионы какого-либо одного или нескольких металлов. К таким белкам принадлежат белки, содержащие негеминовое железо (ферритин, трансферрин и др.). К медьсодержащим белкам относят цитохромоксидазу, пластоцианин (переносчики электронов), белок крови - церулоллазмин; к железосодержащим - лактоферрин (белок молока), трансферрин (белок крови), ферритин и др. Кроме того, известны: никелеплазмин (переносчик никеля в плазме крови), селенопротеины (кровь, мышцы), еанадохром (у морских животных переносчик кислорода).
Фосфопротеины
В качестве простетической группы содержат фосфорную кислоту. К фосфопротеинам от-носят многие питательные белки, например, основной белок молока казеин, белки яичного желтка - вителлин и фосвитин, икры рыб - ихтулин. Они содержат 1-10 % фосфора. Фос-фопротеины найдены в мозге. Кратковременное фосфорилирование-дефосфорилирование ферментов является способом регуляции их активности.
Хромопротеины
В составе белка имеются окрашенные небелковые компоненты. Наиболее распространен-ными представителями хромопротеинов являются флавопротеины и гемопротеины, крас-ное окрашивание которых обусловлено наличием гема с включенным в него атомом железа. К хромопротеинам относят транспортные белки: гемоцианины (моллюски, ракообразные, паукообразные, мечехвосты), гемэритрины (кольчатые черви), хлорокруорины (многоще-тинковые черви).
Пищевая ценность белков определяется наличием незаменимых аминокислот. Согласно этой классификации белки делятся на 3 группы:
1. Полноценные белки. Содержат 10 незаменимых аминокислот в необходимых пропор-циях для обеспечения нормального роста (например, яичный белок, казеин молока).
2. Частично полноценные белки. Эти белки содержат сниженное количество одной или бо-лее незаменимых аминокислот и могут обеспечивать только умеренный рост (например, белок пшеницы и риса содержат недостаточное количество лизина, триптофана). Известно правило, что скорость синтеза белка зависит от незаменимой аминокислоты (лимитирую-щей), концентрация которой наименьшая.
3. Неполноценные белки. Эти белки не содержат одну или более незаменимых аминокис-лот. Не могут обеспечить нормальный рост организма (например, желатин не содержит аминокислоту триптофан).
ЛЕКЦИЯ № 3
НУКЛЕИНОВЫЕ КИСЛОТЫ
План лекции 1. Компоненты нуклеиновых кислот
а) азотистые основания
б) углеводы
в) фосфорная кислота
2. Нуклеозиды
3. Нуклеотиды
4. Вторичная структура ДНК
5. Химические свойства нуклеиновых кислот.
а) кислотный гидролиз
б) щелочной гидролиз
в) ферментативный гидролиз
Нуклеиновые кислоты – важнейшие органические соединения, хранящие всю информацию об отдельной клетке и организме, определяющие его рост и развитие, а также наследственные признаки, передаваемые следующему поколению.
В 1868 г. швейцарский врач Фридрих Мишер выделил из ядер лейкоцитов и спермы лосося новое фосфорсодержащее вещество, соединенное с белками, которое назвал нуклеином (от лат. nucleus – ядро).
Современное название нуклеина – хроматин.
В 1889 г. Рихард Альтман разделил нуклеин на нуклеиновую кислоту и белок и ввел в биохимию термин «нуклеиновая кислота». Нуклеиновые кислоты (ДНК и РНК) представляют собой высокомолекулярные линейные полимеры, построенные из нуклеотидов. Каждый нуклеотид состоит из трех компонентов: азотистого основания, пентозы и остатка фосфорной кислоты.
а) азотистые основания
Азотистые основания – производные ароматических гетероциклических соединений – пурина и пиримидина. В состав нуклеиновых кислот входят два производных пурина – аденин и гуанин, и три производных пиримидина – цитозин, урацил и тимин (рис.1). Все пять азотистых оснований называются главными (мажорными).
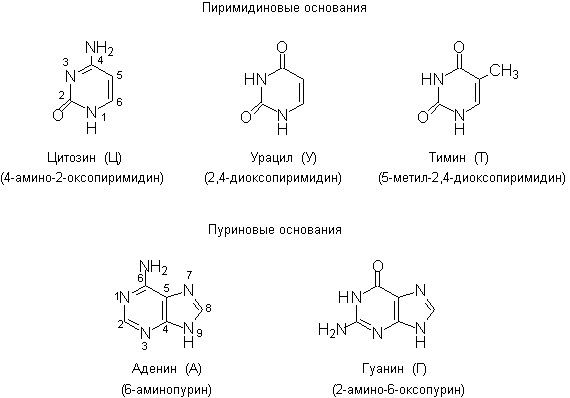
Рис. 1. Основные азотистые
б) углеводы
Углеводные компоненты
Углеводная часть нуклеиновых кислот представлена двумя сходными моносахаридами правого ряда: дезоксирибозой (в ДНК) и рибозой (в РНК), находящимися в β-D-фуранозной форме (рис. 4). Углеродные атомы пентоз номеруются со знаком «штрих», чтобы отличать их от атомов азотистых оснований. Доказано, что замена у дезоксирибозы при С-2’ OH-группы на протон упрочняет связь между С-2’ и С-3’ атомами, что увеличивает прочность молекулы ДНК и способствует компактности её пространственной структуры.
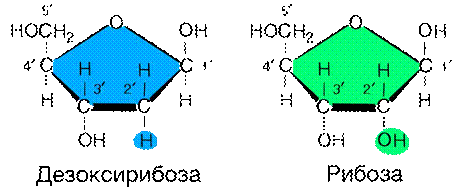
Рис.2. Углеводные компоненты нуклеотидов Фосфорная кислота.
Остатки фосфорной кислоты (H3PO4) входят в состав нуклеотидов и этерифицируют D-рибозу и 2-дезокси-D-рибозу в положениях 3 и 5. В этой связи нуклеотиды и полинуклеотиды можно рассматривать, с одной стороны, как сложные эфиры нуклеозидов (фосфаты), а с другой как кислоты.
Остатки моносахаридов и фосфорной кислоты выполняют структурную функцию и являются носителями гетероциклических оснований.
Нуклеозиды состоят из гетероциклических оснований, связанных с моносахаридом N-гликозидной связью. В образовании этой связи участвуют аномерный атом углерода моносахарида и атомы азота N-1 (у пиримидинового основания) и N-9 (у пуринового основания):
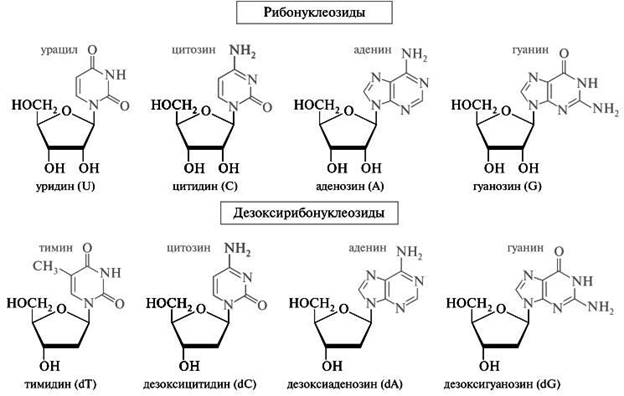
В зависимости от углеводного остатка нуклеозиды делятся на рибонуклеозиды и дезоксирибонуклеозиды. Номенклатурные названия нуклеозидов строятся аналогично названиям гликозидов, например, - аденинрибофуранозид и т. д. Однако чаще используются названия с суффиксами -идин у пиримидиновых и -озин у пуриновых нуклеозидов и приставкой дезокси- у дезоксирибонуклеозидов: цитозин + рибоза = цитидин;
цитозин + дезоксирибоза = дезоксицитидин; аденин + рибоза = аденозин;
аденин + дезоксирибоза = дезоксиаденозин.
Исключением является название тимидин, используемое для дезокситимидина, входящего в состав ДНК.
Нуклеозиды значительно лучше растворимы в воде, чем исходные азотистые основания. Подобно всем гликозидам, нуклеозиды устойчивы к действию щелочей, но при нагревании легко подвергаются кислотному гидролизу с разрывом гликозидной связи и образованием основания и пентозы:
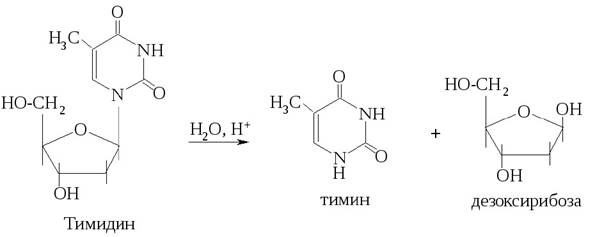
Пиримидиновые нуклеозиды значительно более устойчивы к гидролизу, чем пуриновые. В условиях in vivo гидролиз обоих типов нуклеозидов осуществляется при помощи специфических ферментов, называемых нуклеозидазами.
Нуклеотиды это производные нуклеозидов, которые образуются в результате этерификации пентозного фрагмента фосфорной кислотой. В зависимости от строения пентозы различают рибонуклеотиды (мономерные звенья РНК) и дезоксирибинуклеотиды (мономерные звенья ДНК).
В 2-дезоксирибозе имеются только два положения, по которым может образовываться сложноэфирная связь а именно 3- и 5-положения. В случае рибонуклеотидов фосфатная группа может находиться в положениях 2, 3 и 5. В биологических системах встречаются нуклеотиды всех типов, однако наиболее распространены нуклеозид-5-фосфаты. За счет фосфатного остатка нуклеотиды проявляют свойства кислот и в физиологических условиях (pH 7) находятся в практически полностью ионизированном состоянии.
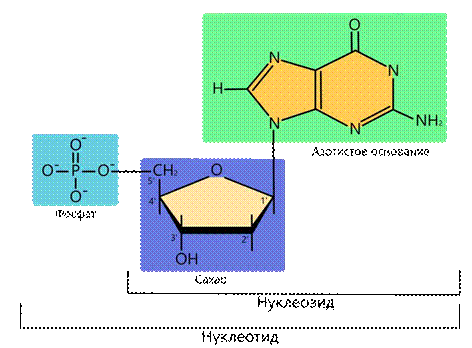
Рис. 1. Строение нуклеотида
Во всех тканях организма в свободном состоянии содержатся не только моно-, но и ди-, а также трифосфаты нуклеозидов. Наиболее известными являются аденозин-5-дифосфат (АДФ) аденозин-5-трифосфат (АТФ).
Нуклеотиды, фосфорилированные в разной степени, способны к взаимопревращениям путем наращивания или отщепления фосфатных групп. Дифосфатная группа содержит одну, а трифосфатная две ангидридные связи, называемые макроэргическими, поскольку они обладают большим запасом энергии. При расщеплении макроэргической связи Р О выделяется энергия, приблизительно равная 32 кДж/моль. Этим объясняется важнейшая роль АТФ как «поставщика» энергии во всех живых клетках.
Ангидридные связи могут гидролизоваться либо специфичными ферментами, либо при кипячении в присутствии HCl. Ни сложноэфирная связь, ни N-гликозидная при этом не расщепляются.
Взаимные превращения АМФ, АДФ и АТФ.
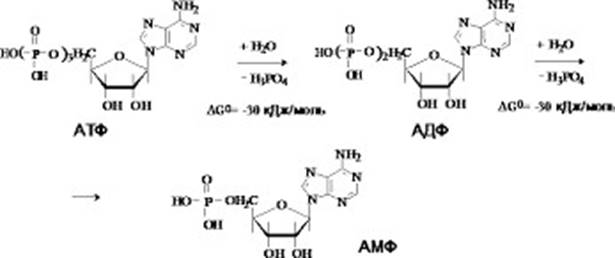
Полинуклеотиды представляют собой линейные гетерополимеры, также состоящие из последовательности мононуклеозидных единиц, соединенных фосфатным мостиком. Полинуклеотиды, состоящие из ковалентно связанных между собой остатков дезоксирибонуклеозидов, называются дезоксирибонуклеиновыми кислотами (ДНК), а полинуклеотиды, состоящие из остатков рибонуклеозидов рибонуклеиновыми кислотами (РНК). В обоих случаях мононуклеозиды связаны между собой при помощи фосфодиэфирных мостиков, соединяющих 3-положение одного мононуклеотида с 5-положением его соседа.
Нуклеиновые кислоты также различаются и по составу входящих в них гетероциклических оснований: урацил входит только в состав РНК, а тимин только в состав ДНК. Аденин, цитозин и гуанин являются постоянными компонентами полинуклеотидов. Молекулярная масса ДНК достигает десятков миллионов. Это самые длинные из известных макромолекул. Значительно меньше молекулярная масса РНК (от нескольких сотен до десятков тысяч). ДНК содержатся в основном в ядрах клеток, РНК в рибосомах и протоплазме клеток.
Первичная структура нуклеиновых кислот.
Первичная структура нуклеиновых кислот это нуклеотидный состав и определенная последовательность нуклеотидных звеньев в полимерной цепи.. Для записи первичной структуры ДНК и РНК используют однобуквенные обозначения нуклеозидов. Приведенные фрагменты ДНК и РНК записывают соответственно: d(A-C-G-T) и (A-C-G-U). Часто букву d опускают, если речь идет о ДНК.
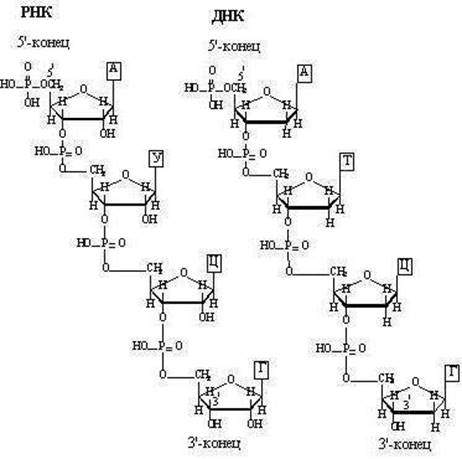
Первичная структура цепи ДНК и РНК.
Нуклеотидный состав ДНК различного происхождения находится в соответствии с правилами Э. Чаргаффа:
1) Все ДНК независимо от их происхождения содержат одинаковое число пуриновых и пиримидиновых оснований. Следовательно, в любой ДНК на каждый пуриновый нуклеотид приходится один пиримидиновый.
2) Любая ДНК всегда содержит в равных количествах попарно аденин и тимин, гуанин и цитозин, что обычно обозначают как А = Т и G = C.
3) Количество оснований, содержащих аминогруппы в положении 4 пиримидинового ядра и 6 пуринового (цитозин и аденин), равно количеству оснований, содержащих оксо-группу в тех же положениях (гуанин и тимин), т. е. A + C=G + T.
Наряду с этим было установлено, что для каждого типа ДНК суммарное содержание гуанина и цитозина не равно суммарному содержанию аденина и тимина, т. е. что (G + C)/(A + T), как правило, отличается от единицы (может быть как больше, так и меньше ее). По этому признаку различают два основных типа ДНК: А-Т-тип с преимущественным содержанием аденина и тимина и GC-тип с преимущественным содержанием гуанина и цитозина.
Для РНК правила Чаргаффа либо не выполняются, либо выполняются с большим приближением.
Вторичная структура нуклеиновых кислот.
Под вторичной структурой нуклеиновых кислот понимают пространственно упорядоченные формы полинуклеотидных цепей. Вторичная структура ДНК представляет собой две параллельные неразветвленные полинуклеотидные цепи, закрученные вокруг общей оси в двойную спираль.
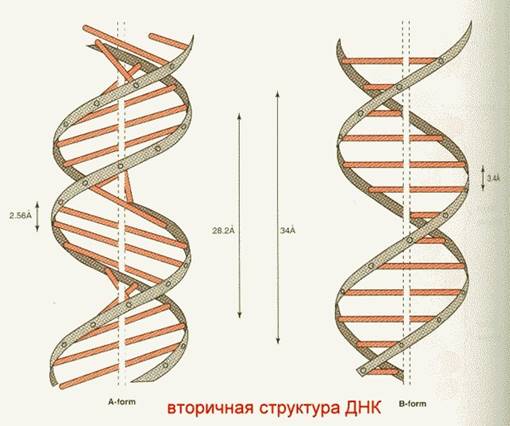
Вторичная структура ДНК.
Такая пространственная структура удерживается множеством водородных связей, образуемых азотистыми основаниями, направленными внутрь спирали. Эти основания составляют комплементарные пары (от лат. complementum дополнение). Образование водородных связей между комплементарными парами оснований обусловлено их пространственным соответствием. Так, пиримидиновое основание комплементарно пуриновому:
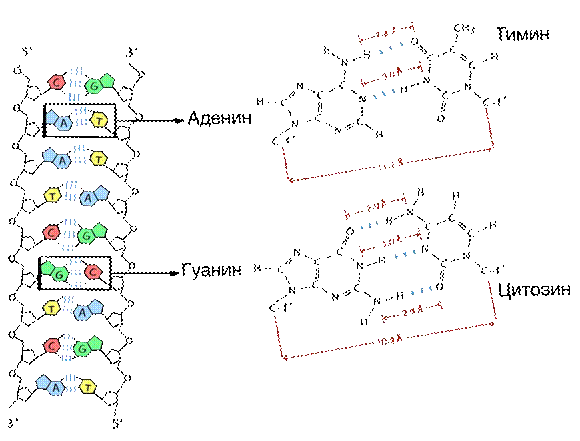
Водородные связи между другими парами оснований не возникают по пространственным причинам. Таким образом, в ДНК:
ТИМИН (Т) комплементарен АДЕНИНУ (А)
ЦИТОЗИН (C) комплементарен ГУАНИНУ (G)
Комплементарность оснований определяет комплементарность цепей в молекулах ДНК. Водородные связи возникают между пуриновым основанием одной цепи и пиримидиновым основанием другой цепи. Иными словами, пуриновым основаниям аденину и гуанину в одной цепи будут соответствовать пиримидиновые основания тимин и цитозин в другой цепи. Таким образом, полинуклеотидные цепи, образующие двойную спираль, не идентичны, но комплементарны между собой:
В сдвоенной молекуле ДНК суммарно число групп А равно числу групп Т, а число групп G числу C.
Комплементарность полинуклеотидных цепей служит химической основой главной функции ДНК хранения и передачи наследственных признаков. Способность ДНК не только хранить, но и использовать генетическую информацию определяется следующими ее свойствами:
1) Молекулы ДНК способны к репликации (удвоению), т.е. могут обеспечить возможность синтеза других молекул ДНК, идентичных исходным, поскольку последовательность оснований в одной из цепей двойной спирали контролирует их расположение в другой цепи;
2) Молекулы ДНК могут совершенно точным и определенным образом направлять синтез белков, специфичных для организмов данного вида.
Вторичная структура РНК.
В отличие от ДНК, молекулы РНК состоят из одной полинуклеотидной цепи и не имеют строго определенной пространственной формы (рис. 3.), т.к. вторичная структура РНК зависит от их биологических функций. Полимерная цепь РНК приблизительно в десять раз короче, чем у ДНК.
Комплементарными парами в РНК являются цитозин-гуанин и урациладенин.
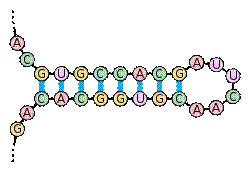
Вторичная структура РНК.
Основная роль РНК непосредственное участие в биосинтезе белка. Известны три вида клеточных РНК, которые отличаются по местоположению в клетке, составу, размерам и свойствам, определяющим их специфическую роль в образовании белковых макромолекул:
1) Информационные (матричные) РНК передают закодированную в ДНК информацию о структуре белка от ядра клетки к рибосомам, где и осуществляется синтез белка;
2) Транспортные РНК собирают аминокислоты в цитоплазме клетки и переносят их в рибосому; молекулы РНК этого типа "узнают" по соответствующим участкам цепи информационной РНК, какие
аминокислоты должны участвовать в синтезе белка;
3) Рибосомные РНК обеспечивают синтез белка определенного строения, считывая информацию с информационной (матричной) РНК.
Химические свойства нуклеиновых кислот.
ДНК и РНК имеют много общих химических и физических свойств. Так, нуклеиновые кислоты хорошо растворимы в воде и плохо растворяются в водных растворах кислот. Существенные различия ДНК и РНК связаны, в основном, с их отношением к гидролизу.
Гидролиз в кислой среде.
Мягкий кислотный гидролиз ДНК оказывает весьма избирательное действие: он приводит к расщеплению N-гликозидных связей между пуриновыми основаниями и дезоксирибозой, связи пиримидиндезоксирибоза при этом не затрагиваются. В результате образуется ДНК, лишенная пуриновых оснований. Гидролиз РНК, проводимый в аналогичных условиях, приводит к образованию пуриновых оснований и пиримидиновых нуклеозид-2'(3')- фосфатов.
Кислотный гидролиз в жестких условиях, приводит к разрыву всех Nгликозидных связей как ДНК, так и РНК и образованию смеси пуриновых и пиримидиновых оснований.
Гидролиз в щелочной среде.
В щелочной РНК легко гидролизуются до нуклеотидов, которые в свою очередь, расщепляются с образованием нуклеозидов и остатков фосфорной кислоты. ДНК, в отличие от РНК, устойчивы к щелочному гидролизу.
Ферментативный гидролиз.
Гидролиз ДНК и РНК также протекает и при участии специфических ферментов нуклеаз. Эти ферменты избирательно действуют на 3- и 5- сложноэфирные связи. Так, фосфодиэстераза, выделенная из яда змей, расщепляет все 3-связи как в ДНК, так и в РНК с образованием нуклеозид5- фосфатов. Фосфодиэстераза, выделенная из селезенки быка, наоборот, гидролизует только 5-связи и высвобождает только нуклеозид-3-фосфаты. Известны дезокси-рибонуклеазы, расщепляющие связи только между определенными парами мононуклеотидов их используют для направленного гидролиза РНК.
Гидролиз ДНК И РНК проводят, в основном, для установления их нуклеотидного состава. Далее выделенные смеси анализируют с использованием хроматографических и спектральных методов анализа, а также электрофореза.
Тема 4. Ферменты. Свойства и химическая природа ферментов. Классификация. Механизм действия ферментов. Классификация ферментов.
2. Свойства ферментов.
3. Механизм действия ферментов.
4. Определение активности ферментов.
5. Иммобилизованные ферменты.
Ферменты представляют собой высокоспециализированный класс веществ белковой природы, используемых живыми организмами для осуществления многих тысяч взаимосвязанных химических реакций, совокупность которых составляет сущность обмена веществ. Ферменты – биологические катализаторы, функциональные единицы клеточного метаболизма. Действуя в строго определенной последовательности, они катализируют сотни многостадийных реакций, в ходе которых расщепляются молекулы питательных веществ, запасается и преобразуется химическая энергия, из простых молекул-предшественников строятся макромолекулы, входящие в состав клетки. Подсчитано, что живая клетка может содержать до 3000 различных ферментов, каждый из которых ускоряет ту или иную химическую реакцию, т.е. выполняет функцию биологических катализаторов. Подобно неорганическим катализаторам, ферменты повышают скорость химических реакций за счет понижения энергии активации. Как и катализаторы неорганической природы, они не вызывают каких-либо химических реакций, а лишь ускоряют существующие и неизменны после реакции. Однако, биологические катализаторы по ряду признаков резко отличаются от неорганических катализаторов.
Свойства ферментов
Первое различие состоит в том, что ферменты «работают» в очень мягких условиях и проявляют чрезвычайно высокую каталитическую активность. Так, например, гидролитический распад белка до аминокислот в присутствии неорганических катализаторов (кислот или щелочей) осуществляется при температуре 1000С и выше за несколько часов. Этот же процесс при каталитическом участии специфических ферментов требует всего нескольких минут и происходит при температуре 30-400С. Принято считать, что неорганический катализатор может ускорить химические реакции до 103, фермент – до 1020 раз.
Второе различие заключается в том, что ферменты обладают необыкновенно высокой специфичностью действия. Каждый фермент катализирует, как правило, одну единственную химическую реакцию. Один фермент – одна реакция. Тем не менее, по специфичности ферменты подразделяются на 2 вида: 1) ферменты с абсолютной специфичностью и 2) ферменты с относительной или групповой специфичностью.
Для ферментов с относительной специфичностью субстратом является группа атомов в молекуле или связь. Например, пепсин. Субстратом для него является пептидная группировка атомов или пептидная связь. Пепсин расщепляет, как известно, белки, т.е. те молекулы, в которых присутствует пептидная группировка.
Для ферментов с абсолютной специфичностью субстратом является сама молекула, вступающего в химическую реакцию вещества. Большинство ферментов обладают абсолютной специфичностью.
Один из важных различий между неорганическими катализаторами и ферментами связан с белковой природой последних. Ферменты проявляют свою активность только в условиях водных растворов и при физиологических значениях рН и температуры среды.
Классификация и номенклатура ферментов
По строению ферменты могут быть простыми и сложными белками. Небелковую часть сложного фермента, которая легко может отделяться от апофермента (белковая часть фермента) и которая, как правило, представлена сложными органическими соединениями, называют коферментом.

Рис. 1. Строение сложного белка-фермента.
Небелковая часть фермента может быть представлена и простыми веществами неорганической природы, чаще ионами металлов, которые оказываются прочно связанными с апоферментом. В этом случае её называют - кофермент.
Из большого числа ферментов можно выделить особый класс - регуляторные ферменты, которые могут воспринимать различные метаболические сигналы и в соответствии с ними изменять свою каталитическую активность. Благодаря действию таких ферментов все ферментативные системы в клетке функционируют координированно, что является необходимым для поддержания жизнеспособности отдельных клеток и целых организмов.
Различают несколько групп регуляторных ферментов. Наибольшее значение из них имеет аллостерические ферменты, которые кроме активного центра содержат ещё второй центр, называемый аллостерическим. Аллостерический центр - это участок молекулы фермента служащий для присоединения определенного низкомолекулярного вещества – медиатора. Медиаторы бывают двух видов: активаторы и ингибиторы, которые вызывают изменение конфигурации активного центра и соответственно, либо увеличение, либо снижение каталитической активности фермента.
В настоящее время известно около 5000 различных ферментов. Согласно международной системе классификации и номенклатуры различают 6 классов ферментов. Каждый класс подразделяется на подклассы, а подклассы на группы.
1. Оксидоредуктазы - катализируют окислительно - восстановительные реакции.
2. Трансферазы - катализируют реакции переноса функциональных
групп и остатков молекул.
3. Гидролазы - катализируют реакции гидролиза.
4. Лиазы - катализируют негидролитическое расщепление связей образованных с участием углерода.
5. Изомеразы - катализируют реакции изомеризации.
6. Лигазы (синтетазы) - катализируют реакции синтеза или образования новых связей.
По международной системе классификации оксидоредуктазы подразделяются на 23 подкласса, трансферазы – на 10, гидролазы – на 13 и т.д.
Системные названия ферментов указывают на тип катализируемой реакции, на характер субстрата и продукта реакции. Очень часто эти названия бывают длинными и в связи с этим неудобными для использования. Международная система классификации и номенклатуры ферментов предполагает присвоение каждому ферменту кодового номера (шифр) из четырехзначной цифры. Первая цифра кода указывает на класс, вторая – на подкласс, третья – на группу, а четвертая – порядковый номер фермента в группе.
Механизм действия ферментов
Первым шагом в механизме действия ферментов всегда является связывание фермента со своим специфичным субстратом и образование фермент-субстратного комплекса.
Образование фермент-субстратного комплекса сопряжено с наличием в его молекуле особых участков, ответственных за связывание субстрата и за непосредственный контакт с ним - активные центры. Это уникальное сочетание аминокислотных остатков, располагающихся в определенной части белковой молекулы, сюда же входят и небелковые компоненты фермента.
Фермент – субстратный комплекс всегда распадается на свободный фермент и продукты реакции.
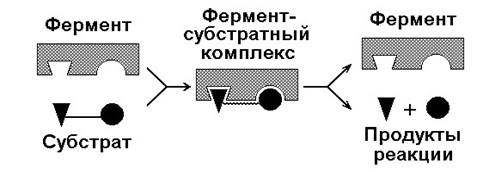
Рис. 2. Схема механизма действия фермента.
Механизм действия ферментов может быть рассмотрен с двух позиций: с точки зрения событий в активном центре и изменения энергетики химических реакций.
С энергетической точки зрения ферменты обеспечивают высокую скорость реакций при оптимальных условиях, существующих в клетке, путём понижения уровня энергии активации (рис.14). Ферменты снижают высоту энергетического барьера, в результате возрастает количество реакционноспособных молекул, следовательно, увеличивается скорость реакции.
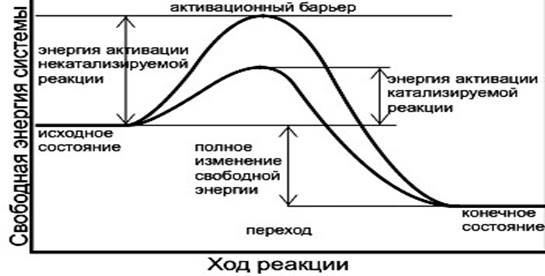
Рис.
3.
Схема механизма действия фермента по изменению энергетики катализируемой реакции.
Активный центр на всех этапах ферментативного катализа нельзя рассматривать как пассивный участок для связывания субстрата. Это комплексная молекулярная "машина", использующая разнообразные химические механизмы, способствующие превращению субстрата в продукт.
В активном центре фермента субстраты располагаются так, чтобы участвующие в реакции функциональные группы субстратов находились в непосредственной близости друг к другу. Активный центр фермента также способствует дестабилизации межатомных связей в молекуле субстрата, что облегчает протекание химической реакции и образование продуктов.
Механизмы ферментативного катализа определяются ролью функциональных групп активного центра фермента в химической реакции превращения субстрата в продукт. Выделяют 2 основных механизма ферментативного катализа: кислотно-основной катализ и ковалентный катализ.
Кроме активного центра, некоторые ферменты имеют дополнительный, регуляторный или аллостерический (allos – другой, steros – пространственный) центр, с которым взаимодействуют аллостерические регуляторы или модуляторы (активаторы и ингибиторы). Аллостерические ферменты подразделяются на две группы: 1) гомотропные 2) гетеротропные.
Гомотропные ферменты активизируются своими же субстратами, т.е. у них субстрат и активатор одно и то же вещество. Активный центр одновременно может выполнять функции аллостерического.
Изучение аллостерической регуляции активности ферментов, особенно процессов ингибирования, имеют большое практическое значение. Оно позволяет определять последовательность реакций в сложных многоступенчатых биохимических процессах, выявлять изоформы различных ферментов. Кроме того, различные ингибиторы ферментов широко применяются в медицинской практике как терапевтические средства при патологиях инфекционной и незаразной этиологии.
Определение активности ферментов
Одним из направлений энзимологии является энзимодиагностика, которая развивается, во-первых, по пути применения высокоочищенных ферментов в качестве избирательных реагентов для открытия и количественного определения с диагностической целью химических веществ в биологических жидкостях, во-вторых, по пути обнаружения и определения активности самих ферментов в различных тканях.
Для диагностики различных патологических процессов в организме широко используются ферментные тесты, отличающиеся от других химических диагностических тестов высокой чувствительностью и специфичностью.
В настоящее время известно множество различных тестов, основанных на количественном определении активности ферментов в различных тканях и биологических жидкостях. При диагностике различных заболеваний используют показатели активности десятков ферментов и их изоферментов.
В клинической практике часто определяют активность аспартатаминотрансферазы, аланинаминотрансферазы, лактатдегидрогеназы, аргиназы, алкоголдегидрогеназы, цитохромоксидазы, амилазы и др.
В основе всякого количественного определения ферментативного действия или активности действия фермента находятся изменения, которые происходят с субстратом соответствующей ферментативной реакции.
Наиболее часто активность действия ферментов выражается количеством вещества, которое за строго определенное время и в строго определенных условиях подвергалось тому или иному изменению. Ферментативное действие может быть оценено также временем, необходимым для строго определенного изменения субстрата.
Согласно заключения Комиссии по ферментам Международного биохимического союза, единица активности (Е) фермента – это количество фермента, которое катализирует превращение одного микромоля субстрата за 1 мин при стандартных условиях.
Иммобилизованные ферменты
Иммобилизованные ферменты (от лат. immobiiis - неподвижный), препараты ферментов, молекулы которых связаны с твердой матрицей, или носителем (как правило, полимером), сохраняя при этом полностью или частично свои каталитические свойства.
В конце 60-х – начале 70-х гг. на базе технической биохимии, химической энзимологии и ряда инженерных дисциплин возникло новое научно-техническое направление биотехнологии – инженерная энзимология, к которой относят систему методов получения, очистки, стабилизации и применения ферментов.
Ферменты в качестве биологических катализаторов применяются в различных отраслях промышленности - пищевой, текстильной, фармацевтической, кожевенной, в медицине, сельском хозяйстве, в тонком органическом синтезе и т.д. Более широкое использование ферментов в биотехнологии до последнего времени сдерживалось вследствие ряда причин, а именно: трудоемкости отделения ферментов от исходных реагентов и продуктов реакции; нестабильности ферментов при хранении и при действии различных факторов; высокой стоимости чистых ферментных препаратов.
Создание биокатализаторов нового поколения - иммобилизованных, т.е. связанных ферментов открыло перед прикладной энзимологией новые перспективы.
Иммобилизованные ферменты имеют существенные преимущества. Так, например, они легко отделимы от реакционной среды. Иммобилизованные ферменты технологичны, что определяется возможностью вести биотехнологический процесс непрерывно и регулировать скорость катализируемой реакции. Подбором соответствующих носителей и методов иммобилизации можно целенаправленно модифицировать такие свойства ферментов, как специфичность, зависимость активности от рН и температуры среды и др.
Иммобилизованные ферменты можно использовать, главным образом, в трех основных направлениях:
1. Аналитическое исследование различных химических и биологических веществ, как в живом организме, так и в объектах окружающей среды.
2. Лечебные средства
3. Применение в различных производствах.
Тема 5. Химизм действия ферментов. Дыхательные ферменты.
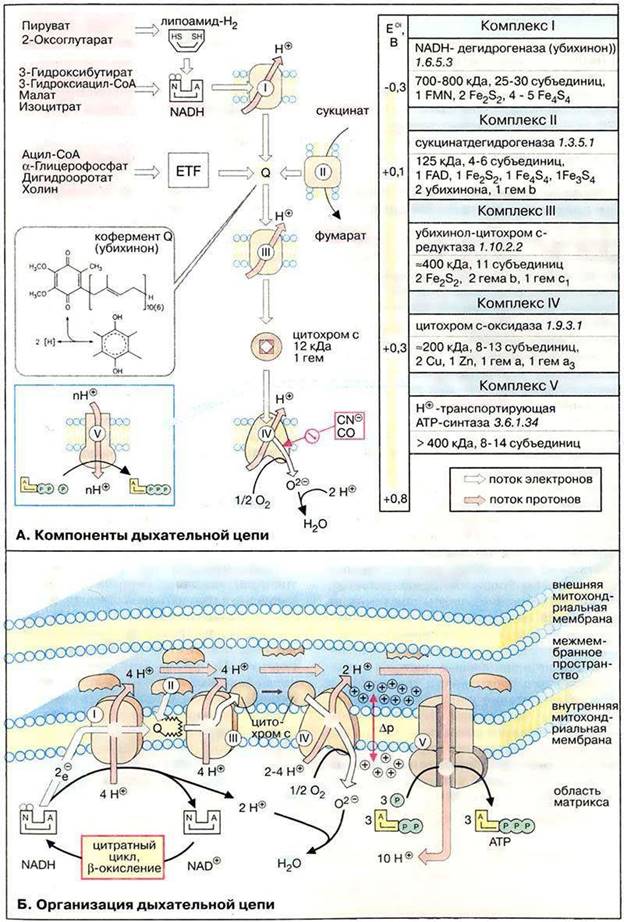
Дыхательная цепь включает множество белков-переносчиков
Всего цепь переноса электронов (англ. electron transport chain) включает в себя разнообразные белки, которые организованы в 4 больших мембраносвязанных мульферментных комплекса. Также существует еще один комплекс, участвующий не в переносе электронов, а синтезирующий АТФ.
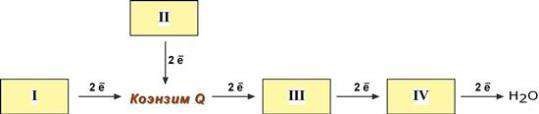
Блок-схема дыхательной цепи
Дыхательная цепь — это система окислительно-восстановительных ферментов, встроенных во внутреннюю мембрану митохондрии.
Этот комплекс также имеет рабочее название НАДН-дегидрогеназа, содержит ФМН, 42 белковых молекулы, из них не менее 6 железосерных белков.
1. Принимает электроны от НАДН и передает их на коэнзим
Q (убихинон).
2. Переносит 4 иона Н+ на наружную поверхность внутренней митохондриальной мембраны.
Железосерные белки (FeS-белки) – это белки содержащие атомы железа, которые соединены с атомами серы и с серой остатков цистеина. В результате образуется железо-серный центр.

Данный комплекс как таковой не существует, его выделение условно. К нему относятся ФАД-зависимые ферменты, расположенные на внутренней мембране – например, ацил-SКоА-дегидрогеназа (β-окисление жирных кислот), сукцинатдегидрогеназа (цикл трикарбоновых кислот), митохондриальная глицерол-3-фосфат-дегидрогеназа (челночный механизм переноса атомов водорода).
1. Восстановление ФАД в окислительно-восстановительных реакциях.
2. Обеспечение передачи электронов от ФАДН2 на железосерные белки внутренней мембраны митохондрий. Далее эти электроны попадают на коэнзим Q (убихинон).
По другому данный комплекс называется цитохром с редуктаза. В его составе имеются молекулы цитохрома b и цитохрома c1, железо-серные белки. Комплекс представляет собой 2 мономера, в каждом из которых насчитывается 11 полипептидных цепей. Функция
1. Принимает электроны от коэнзима Q и передает их на цитохром с.
2. Переносит 2 иона Н+ на наружную поверхность внутренней митохондриальной мембраны.
В этом комплексе находятся цитохромы а и а3, он называется также цитохромоксидаза, состоит из 13 субъединиц. В комплексе имеются ионы меди, соединенные с белками комплекса через HS-группы цистеина, и формирующие центры, подобные тем, что имеются в железо-серных белках.
1. Принимает электроны от цитохрома с и передает их на кислород с образованием воды.
2. Переносит 4 иона Н+ на наружную поверхность внутренней митохондриальной мембраны.
Пятый комплекс – это фермент АТФ-синтаза, состоящий из множества белковых цепей, подразделенных на две большие группы:
• одна группа формирует субъединицу FО (произносится со звуком "о", а не "ноль" т.к олигомицин-чувствительная) – ее функция каналообразующая, по ней выкачанные наружу протоны водорода устремляются в матрикс.
• другая группа образует субъединицу F1 – ее функция каталитическая, именно она, используя энергию протонов, синтезирует АТФ.
Механизм работы АТФ-синтазы получил название вращательный катализ.
Тема 6. Обмен белков. Биосинтез белка в живой клетке.
Белковый обмен, совокупность превращений белков и продуктов их распада — аминокислот в организмах. Белковый обмен — существенная часть обмена веществ. Поскольку обмен аминокислот тесно связан с обменом других азотистых соединений, белковый обмен часто включают в более общее понятие азотистого обмена.
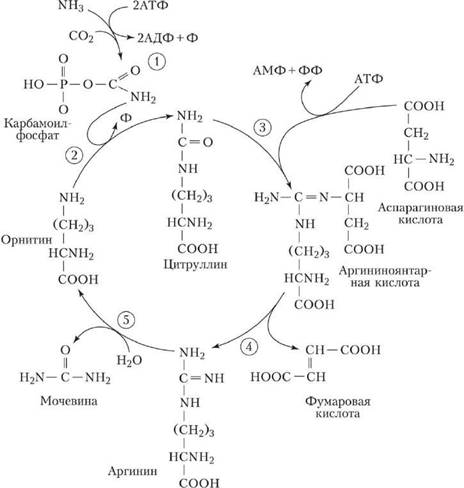
Цикл мочевины или орнитиновый цикл (цикл Кребса — Гензелейта) — последовательность биохимических реакций млекопитающих и некоторых рыб, в результате которой азотсодержащие продукты распада преобразуются в орнитин и мочевину, которая в свою очередь выделяется почками.
Орнитиновый цикл
Большая часть свободного аммиака, а также аминного азота в составе АК (в основном глутамин, аланин) поступают в печень, где из них синтезируется нетоксичное и хорошо растворимое в воде соединение — мочевина. Мочевина является основной формой выведения азота из организма человека.
Синтез мочевины происходит в цикле, который замыкается орнитином. Цикл открыли в 40-х годах XX века немецкие биохимики Г. Кребс и К. Гензелейт.
Мочевина (карбамид) — полный амид угольной кислоты — содержит 2 атома азота, один из аммиака, другой – из асп.
Предварительно в митохондриях под действием карбамоилфосфатсинтетазы Iс затратой 2 АТФ аммиак связывается с СО2с образованием карбамоилфосфата:
(Карбамоилфосфатсинтетаза II локализована в цитозоле клеток всех тканей и участвует в синтезе пиримидиновых нуклеотидов).
1. В митохондриях орнитинкарбамоилтрансферазапереносит карбамоильную группу карбамоилфосфата на орнитин и образуется — цитруллин.
2. 2. В цитозоле аргининосукцинатсинтетазас затратой 1 АТФ (двух макроэргических связей) связывает цитруллин с аспартатом и образует аргининосукцинат (аргининоянтарная кислота). Фермент нуждается в Mg2+. Аспартат — источник второго атома азота мочевины.
3. 3. В цитозоле аргининосукцинатлиаза(аргининсукциназа) расщепляет аргининосукцинат на аргинин и фумарат (аминогруппа аспартата оказывается в аргинине).
4. 4. В цитозоле аргиназагидролизует аргинин на орнитин и мочевину. У аргиназы кофакторы ионы Са2+или Мn2+, ингибиторы - высокие концентрации орнитина и лизина.
Образующийся орнитин взаимодействует с новой молекулой карбамоилфосфата, и цикл замыкается.
Фумарат, образующийся в орнитиновом цикле, в цитозолепревращается в ЩУК, который переаминируется с аланином или глутаматом с образованием аспартата. Аланин поступает главным образом из мышц и клеток кишечника:
Малат может направиться в митохондрии и включиться в ЦТК.
Пируват, образующийся в этих реакциях из аланина, используется для глюконеогенеза.
Общее уравнение синтеза мочевины:
CO2+NH3+ асп + 3 АТФ + 2 Н2О → мочевина + фумарат + 2АДФ +
АМФ + 2Фн + ФФн
На синтез 1 мочевины расходуются 4 макроэргических связи 3 АТФ. Дополнительные затраты энергии связаны с трансмембранным переносом веществ и экскрецией мочевины. Энергозатраты при этом частично компенсируются:
• при окислительном дезаминировании глутамата образуется 1 молекула НАДН2, которая обеспечивает синтез 3 АТФ;
• в ЦТК, при превращении малата в ЩУК образуется еще 1
молекула НАДН2, которая также обеспечивает синтез 3 АТФ; Орнитиновый цикл в печени выполняет 2 функции:
1. превращение азота АК в мочевину, которая экскретируется и предотвращает накопление токсичных продуктов, главным образом аммиака;
2. синтез аргинина и пополнение его фонда в организме.
Полный набор ферментов орнитинового цикла есть только в гепатоцитах. Отдельные же ферменты орнитинового цикла обнаруживаются в разных тканях. Вэнтероцитах, есть карбамоилфосфатсинтетаза I и орнитинкарбамоилтрансфераза, следовательно, может синтезироваться цитруллин. Впочкахесть аргининосукцинатсинтетаза и аргининосукцинатлиаза. Цитруллин, образовавшийся в энтероцитах, может поступать в почки и превращаться там в аргинин, который переносится в печень и гидролизуется аргиназой. Активность этих рассеянных по разным органам ферментов значительно ниже, чем в печени.
Тема 7. Гормоны. Механизм действия гормонов. Классификация.
Одной из удивительных особенностей живых организмов является их способность сохранять постоянство внутренней среды – гомеостаз – при помощи механизмов саморегуляции, в которых одно из главных мест принадлежит гормонам. У высших животных координированное протекание всех биологических процессов не только в целостном организме, но и в микропространстве отдельной клетки и даже в отдельном субклеточном образовании (митохондрии, микросомы) определяется нейрогуморальными механизмами, сложившимися в процессе эволюции. При помощи этих сигналов организм воспринимает разнообразные сигналы об изменениях в окружающей и внутренней средах и тонко регулирует интенсивность процессов обмена. В регуляции этих процессов, в осуществлении протекания множества реакций гормоны занимают промежуточное звено между нервной системой и действием ферментов, которые непосредственно регулируют скорость обмена веществ. Любые нарушения синтеза или распада гормонов, вызванные разнообразными причинными факторами, включая заболевания эндокринных желез (состояние гипо- и гиперфункции) или изменения структуры и функций рецепторов и внутриклеточных посредников, приводят к изменению нормального синтеза ферментов и соответственно к нарушению метаболизма.
Учение о гормонах выделено в самостоятельную науку – эндокринологию. Современная эндокринология изучает химическую структуру гормонов, образующихся в железах внутренней секреции, зависимость между структурой и функцией гормонов, молекулярные механизмы действия, а также физиологию и патологию эндокринной системы. В наши дни эндокринология превратилась в один из самых бурно развивающихся разделов биологической науки. Она имеет свои цели и задачи, специфические методологические подходы и методы исследования.
1. Общее представление о гормонах
Характерная особенность многоклеточных организмов – наличие дифференцированных тканей. Последние обладают специализированными функциями, обеспечивающими выживание организма.
Для координации тканевых ответов на изменение условий внешней и внутренней среды необходимы механизмы межклеточной коммуникации. В ходе эволюции сформировались две основные системы, выполняющие эту функцию: нервная, для которой характерны высокая скорость распространения сигнала, строгая направленность и кратковременность действия и эндокринная, для которой характерны наличие разнообразных гормонов, которые секретируются специфическими железами и затем транспортируются, воздействуя на прилежащие или удаленные ткани. Эти две системы перекрываются и накладываются друг на друга. Важную роль играет нервная регуляция эндокринной функции; многие нейромедиаторы (катехоламины, ацетилхолин) сходны с гормонами по способу синтеза, высвобождения, транспорту и механизму действия.
Гормоны (от греч. hormaino – побуждаю) − это биологически активные вещества, синтезируемые специализированными клетками и железами внутренней секреции, поставляемые кровью в другие органы и ткани, где оказывают регулирующее влияние на обмен веществ и физиологические функции.
Однако исходное определение слишком узко. Установлено, что гормоны способны воздействовать на прилегающие клетки данной ткани (паракринный эффект), а также на клетки, в которых они синтезируются (аутокринный эффект).
Учение о гормонах выделено в самостоятельную науку - эндокринологию (изучает химическую структуру гормонов, зависимость между структурой и функцией, механизм действия, физиологию и патологию эндокринной системы).
Гормонам присущи следующие общие биологические признаки.
1. Специфичность − своеобразие его химической структуры, функции и места образования; Подобные вещества выделяют также клетки некоторых органов, не относящихся к железам внутренней секреции (клетки желудочнокишечного тракта, тучные клетки соединительной ткани, клетки почек, клетки эндотелия и др.). В отличие от гормонов эти биологически активные вещества действуют в местах образования и обозначаются как гормоноиды (гормоноподобные вещества).
2. Высокая биологическая активность (эффект проявляется в присутствии чрезвычайно малых концентраций гормона (10-11 – 10-6 М).
3. Секретируемость – ряд специфических, биологически активных веществ может образовываться в эндокринной железе в качестве промежуточных продуктов биосинтеза гормонов. Например, 11дезоксикортизол, образующийся в коре надпочечников и обладающий биологической активностью, в норме не секретируется в кровь.
4. Дистанционность действия, т.е. гормоны регулируют обмен веществ и функции эффекторных клеток на расстоянии.
В основе каждой эндокринной функции (кортикостероидной, тиреоидной, соматотропной и т.д.) лежит образование специфических гормонов в соответствующей железе. Однако, биосинтез и секреция гормонов не исчерпывают понятия «эндокринная функция». Эндокринная функция – сложноорганизованная система, состоящая из следующих компонентов:
- биосинтез и секреция гормонов (или прогормонов) в железе;
- процессы специфической регуляции и саморегуляции функций
железы;
- специфический транспорт секретируемых гормонов в крови;
- система специфического метаболизма гормонов в периферических тканях и их экскреция;
- специфическое взаимодействие гормонов с реагирующими тканями.
Биосинтез и секреция гормонов. Центральным звеном любой эндокринной функции является продукция гормонов соответствующей железой. Продукция гормонов железой складывается из двух процессов.
1. Биосинтез гормона, в результате которого формируется его химическая структура.
2. Секреция образовавшегося гормона из железы в кровь.
Биосинтез гормонов - это цепь биохимических реакций, приводящих к формированию специфической структуры гормональной молекулы. Как химическая природа активных гормонов, так и механизмы их биосинтеза весьма разнообразны – могут образовываться из липидных предшественников, в результате модификации аминокислоты тирозина, путем белкового синтеза. Некоторые гормоны синтезируются в своей конечной форме (альдостерон, гидрокортизон, эстрадиол, катехоламины), другие перед секрецией или для приобретения полной биологической активности должны подвергаться модификации (инсулин синтезируется в виде проинсулина, у паратгормона есть по крайней мере два пептидапредшественника, содержащие последовательности, отщепление которых необходимо для проявления полной биологической активности).
Генетический контроль биосинтеза осуществляется в зависимости от природы синтезируемого гормона:
- либо на уровне иРНК самого гормона (в случае белково-пептидных гормонов);
- либо на уровне ферментов, которые осуществляют биосинтез того либо иного гормона (для гормональных стероидов, производных аминокислот и небольших пептидов типа рилизинг-факторов).
Секреция гормонов представлена совокупностью процессов, обусловливающих освобождение синтезированных гормональных соединений из эндокринных клеток в венозную кровь и лимфу. Секреторные процессы протекают спонтанно, обеспечивая некий базальный уровень гормонов в циркулирующих жидкостях. Секреторный процесс осуществляется железистыми клетками отдельными дискретными порциями. “Квантовый“ характер гормональной секреции обусловлен, по-видимому, циклическим характером процессов биосинтеза, внутриклеточного депонирования и траспорта гормонов. По особенностям механизмов секреторные процессы можно разделить на 3 типа.
1. Освобождение гормонов из клеточных секреторных гранул (секреция белково-пептидных гормонов и катехоламинов).
2. Освобождение гормонов из белковосвязанной формы (секреция тиреоидных гормонов).
3. Относительно свободная диффузия гормонов через клеточные мембраны (стероидные гормоны).
Катаболизм гормонов.
Катаболизм гормонов - это совокупность процессов ферментативной деградации исходной химической структуры гормональных соединений. В катаболизирующих органах наряду с необратимой инактивацией могут протекать обменные процессы, приводящие к активации, реактивации, взаимопревращениям гормонов и возникновению новой гормональной активности. К активации относится превращение тироксина в трииодтиронин, к реактивации - переход кортизона в кортизол, примером взаимопревращений гормонов разного типа являются превращения андрогенов в эстрогены в гипоталамусе. В качестве показателя интенсивности метаболических процессов на уровне целого организма используется величина периода полураспада. Это время, за которое концентрация введенной в кровь порции радиоактивного гормона необратимо уменьшается вдвое. Тиреоидные гормоны, в особенности тироксин, катаболизируется очень медленно (сутки), а катехоламины - исключительно быстро (секунды, минуты). Основные пути катаболизма для стероидных гормонов – это восстановление двойной связи в кольце А, окислениевосстановление некоторых кислородсодержащих функциональных групп и гидроксилирование углеродных атомов. Для катехоламинов существует два доминирующих пути – это окислительной дезаминирование боковой цепи и оксиметилирование гидроксила у С3 атома кольца. Периферический метаболизм белково-пептидных гормонов изучен в настоящее время недостаточно. Однако, известно, что они быстро исчезают из крови вследствие работы специфических пептидаз. В составе выводимых жидкостей плохо растворимые в воде метаболиты стероидных гормонов экскретируются в основном в форме глюкуронидов, сульфатов и некоторых других эфиров, обладающих высокой водорастворимостью. Метаболиты аминокислотных гормонов экскретируются главным образом в свободной форме. Метаболиты белково-пептидных гормонов выводятся преимущественно в форме свободных аминокислот или их солей и небольших пептидов. Гормональные метаболиты экскретируются в первую очередь с мочой и желчью.
2. Классификация гормонов
По химической природе гормоны можно разделить на 3 группы: a) гормоны белковой и пептидной природы (гормоны гипофиза, поджелудочной железы, паращитовидных желез, тимуса); b) низкомолекулярные производные аминокислот (гормоны мозгового слоя надпочечников и иодтиронины щитовидной железы); c) гормоны стероидной природы (гормоны половых желез и коркового слоя надпочечников).
3. Механизм действия гормонов
В управлении метаболизмом гормоны участвуют следующим образом. Поток информации о состоянии внутренней среды организма и об изменениях, связанных с внешними воздействиями поступает в нервную систему, там перерабатывается и формируется ответный сигнал. Он поступает к органам– эффекторам в виде нервных импульсов по цетробежным нервам и опосредованно через эндокринную систему.
Пунктом, где сливаются потоки нервной и эндокринной информации является гипоталамус – сюда поступают нервные импульсы из разных отделов головного мозга. Они определяют продукцию и секрецию гипоталамических гормонов, влияющих в свою очередь через гипофиз на продукцию гормонов периферическими эндокринными железами. Гормоны периферических желез, в частности мозгового вещества надпочечников, контролируют секрецию гипоталамических. В конечном счете, содержание гормона в кровотоке поддерживается по принципу саморегуляции. Высокий уровень гормона выключает или ослабляет по механизму отрицательной обратной связи его образование, низкий уровень усиливает продукцию.
Гормоны действуют на ткани избирательно, что обусловлено неодинаковой чувствительностью к ним тканей. Органы и клетки, наиболее чувствительные к влиянию определенного гормона, принято называть мишенью гормона (орган-мишень или клетка-мишень).
Концепция ткани- мишени. Ткань-мишень – это такая ткань, в которой гормон вызывает специфическую физиологическую (биохимическую) реакцию. Общую реакцию ткани-мишени на действие гормона определяет целый ряд факторов. Прежде всего, это локальная концентрация гормона вблизи ткани-мишени, зависящая от:
1. скорости синтеза и секреции гормона;
2. анатомической близости ткани-мишени к источнику гормона;
3. констант связывания гормона со специфическим белком-
переносчиком (если такой существует);
4. скорости превращения неактивной или малоактивной формы гормона в активную;
5. скорости исчезновения гормона из крови в результате распада или выведения.
Собственно тканевой ответ определяется: - относительной активностью и (или) степенью занятости специфических рецепторов - состоянием сенситизации - десентизации клетки. Специфичность гормонов по отношению к клеткам-мишеням обусловлена наличием у клеток специфических рецепторов.
Все рецепторы гормонов можно разделить на 2 типа:
1) локализованные на наружной поверхности клеточной мембраны; 2) расположенные в цитоплазме клетки.
Свойства рецепторов:
- четкая субстратная специфичность;
- насыщаемость;
- сродство к гормону в пределе биологических концентраций гормона; - обратимость действия.
В зависимости от того, где в клетке происходит передача информации, можно выделить следующие варианты действия гормонов:
1) Мембранный (локальный).
2) Мембранно-внутриклеточный или опосредованный.
3) Цитоплазматический (прямой).
Мембранный тип действия реализуется в месте связывания гормона с плазматической мембраной и заключается в избирательном изменении ее проницаемости. По механизму действия гормон в данном случае выступает как аллостерический эффектор транспортных систем мембраны. Так, например, обеспечивается трансмембранный перенос глюкозы под действием инсулина, аминокислот и некоторых ионов. Обычно мембранный тип действия сочетается с мембранно-внутриклеточным.
Мембранно-внутриклеточное действие гормонов характеризуется тем, что гормон не проникает в клетку, а влияет на обмен в ней через посредник, который является как бы представителем гормона в клетке – вторичным посредником (первичный посредник – сам гормон). По типу вторичных посредником действуют циклические нуклеотиды (цАМФ, цГМФ) и ионы кальция.
Тема 8. Витамины Классификация. Распространение витаминов в природе. Общее действие витаминов. Авитаминоз. Витамины группы А, D, E , К. Витамины группы В. Биотин. Аскорбиновая кислота.
.1. Общая характеристика витаминов
Витамины — низкомолекулярные, разнообразные по химическому строению органические вещества, принимающие участие во многих реакциях клеточного метаболизма.
В отличие от белков, жиров и углеводов витамины 1- не являются структурными компонентами клетки; 2 - не используются в качестве источника энергии.
Большинство витаминов не синтезируются в организме человека и животных, но некоторые синтезируются микрофлорой кишечника и тканями в минимальных количествах, поэтому основным источником витаминов является пища.
Витамины — вещества нестойкие, они легко разрушаются высокой температурой, действием сильных гидроксидов, кислородом воздуха, ионизирующими излучениями и другими факторами.
Витамины были открыты в конце XIX столетия благодаря работам русских ученых Н.И. Лунина и В.В. Пашутина, впервые показавших необходимость для полноценного питания кроме белков, жиров и углеводов еще каких то неизвестных веществ. Н.И. Лунин провел эксперимент на 2 группах мышей, одну из которых он кормил цельным молоком, а другую – смесью из белков, жиров и углеводов молока. Вторая группа мышей стала болеть, отставать в росте и развитии. В 1912 году польский ученый Коземир Функ, изучая компоненты, входящие в состав шелухи риса и предохраняющие от болезни бери-бери, и полагая, что в их состав должны входить аминные группировки, предложил назвать эти неизвестные вещества витаминами, т.е. аминами жизни.
Известно 3 состояния связанные с витаминами:
1 – авитаминоз - полное отсутствии витаминов в кормах.
2 - гиповитаминоз - недостаток витаминов в кормах.
3 – гипервитаминоз – избыточное поступление витаминов с кормом.
В настоящее время авитаминозы практически отсутствуют, но часто встречаются гиповитаминозы. Причины их вызывающие делятся на 2 группы: 1- экзогенные - отсутствие или недостаток витаминов в рационе; 2 – эндогенные – а) нарушение процессов всасывания витаминов в желудочнокишечном тракте при его заболевании, при заболевании печени и желчного пузыря; 2)наличие в кормах антибиотиков и сульфаниламидных препаратов, которые подавляют кишечную микрофлору, вырабатывающую витамины; 3) некоторые физиологические состояния организма (беременность, острые и хронические заболевания, тяжелая работа, рост и развитие молодняка, высокая продуктивность), при котором необходимо повышенное потребление витаминов.
Определенное значение в развитии авитаминозов и гиповитаминозов имеют антагонисты витаминов (антивитамины), близкие по структуре к соответствующим витаминам. Антивитамины являются их «ложными заменителями» и включаясь в естественную цепь реакций обмена, нарушают его нормальное течение. Очевидно, в основе действия антивитаминов лежит «конкурентное» вытеснение антивитамином соответствующего витамина из ферментного комплекса. В результате образуется недеятельный фермент, метаболизм нарушается и возникает тяжелое заболевание.
В качестве примеров антивитаминов могут быть такие вещества: дикумарол — витамин К, сульфамидные препараты— парааминобензойная кислота, аминоптерин — фолиевая кислота, дезоксипиридоксин — витамин В6, пиритиамин — тиамин (B1), пиридин-3-сульфокислота — амид никотиновой кислоты (РР), а также не исключается антивитаминное действие солей тяжелых металлов в желудочно-кишечном тракте.
2. Классификация и номенклатура витаминов
По химическому строению витамины делят на витамины алифатического ряда, ациклического ряда, ароматического ряда, гетероциклического ряда. По физико-химическим свойствам витамины разделяют на две группы: витамины, растворимые в жирах (липовитамины), и витамины, растворимые в воде (гидровитамины).
Витамины принято обозначать большими буквами латинского алфавита (A, D, Е, В1, В2 и т. д.), а также по болезни (которую излечивает данный витамин) с прибавкой «анти» (антиксерофтальмический, антирахитный, антиневритный и т. д.) или по химическому (условному) названию (ретинол, кальциферол, биотин, аскорбиновая кислота и т. д.).
К группе жирорастворимых витаминов относятся витамины A, D, Е, К и F, а водорастворимым — В1, В2, В3, В5, В6, Вс, B12, С, Р, Н. К группе витаминоподобных веществ относятся холин, инозит, витамины В13, В15 убихинон и др.
3. Жирорастворимые витамины
Витамин А, ретинол, антиксерофтальмический По химическому строению витамин А представляет собой продукт конденсации βионового кольца, двух остатков изопрена и первичного спирт:
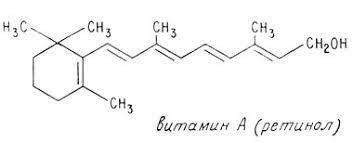
Β ионовое кольцо остаток изопрена ретинол – витамин А1
Биохимические функции. Витамин А принимает участие в реакциях светоощущения, а именно участвует в образовании сложного белка родопсина, который состоит из белка опсина и витамина А (ретиналь)- зрительного пигмента сетчатки глаза.
При недостатке или отсутствии в организме животных витамина А наблюдают остановку роста, снижении продуктивности, легкой восприимчивостью к инфекции.
Нахождение в природе. В свободном виде витамин А содержится в печени рыб (треска, тунец, палтус) – до 37 000 мг/100г, печени к.р.с. – 30 мг/100г, рыбьем жире, молозиве и молоке коров, в рыбной и мясокостной муке и других кормах животного и растительного происхождения. Витамин D, антирахитический, кальциферол Роль витамина D в обмене веществ.
Витамин D влияет на всасывание кальция из кишечника в кровь. Витамина D индуцирует синтез в стенке кишечника белка-переносчика, транспортирующего кальций через мембраны ворсинок кишечника в кровь.
Витамины группы D являются производными стероидов. Известно более 10 производных стероидов, обладающих активностью витамина D. Физиологическое значение для питания животных имеют только витамины D2 и D3.
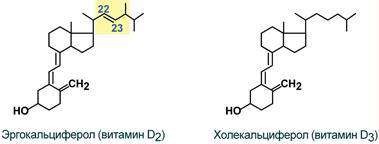
Недостаток витаминов группы D приводит к возникновению рахита у молодых животных и остеомаляции (ломкость костей) у взрослых, у старых - остеопороз.
Распространение в природе. Витаминов группы D много в печени и печеночном жире, рыбьем жире, рыбной муке, яичном желтке, молоке и других кормах животного происхождения. Растения содержат мало витамина
D, за исключением кукурузы в фазе восковой спелости. Витамин
Е, антистерильный, токоферол
Витамин Е представляет собой группу веществ, которые являются производными хромана и называются токоферолами. В настоящее, время известно 7 токоферолов, но в природе широко распространены лишь α-, β- и γ-токоферолы. Наивысшей биологической активностью обладает α – токоферол:
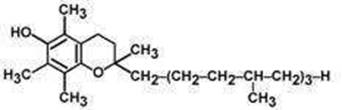
Биологическая роль. Витамины группы Е действуют в организме как биокатализаторы играют роль антиокислителей по отношению к определенным жирным кислотам, витамину А и каротинам. α - токоферол влияет на процесс клеточного дыхания, тесно связан с активностью ферментов, содержащих S. Защищает клeтoчные мембраны,мембраны митохондрий, рибосом и ядра.
Недостаток витамина вызывает у самцов дегенеративные изменения в семенниках, приводящие к бесплодию вследствие нарушения или прекращения сперматогинеза.
Распространение в природе: Витамины группы Е относят к числу устойчивых и широко распространенных в природе соединении. Наиболее богаты витамином Е семена злаков и отжатые из нихмасла (масло хлопковое – 350 мг на 100 гр продукта), a также ягоды шиповника и семена яблок. Много витамина Е находится в мышцах свиней, крупного рогатого скота и овец, сливочном масле и яичном желтке.
Витамин К, антигеморрагический, филлохинон
Биологическая роль. Витамин К существует в нескольких формах – витамерах: К1 – филлохинон, К2 – мезохинон. Витамин К необходим для синтеза в печени некоторых белков и ферментных систем необходимых для свертывания крови. Витамин K1 принимает участие в переносе электронов в дыхательной цепи и окислительном фосфорилировании
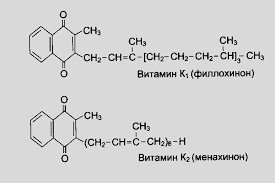
При гиповитаминозе К у животных появляются подкожные и внутримышечные кровоизлияния (гемморагии) и снижается скорость свертывания крови, возникают анемии. Ухудшается общее состояние, выпадает шерсть. К недостатку особенно чувствительны птицы. Антивитамины – дикумарол, салициловая кислота и кокцидиостатики.
Распространение в природе: Витамином К богаты зеленые корма и все виды травяной муки. Значительное количество витамина К содержится в листьях каштана и ягодах рябины. Кроме того, высокое содержание этого витамина отмечается в рыбной и мясокостной муке, печени свиней и других тканях. Витамин К2 синтезируется микроорганизмами в том числе микрофлорой толстого отдела кишечника и преджелудков жвачных.
Витамин F, полиненасыщенные жирные кислоты, антисклеротический
Витамин F (англ. fat – жир) представляет собой набор полипенасыщенных жирных кислот. Наиболее распространены из этих кислот: линолевая, линоленовая и арахидоновая. Они широко представлены в растительных маслах (кукурузное, льняное, подсолнечное и др.) и не синтезируются в организме животных и человека.
Линолевая С17Н31СООН 18:2 (9;12)
Линоленовая С17Н29СООН 18:3 (9;12;15)
Арахидоновая С19Н31СООН 20:4 (5;8;11;14)
Одним из характерных признаков недостатка линолевой, линоленовой и арахидоновой кислот является нарушение обмена холина, холестерола и фосфора.
Тема 9. Углеводы – основа жизнедеятельности живых организмов.
Классификация. Моносахариды, взаимопревращение, свойства. Функции углеводов
1. Энергетическая (глюкоза, гликоген).
2. Структурная (гиалуроновая кислота).
3. Антикоагулирующая (гепарин).
4. Гомеостатическая (поддерживает, в частности, водноэлектролитный баланс и осмотическое давление крови).
5. Механическая (входят в состав соединительной ткани).
Классификация углеводов
Моносахариды, которые не могут быть гидролизованы на более простые сахара. В зависимости от числа атомов углерода их подразделяют на триозы, тетрозы, пентозы, гексозы. В зависимости от присутствия альдегидной или кетоновой группы на альдозы и кетозы.
Дисахариды состоят из двух остатков моносахаридов:
1)
![]() сахароза
состоит из остатков глюкозы и фруктозы, соединенных -1,4-гликозидной связью;
сахароза
состоит из остатков глюкозы и фруктозы, соединенных -1,4-гликозидной связью;
2)
![]() лактоза
состоит из остатков глюкозы и галактозы, соединенных -1,4-гликозидной связью;
лактоза
состоит из остатков глюкозы и галактозы, соединенных -1,4-гликозидной связью;
3)
![]() мальтоза
состоит из двух остатков глюкозы, соединенных -1,4гликозидной связью;
мальтоза
состоит из двух остатков глюкозы, соединенных -1,4гликозидной связью;
4)
целлобиоза состоит из двух остатков глюкозы, соединенных ![]() 1,4-гликозидной
связью.
1,4-гликозидной
связью.
Гомополисахариды - длинные разветвленные цепи, состоящие из одних и тех же моносахаридов:
1)
![]()
![]() крахмал - полимер глюкозы,
соединенной -1,4 и -1,6гликозидными связями. При этом неразветвленные цепи
образуют амилозу (20%), а разветвленные амилопектин (80%);
крахмал - полимер глюкозы,
соединенной -1,4 и -1,6гликозидными связями. При этом неразветвленные цепи
образуют амилозу (20%), а разветвленные амилопектин (80%);
2) гликоген - животный крахмал, состоящий из остатков глюкозы. Это более разветвленный полимер, чем крахмал. При частичном гидролизе крахмала или гликогена образуются декстрины (более короткие
разветвленные цепи);
3)
![]() целлюлоза
- главный компонент структурной основы растительных клеток. Это линейный
полимер глюкозы, соединенной -1,4гликозидными связями.
целлюлоза
- главный компонент структурной основы растительных клеток. Это линейный
полимер глюкозы, соединенной -1,4гликозидными связями.
Гетерополисахариды состоят из разных мономеров:
1) гепарин содержит остатки D-глюконат-2-сульфита и Nацетилглюкозамин-6-сульфата;
2) гиалуроновая кислота состоит из остатков D-глюкуроновой кислоты и остатков N-ацетилглюкозамина. Входит в состав соединительной ткани и участвует в регуляции проницаемости кканей.
Переваривание и всасывание углеводов
У моногастричных животных в ротовой полости под действием амилазы (a, b) слюны происходит частичный гидролиз гликозидных связей полисахаридов (крахмала). Но активность этого фермента низкая, особенно у плотояндых.
В желудке специфических ферментов нет, а амилаза при низкой рН быстро инактивируется.
В тонком отделе кишечника происходит основной гидролиз сахаров. Крахмал под действием амилазы поджелудочной железы, протоки которой открываются в 12-перстную кишку расщепляется до мальтозы и изомальтозы. Этот дисахарид, а также сахароза и лактоза расщепляются специфическими гликозидазами - мальтазой, изомальтазой, сахаразой и лактазой. Эти ферменты продуцируются клетками слизистой и не поступают в просвет, а действуют на поверхности оболочки кишечника. Это т.н. пристеночное пищеварение. Дисахариды расщепляются до моносахаридов: глюкозы, фруктозы и галактозы, которые всасываются в стенки кишечника и поступают в кровь. Проникновение моносахаридов через клеточные мембраны происходит путем облегченной диффузии при участии специальных ферментов транслоказ. Глюкоза и галактоза еще проникают и путем активного транспорта за счет градиента концентраций ионов Na+, который создается Na+-К+-АТФ-азой (насос).
У полигастричных животных в ротовой полости переваривание сахаров не происходит из-за отсутствия ферментов.
В рубце (первом из преджелудков) происходит 50% переваривания сахаров. Ферменты вырабатываются микрофлорой рубца (мальтаза, сахараза, целлюлаза). Образовавшиеся в результате ферментативного гидролиза поли- и дисахаридов моносахара под действием бактерий рубца подвергаются процессам брожения, среди которых выделяют следующие виды:
1) уксуснокислое (Глю = уксусная кислота + СО2);
2) пропионовокислое (Глю = пропионовая кислота + СО2);
3) маслянокислое (Глю = масляная кислота + СО2);
4) молочнокислое (Глю = молочная кислота + СО2).
Все эти кислоты называются летучими жирными кислотами (ЛЖК). Наилучший вариант, когда уксуснокислое брожение составляет 70% и хуже когда преобладает маслянокислое. ЛЖК всасываются в стенки сетки и книжки и идут на энергетические нужды организма.
В сычуге (истинный желудок, имеет строение как и у моногастричных) переваривания углеводов не происходит из-за отсутствия ферментов.
В тонком отделе кишечника идет переваривание остатков сахаров как и у моногастричных животных.
Гликолиз
Анаэробное превращение глюкозы локализуется в цитозоле и
включает два этапа из 11 ферментативных реакций.
Первый этап гликолиза – подготовительный, здесь происходит затрата энергии АТФ, активация глюкозы и образование из нее триозофосфатов.
Первая реакция гликолиза сводится к превращению глюкозы в реакционноспособное соединение за счет фосфорилирования 6-го, не включенного в кольцо, атома углерода. Эта реакция является первой в любом превращении глюкозы, катализируется гексокиназой.
Вторая реакция необходима для выведения еще одного атома углерода из кольца для его последующего
фосфорилирования
(фермент глюкозофосфат-изомераза). В результате образуется фруктозо-6-фосфат.
Третья реакция – фермент фосфофруктокиназа фосфорилируе т фруктозо-6-фосфат с образованием почти симметричной молекулы фруктозо-1,6дифосфата. Эта реакция является главной в регуляции скорости гликолиза.
В четвертой реакции фруктозо-1,6дифосфат разрезается пополам фруктозо-1,6дифосфат-альдолазой с образованием двух фосфорилированных триоз-изомеров – альдозы глицеральдегида (ГАФ) и кетозы диоксиацетона (ДАФ).
Пятая реакция подготовительного этапа – переход глицеральдегидфосфата и диоксиацетонфосфата друг в друга при участии триозофосфатизомеразы.
Равновесие реакции сдвинуто в пользу диоксиацетонфосфата, его доля составляет 97%, доля глицеральдегидфосфата – 3%. Эта реакция, при всей ее простоте, определяет дальнейшую судьбу глюкозы:
при нехватке энергии в клетке и активации окисления глюкозы диоксиацетонфосфат превращается в глицеральдегидфосфат, который далее окисляется на втором этапе гликолиза,при достаточном количестве АТФ, наоборот, глицеральдегидфосфат изомеризуется в диоксиацетонфосфат, и последний отправляется на синтез глицеррол-3-фосфата для образования фосфатидной кислоты и далее тривцилглицеролов.
![]() Второй этап гликолиза – это освобождение энергии,
содержащейся в глицеральдегидфосфате, и запасание ее в форме АТФ.
Второй этап гликолиза – это освобождение энергии,
содержащейся в глицеральдегидфосфате, и запасание ее в форме АТФ.
Шестая реакция гликолиза
(фермент глицеральдегидфосфат-дегидрогеназа) – окисление глицеральдегидфосфата до кислоты и присоединение к ней фосфорной кислоты приводит к образованию макроэргического соединения 1,3дифосфоглицериновой кислоты и НАДН.
В седьмой реакции (фермент фосфоглицераткиназа) энергия фосфоэфирной связи, заключенная в 1,3дифосфоглицерате тратится на образование АТФ. Реакция получила дополнительное название – реакция субстратного фосфорилирования, что уточняет источник энергии для получения макроэргической связи в АТФ (от субстрата реакции) в отличие от окислительного фосфорилирования (использование энергии электрохимического градиента ионов водорода на мембране митохондрий).
Восьмая реакция – синтезированный в предыдущей реакции 3-фосфоглицерат под влиянием фосфоглицератмутазы изомеризуется в 2-фосфоглицерат.
Девятая реакция – фермент енолаза отрывает молекулу воды от 2фосфоглицериновой кислоты и приводит к образованию макроэргической фосфоэфирной связи в составе фосфоенолпирувата.
переносе пируваткиназой макроэргического
фосфата с фосфоенолпирувата на АДФ с образованием пировиноградной кислоты и АТФ.
Последняя реакция бескислородного окисления глюкозы, одиннадцатая – образование молочной кислоты из пирувата под действием лактатдегидрогеназы. Важно то, что эта реакция осуществляется только в анаэробных условиях. Эта реакция необходима клетке, так как НАДН, образующийся в 6-й реакции, в отсутствие кислорода не может окисляться в митохондриях.
Тема 10. Общая характеристика липидов. Классификация.
Биологическое значение Физические и химические свойства жиров.
Липиды- это гидрофобные вещества биологического происхождения; они плохо растворимы в воде и хорошо – в органических растворителях.
Химическая классификация липидов
В зависимости от способности к гидролизу с образованием в щелочной среде солей высших карбоновых кислот (мыл) липиды делятся на две группы:
1. Неомыляемые – однокомпонентные (не подвергаются гидролизу): а) жирные кислоты б) эйкозаноиды-гормоны, производные ПНЖК в) стерины (ХС) и стероиды (желчные кислоты, стероидные гормоны, витамин Д) г) изопреноиды (Q, витамины А, Е, К)
2.Омыляемые: а) простые липиды (двухкомпонентные): жиры, стероиды (эфиры ХС), воски б) сложные липиды (трех - и более компонентные)
• фосфолипиды, которые в зависимости от входящего в их состав спирта делятся на глицеро- и сфингофосфолипиды
• гликолипиды (цереброзиды и ганглиозиды).
По биологической классификации липиды делятся на три группы: I. Жиры, которые выполняют следующие функции:
1. Энергетическая (1 грамм жира при окислении дает 9 ккал, в то время как белки и углеводы – по 4 ккал. Поэтому жителям низкотемпературных регионов для восполнения теплоэнерготрат необходима большая доля жиров в пищевом рационе).
2. Корреляция с плодовитостью (половое развитие – это результат достаточной выработки половых гормонов, а также гормона лептина, который синтезируют клетки белой жировой ткани. При отсутствии достаточного количества жира, которое в норме составляет в среднем у мужчин – 10 кг, у женщин – 17 кг, снижается плодовитость у мужчин, а у женщин нарушается менструальный цикл и, следовательно, снижается вероятность оплодотворения яйцеклетки)
3. Резерв эндогенной воды, которая образуется в ДЦ, куда при окислении отдают свои водороды жирные кислоты – самые восстановленные соединения.
4. Источники жирорастворимых витаминов – А, Д, Е, К
. 5. Предшественники других важных веществ (например, ацетил-КоА).
6. Защитный барьер (теплоизоляция, защита от механических воздействий).
II. Липоиды. К ним относятся фосфо- и гликолипиды, ХС
1. Мембранная- это главная функция липоидов, так как все мембраны представляют собой белково-липидные комплексы (протеолипиды)
2. Специфические функции (изложены ниже, см. «Функции липоидов»).
III. Биологически активные вещества
1. Жирорастворимые витамины (А, Д, Е, К)
2. Липидные гормоны: стероиды (эстрадиол, тестостерон, кортизол, альдостерон, прогестерон, кальцитриол ), эйкозаноиды (простаноиды и лейкотриены), фосфолипиды (ФАТ), ретиноиды (ретиноат)
3. Липидные вторые посредники (ИФ3, ДАГ, ФИФ2, ФИФ3).
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.