
План учебного занятия № 20
Дата Предмет Химия группа
Ф.И.О. преподавателя: Кайырбекова И.А.
Тема: Циклоалканы.
Цели: Изучить циклоалканы, как один из классов карбоциклических соединений.
Задачи: Образовательные:
- продолжить формирование понятия об основных классах углеводородов; начать формировать понятие о карбоциклических соединениях; изучить строение, номенклатуру и изомерию циклоалканов; рассмотреть основные способы получения и применения циклоалканов; изучить химические свойства циклоалканов и генетическую связь с другими классами углеводородов.
Развивающие:
- развивать когнитивную сферу учащихся ; общеучебные умения и навыки учащихся; развивать умения анализировать и делать самостоятельные выводы;
Воспитательные:
- прививать культуру умственного труда и сотрудничества; воспитывать дисциплинированность; коллективизм и чувство ответственности; способствовать созданию благоприятного психо-эмоционального климата на уроке;
Тип урока: урок усвоения новых знаний.
ІІ. Ожидаемые результаты:
А) Учащиеся должны знать: строение, свойства циклоалканов
Ә) Учащиеся должны уметь: сравнивать, доказывать
б) учащиеся должны владеть: работы с химическими реактивами соблюдая ТБ
ІІІ. Метод и приемы каждого этапа занятия: словесно- наглядный, объяснительно- илюстративный IV. Средства: интерактивная доска, учебник
Ход урока
1. Организационный момент. Вступление. Оценка эмоционального состояния учащихся по 10-балльной шкале.
 2. Проверка домашнего задания. Решить задачу:
2. Проверка домашнего задания. Решить задачу:
При сжигании 2,1 г вещества образуется 6,6 г
оксида углерода (IV) и 2,7 г воды. Плотность паров этого вещества по воздуху равна
2,91. Определите молекулярную формулу данного вещества.
3. Фронтальная беседа по вопросам:
а) Какие вещества называют гомологами?
изомерами?
б) Почему углеводороды называют предельными?
в) Почему углеводородная цепь (у предельных
углеводородов) имеет зигзагообразное строение? Почему эта цепь может принимать
в пространстве разные формы?
г) Почему атомы углерода соединяются в цепи?
д) В чем причина многообразия органических
соединений?
 II. Изучение нового материала (лекция)
II. Изучение нового материала (лекция)
1. Понятие о циклопарафинах.
Кроме рассмотренных предельных углеводородов с
открытой цепью атомов - парафинов, существуют углеводороды замкнутого,
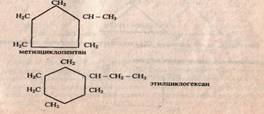
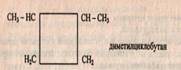
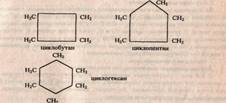
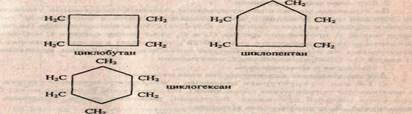
циклического строения. Их называют циклопарафинами, например:
Общая формула циклопарафинов: СпН2п.
Циклопарафины называют также циклоалканами. Пяти-
и шестичленные циклопарафины были впервые открыты в нефти профессором
Московского университета В. В. Марковниковым. Отсюда их другое название - нафтены.
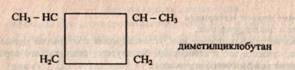
Молекулы циклопарафинов часто содержат боковые углеродные цепи:
 2. Строение циклопарафинов. Каждый атом углерода в циклоалканах находится в состоянии sp3-гибридизации
и образует четыре δ-связи С - С и С - Н. В простейших циклах С3 и С4 углы между связями С -
С сильно отличаются от тетраэдрического угла 109°28 что создает в молекулах
напряжение и обеспечивает их высокую реакционную способность.
2. Строение циклопарафинов. Каждый атом углерода в циклоалканах находится в состоянии sp3-гибридизации
и образует четыре δ-связи С - С и С - Н. В простейших циклах С3 и С4 углы между связями С -
С сильно отличаются от тетраэдрического угла 109°28 что создает в молекулах
напряжение и обеспечивает их высокую реакционную способность.
![]()
 Свободное вращение вокруг связей С-С, образующих цикл, невозможно.
Свободное вращение вокруг связей С-С, образующих цикл, невозможно.
3. Изомерия и номенклатура. Для циклоалканов
характерны два вида изомерии.
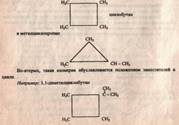
а) 1-й вид — структурная изомерия -
изомерия углеродного скелета Но структурная изомерия может быть обусловлена
разными причинами. Во-первых, размером цикла. Например,
для циклоалкана С4Н8 существует
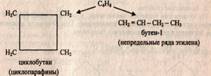
два вещества: Также к структурной изомерии относится межклассовая. Например,
для вещества С4Н8 можно
записать структурные формулы веществ, относящихся к разным классам
углеводородов.
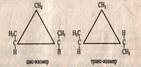
б) 2-й вид - пространственная изомерия у некоторых замещенных циклоалканов обусловлена отсутствием свободного вращения вокруг связей С - С в цикле.Например, в молекуле 1,2-диметилциклопропанадве группы СН3 могут находиться по одну сторону от плоскости цикла (цис-изомер) или по разные стороны (транс-изомер).
4. Физические свойства циклопарафинов.
При обычных условиях первые два члена ряда (С3 и С4)
- газы, C5 – С10 -
жидкости, высшие - твердые вещества. Температуры кипения и плавления
циклоалканов, как и их плотности, несколько выше, чем у парафинов с равным
числом атомов углерода. Как и парафины, циклоалканы практически нерастворимы в
воде.
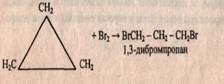
 5. Химические свойства.
5. Химические свойства.
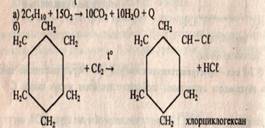
По химическим свойствам циклоалканы, в частности циклопентан и циклогексан, сходны
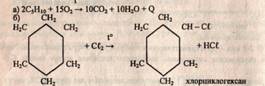
с предельными углеводородами. Они химически малоактивны, горючи, вступают в
реакцию замещения с галогенами.
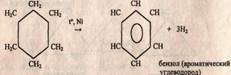
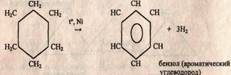
в) Также они вступают в реакцию дегидрирования в
присутствии никелевого катализатора. По химическому характеру малые циклы
(циклопропан и циклобутан) склонны к реакциям присоединения, в
результате которых происходит разрыв цикла и образуются парафины и их
производные, чем они напоминают ненасыщенные соединения.
 а) Присоединение брома
а) Присоединение брома
Получение циклопарафинов.
а) Циклопентан, циклогексан и их производные составляют основную часть некоторых сортов нефти. Поэтому их получают в основном из нефти.
б) Общим способом получения циклоалканов является действие металлов на дигалогенопроизводные алканов.
 7.Применение циклоалканов. широко используются для синтеза красителей, медикаментов и т.д.
Циклопропан применяют для наркоза. Циклопентан используется
как добавка к моторному топливу для повышения качества последнего и в разных
синтезах. Циклогексан используют главным образом для синтеза адипиновой кислоты
и капролактама - полупродуктов для производства синтетических волокон найлон и
капрон.
7.Применение циклоалканов. широко используются для синтеза красителей, медикаментов и т.д.
Циклопропан применяют для наркоза. Циклопентан используется
как добавка к моторному топливу для повышения качества последнего и в разных
синтезах. Циклогексан используют главным образом для синтеза адипиновой кислоты
и капролактама - полупродуктов для производства синтетических волокон найлон и
капрон.
IV. Закрепление знаний и умений.
Задача 1. При сгорании вещества массой 4,2 г образуется 13,2 г оксида углерода (IV) и 5,4 г воды. Плотность паров этого вещества по воздуху равна 2,9. Определите молек. формулу данного
вещества.
Задача 2. При сгорании 7,5 г вещества образуется 11 г оксида углерода (IV) и 4,5 г воды. Плотность паров этого вещества по водороду равна 14. Определите молекулярную формулу данного вещества.
V. Домашнее задание: Конспект
№1.Закончите уравнения: циклопропан + водород; сгорания циклопропана; циклогексана.
№2. Составьте уравнения реакции, при помощи которых можно получить: циклобутан из бутана; бутан из циклобутана; углекислый газ из циклопропана; бензол из гексана.
№3 Определите объем циклобутана, если при его сжигании выделилось 134,4 литра углекислого газа.
Циклоалканы
 1. Понятие
о циклопарафинах.
1. Понятие
о циклопарафинах.
Кроме рассмотренных предельных углеводородов с
открытой цепью атомов - парафинов, существуют углеводороды замкнутого,
циклического строения. Их называют циклопарафинами, например:
Общая формула циклопарафинов: СпН2п.
Циклопарафины называют также циклоалканами. Пяти-
и шестичленные циклопарафины были впервые открыты в нефти профессором
Московского университета В. В. Марковниковым. Отсюда их другое название - нафтены.
Молекулы циклопарафинов часто содержат боковые углеродные цепи:
2. Строение циклопарафинов. Каждый атом
углерода в циклоалканах находится в состоянии sp3-гибридизации и
образует четыре δ-связи С - С и С - Н. В простейших циклах С3 и С4 углы
между связями С - С сильно отличаются от тетраэдрического угла 109°28 что
создает в молекулах напряжение и обеспечивает их высокую реакционную
способность.
 3. Изомерия и номенклатура. Для циклоалканов характерны два вида изомерии.
3. Изомерия и номенклатура. Для циклоалканов характерны два вида изомерии.
а) 1-й вид — структурная изомерия -
изомерия углеродного скелета Но структурная изомерия может быть обусловлена
разными причинами. Во-первых, размером цикла. Например,
для циклоалкана С4Н8 существует
два вещества: Также к структурной изомерии относится межклассовая. Например,
для вещества С4Н8 можно
записать структурные формулы веществ, относящихся к разным классам
углеводородов.
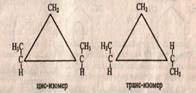
б) 2-й вид - пространственная изомерия у некоторых замещенных циклоалканов обусловлена отсутствием свободного вращения вокруг связей С - С в цикле.Например, в молекуле 1,2-диметилциклопропанадве группы СН3 могут находиться по одну сторону от плоскости цикла (цис-изомер) или по разные стороны (транс-изомер).
4. Физические
свойства циклопарафинов.
При обычных условиях первые два члена ряда (С3 и С4)
- газы, C5 – С10 -
жидкости, высшие - твердые вещества. Температуры кипения и плавления
циклоалканов, как и их плотности, несколько выше, чем у парафинов с равным
числом атомов углерода. Как и парафины, циклоалканы практически нерастворимы в
воде.
![]()
 5. Химические свойства.
5. Химические свойства.
По химическим свойствам циклоалканы, в частности циклопентан и циклогексан, сходны
с предельными углеводородами. Они химически малоактивны, горючи, вступают в
реакцию замещения с галогенами.
в) Также они вступают в реакцию дегидрирования в
присутствии никелевого катализатора. По химическому характеру малые циклы
(циклопропан и циклобутан) склонны к реакциям присоединения, в
результате которых происходит разрыв цикла и образуются парафины и их производные,
чем они напоминают ненасыщенные соединения.
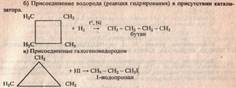 а) Присоединение брома
а) Присоединение брома
Получение циклопарафинов.
а) Циклопентан, циклогексан и их производные составляют основную часть некоторых сортов нефти. Поэтому их получают в основном из нефти.
б) Общим способом получения циклоалканов является действие металлов на дигалогенопроизводные алканов.
7.Применение циклоалканов. широко используются для синтеза красителей, медикаментов и т.д. Циклопропан применяют для наркоза. Циклопентан используется как добавка к моторному топливу для повышения качества последнего и в разных синтезах. Циклогексан используют главным образом для синтеза адипиновой кислоты и капролактама - полупродуктов для производства синтетических волокон найлон и капрон.
V. Домашнее задание: Конспект
№1.Закончите уравнения: циклопропан + водород; сгорания циклопропана; циклогексана.
№2. Составьте уравнения реакции, при помощи которых можно получить: циклобутан из бутана; бутан из циклобутана; углекислый газ из циклопропана; бензол из гексана.
№3 Определите объем циклобутана, если при его сжигании выделилось 134,4 литра углекислого газа.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.