
Интегрированный урок химия + история
Обобщение по теме
«Явления, происходящие с веществами»
Учитель химии: Сергеев А.А.
Учитель истории: Нечаев С.Ю.

Интегрированный урок химия + история
Обобщение по теме «Явления, происходящие с веществами» в 7 классе
Цели урока:
Образовательные – проверить прочность усвоения учащимися пройденного материала, выявить типичные ошибки и пробелы в знаниях, с целью их последующего усвоения.
Развивающие – формировать умение выделять главное, грамотно излагать материал, логически мыслить, развивать химическую речь, обеспечить эмоциональное восприятие, создавая на уроке ситуацию , вызывающую интерес к предмету.
Воспитательные – воспитывать наблюдательность, умение работать в коллективе и индивидуально, самостоятельность, умение преодолевать трудности, прививать чувство взаимопомощи.
Оборудование: наличие интернет, проектор + ПК, экран, реактивы и посуда для опыта (ацетат свинца, уксусная кислота, йодид калия)
Ход урока.
І. Организационный момент. Добрый день ребята вы все сегодня прекрасно выглядите. Сегодня у нас на уроке присутствуют гости, поэтому поздоровайтесь с ними. Наш урок будет не совсем обычным поэтому я пригласил на него нашего учителя истории которого вы все хорошо знаете это Сергей Юрьевич. Поэтому предлагаю начать наш урок. (3 мин.)
ІІ. Мотивация
Мультфильм (2 мин.)
О чём же этот мультфильм, ребята? Какова тема нашего сегодняшнего урока?
ІІІ. Сообщение темы урока
Сегодня 20 февраля
Тема нашего урока «Явления, происходящие с веществами» слайд 1
ІV. Актуализация знаний.
Я приготовил для вас небольшую Самостоятельную работу задания которой могут встретиться вам ЕГЭ.
(5 минут) слайд 2
Что из перечисленного относится к физическим, а что к химическим явлениям? В ответе поставьте Ф, если физическое явление, и X – если химическое явление.
1) Плавление алюминия; Ф
2) на медных предметах образуется зеленый налет; Х
3) если к духам или одеколону прилить воду, то происходит помутнение раствора; Ф
4) испарение воды; Ф
5) серебряные ложки со временем чернеют; Х
6) ржавление гвоздя. Х
Найдите соответствие между веществами и их свойствами.
|
1 Вода |
а) Не поддерживает горение |
|
2 Алюминий |
б) Сладкий на вкус |
|
3 Кислород |
в) Пластичный |
|
4 Углекислый газ |
г) Поддерживает дыхание |
|
5 Сахар |
д) Жидкое агрегатное состояние. |
Ответ: 1-д; 2-в; 3-г; 4-а; 5-б
Давайте поменяемся своими работами и проверим друг друга.
V. Основная часть. (40 мин. коллективная работа по презентации самостоятельная работа за ПК + 5 мин. опыт).
Слайд 3 «Рецепт1»
Возьмите горшок свежей земли, добавьте туда фунт красной меди и полстакана холодной воды, и всё это прокипятите в течение получаса. После чего добавьте к составу три унции окиси меди и прокипятите один час; затем добавьте две с половиной унции мышьяка и прокипятите ещё один час. После этого добавьте три унции хорошо размельчённой дубовой коры и оставьте кипеть полчаса; добавьте в горшок унцию розовой воды, прокипятите двенадцать минут. Затем добавьте три унции сажи и кипятите до тех пор, пока состав не окажется готов.
Учитель химии: Ребята, перед вами рецепт некоего химического продукта.
- Какие вещества в нем указаны? ......
-Что предполагается сделать с этими веществами ? .... (смешать, нагреть)
- Если есть рецепт, то, в результате, из него должно что-то получиться. Как вы думаете что?
Ответы учеников (все ответы сводятся к тому, что это рецепт отравы).
Учитель химии: Неверно.
Учитель истории: Извините, что вклиниваюсь в вашу беседу. А вы не хотите посмотреть на этот рецепт с другой точки зрения? Я историк и привык рассматривать всё с точки зрения место, время, события. Давайте определимся с местом.
- Дело было в России? (если «да», то почему, если «нет», то почему.
В результате, при помощи слов «фунт», «унция» определяем, что это не Россия).
- Теперь определимся со временем. Рецепт был написан в настоящее время?
Докажите.
(в результате приходим к выводу, что современные химики не смешивают вещества в горшках, следовательно, это было достаточно давно).
Даю подсказку – ещё один рецепт того же самого.
Слайд 4 «Рецепт 2»
Возьми, сын мой, философской ртути и накаливай, пока она не превратится в красного льва. Дигедрируй этого красного льва на песчаной бане с кислым виноградным спиртом, выпари жидкость, и ртуть превратится в камедеобразное вещество, которое можно резать ножом. Положи его в обмазанную глиной реторту и не спеша дистиллируй. Собери отдельно жидкости различной природы, которые появятся при этом. Ты получишь безвкусную флегму, спирт и красные капли. Киммерийские тени покроют реторту своим тусклым покрывалом. Он загорится, приняв вскоре великолепный лимонный цвет.
Учитель химии: Странно, учитель истории сказал, что это рецепт одного и того же продукта, а я вижу другие химические реакции. А вы, ребята, видите? Какие? (дистилляция, горение, дети также называют изменение агрегатного состояния – выпаривание).
Учитель истории: Химические реакции вы разобрали, а результат стал понятен? (нет).
Давайте разбираться дальше. Мы встретили много новых непонятных слов. Каких? (называют).
Предлагаю найти их значение в интернете при помои ваших мобильных телефонов.
Самостоятельная работа в малых группах у ПК или на своих смартфонах
(7 мин).
(обучающиеся ищут значение новых слов, понятие «философская ртуть» приводит их к эпохе алхимиков).
Учитель истории: Слайд 5
Алхимия — мистическая наука, появившаяся задолго до нашей эры. Ее служители пытались найти эликсир молодости и так называемый философский камень — вещество, превращающее металл в золото.
Природу алхимики считали живой и были уверены, что металлы растут и созревают в недрах Земли от смеси серы с ртутью. Золото рассматривали как созревший металл, а железо — как недозревший. Задачей алхимика было изобрести философский камень — вещество, ускоряющее "дозревание" металла и превращающее его в золото. Тот, кому это удастся, якобы сможет не только превратить металл в золото, но и создать из него эликсир молодости. Несмотря на фантастичность задачи, алхимики получили достаточно много практических и важных результатов. Они изобрели аппараты для очистки жидкости и кристаллизации солей. Научились применять в медицине химические элементы. Результаты своей работы держали в тайне. Потому что, с одной стороны, опытами могли воспользоваться мошенники, искатели золота. С другой — алхимика могли объявить магом и чернокнижником и наказать или даже казнить.
Предлагаю посмотреть на продолжение первого рецепта, чтобы точно удостовериться, какой продукт должен был в итоге получиться.
Слайд 6
..Чтобы узнать, сварен ли он до конца, надо опустить в него гвоздь: если состав действует на гвоздь, снимайте с огня.
Этот состав позволит вам добыть полтора фунта золота; если же не действует, это — признак того, что состав недоварен. Жидкостью можно пользоваться четыре раза.
Физкультминутка. Вы наверное немножко устали поэтому предлагаю немного расслабится Участники встают . Дождь это физическое явление, знаете ли вы что такое австралийский дождь? Нет? Тогда давайте вместе послушаем, какой он. Сейчас вы будете повторять мои движения. Следите внимательно! Слайд 7
§ В Австралии поднялся ветер. (Ведущий трет ладони).
§ Начинает капать дождь. (Клацанье пальцами).
§ Дождь усиливается. (Поочередные хлопки ладонями по груди).
§ Начинается настоящий ливень. (Хлопки по бедрам).
§ А вот и град – настоящая буря. (Топот ногами).
§ Буря стихает. (Хлопки по бедрам).
§ Дождь утихает. (Хлопки ладонями по груди).
§ Редкие капли падают на землю. (Клацанье пальцами).
§ Тихий шелест ветра. (Потирание ладоней).
§ Солнце! (Руки вверх).
Учитель химии: Посмотрите, сколько химических реакций использовали алхимики при попытках получения золота. Теперь давайте вернёмся в настоящее время и подумаем, какие из этих химических реакций используются для получения золота в нашем веке. (Обсудив, приходим к выводу, что люди так и не научились получать золото путём химических реакций – золото приходится добывать).
А вот получать вещества похожие на золото мы можем попробовать прямо на нашем сегодняшнем уроке. Давайте почувствуем себя алхимиками – попробуем получить вещество похожее на золото. Слайд 8
Опыт «Золотой дождь»
(Для проведения этого опыта необходимо взвесить равные количества ацетата свинца(II) и йодида калия. Я советую по 0,5г. Далее готовят два раствора. В два химических стакана наливают по 50 мл дистиллированной воды. В один добавляют ~1мл столового уксуса (или ~0,2 мл концентрированной уксусной кислоты) и растворяют ацетат свинца. Кислота добавляется для того, чтобы подавить гидролиз ионов Pb2+. Во втором растворяют KI. Затем оба раствора сливают в колбу из огнеупорного стекла объёмом 150мл. При этом происходит реакция двойного обмена между ацетатом свинца и йодидом калия:
Pb(CH3COO)2 + 2KI => 2KCH3COO + PbI2
После смешивания растворов выпадает жёлтый осадок йодида свинца. Смеси растворов в колбе необходимо дать отстояться, чтобы осадок осел полностью. После этого с осадка осторожно сливают жидкость и вместо неё доливают 100мл дистиллированной воды. Теперь раствор необходимо нагреть до кипения и кипятить в течении 2-3мин. Осадок должен раствориться полностью.
Если всё было сделано правильно, то после охлаждения раствора выпадет множество золотистых кристалликов, которые при встряхивании колбы будут парить в толще воды. Размер кристалликов очень сильно зависит от скорости охлаждения: чем медленнее охлаждать, тем более крупными и красивыми будут кристаллики. Для большей их прочности перед кипячением в раствор добавляют немного глицерина (~0,5мл на 100 мл раствора). Слайд 9
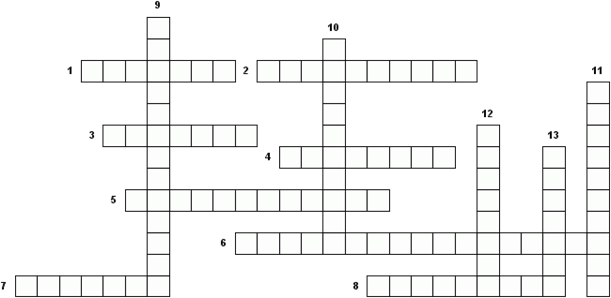
Для проведения этого опыта нужно время поэтому пока остывает раствор предлагаю вам отгадать кроссворд. Слайд 10
1. Любые изменения, которые происходят с телами. (явления)
2. Явления, в результате которых одни вещества превращаются в другие. (химические)
3. Реакция, сопровождающаяся выделением тепла и света.(горения)
4. Явление, связанное со светом.(световое)
5. Явление, связанное с изменением положения какого-либо тела по отношению к другим телам.(механическое)
6. Тела, способные после натирания притягивать лёгкие предметы.(наэлектризованные)
7. Горючие материалы, сжигаемые для использования выделяющейся теплоты.(топливо)
8. Реакция взаимодействия веществ с кислородом.(окисление)
9. Энергия, получаемая на тепловых электростанциях. (электричество)
10. Явления, при которых вещества остаются прежними. (физические)
11. Тела, излучающие свет. (светящиеся)
12. Явления, связанные с нагреванием и охлаждением тел. (тепловые)
13. Процесс медленного окисления питательных веществ в живом организме. (дыхание)
Учитель химии. (Выводы - обобщение). Слайд 11-12
VI. Рефлексия:
Учитель истории: В ходе урока вы попытались овладеть самым главным в процессе познания – умением находить истину с помощью доказательств, то есть проводить исследования. Многие учёные прошлых веков опирались в своих изысканиях лишь на интуицию и в результате нередко ошибались. Мы же смогли справиться с задачей.
Учитель химии: Без химических реакций невозможна жизнь и все многообразие веществ. И наша задача, изучив этот мир, постараться использовать полученные знания во благо.
Предлагаю вам поучаствовать в конкурсе «Закончите предложение» Слайд 13
1. Теперь я знаю, что ...
2. Теперь я знаю, как ...
3. Теперь я умею...
4. Меня удивило...
VIІ. Домашнее задание. Слайд 14
§ 14 повторить
Упражнение № 6
Творческое задание – Сделать подборку стихов, загадок, пословиц о химических и физических явлениях.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.