
По их способности растворяться в воде основания делят на растворимые и практически нерастворимые.
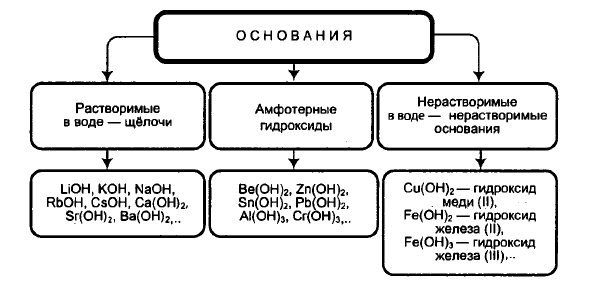
Примеры: Примеры:
NaOH — гидроксид натрия, Cu(OH)2 — гидроксид меди(II),
KOH — гидроксид калия, Fe(OH)2 — гидроксид железа(II), Ca(OH)2 — гидроксид кальция. Cr(OH)2 — гидроксид хрома.

|
Основания |
Химические свойства |
|
Щелочи (во всех реакциях участвуют ионы ОН-, (что видно из кратких ионных уравнений), следовательно, они обуславливают общие химические свойства щелочей) |
1. Действие на индикаторы: фенолфталеин — малиновый цвет, метилоранж — желтый цвет, лакмус — синий цвет |
|
2. диссоциация: NaOH → Na+ +ОН- При диссоциации образуются ионы ОН-, которые изменяют окраску индикаторов и придают мылкость растворам щелочей. |
|
|
3. Основание + кислота → соль + вода |
|
|
|
2КОН + 2НСl → 2КС1 + Н20 |
|
|
4. Щелочь + кислотный оксид → соль + вода Ва(ОН)2 + СO2 → ВаСО3 + Н2O |
|
|
5. Щелочь + соль 1 → соль 2 + основание 2KOH + CuSO4 → K2SO4 + Cu(OH)2↓ |
|
Нерастворимые основания |
1. Основание + кислота → соль + вода 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6Н2O |
|
2. Основание → t°→ оксид + вода 2Fe(OH)3 → t°→ Fe2O3 + ЗН2O, Си(ОН)2 → t°→ СuО + Н2O |
|
|
Амфотерные гидроксиды (у амфотерных гидроксидов в кислой среде равновесие смещается в сторону образования солей, а в щелочной - в сторону образования гидрокомплексов) |
1. Амфотерный гидроксид + кислота → соль + вода Zn(OH)2 + 2НСl → ZnCl2 + 2Н2O |
|
2. Амфотерный гидроксид + щелочь → соль + вода Zn(OH)2 + 2NaOH → Na2ZnO2 + 2Н2O |
Способы получения оснований
|
Способ получения |
Примеры |
Примечание |
|
Взаимодействие металлов или их оксидов с водой |
2Na + 2Н2O → 2NaOH + Н2↑ К2O + Н2O → 2КOН |
Так можно получить только щелочи |
|
Действие щелочей на водные растворы солей |
FeSO4 + 2NaOH → Fe(OH)2↓ + Na2SO |
Так можно получить нерастворимые основания |
|
Электролиз растворов солей |
2KCl + 2H2O → I, графит, электроды → 2KOH + + H2↑ + Cl2↑ |
Промышленный способ получения КОН и NaOH |
 Составьте
уравнение химических реакций по предложенным схемам
Составьте
уравнение химических реакций по предложенным схемам NaOH + H2SO4 =
Ca(OH)2 + P2O5 =
NaOH + Al + H2O =
Fe (OH)2 (t) =
Ni(OH)2 + HCl =
Zn(OH)2 + KOH =
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.