Памятка "Химические реакции" 9 класс
Памятки
docx
химия
9 кл
04.05.2017
Химические реакции происходят при смешении или физическом контакте реагентов самопроизвольно, при нагревании, участии катализаторов (катализ), действии света (фотохимические реакции), электрического тока (электродные процессы), ионизирующих излучений (радиационно-химические реакции), механического воздействия (механохимические реакции), в низкотемпературной плазме (плазмохимические реакции) и т. п. Взаимодействие молекул между собой происходит по цепному маршруту: ассоциация — электронная изомеризация — диссоциация, в котором активными частицами являются радикалы, ионы, координационно-ненасыщенные соединения. Скорость химической реакции определяется концентрацией активных частиц и разницей между энергиями связи разрываемой и образуемой.
Химические процессы, протекающие в веществе, отличаются и от физических процессов, и от ядерных превращений. В физических процессах каждое из участвующих веществ сохраняет неизменным свой состав (хотя вещества могут образовывать смеси), но могут изменять внешнюю форму или агрегатное состояние.
В химических процессах (химических реакциях) получаются новые вещества с отличными от реагентов свойствами, но никогда не образуются атомы новых элементов. В атомах же участвующих в реакции элементов обязательно происходят видоизменения электронной оболочки.
памятка химические реакции.docx
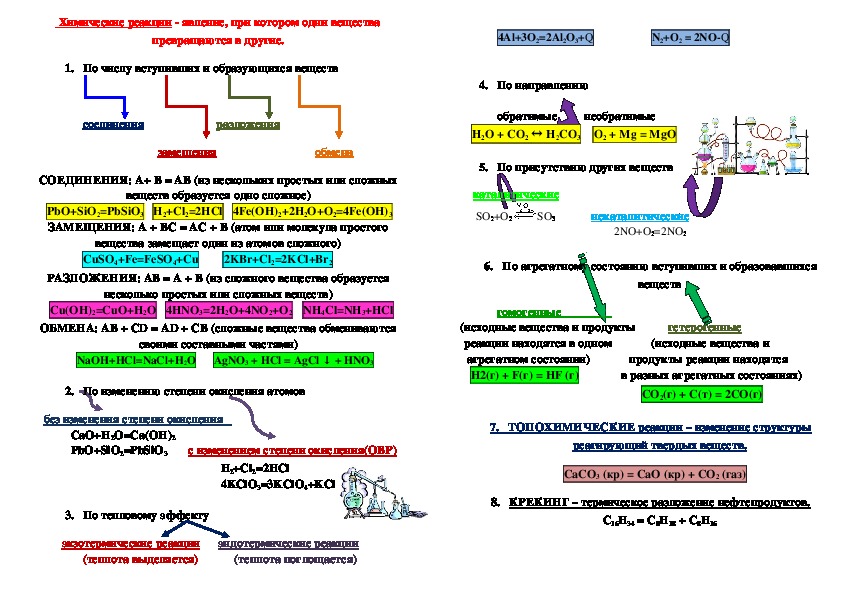
Химические реакции явление, при котором одни вещества
превращаются в другие.
1. По числу вступивших и образующихся веществ
соединения разложения
замещения обмена
СОЕДИНЕНИЯ: А+ В = АВ (из нескольких простых или сложных
веществ образуется одно сложное)
PbO+SiO2=PbSiO3 H2+Cl2=2HCl 4Fe(OH)2+2H2O+O2=4Fe(OH)3
ЗАМЕЩЕНИЯ: А + ВС = АС + В (атом или молекула простого
вещества замещает один из атомов сложного)
CuSO4+Fe=FeSO4+Cu 2KBr+Cl2=2KCl+Br2
РАЗЛОЖЕНИЯ: AB = A + B (из сложного вещества образуется
несколько простых или сложных веществ)
Cu(OH)2=CuO+H2O 4HNO3=2H2O+4NO2+O2 NH4Cl=NH3+HCl
ОБМЕНА: AB + CD = AD + CB (сложные вещества обмениваются
NaOH+HCl=NaCl+H2O AgNO3 + HCl = AgCl
своими составными частями)
+ ↓ HNO3
2. По изменению степени окисления атомов
без изменения степени окисления
CaO+H2O=Ca(OH)2
PbO+SiO2=PbSiO3 с изменением степени окисления(ОВР)
H2+Cl2=2HCl
4KClO3=3KClO4+KCl
3. По тепловому эффекту
экзотермические реакции эндотермические реакции
(теплота выделяется) (теплота поглощается)
4Al+3O2=2Al2O3+Q N2+O2 = 2NOQ
4. По направлению
обратимые необратимые
Н2О + СО2 ↔ Н2СО3 О2 + Mg = MgO
5. По присутствию других веществ
каталитические
SO2+O2
SO3 некаталитические
2NO+O2=2NO2
6. По агрегатному состоянию вступивших и образовавшихся
веществ
гомогенные
(исходные вещества и продукты гетерогенные
реакции находятся в одном (исходные вещества и
агрегатном состоянии) продукты реакции находятся
Н2(г) + F(г) = HF (г) в разных агрегатных состояниях)
СО2(г) + С(т) = 2СО(г)
7. ТОПОХИМИЧЕСКИЕ реакции – изменение структуры
реагирующий твердых веществ.
СаСО3 (кр) = СаО (кр) + СО2 (газ)
8. КРЕКИНГ – термическое разложение нефтепродуктов.
С16Н34 = С8Н18 + С8Н16 9. ГИДРОЛИЗ – процесс взаимодействия соли с водой,
приводящий к образованию слабого электролита.
Na2CO3 + H2O = NaHCO3 + NaOH
CuCl2 + H2O = CuOHCl + HCl
Материалы на данной страницы взяты из открытых истончиков либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.
04.05.2017
Посмотрите также:
© ООО «Знанио»
С вами с 2009 года.
![]()
О портале


