
Мочевыделительная система включает почки, мочеточники, мочевой пузырь и мочеиспускательный канал.
Почки называют «центральным органом гомеостаза», так как в результате их деятельности обеспечивается сохранение ионного состава и объема биологических жидкостей.
Почки поддерживают постоянство внутренней среды благодаря способности:
- контролировать баланс натрия, калия, магния, водородных ионов;
- участвовать в обмене белков, углеводов, липидов;
- выделять ряд гормонов и биологически активных веществ.
Почки выполняют следующие функции:
- экскретируют (выделяют) продукты метаболизма;
- регулируют концентрацию солей и объем воды в организме;
- поддерживают кислотно-основное состояние плазмы (рН);
- секретируют ренин, эритропоэтин, кинины, простагландины.
Структурно-функциональной единицей почки, участвующей в образовании мочи, является нефрон. Их общее количество в почке массой 150 г. составляет 1-1,2 млн. Каждый нефрон начинается небольшой капсулой, имеющей форму двустенной чаши (капсула Шумлянского-Боумена), внутри которой находится клубочек.
Почечный клубочек представляет собой сеть капилляров, образованных приносящей артериолой, и предназначен для фильтрации плазмы.
Стенка капилляра состоит из трех слоев: эндотелия, гломерулярной базальной мембраны и эпителиальных клеток, покрывающих капиллярные петли. Петли капилляров клубочка собираются в одну отводящую артериолу, просвет которой меньше просвета приводящей артериолы. Между стенками капсулы имеется полость, от которой начинается просвет канальца.
Особенностью работы клубочкового капилляра является то, что в отличие от тканевого капилляра, он работает только в одном направлении из капилляра в пространство канальцев нефрона.
На границе коркового и мозгового слоя почки располагаются юкстамедуллярные нефроны, обладающие внутрисекреторной функцией (выделяют ренин).
В обычных условиях одновременно работает только часть клубочков, поэтому нормальные почки имеют значительный функциональный резерв. Почки обладают широко развитой сосудистой сетью, обеспечивающей очень энергичное кровообращение, превосходящее кровообращение в большинстве других органов в 20 раз. Благодаря существующей в почках автономной системе ауторегуляции, почечный кровоток мало чувствителен к колебаниям системного артериального давления в пределах от 80 до 180 мм рт.ст. При падении давления ниже 60 мм рт. ст. процесс клубочковой фильтрации прекращается.
Многообразие почечных функций обеспечивается слаженной работой клубочков и канальцев почек, где происходят клубочковая фильтрация и канальцевая реабсорбция и секреция.
Показателем согласованной деятельности клубочков и канальцев (нефрона в целом) являются: скорость клубочковой фильтрации, сохранение баланса натрия, объема внеклеточной жидкости, рН крови и сохранение способности к мочеобразованию и выделению мочи. Выполнение почечных функций зависит от состояния почечного кровотока. Почка получает 22-25% крови от минутного объема сердца. Нормальный почечный кровоток составляет 100 мл/мин (плазмоток – 600 мл/мин).
В капиллярах клубочков, куда каждую минуту притекает больше 1 литра крови, происходит важнейший процесс ‑ ультрафильтрация – образование первичной мочи. У здорового человека объем клубочковой фильтрации составляет 120-130 мл/мин.
Поступление первичной мочи в капсулу клубочков происходит под действием фильтрационного давления. фильтрационное давление – это разность между гидростатическим давлением в капиллярах клубочков (45 мм рт ст) и суммой коллоидно-осмотического давления плазмы крови (20 мм рт ст) и давления в капсуле Боумена (10 мм рт ст).
Фильтрационное давление равно [45 – (20 + 10)] = 15 мм рт ст.
Конечный продукт деятельности почек – вторичная моча образуется в результате трех процессов, происходящих в нефроне:
- ультрафильтрации (клубочковая фильтрация);
- канальцевой секреции;
- канальцевой реабсорбции.
Клубочковый фильтрат, переходящий в капсулу Боумена в результате ультрафильтрации, почти идентичен составу плазмы за исключением содержания крупномолекулярных белков, которые не проходят через стенку клубочковых капилляров. Из капсулы Боумена ультрафильтрат переходит в систему канальцев: проксимальный первичный извиток каналец, петлю Генле, дистальный вторичный извиток каналец и собирательные трубочки. В канальцах почек ультрафильтрат (первичная моча) подвергается значительным изменениям – происходит обязательная реабсорбция воды и растворенных в ней составных частей и наряду с этим процессы секреции в просвет канальцев некоторых веществ.
В просвет проксимальных канальцев ежесуточно поступает 115-180 л. первичной мочи из нее 80% натрия, хлоридов, калия и воды подвергается реабсорбции (обратному всасыванию). Здесь же почти полностью реабсорбируются глюкоза, низкомолекулярные белки и большая часть аминокислот. Соотношение воды и солей в реабсорбируемой жидкости остается постоянным, то есть проксимальный отдел канальцев не участвует в процессах концентрации и разведения мочи.
Эти процессы осуществляются в петле Генле и дистальном отделе канальцев. В нисходящем колене петли Генле всасывается только вода, поэтому возрастает плотность первичной мочи в восходящем колене петли Генле, не всасывается вода, но реабсорбируются натрий, хлор, кальций и мочевина, то есть происходит разведение мочи. В дистальном извитом канальце и собирательных трубочках в зависимости от потребностей организма происходит факультативная реабсорбция воды, регулируемая антидиуретическим гормоном и реабсорбция натрия, регулируемая альдостероном. В этом же отделе происходит секреция калия в просвет канальцев. Количество всосавшейся в кровь воды и натрия зависит от потребностей организма. Следовательно, моча может выделяться различной плотности. Относительная плотность мочи у здорового взрослого человека колеблется от 1002 до 1035. В конечной моче концентрация натрия может быть в 140 раз ниже его концентрации в плазме крови.
Снижение скорости клубочковой фильтрации ниже 70 мл/мин. является одним из показателей нарушения функции клубочков. В норме скорость клубочковой фильтрации равна 130 ± 18 мл/мин у мужчин и 120 ± 14 мл/мин – у женщин. Снижение скорости клубочковой фильтрации может быть вызвано разными патологическими процессами в паренхиме почек, а также внепочечными факторами.
I. Экстраренальные факторы
1. Нарушения системного и местного кровообращения:
- снижение артериального давления ниже 80 мм рт ст (коллапс, кардиальная форма недостаточности кровообращения);
- уменьшение объема циркулирующей крови (кровопотеря);
- уменьшение почечного кровотока (спазм приносящих артериол клубочка при испуге; артериальная гипертензия);
- врожденные дефекты аорты (сужение), сужение почечных артерий;
- тромбоз, эмболия, атеросклероз аорты и почечных артерий.
2. Повышение онкотического давления выше 25-30 мм рт ст:
- обезвоживание организма; переливание больших объемов кровозаменителей; гиперпротеинемия.
3. Повышение симпатической активности: испуг; травма; стрессовые ситуации.
II. Ренальные факторы
1. Увеличение давления в капсуле Боумена выше 20 мм рт ст:
- замедление реабсорбции жидкости в проксимальном отделе канальцев; закупорка просвета канальцев цилиндрами;
- препятствие току мочи в мочевых ходах (камни).
2. Уменьшение количества функционирующих клубочков (уменьшение фильтрационной площади (в норме 1,5 м2 – 2 м2).
- острые и хронические воспалительные процессы в клубочках;
- васкулиты; хроническая почечная недостаточность.
3. Нарушение трофики клубочковой мембраны.
- нарушение кровоснабжения почек; гипоксия; токсические влияния.
Не всегда снижение скорости клубочковой фильтрации следует рассматривать как признак патологии почек. У здоровых людей умеренное снижение почечного кровотока и скорости клубочковой фильтрации возможно в вертикальном положении тела, при физической нагрузке, перегревании и возрастной инволюции.
Последствием значительного снижения скорости клубочковой фильтрации может быть снижение суточного количества мочи ‑ олигурия (в норме 1-1,5 л). На кровоток почек оказывают влияние нервные и гуморальные факторы, поэтому снижение диуреза может наблюдаться и у здоровых людей при испуге, стрессовых ситуациях, травмах.
При заболеваниях почек, сопровождающихся снижением скорости клубочковой фильтрации, возможно накопление в крови веществ, выведение которых обусловлено клубочковой фильтрацией.
Это азотистые шлаки (мочевина и креатин). Повышение в крови уровня этих веществ называется азотемией. Последствием снижения фильтрации может быть нарушение состава внеклеточной жидкости, с задержкой натрия и воды, накоплением водородных ионов и развитием гиперкалиемии.
Увеличение клубочковой фильтрации наблюдается при:
- повышении гидростатического давления (рассасывание отеков, прием жидкости);
- снижении онкотического давления плазмы крови (гидремия, повышенный прием жидкости, схождение отеков, циррозы печени, гепатиты);
- гипопротеинемии – уменьшении содержания белков (белково-калорийное голодание);
- протеинурии – появление белка в моче (нефротический синдром);
- спазме отводящей артериолы или расслаблении приводящей артериолы (сахарный диабет, подъем температуры при лихорадке);
- введении солевых растворов;
- беременности.
В клинике скорость клубочковой фильтрации определяют по клиренсу (очищению) почками плазмы крови от какого-либо вещества. Например, эндогенного креатинина или введенного инулина.
Клиренс (С) – объем плазмы, очищенной почками от какого-либо вещества (эндогенного креатинина или введенного инулина) в единицу времени рассчитывается по формуле:
![]()
где U и Р – концентрация тест вещества в моче и плазме соответственно;
V – величина минутного диуреза. Снижение клиренса креатинина наблюдается при нарушении клубочковой фильтрации.
Итак, показателями, характеризующими нарушения клубочковой фильтрации, являются: азотемия; олигурия; снижение клиренса креатинина.
К расстройствам функций канальцев относятся нарушения концентрирования и разведения мочи, выделения (экскреции) натрия и калия, выделения водородных ионов.
Эти функции обеспечиваются многими факторами – интенсивностью почечного кровотока, кровоснабжением мозгового слоя почки, нервными и гормональными влияниями и функционированием транспортных систем канальцевого аппарата.
Почки – главный орган, регулирующий содержание натрия в организме. Объем внеклеточной жидкости зависит от общего содержания натрия, поэтому любому изменению содержания натрия сопутствует изменение объема внеклеточной жидкости. В физиологических условиях 65-80% фильтруемых в клубочках натрия и воды реабсорбируются в проксимальных канальцах, поэтому соотношение воды и растворенных веществ в просвете канальца остается постоянным и изотоничным плазме. В регуляции реабсорбции натрия имеют значение:
- скорость клубочковой фильтрации;
- гормоны, влияющие на транспорт натрия в канальцах (альдостерон).
В норме изменение количества фильтруемого натрия «исправляется» соответствующим изменением его реабсорбции (клубочко-канальцевый баланс). Клубочко-канальцевый баланс может нарушаться при патологических процессах, снижающих общую фильтрующую поверхность, или увеличивающих проницаемость клубочкового фильтра.
Уменьшение реабсорбции ионов натрия и воды возникают при:
- нарушении гормональной регуляции (недостаточное образование альдостерона или его блокирование диуретическими средствами, недостаточная продукция вазопрессина ‑ антидиуретического гормона);
- действии некоторых ингибиторов метаболизма на реабсорбцию ионов натрия (ртутные диуретики, блокирующие сульфгидрильные группы ферментов, участвующих в активном транспорте ионов);
- повышении содержания в первичной моче осмотически активных веществ (глюкоза, мочевина) которые, удерживая воду в просвете канальцев, ограничивают ее реабсорбцию (осмотический диурез);
- врожденной нечувствительности канальцев нефрона к альдостерону;
- денервации почки или введении адреноблокаторов;
- воспалительных, дистрофических, атрофических и некротических изменениях эпителия канальцев и окружающей межуточной ткани.
Все перечисленные причины приводят к понижению или полной потере способности канальцевого аппарата концентрировать и разводить мочу.
Увеличение реабсорбции ионов натрия и воды возникает при:
- избыточной продукции альдостерона (гормона коры надпочечников, стимулирующего реабсорбцию ионов натрия в канальцах и выделение ионов калия) наблюдается при синдроме Кона, нефротическом синдроме, легочном сердце, циррозе печени, декомпенсированных пороках сердца;
- активации симпатической системы (например, при гиповолемии);
- избыточной продукции антидиуретического гормона.
Канальцевая протеинурия бывает двух типов:
- протеинурия (белок в моче), связанная с нарушением реабсорбции белка из клубочкового фильтрата;
- протеинурия, связанная с разрушением клеток канальцев.
Первый тип наблюдается при:
- отравлении кадмием, фенацитином; гипоксии; ожогах;
- гипервитаминозе D; трансплантации почек; септицемии.
При этой форме протеинурии белка в моче сравнительно немного и они низкомолекулярные.
Второй тип протеинурии возникает при тяжелых формах поражения канальцев. В моче появляются белки с большой молекулярной массой.
При этом типе протениурии в моче могут появляться гиалиновые, эпителиальные и зернистые цилиндры – своеобразные слепки просвета канальцев, состоящие из свернувшегося белка или распавшихся эпителиальных клеток.
Нарушение реабсорбции глюкозы проявляется в виде глюкозурии – выделения глюкозы с мочой. Глюкозурия может быть почечного и внепочечного происхождения.
Внепочечная глюкозурия возникает при гипергликемии, превышающей почечный порог (170-180 мг %), например, при сахарном диабете. Почечная глюкозурия наблюдается при:
- хронических заболеваниях почек;
- интоксикации ртутью, свинцом, ураном;
- наследственных аномалиях ‑ генетически обусловленный дефицит ферментов (гексокиназа, глюкозо-6-фосфатаза), обеспечивающих канальцевую реабсорбцию глюкозы.
Понятия о нарушениях диуреза. Патологические составные части мочи
Анатомические, физиологические и биохимические особенности почек определяют характер патологических нарушений в самих почках и в организме.
Почки являются важным органом по поддержанию гомеостаза организма, обусловленного постоянством объема жидкостей (изоволемия), их осмотической концентрацией (изотония), ионным составом (изоиония), концентрацией ионов водорода (изогидрия). Эти показатели могут изменяться при нарушении деятельности почек. Нарушение экскреторной функции почек в виде синдрома недостаточности почек (уремия) является частым исходом патологических процессов, развивающихся в почках.
Почки участвуют в выведении камнеобразующих солей неорганической и органической природы, их растворимости и выведении с мочой. Повышение концентрации камнеобразующих солей в моче может быть обусловлено как почечными, так и внепочечными механизмами и снижением их растворимости, что приводит к развитию почечнокаменной болезни.
Почки обладают слабой сопротивляемостью в отношении патологических микроорганизмов, поэтому возникновение заболеваний почек часто связано с гематогенной или восходящей инфекцией (острый и хронический пиелонефрит).
Количество мочи, образуемой почками в единицу времени, равно разности между количеством жидкости профильтровавшейся в клубочках и реабсорбировавшейся в канальцах. Нормальный диурез равен 1-1,5 литрам в сутки. Увеличение суточного количества мочи называется полиурией, уменьшение – олигурией (диурез не более 400 мл в сутки). Отделение мочи не более 50-100 мл в сутки называют анурией. При закупорке мочевых путей может развиться полное прекращение диуреза.
Объем и состав мочи у здоровых людей могут значительно меняться в зависимости от количества принятой жидкости и качества пищи. При употреблении большого количества воды почки могут выделять большое количество мочи низкой плотности (гипотоничная моча) – полиурия. При сухоедении выделяется небольшое количество гипертонической (высокой относительной плотности) мочи. Относительная плотность мочи у здорового человека в течение суток значительно колеблется от 1002 до 1035.
Причинами полиурии могут быть различные физические и химические факторы внешней среды, влияющие на организм. Понижение температуры окружающей среды вызывает спазм периферических сосудов с последующим повышением артериального давления и полиурией. К мочегонным веществам относятся хлористый и двууглекислый натрий, глюкоза. Введение этих веществ в организм или повышение их содержания в крови при патологических состояниях вызывает повышенное отделение мочи – полиурию.
Большое количество мочи наблюдается при нарушении углеводного обмена, характерного для сахарного диабета. Характерным признаком полиурии при сахарном диабете является высокое содержание сахара – глюкозурия и высокий удельный вес мочи.
Особенно много мочи (20-40 л в сутки) наблюдается при несахарном диабете, при этом моча имеет низкий удельный вес и не содержит сахара, развивается при пониженном образовании антидиуретического гормона. Несахарный диабет помимо полиурии характеризуется повышенной жаждой – полидипсией, имеющей компенсаторный характер, предохраняющий организм от обезвоживания, и частыми позывами на мочеиспускание – поллакиурией. Причиной поллакиурии является повышение чувствительности нервных рецепторов мочевого пузыря, возникающее в связи с усилением мочеобразования или с изменением состава мочи. Повышенное раздражение рецепторов мочевого пузыря наблюдается при развитии воспалительных и опухолевых процессов слизистой оболочки мочевого пузыря (цистит) и при образовании камней в полости мочевого пузыря. Поллакиурия появляется при сужениях (стриктурах) мочеиспускательного канала различного происхождения, например, при увеличении (гипертрофии) предстательной железы.
От полиурии надо отличать никтурию, при которой наибольшее количество мочи выделяется в ночное время без значительного нарушения общего суточного количества мочи. Никтурия является одним из ранних признаков нарушения почечной функции (нефросклерозы, диффузные гломерулонефриты) и развивающегося ослабления сердечной деятельности.
Олигурия – уменьшение количества отделяемой мочи, может быть внепочечного и почечного происхождения.
Олигурия внепочечного происхождения возникает при:
- боли;
- сильных психических травмах;
- раздражении 12-перстной и слепой кишок; резком растяжении ампулы прямой кишки;
- новообразованиях и воспалительных процессах промежуточного мозга и дна IV желудочка, т.е. областей, имеющих отношение к регуляции водного обмена в организме.
Олигурию вызывают:
- потеря больших количеств воды (длительная ходьба, горные восхождения, напряженная физическая работа, усиленное потоотделение, неукротимая рвота, обильные поносы);
- отеки;
- вторая стадия лихорадки;
- образование обильных экссудатов;
- нарушения кровообращения в малом и большом кругах кровообращения.
Олигурия почечного происхождения появляется при нефроциррозе и в начальном периоде острого гломерулонефрита. Часто следствием олигурии является олакизурия – редкое мочеиспускание.
Анурия – кратковременное или длительное прекращение отделения мочи почками.
В механизме рефлекторной анурии основную роль играет спазм приносящих артериол.
Мочеотделение может прекращаться на несколько дней под влиянием чрезвычайной психической травмы. Анурия наблюдалась у людей, перенесших землетрясение. Иногда анурия развивается при приступах калькулезного холецистита, лапаротомии, оперативных вмешательствах на внутренних органах.
Между обеими почками осуществляется функциональная взаимосвязь через почечно-нервные сплетения и путем рено-ренальных рефлексов. Поэтому патологические процессы в одной почке могут вызывать спазм сосудов в другой здоровой почке, что приводит к развитию анурии.
По происхождению все анурии разделяются на следующие виды:
- рефлекторные, возникающие в результате висцеро-висцеральных рефлексов;
- почечные (истинные) при воспалительных или дегенеративных процессах в почках;
- преренальные – в связи с прекращением притока крови к почкам в результате перегиба, сдавления почечных сосудов опухолями или их тромбоза и эмболии;
- субренальные (ложные) нарушения в мочевыводящих путях;
- экстраренальные (интоксикации, отравления, шок, ослабление сердечной деятельности, кровопотери, диарея).
Выделение белка с мочой называется протеинурией, при этом чаще всего выводится альбумин – альбуминурия.
Различают следующие виды альбуминурии:
- физиологические;
- патологические;
- почечные;
- внепочечные;
- преходящие.
Физиологические альбуминурии
Здоровый человек выделяет с мочой 150-200 мг белка, 60% которого составляют белки сыворотки альбумины и 40% гликопротеины, секретируемые клетками восходящею сегмента петли Генле. В небольшом количестве в нормальной моче содержится секреторный IgA. В нормальной моче белок обычно не находят при использовании рутинных (обычных) методов. Появление белка в моче выше нормы называется протеинурией.
Появление белка в моче у здоровых людей может быть связано с:
- введением белковых растворов;
- переливанием крови;
- напряженной мышечной работой;
- спортивными состязаниями;
- употреблением пищи богатой белком.
Три основных механизма могут обусловить развитие протеинурии:
- изменение проницаемости клубочков, способствующее повышенной фильтрации сывороточных белков, особенно альбумина;
- нарушение реабсорбции белков в канальцах;
- фильтрация белков с измененной структурой или низкомолекулярных белков, если их количество превышает реабсорбционные способности канальцев.
Протеинурия, связанная с повреждением гломерулярного фильтра, называется гломерулярной (почечной) протеинурией.
Два основных фактора способствуют увеличению проницаемости гломерул (клубочков):
- непосредственное повреждение фильтрационного барьера патологическим процессом (например, гломерулонефрит);
- гемодинамический фактор, связанный с увеличением гломерулярного капиллярного давления (при застойно-сердечной недостаточности и тяжелой артериальной гипертонии).
Гломерулярная протеинурия характеризуется высоким содержанием белка в моче, свыше 4-5 г/сут, а при нефротическом синдроме может достигать 50 г/сут.
Обычно в моче преобладают альбумины (до 60%), но при тяжелых формах гломерулонефрита в моче появляются и глобулины.
При поражении канальцев (синдром Фанкони, интоксикация кадмием, закупорка мочевых путей, радиационный нефрит) развивается канальцевая протеинурия. Общее содержание белка при канальцевой протеинурии не превышает 1-2 г/сут.
Протеинурию при миеломной болезни и других заболеваниях сопровождающихся повышением концентрации аномальных белков в крови называют протеинурией «перегрузки». Причиной появления этих белков в моче является снижение реабсорбционных возможностей канальцев.
Патологические альбуминурии
Патологическая альбуминурия внепочечного происхождения наблюдается при:
- расстройствах кровообращения в почках рефлекторного (внезапное охлаждение тела) и механического характера (сдавление почечной артерии или вены, застойные явления в системе воротной вены и нижней полой вене);
- кислородном голодании почек;
- декомпенсации сердечно-сосудистой системы.
Ортостатическая протеинурия (у лиц не старше 30 лет) характеризуется появлением белка в моче в положении стоя и уменьшением протеинурии в положении лежа. Часть подростков с ортостатической протеинурией имеют искривление позвоночника кпереди (лордоз) в грудной и поясничной областях. Устранение лордоза корсетом прекращает протеинурию. Прогноз ортостатической протеинурии благоприятный, так как у пациентов не развивается почечная недостаточность.
Заболевания половых органов, мочевыводящих путей сопровождаются ложной протеинурией внепочечного происхождения. Ложная протеинурия наблюдается в послеродовом и менструальном периодах и у беременных.
Патологическая протеинурия почечного происхождения наблюдается при:
- гломерулонефритах;
- нефрозах;
- острых и хронических инфекциях и интоксикациях (скарлатина, ангина, ревматизм, сепсис);
- отравлении солями тяжелых металлов и салициловыми препаратами.
Гемоглобинурия и гематурия
Выделение с мочой несвязанного с эритроцитами гемоглобина называется гемоглобинурией. Она может быть связана с присутствием гемоглобина в крови (гемоглобинемия) или с распадом эритроцитов в моче при явлении гематурии, в этом случае гемоглобинурия называется ложной. Гемоглобин в плазме крови, а затем в моче появляется после быстрого разрушения эритроцитов в кровяном русле, когда костный мозг, селезенка и печень не «успевают» усваивать всю массу распавшихся эритроцитов.
Гемолиз (распад) эритроцитов наблюдается при:
- переливании несовместимой крови;
- отравлениях гемолитическими ядами;
- гемолитических и злокачественных анемиях;
- гемолитической желтухе;
- обширных ожогах.
Моча при гемоглобинурии имеет окраску от бледно-розового до интенсивного черного цвета; кроме оксигемоглобина и восстановленного гемоглобина в ней находят метгемоглобин, билирубин, уробилиноген и уробилин. Гемоглобинурия часто сопровождается увеличением селезенки, желтухой.
Пароксизмальная (приступообразная) гемоглобинурия может наблюдаться при сильном охлаждении ног или всего тела, при длительной мышечной работе. Пароксизмальная гемоглобинурия характеризуется внезапным повышением температуры тела, рвотой, болями в области почек, мышцах, суставах, выделением темно-красной мочи.
Появление эритроцитов в моче в значительном количестве называется гематурией.
Причиной гематурии могут быть:
- диффузные и очаговые гломерулонефриты;
- туберкулез и злокачественные новообразования почек;
- отравление сулемой, мышьяком;
- нарушения микроциркуляции в почках;
- почечнокаменная болезнь.
Гематурия является симптомом многих заболеваний (рис. 6-7). Чтобы составить представление об источнике гематурии проводят пробу с тремя стаканами. Больному предлагают при одном мочеиспускании собрать первую, вторую и последнюю порцию мочи в три отдельных сосуда с тем, чтобы сравнить их окраску.
При гематурии из мочеиспускательного канала окрашивается первая порция мочи.
При пузырной гематурии окрашивается последняя порция мочи, так как кровь обычно оседает на дне мочевого пузыря и выделяется с последней порцией мочи. При гематурии почечного происхождения кровь перемешивается с мочой и равномерно окрашивает содержимое всех трех стаканов. Присутствие в моче длинных червеобразных сгустков, эритроцитарных цилиндров, песка, альбуминурия подтверждают почечное происхождение гематурии (моча при нефрите имеет цвет «мясных помоев»).
Появление лейкоцитов в моче свыше 3 в поле зрения называется лейкоцитурией, которая обусловлена инфекцией мочевого тракта.
Цилиндрурия – выделение мочи, содержащей в своем составе различные виды мочевых цилиндров: гиалиновых, зернистых, восковидных и эпителиальных. Цилиндры образуются в почечных канальцах и свидетельствуют о наличии патологии почек (поражение клубочкового аппарата или инфекции паренхимы почек). Все мочевые цилиндры состоят из свернувшегося в просвете почечных канальцев белка и/или клеток. В условиях щелочной мочи цилиндры не образуются. Чаще цилиндры появляются в моче, содержащей желчные кислоты.
Гомогенные, стекловидные гиалиновые цилиндры встречаются в физиологических условиях и появляются в большом количестве при застойных процессах в почках, пиелонефритах, туберкулезе, опухолях.
Зернистые цилиндры встречаются при тяжелых поражениях канальцев (нефрозо-нефрит). Они непрозрачны, покрыты капельками жира, частичками распавшегося почечного эпителия и солями мочевой кислоты.
При тяжелом остром и хроническом нефрите появляются грубые и широкие восковидные цилиндры.
Эпителиальные цилиндры состоят из мало измененных или имеющих зернистое и жировое перерождение клеток почечного эпителия.
Мочевые цилиндры могут содержать бактерии, лейкоциты, эритроциты.
Появление зернистых, восковидных и особенно эпителиальных цилиндров свидетельствует о глубоких дегенеративных процессах в почечном эпителии.
Подсчитывают количество цилиндров в полусуточной порции мочи. Установлено, что при геморрагической форме гломерулонефрита число гиалиновых цилиндров может превышать 2000000 (вместо 5000 в норме).
Нарушение выделения солей – кристаллурия может быть связана с патологией вводно-солевого обмена в организме.
Концентрационная способность почек. Почки здоровых людей в течение суток могут выводить громадное количество мочи (до 20 л) и легко концентрируют все продукты азотистого и солевого обмена веществ.
Мочевина в почках концентрируется в 60 раз, креатинин – в 75 раз, аммиак – в 40 раз, мочевая кислота – в 25 раз, соли серной кислоты – в 60-90 раз. Удельный вес мочи может достигать 1028-1036, суточное количество мочи при сухоедении не превышает 500-550 мл.
Понижение концентрационной способности почек называется гипостенурией. Состояние гипостенурии отличается тем, что, несмотря на сухоедение, общее суточное количество мочи увеличено, но она с низким удельным весом 1012-1014. При хронических гломерулонефритах почки выделяют 2-3 л мочи в сутки с удельным весом 1010-1012. Монотонно низкий удельный вес наблюдается при гломерулонефритах. Такое функциональное состояние почек называется изостенурией.
Для определения функциональной способности почек к разведению и концентрированию применяют пробу Зимницкого, особенно у тяжелых почечных больных.
Больной находится на обычном пищевом и питьевом режиме. Моча собирается в течение суток через каждые три часа. В каждой порции определяют количество мочи и ее удельный вес, содержание хлоридов и мочевины.
У здорового человека количество выделенной мочи и концентрация каждой порции колеблется в широких пределах в зависимости от принятой пищи и питья. Чем сильнее нарушена деятельность почек, тем меньше колебания, тем ближе друг к другу цифры удельного веса и объема мочи в отдельных порциях.
В норме дневной диурез выше ночного. При развитии почечной недостаточности это соотношение нарушается.
Оценивать функцию почек можно и по нагрузке чужеродными веществами, например, введением фенолового красного (фенолрота). Проба проводится следующим образом.
Больному дают выпить 2 стакана воды за 30 минут до исследования, вводят катетеры в каждый мочеточник, внутривенно вводят краситель. Через 5 минут собирают мочу из катетеров в пробирки, содержащие несколько капель 10% раствора едкого натрия. Следующие порции берут через 15 и 30 минут в течение часа. Отмечают моменты появления, а затем исчезновения краски (моча в пробирке приобретает пурпурно-красный цвет, который постепенно бледнеет) и определяют процент выделенной краски в каждой порции в отдельности.
При здоровых почках краска появляется в моче через 5 минут после ее введения.
Моча обеих почек вместе должна содержать в первые 15 минут 35-45%, в первые 30 минут – 50-60%, а через 1 час – 65-80% краски.
При нарушении функции канальцев снижается клиренс фенолрота, т.е. задерживается выведение краски.
Показателями, характеризующими нарушение функции канальцев почек, являются:
- снижение клиренса фенолрота;
- гипостенурия – снижение концентрационной способности почек;
- глюкозурия – появление сахара в моче.
Почечная недостаточность – это синдром, характерным признаком которого является значительное снижение или прекращение экскреторной и других функций почек.
Различают острую и хроническую недостаточность почек.
Острая почечная недостаточность (ОПН) характеризуется внезапным нарушением функций почек, сопровождающимся накоплением в крови азотистых шлаков и прогрессирующей азотемией. Некоторые формы острой почечной недостаточности относятся к потенциально обратимым патологическим процессам, поскольку функции почек при ОПН могут быть восстановлены при своевременном устранении повреждающего фактора.
В зависимости от этиологических факторов ОПН подразделяется на: преренальную, ренальную и постренальную.
К преренальным причинам относятся:
- острая сосудистая недостаточность (различные виды шока – травматический, кардиогенный, анафилактический);
- обезвоживание организма и потеря электролитов (чрезмерное потоотделение, рвота, понос, обширные ожоги, длительный прием мочегонных средств);
- массивный некроз тканей (гангрена, инфаркт, синдром раздавливания тканей);
- выраженный гемолиз при переливании несовместимой крови.
Функции самих почек на начальном этапе сохранены, но они не могут реализоваться из-за уменьшения тока крови в почках, при этом снижается эффективное фильтрационное давление и в крови накапливаются токсические продукты, которые должны были выводиться почками.
К ренальным причинам относятся:
- заболевания почек (острый гломерулонефрит, острый интерстициальный нефрит, некроз канальцев);
- прямое действие на ткань почек разнообразных токсинов (солей тяжелых металлов, крепких кислот, грибных и змеиных ядов, яда насекомых, лекарственных препаратов – антибиотиков, сульфаниламидов, барбитуратов; токсинов, образующихся при криминальных абортах, сепсисе);
- тромбоз и эмболия почечных артерий и вен, системные васкулиты.
К постренальным причинам относятся:
- длительная закупорка мочевыводящих путей (камни, опухоль мочеточника, закрытие их просвета гнойными пробками или кровяными сгустками);
- сдавление мочевыводящих путей извне при опухолях тазовых органов и забрюшинного пространства, увеличенной маткой при беременности;
- стриктуры мочеиспускательного канала.
Особым видом острой почечной недостаточности является аренальная недостаточность, возникающая при тяжелых травмах обеих почек или при их удалении по жизненным показаниям.
Основным патогенетическим звеном в развитии ОПН является нарушение внутрипочечного кровообращения и развитие гипоксии.
При острой почечной недостаточности из-за прекращения или снижения кровоснабжения почек уменьшается объем почечной фильтрации и нарушается выведение отдельных веществ, нарушается реабсорбционная функция канальцев.
В зависимости от продолжительности ишемии и баланса между тяжестью повреждения и компенсаторной возможностью внутриклеточных механизмов достигается определенный функциональный дисбаланс, который определяет дальнейшее прогрессирование или восстановление функций клеток.
Прекращение или уменьшение доставки кислорода к клеткам приводит к нарушению функций митохондрий. Результатом этого является снижение синтеза АТФ – возникает энергетический голод, что вызывает повреждение клеток. Ишемическое повреждение эндотелия сосудов способствует повышению проницаемости сосудистой стенки и усилению диффузии плазмы. В результате повышается вязкость крови. Это способствует развитию сладжирования крови, образованию микротромбов, усиленному ее свертыванию и развитию ДВС-синдрома. Следствием этих изменений является снижение фильтрационного давления и клубочковой фильтрации. Если нарушение почечного кровотока непродолжительно, то острая почечная недостаточность является обратимой – это функциональная фаза ОПН. Если ишемия почек затягивается, то возникают необратимые структурные изменения клубочков и канальцев – это уже структурная фаза ОПН.
Независимо от этиологического фактора клиническое течение острой почечной недостаточности однотипно.
В течение острой почечной недостаточности выделяют 4 стадии.
Начальная стадия – длится от нескольких часов до суток, характеризуется симптомами основного заболевания. Признаки нарушения функций почек еще отсутствуют, но на первый план выступают нарушения гемодинамики.
Вторая стадия – олигоанурии – продолжается около 2-х недель. Эта стадия характеризуется снижением диуреза ниже 500 мл, а через сутки олигурия сменяется анурией (суточный диурез менее 100 мл). В эту стадию значительно снижен почечный кровоток, из-за чего снижается процесс фильтрации в клубочках с последующим нарушением функций канальцев. Нарушается реабсорбция натрия, хлоридов, бикарбонатов. Моча имеет низкий удельный вес.
Нарушения функций разведения и концентрирования мочи обусловлены расстройством концентрационной способности дистальных канальцев из-за потери их чувствительности к антидиуретическому гормону.
Наряду с резким снижением диуреза, вплоть до полного его прекращения, наблюдаются гиперазотемия, нарушение водно-электролитного гомеостаза и кислотно-основного равновесия.
Основными клиническими проявлениями этой стадии являются: отек головного мозга, интерстициальный отек легких; картина водного отравления; тяжелые нарушения деятельности системы кровообращения – снижение сократительной функции сердца, нарушения сердечного ритма (экстрасистолия, брадикардия, блокада); снижение артериального давления с переходом в гипертензию; расстройство дыхания по типу дыхания Куссмауля; тяжелые расстройства функций нервной системы (головная боль, рвота, арефлексия, нарушение сознания, судороги, кома). Эти явления обусловлены нарушениями гомеостаза.
Большая часть больных погибает на высоте этой стадии. При благоприятном течении заболевания, а главное при проведении эффективных терапевтических мероприятий через 5-10 дней наступает переход в третью стадию.
Третья стадия – стадия восстановления диуреза и развития полиурии.
Восстановлению диуреза предшествует повышение скорости клубочковой фильтрации в действующих нефронах (в начальном периоде полиурии), а через несколько месяцев увеличивается масса действующих нефронов. Канальцевые функции восстанавливаются более медленными темпами.
Четвертая стадия – стадия выздоровления продолжается от 6 месяцев до 2-х лет и характеризуется постепенной нормализацией объема диуреза, функций канальцевого эпителия, величин клиренса эндогенного креатинина.
Осложнения при острой почечной недостаточности определяются тяжестью расстройств функций сердечно-сосудистой системы, патологией крови (анемия, нарушение функций тромбоцитов под влиянием увеличения оксида азота), неврологическими расстройствами (судороги, уремическая энцефалопатия).
Присоединение инфекций самая частая причина смерти пациентов с острой почечной недостаточностью. Это связано с подавлением иммунных механизмов (снижение хемотаксиса и фагоцитарной активности нейтрофилов, относительной лимфопенией и нарушением клеточно-опосредованной иммунной защиты).
Хроническая почечная недостаточность (ХПН) – синдром, развивающийся в связи с нарастающей гибелью нефронов. Проявления ХПН появляются при снижении числа действующих нефронов до 30%. Уменьшение числа действующих нефронов до 15-10% сопровождается развитием уремии и коматозного состояния.
Причины развития ХПН можно условно разделить на 3 группы.
Преренальные (хронические артериальные гипертензии, прогрессирующий стеноз почечных артерий).
Ренальные (хронические заболевания почек – гломерулонефриты, пиелонефриты, поликистоз; патология других органов, сопровождающихся повреждением почек (сахарный диабет, системная красная волчанка).
Постренальные (обструкция мочевыводящих путей; токсическое воздействие лекарственных препаратов).
В зависимости от степени нарушения функций почек и расстройств гомеостаза выделяют 3 стадии развития ХПН, каждая из которых подразделяется на фазы А и Б.
Первая стадия – латентная, характеризуется нормальными показателями концентрации креатинина в плазме крови и объема клубочковой фильтрации, но при проведении нагрузочных проб на разведение и концентрацию выявляется уменьшение функционального резерва почек.
Вторая стадия – гиперазотемическая, характеризуется снижением скорости клубочковой фильтрации на 75% (гибель 75% нефронов). Эта стадия сопровождается высокой азотемией, расстройством водно-электролитного баланса, нарушением концентрирования мочи, гиперволемией, гиперкальциемией, гиперфосфатемией и развитием метаболического ацидоза. Дальнейшее прогрессирование ХПН приводит к третьей стадии или стадии уремии.
Третья стадия – стадия уремии – характеризуется снижением объема клубочковой фильтрации до 15-10%, высокой азотемией, расстройством функций многих органов и систем.
Обнаружено свыше 200 токсических веществ, накопление которых в крови при хронической почечной недостаточности определяет интоксикацию организма. Интоксикация проявляется анорексией, диспептическими расстройствами, снижением массы тела, общей слабостью, головной болью, апатией, нарушениями вкуса, мучительным зудом, полиневритом, прогрессирующей анемией, нарушением дыхания, развитием уремического перикардита, миокардита, плеврита, судорогами и развитием комы.
В начальной стадии хронической почечной недостаточности наблюдается полиурия, объем суточной мочи достигает 2-4 л, наиболее ранним отклонением от нормы является увеличение ночного диуреза – никтурия. Развитие полиурии связано с тем, что оставшиеся действующие нефроны (25% от нормы) работают с повышенной нагрузкой. Это приводит к увеличению объема фильтрации, а значит к увеличению первичной мочи. Способность канальцев реабсорбировать воду уменьшается и снижается их способность к концентрированию мочи, поэтому развивается гипо-, а в дальнейшем изостенурия (удельный вес мочи не превышает 1008-1010). Нарушение реабсорбции связано со снижением чувствительности эпителия канальцев к альдостерону и антидиуретическому гормону.
Полиурию рассматривают как компенсаторный механизм, так как при этом с мочой выводятся и метаболиты, подлежащие выведению из организма, в том числе и азотистые шлаки. Благодаря этому механизму при хронической почечной недостаточности длительное время организм защищен от переизбытка жидкости и нарушения гомеостаза.
Переход в стадию олигурии происходит тогда, когда количество действующих нефронов становится меньше 10%. При этом клубочковая фильтрация резко снижается до 10 мл/мин (норма 120-130 мл/мин). объем суточной мочи начинает падать (менее 500 мл). нарушается функция концентрирования и разведения мочи. В эту стадию у пациента развивается водная «интоксикация», гипонатриемия и развивается ренальный (азотемический) ацидоз.
Развитие второй и третьей стадии хронической почечной недостаточности сопровождается нарушением продукции эритропоэтина и витамина Д3. Недостаток эритропоэтина обусловливает развитие анемии. Нарушение образования гидроксикальциферола – метаболита витамина Д3, который в норме образуется в клетках проксимальных канальцев, является причиной нарушения минерализации костей в связи с развитием вторичного гиперпаратиреоза и остеодистрофий.
Гиперпаратиреоз связан также с потерей способности почек поддерживать баланс фосфатов. При снижении скорости клубочковой фильтрации реабсорбция фосфатов падает с 90% до 15%, т.е. увеличивается выведение фосфатов. Это стимулирует секрецию паратгормона, вызывающего задержку фосфатов, это обусловливает снижение уровня ионизированного кальция в плазме и усиление проявлений вторичного гиперпаратиреоза.
Для ХПН характерно расстройство обмена глюкозы, развивается потеря чувствительности тканей к инсулину. При ХПН в крови накапливаются пептидные гормоны (гастрин, глюкагон, гормон роста, фолликулостимулирующие гормоны и др.).
1. Одним из внепочечных проявлений при остром или хроническом поражении клубочков нефрона, связанным с нарушением почечного кровотока, является артериальная гипертония. В настоящее время не вызывает сомнений, что почка способствует как повышению, так и понижению артериального давления.
В эпителиоидных клетках юкстагломерулярного (околоклубочкового) аппарата почек образуется ренин-протеолитический фермент. Он соединяется с ангиотензиногеном плазмы крови, превращает его в ангиотензин I, который под действием конвертирующего фермента крови превращается в ангиотензин II, обладающий сосудосуживающим эффектом.
Сосудосуживающий эффект ангиотензина II усиливается симпатическим отделом вегетативной нервной системы, альдостероном.
В норме ангиотензин быстро исчезает из системы кровообращения, так как разрушается в почках под действием фермента ангиотензиназы. При нарушении гемодинамики в обеих почках их ангиотензиназная активность резко снижается, что способствует повышению артериального давления.
Ренин-ангиотензиновый механизм является пусковым механизмом развития гипертонии. Тот факт, что после удаления обеих почек развивается стойкая хроническая гипертензия дали повод для предположения, что почки обладают депрессорной функцией. Нормальные почки обладают способностью контролировать действие почечных и внепочечных прессорных веществ (вазопрессин, катехоламины, альдостерон), т.е. обладают антипрессорной (противогипертензивной) функцией. Эта функция осуществляется фосфолипидным ингибитором ренина и простагландинами типа А и Е. Выключение этой функции при нарушении кровообращения в почке ведет к развитию гипертонии.
Простагландины образуются в мозговом веществе почек. Контроль за секрецией простагландинов осуществляется ангиотензинном II. Повышенное его количество в плазме крови стимулирует образование простагландинов. Простагландины не только расширяют артериолы, но и вызывают усиленное выведение натрия с мочой, что также предотвращает развитие гипертонии.
2. Вторым внепочечным проявлением, связанным с поражением клубочков нефронов, является анемия. В основе развития анемии лежит нарушение функции юкстамедуллярного аппарата, выражающееся:
- уменьшением продукции эритропоэтина;
- увеличением выработки ингибитора эритропоэза.
Следствием выпадения эритропоэтической функции почек является развитие анемии. Развивающаяся анемия является нормоцитарной; гипорегенераторной.
В механизмах развития анемии при заболевании почек имеют значение: угнетение функций костного мозга азотистыми веществами; развивающаяся гематурия; потеря трансферрина при значительной протеинурии; дефицит цианкобаламина.
3. Третьим внепочечным синдромом является нарушение гемокоагуляции. В физиологических условиях почки участвуют в синтезе урокиназы, гепарина, факторов свертывания (V, VII, VIII, IX и X), депонировании и выделении гепарина и веществ, обладающих коагулирующим и антикоагулирующим действием.
В поддержании коагуляционно-фибринолитического равновесия важную роль играет урокиназа (белок синтезируемый эндотелиальными клетками юкстамедуллярного аппарата почки). Ее роль состоит в: активации фибринолитической системы крови и мочи, направленной на растворение фибрина в сосудах клубочков; предотвращении нарушений клубочковой фильтрации и образования кровяных сгустков по ходу мочевых путей; растворении уромукополисахаридов, которые являются основой для образования мочевых камней.
При очаговом и диффузном гломерулонефрите наблюдается гиперкоагуляция крови и понижение активности фибринолиза. В терминальной стадии заболевания развивается гипокоагуляция крови с клиническими проявлениями гемморрагического синдрома.
Уремия – сложный клинический симптомокомплекс, заключающийся в аутоинтоксикации организма продуктами обмена веществ и экзогенными соединениями в норме выводимыми почками. Непосредственной причиной развития уремии является почечная недостаточность (острая или хроническая).
Основными факторами повреждения тканей и органов при уремии и почечной коме являются:
- интоксикация организма избытком аммонийных соединений (аммиаком, производными аммония), образующихся в процессе трансформации мочевины в кишечнике;
- токсическое действие продуктов метаболизма ароматических аминокислот (фенол, индол, скатол);
- повреждение мембран и ферментов клеток;
- нарушение энергетического обеспечения клеток органов и тканей;
- нарастание ацидоза.
В патогенезе уремии лежат следующие механизмы:
- нарушение объема фильтрации и экскреции азотистых соединений;
- нарушение контроля выведения воды и электролитов;
- расстройство метаболизма витамина Д3;
- снижение выработки эритропоэтина, простагландинов, кининов и др. веществ.
Накопление азотистых шлаков оказывает ряд токсических эффектов:
- ингибирует потребление кислорода мозгом;
- повышает проницаемость клеточных мембран и чувствительность миокарда к гиперкалиемии;
- повышает агрегацию тромбоцитов;
- вызывает адинамию и депрессию;
- вызывает расстройства желудочно-кишечного тракта.
Перечисленные эффекты приводят к нарушению функции и структуры большинства органов.
Развивается дистрофия миокарда из-за гипоксии, дефицита макроэргов и артериальной гипертензии. В результате гиперкалиемии и гипермагниемии возникает экстрасистолия, может развиться блокада и даже остановка сердца.
Развивается отек легких, нарушается функция внешнего дыхания, что проявляется дыханием Куссмауля, которое сменяется дыханием Чейн-Стокса.
Анемия развивается из-за нехватки эритропоэтина. Тромбоцитопения лежит в основе кровоточивости.
Азотистые метаболиты начинают выделяться через потовые железы, дыхательные пути, пищеварительный тракт, серозные оболочки и полости суставов.
Следствием этого являются кожный зуд, характерный уремический запах изо рта (запах мочи и аммиака), налет мочевины на коже, слизистой рта, желудка и кишечника, рвота, понос, перикардит, плеврит. Перикардит проявляется шумом трения перикарда у основания сердца. Этот шум называют «похоронным звоном». Нарушения со стороны нервной системы выражаются психической депрессией, потерей сознания, коматозным состоянием, судорагами, параличами жизненно важных центров. Эти нарушения связаны с интоксикацией, гипоксией, расстройством кислотно-основного равновесия.
Терминальным признаком уремического отравления является гипотермия. Температура тела падает до 32 и даже 30°С. Смерть наступает при низкой температуре тела.
Для нормализации нарушений гомеостаза и очищения крови больных от «уремических токсинов» применяют гемодиализ – искусственную почку, что позволяет продлить жизнь таких больных на несколько лет. Более радикальным методом является пересадка почки.
Нефротический синдром это клинико-биохимический симптомокомплекс, характеризующийся высокой протеинурией (до 10-20 г/сутки), гипопротеинемией, гиперхолестеринемией и развитием распространенных отеков.
По происхождению нефротический синдром бывает первичным и вторичным.
В основе возникновения первичного нефротического синдрома чаще всего лежит генетически обусловленный дефицит обмена веществ (липоидный нефроз) или трансплацентарный перенос специфических противопочечных антител от матери к плоду (врожденный семейный нефроз).
Вторичный нефротический синдром развивается при:
хронических инфекционный процессах; нефропатии беременных; сахарном диабете; системной красной волчанке; амилоидозе; стафилококковом сепсисе; сывороточной болезни; отравлении солями тяжелых металлов; обширных ожогах; радиационном поражении; применении некоторых лекарственных средств (сульфаниламиды, кортикостероиды, пенициллины); при болезнях системы крови.
Основой развития нефротического синдрома является увеличение проницаемости стенки капиллярных сосудов для плазменных белков, обусловленной иммунологическими механизмами.
Источниками антигенов могут быть экзогенные факторы: бактериальные, вирусные, паразитарные, лекарственные, пищевые и др. Эндогенными антигенами могут быть ДНК, денатурированные нуклеопротеины, белки опухолевого происхождения и др. Антитела, продуцируемые в ответ на антигены, принадлежат к классу IgM.
Выраженная протеинурия, обусловливает гипоальбуминемию, это приводит к понижению онкотического давления в плазме и усиленному выходу жидкости из сосудов в межклеточное пространство. Возникает гиповолемия, это активирует ренин-ангиотензин-альдостероновую систем, в результате повышается секреция альдостерона и антидиуретического гормона. Это приводит к задержке в организме воды и натрия. Объем крови увеличивается, но происходит ее разжижение, нарастает гипопротеинемия и гипоонкия, в связи с чем вода не задерживается в кровяном русле и перемещается в ткани, способствуя развитию отеков.
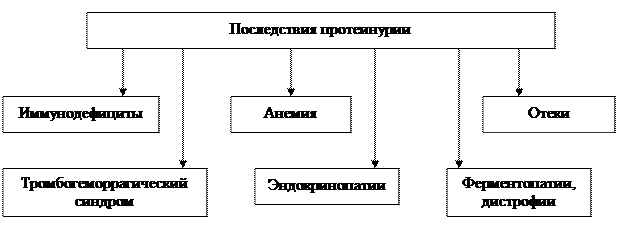
Последствия потери белков при нефротическом синдроме.
При нефротическом синдроме развивается гиперлипидемия, в крови повышается содержание холестерина, триглицеридов, фосфолипидов.
Гиперлипидемия патогенетически связана с нарушением белкового обмена и угнетением липолитической активности плазмы крови.

Патогенез отеков при нефротическом синдроме.
В результате повышения проницаемости сосудистой стенки при нефротическом синдроме происходит усиленное выведение с мочой белковых субстанций, в том числе иммуноглобулинов, факторов свертывания, витаминсвязывающих белков, трансферрина и других металлосвязывающих белков.
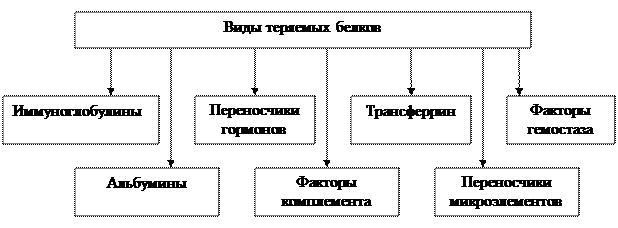
Белки, теряемые организмом при нефротическом синдроме.
В связи с этими потерями наблюдается склонность к тромбоэмболии, понижению устойчивости к инфекциям, развитию железодефицитной анемии, развитию гиповитаминозов Д и С, гипокальциемии.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.