Педагогический контроль с использованием информационных технологий в среднем профессиональном образовании в преподавании учебной дисциплины химии.

Государственное
автономное профессиональное образовательное учреждение Республики Башкортостан
«Бирский медико-фармацевтический колледж»
Методическая разработка
практического занятия
ОП.10 « Аналитическая химия»
по специальности 33.02.01 Фармация с использованием информационно-компьютерных технологий при изучении методик выполнения работ по йодометрии
 тема:
тема:
«Приготовление стандартного раствора К2Сr2О7.
Определение точной концентрации
раствора Na2S2O3»
Автор: Чернова Елена Викторовна
Бирск – 2024
|
Рассмотрена и одобрена на заседании цикловой комиссии общепрофессиональных дисциплин Протокол № 9 от «25» 01 2023 г. _______________________________________ Председатель ЦК О.Н. Стишакова |
Составлена в соответствии с требованиями ФГОС СПО специальности 33.02.01 Фармация утвержденным приказом министерства образования и науки Российской Федерации 13.07.2021 года № 449 ____________________________ Зам. директора по учебной работе С.В.Трухина |
Разработчик:
Е.В. Чернова – преподаватель общепрофессиональных дисциплин ГАПОУ РБ «Бирский медико-фармацевтический колледж»
Рецензент:
О.Н.Стишакова - преподаватель высшей квалификационной категории ГАПОУ РБ «Бирский медико-фармацевтический колледж», председатель ЦМК общепрофессиональных дисциплин
Рецензия на методическую разработку практического занятия
преподавателя аналитической химии
ГАПОУ РБ «Бирский медико-фармацевтический колледж»
Черновой Елены Викторовны
Методическая разработка практического занятия по теме: «Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3» составлена в соответствии с требованиями Федерального государственного образовательного стандарта СПО специальности 33.02.01 Фармация.
В данной методической разработке занятия поставлена цель: изучить и обобщить теоретический материал по теме, установить содержание (количества) или концентрации компонента в анализируемом объекте – количественный анализ. Определения точного содержания отдельных элементов и их соединений в исследуемом веществе или смеси веществ. Необходимо знать классы и соединения неорганической химии, владеть основополагающими химическими понятиями, теориями, законами и закономерностями. Уверенное пользование химической терминологией и символикой. Четко обозначены задачи данного практического занятия, для достижения, которых преподаватель использует комбинированный метод с включением элементов информационных технологий. Кроме того, использует постановку проблемных вопросов при закреплении повторяемого материала, обращение к наглядным пособиям и компьютерным средствам обучения и выполнении исследовательских заданий.
Занятие имеет обширные межпредметные и внутрипредметные связи. Материал структурирован в соответствии с логикой изложения, в краткой и доступной форме. Соблюдены санитарно-гигиенические требования к проведению занятия с использованием компьютера и учтена техника безопасности при работе информационных технологий.
Наглядность усиливается при использовании информационно компьютерных технологий, что подводит студента к ситуации повторяемого материала. Хорошо продуманы ИКТ, уместны слайды презентации, сопровождающие рассказ преподавателя.
Важным этапом является изучение и закрепление полученного материала. Для контроля преподаватель использует задачи. По окончанию занятия задается домашнее задание.
Использование преподавателем ИКТ будет способствовать результативности обучения, достижению целей урока, эффективному закреплению материала, оперативному контролю знаний студентов и повышению качества обучения
Методическая разработка практического занятия может быть рекомендована для использования в образовательных учреждениях СПО.
Председатель ЦК общепрофессиональных дисциплин
ГАПОУ РБ «Бирский медико-фармацевтический колледж», отличник здравоохранения РБ, _____________О.Н. Стишакова
Содержание
1. Аннотация …………………………………………………………………...5.
2. Структура методической разработки ………………………………………7
3. Методический блок………………………………………………………….8
4. Информационный блок……………………………………………………..12
5. Приложение 1……………………………………………………………….16
6. Приложение 2……………………………………………………………….18
7. Приложение 3……………………………………………………………….19
8. Приложение 4……………………………………………………………….20
9. Приложение 5……………………………………………………………….22
10. Кроссворд…………………………………………………………………...23
11. Приложение 6………………………………………………………………24
Аннотация
Методическая разработка практического занятия ОП. 10 Аналитическая химия специальность Фармация по теме: «Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3» составлена в соответствии с требованиями Федерального государственного образовательного стандарта СПО специальности 33.02.01 Фармация.
Данное практическое занятие направлено на изучение и обобщение теоретического материала по теме, установить содержание (количества) или концентрации компонента в анализируемом объекте – количественный анализ. Который предназначен для определения точного содержания отдельных элементов и их соединений в исследуемом веществе или смеси веществ. Повторить классы и соединения неорганической химии, владеть основополагающими химическими понятиями, теориями, законами и закономерностями. Уверенное пользование химической терминологией и символикой. Четко обозначены задачи данного занятия, для достижения, которых преподаватель использует комбинированный метод с включением элементов информационных технологий. Кроме того, использует постановку проблемных вопросов при закреплении повторяемого материала, обращение к наглядным пособиям и компьютерным средствам обучения и выполнении исследовательских заданий. Методическая разработка практического занятия является составной частью учебно - методического комплекса «Аналитическая химия».
Данное практическое занятие аналитической химии предусматривает применение методов: словесных, наглядных и практических, компьютерной технологии, что позволяет многосторонне развивать студентов, их мышление и навыки, приучает к определенным логическим операциям, воспитывает у учащихся научное мировоззрение, развивает их личностные качества (способности, волю, интерес) и помогает выработке осознанной мотивации обучения.
Большое значение для усвоения материала имеет использование на уроке информационно-коммуникационных технологий и возможность работать с ними самостоятельно. Продуманная последовательная постановка этапов занятия способствует развитию умения анализировать и синтезировать материал. Сначала повторяется пройденный материал, затем под руководством преподавателя, для проверки знаний и умений используется тестовый опрос в программе гипер - теста. Во время закрепления материала с использованием информационных технологий презентацией Microsoft Office Power Point на тему «Количественный анализ лекарственных веществ». Для закрепления умений практического занятия по данной теме «Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3» предлагается решить задачи и задания на бумажном носителе. Организация образовательного процесса по данной теме предусматривает использование современных педагогических технологий: методик проблемного обучения, игровых технологий, информационно – коммуникативных технологий обучения. Работа включает аннотацию, выписку из календарно – тематического плана, задания для оценки и коррекции занятий, полученных на предыдущем занятии, профессионально компетентностные задачи, тестовые задания, перечень литературы и средств обучения.
Методическая разработка практического занятия определяет межпредметные и внутрипредметные связи, что предусматривает:
1) сформированность представлений о месте химии в современной научной картине мира; понимание роли химии в формировании кругозора и функциональной грамотности человека для решения практических задач;
2) владение основополагающими химическими понятиями, теориями, законами и закономерностями; уверенное пользование химической терминологией и символикой;
3) владение основными методами научного познания, используемыми в химии: наблюдение, описание, измерение, эксперимент; умение обрабатывать, объяснять результаты проведенных опытов и делать выводы; готовность и способность применять методы познания при решении практических задач;
4) сформированность умения давать количественные оценки и проводить расчеты по химическим формулам и уравнениям;
5) владение правилами техники безопасности при использовании химических веществ;
6) сформированность собственной позиции по отношению к химической информации, получаемой из разных источников.
Методическая разработка практического занятия аналитической химии может быть рекомендована для использования в образовательных учреждениях СПО.
Методическая разработка структурирована и содержит:
Ø Методический блок, где даны рекомендации по работе с методической разработкой, указана название общепрофессиональной дисциплины, курс и тема. Приведена краткая аннотация урока, определены цели и задачи занятия, актуальность темы, мотивация, оснащение, указаны междисциплинарные связи, список литературы, домашнее задание, представлена хронологическая карта занятия;
Ø Информационный блок, где представлен теоретический материал по изучаемой тематике. Данная информация поможет студенту подготовиться к практическому занятию, что дает возможность более эффективно сформировать общие и профессиональные компетенции;
Ø Блок контроля знаний включает два вида контроля на занятии: оценка и коррекция знаний предыдущей темы в виде решения тестового контроля;
Ø Практический блок состоит из решений профессионально - компетентностных задач по алгоритму.
Цель создания методической разработки практического занятия по ОП.10 Аналитическая химия, специальность Фармация
Методическая разработка практического занятия создана с целью методического обеспечения образовательного процесса по реализации требований основной профессиональной образовательной программы по специальности 33.02.01 Фармация СПО общепрофессиональных дисциплин ОП.10 Аналитическая химия. «Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3 », а также с целью обмена опытом и оказания методической помощи преподавателю по эффективному формированию необходимых профессиональных и общих компетенций, знаний и умений у студентов первого курса.
Методический блок
Рекомендации по работе с методической разработкой.
1. Методическая разработка практического занятия аналитической химии содержит перечень целей, отражающих формирование необходимых знаний и умений. Педагогические подходы и методы, представленные в методической разработке, позволяют педагогу выбрать наиболее оптимальные действия для эффективного раскрытия индивидуальных способностей и возможностей обучающихся;
2. Оснащение занятия включает предметное и визуальное обеспечение (открытая модульная система, цифровые обучающие и контролирующие программы, презентация);
3. Хронологическая карта отражает этапы занятия, ориентировочное планируемое время на их выполнение, раскрывает деятельность педагога и обучающихся на каждом этапе занятия;
4. Информационный блок комбинированного занятия включает материал, предназначенный для организации самостоятельной деятельности студентов;
5. Для оценки и коррекции знаний, полученных на предыдущих занятиях, используется интерактивный опрос с использованием ИКТ, включающая выполнение заданий на выбор студентов, что позволяет погружать студентов в атмосферу интеллектуальной деятельности предельно близкую к профессиональной практической работе.
Название общепрофессиональной дисциплины: ОП.10 «Аналитическая химия»
Краткая аннотация занятия:
Курс, специальность: 1 курс, специальность 33.02.01 Фармация
Тема раздела: Количественный анализ
Тема занятия: Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3
Эпиграф занятия: «Всегда и в каждом деле для сознательности совершаемых в нем действий полезно подсчитать».
Вид занятия: практическое
Метод изложения: объяснительно-иллюстративный, продуктивный
Продолжительность: 90 мин.
Место проведения: кабинет лаборатории аналитической химии
Цель занятия: Данное практическое занятие аналитической химии направлено на изучение и обобщение теоретического материала, определение количественного содержания отдельных составных частей исследуемого вещества при использовании различных методов: химических, физических и физико-химических.
Содержание дисциплины должно быть ориентировано на подготовку студентов к освоению профессиональных модулей в соответствии с ФГОС СПО по специальности 33.02.01 Фармация и овладению профессиональными компетенциями (ПК):
ПК 1.1. Организовать прием, хранение лекарственных средств, лекарственных средств, лекарственного сырья и товаров аптечного ассортимента в соответствии с требованиями нормативно-правовой базы.
ПК 1.6. Соблюдать правила санитарно-гигиенического режима, охраны труда, техники безопасности и противопожарной безопасности.
ПК 1.7. Оказывать первую медицинскую помощь.
ПК 2.1. Изготавливать внутриаптечную заготовку и фасовать лекарственные средства для последующей реализации.
ПК 2.3. Владеть обязательными видами внутриаптечного контроля лекарственных средств.
ПК 2.4. Соблюдать правила санитарно-гигиенического режима, охраны труда, техники безопасности и противопожарной безопасности.
Задачи практического занятия аналитической химии:
Дидактические задачи:
· закрепить теоретические знания по решению упражнений на химическое равновесие с целью определения и регулирования направления протекания химических реакций;
· закрепить теоретические знания направления реакций протекания ОВ реакций с целью определения и регулирования направления протекания химических реакций;
· закрепить теоретические знания в определении условия образования и растворения осадка с целью определения и регулирования направления протекания химических реакций;
· готовить стандартный раствор, устанавливать точную концентрацию с целью определения и регулирования направления протекания химических реакций;
· закрепить теоретические знания по теме: «Окислительно-восстановительные реакции»;
· закрепить теоретические знания по теме: «Сравнительная характеристика строения и химических свойств элементов неорганической химии»;
Развивающие задачи:
· развивать приемы сравнения, сопоставления, анализа и обобщения знаний;
· продолжить формирование исследовательских умений студентов, умений планировать свою деятельность, использовать свои предметные знания в повседневной жизни.
· развивать самостоятельность действий и суждений студентов, способствовать их самореализации и креативности.
Воспитательные задачи:
· способствовать развитию представлений о познаваемости мира, пониманию собственных интеллектуальных достижений как целостной характеристики современного человека;
· воспитывать интерес к своей профессии, стремление к творчеству и новаторству;
· воспитывать чувство ответственности за свое здоровье и здоровье окружающих;
· воспитывать аккуратность, внимательность, точность.
Формы реализации методов: практическое: проблемно-поисковый, исследовательский и репродуктивный характер деятельности с применением ИКТ технологии (интерактивная доска) в процессе объяснения материала урока самостоятельная работа.
Формы организации познавательной деятельности:
- фронтальная – при обсуждении закрепляющего материала, фронтальном опросе;
- индивидуальная – при самостоятельной работе с презентацией Microsoft Office Power Point; при выполнении индивидуальных презентаций и тестов; при самооценке.
Приемы обучения: Постановка проблемных вопросов; обращение к наглядным и компьютерным средствам обучения; выполнение исследовательских заданий.
Ожидаемый результат: Усвоение студентами группы материала практического занятия, выработка умения применения полученных знаний в жизненных ситуациях.
Приобретаемые навыки обучающихся:
-навыки самостоятельной работы с учебным материалом,
-навыки работы с ПК, электронной презентацией,
-навыки самообразования,
-навыки устной и письменной речи,
- навыки самоконтроля,
-навыки самоанализа учебной деятельности;
· Оценка, приобретенных знаний:
Общая успеваемость 100 %
Качественная успеваемость >80%
Оснащение: компьютер, интерактивная доска с мультимедийным проектором;
презентация урока «Классы неорганических соединений»; Периодическая система химических элементов Д.И.Менделеева, методические указания для студентов, тестовые задания.
Междисциплинарные связи:
Учебные дисциплины: Неорганическая химия, органическая химия, математика, физика, основы патологии, анатомия и физиология человека .
Домашнее задание
Выполнить задания.
Учебно-методическая структура практического занятия
|
Деятельность преподавателя |
Деятельность студентов |
Методическое обоснование |
|
I. Организационный этап – 1 мин. |
||
|
1.Преподаватель приветствует студентов 2.Обращает внимание на внешний вид, готовность аудитории к занятию 3.Отмечает отсутствующих студентов |
1.Приветствуют преподавателя 2.Дежурный докладывает об отсутствующих студентах |
-Воспитание организованности, дисциплинированности -Осуществление психологического настроя к учебной деятельности, делового подхода - Активизация внимания, организация студентов к работе |
|
II. Мотивация занятия с использованием поставленного проблемного вопроса – 2 мин. |
||
|
1.Знакомит с темой занятия, его целями, задачами, планом 2.Подчеркивает актуальность темы.
|
1.Внимательно слушают преподавателя 2.Продумывают ход этапов учебной деятельности 3.Оценивают значимость данной темы в будущей профессии фармацевта
|
-Создание целостного представления о практическом занятии -Концентрация внимания студентов на предстоящей работе -Формирование интереса и развитие осмысленной мотивации учебной деятельности |
|
III. Закрепление и обобщение теоретического материала через повторение и актуализацию опорных знаний с помощью компьютерного тестирования – 16мин. |
||
|
1. Проводит для актуализации знаний тестовый контроль по данной теме «Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3» с использованием информационных технологий гипер – теста, после выполнения программа автоматически выставляет оценку (Приложение 1), -Предлагает выставить себе оценку в путеводитель (Приложение 2)
|
1.Внимательно слушают
2.Отвечают на тесты на компьютерах
3.Выставляют оценку в путеводитель |
- Закрепление полученных знаний на теоретическом занятии, более прочное усвоение - Тренировка памяти - Формирование логики суждений - Повышение интереса к предмету, оптимизация и актуализация знаний состава и свойств элементов и их соединений - Организует повторение ранее изученного материала (межпредметная и внутрипредметная связь) |
|
IV. Практическая часть – 40 мин. |
||
|
1. Систематизирует знания в качестве закрепления презентации Microsoft Office Power Point по теме «Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3»
2. Фронтальный опрос студентов по мультимедийной презентации (Приложение 3) • Предлагает выставить себе оценку в путеводитель за самостоятельную работу 3. Выполняется самостоятельные задания различных форм. 4.Помогает и контролирует работу 5.Контролирует и корректирует деятельность студентов
|
1.Внимательно слушают преподавателя. 2.После проверки просмотра мультимедийного пособия формулируют вывод 3. Внимательно слушают преподавателя
4. Ориентироваться в различных классах неорганической химии. 5.Отвечают на вопросы 6.Ведут записи в рабочих тетрадях с выполнением заданий предлагаемых методических рекомендаций для студентов.
|
- Осмысление материала студентами -Формирование познавательных интересов, концентрация внимания на закрепляемой теме -Развитие самостоятельности
- Повышение интереса к предмету, оптимизация и актуализация знаний общей и неорганической химии |
|
1. Организует самостоятельную работу студентов с использованием методических рекомендаций для студентов практического занятия по аналитической химии. При выполнении практической манипуляции. 2.Помогает и контролирует работу студентов при выполнении практической работы (Приложение 4) 3. Фронтальный опрос студентов по методическим рекомендациям выполненных заданий |
1. Внимательно слушают преподавателя 2.Самостоятельно работают с методическими рекомендациями, приготавливая стандартный раствор К2Сr2О7. Определение точной концентрации раствора Na2S2O3 3. Используя лекции и учебник делают записи в рабочих тетрадях 4. При необходимости обращаются за помощью к преподавателю 5. Отвечают на вопросы
|
- Осмысление материала студентами -Формирование познавательных интересов, концентрация внимания на изучаемой теме -Развитие самостоятельности
- оптимизация и актуализация знаний - Выработка навыков работы с учебной литературой - Закрепление изученного материала |
|
Физкультминутка – 1мин |
||
|
1.Организация проведения физкультминутки на занятии при длительной работе с компьютерными технологиями, с целью профилактики усталости глаз (Приложение 5) |
1.Проведение физкультминутки одним из студентов 2.Выполнение упражнений
|
- Профилактика усталости глаз, смена деятельности -Развитие самостоятельности
|
|
V. Закрепление изучаемого практического материала 20 мин. |
||
|
1.В качестве самостоятельной работы организует проверку мультимедийного пособия по теме ««Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3» в программе Microsoft Office Power; Проверяет и оценивает самостоятельную работу студента
|
1.Показывают презентацию 2.Отвечают на вопросы 3.При необходимости дополняют, исправляют друг друга 4.Выставляют оценку в путеводитель по уроку |
-Определение степени усвоения изученного материала -Развитие логического мышления, внимания, памяти -Формирование интереса к предмету |
|
2.Предлагает фронтально решить кроссворд с использованием компьютерных технологий по теме «» 3.Организует деятельность Выполнение химических реакций с целью доказательства химических свойств кислот и солей, в том числе лекарственных учащихся по применению полученных знаний. · Предлагает выставить оценку в путеводитель |
1.Отвечают на вопросы кроссворда 2.Осуществляют деятельность по применению полученных знаний. 3.Записывают ответы в тетрадь, с использованием интерактивной доски 4.При необходимости дополняют, исправляют друг друга 5.Выставляют оценку в путеводитель по уроку |
-Техника запоминания и длительного хранения в памяти -Определение степени усвоения изученного материала -Развитие логического мышления, внимания, памяти
|
|
1.Предлагает решить ситуационные задачи, малыми группами по 2 человека (Приложение 6) · Предлагает выставить оценку в путеводитель |
1.Отвечают на ситуационные задачи 2.Выставляют оценку в путеводитель по уроку
|
-Определение степени усвоения изученного материала -Развитие логического мышления, внимания, памяти -Формирование интереса к предмету и профессии фармацевта |
|
VI. Рефлексия – 7 мин |
||
|
1.Предлагает выставить оценку в путеводитель по уроку 2.Контролирует, координирует и корректирует деятельность студентов 3.Заслушивают индивидуальное сообщение (домашнее задание) на тему: интересные факты «Химия вокруг нас» (Приложение 7)
4.Организует деятельность учащихся по самооценке своей работы
|
1. Выставляют оценки в путеводитель по уроку
2.Ведут записи в тетради.
3.Организует деятельность учащихся по самооценке своей работы
4.Благодарность учащимся за хорошую работу на уроке (по необходимости). |
- Развитие логического мышления, внимания, памяти - Формирование интереса к предмету -Стимулирование познавательной деятельности студентов и интереса к самостоятельному освоению - Организует деятельность учащихся по самооценке своей работы - Благодарность учащимся за хорошую работу на уроке (по необходимости). |
|
VII. Подведение итогов – 5 мин. |
||
|
1.Анализирует работу студентов в целом 2. Аргументация выставленных отметок. Замечания по занятию, предложения о возможных позитивных изменениях на последующих уроках. 3.Намечает перспективы на следующее занятие |
1.Слушают, анализируют слова преподавателя
2.Делают для себя выводы о сформированных компетенциях на занятии |
-Развитие умения аналитической деятельности -Формирование самооценки и самоконтроля |
|
VIII. Домашнее задание – 1 мин. |
||
|
1.Предлагает записать особенности домашнего задания.
|
1.Записывают домашнее задание |
-Стимулирование познавательной деятельности студентов и интереса к самостоятельному освоению - Выработка навыков работы с учебной литературой - Закрепление изученного материала |
Приложение 1
Тестовый входной контроль для актуализации знаний по аналитической химии «Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3»
1.Метенамин в лекарственных формах определяют методом:
А) Алкалиметрии.
Б) Ацидиметрии (прямое титрование). (+)
В) Ацидиметрии (обратное титрование).
Г) Йодометрии.
2.В результате взаимодействия глюкозы с реактивом Фелинга при нагревании образуется:
А) Красное окрашивание.
Б) Осадок кирпично-красного цвета. (+)
В) Осадок белого цвета.
Г) Сине-фиолетовое окрашивание.
3.Фармакопейный метод количественного определения натрия цитрата для инъекций:
А) Метод комплексонометрии.
Б) Метод ионнообменной хроматографии. (+)
В) Метод алкалиметрии.
Г) Метод рефрактометрии.
4.Фармакопейный метод количественного определения натрия гидроцитрата для инъекций:
А) Ацидиметрия.
Б) Аргентометрия.
В)Алкалиметрия. (+)
Г) Йодометрия.
5. Химические свойства, которые лежат в основе количественного определения бензойной кислоты:
А) Восстановительные.
Б) Окислительные.
В) Кислотные. (+)
Г) Способность вступать в реакцию замещения на галогены.
6.Фармакопейный метод количественного определения эфедрина гидрохлорида:
А) Перманганатометрия.
Б) Алкалиметрия.
В) Ацидиметрия в неводной среде. (+)
Г) Броматометрия.
7. Рабочий раствор в иодометрии
А) тиосульфат натрия +
Б) серная кислота
В) метиолранж
Г) крахмал
8. Индикатор в иодометрии
А) фенолфталеин
Б) крахмал +
В) метиловый оранжевый
Г) иод
9. Метод применяется
А) анализ лекарственных препоратов +
Б) концентрация растворов
В) обнаружение катионов
Г) обнаружение анаионов
10. Химические свойства, которые лежат в основе количественного определения ацетилсалициловой кислоты методом алкалиметрии:
А)Восстановительные.
Б) Окислительные
В)Кислотные. (+)
Г)Способность вступать в реакцию замещения на галогены.
Приложение 2
Путеводитель практического занятия:
««Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3»
ФИО студента ____________________________________________________
|
Этап урока |
Цели этапа |
Самооценка |
Оценка преподавателя |
Примечание |
|
|
Закрепление и обобщение теоретического материала через повторение, и актуализацию опорных знаний с помощью компьютерного тестирования |
|||||
|
1. Входной контроль теста «Количественный анализ в аналитической химии»
|
· Формирование логики суждений · Актуализация опорных знаний и подготовка воспроизведения теоретического материала на занятии |
|
|
Тестовые задания |
|
|
2.Фронтальный опрос студентов по мультимедийной презентации |
Формулируют знания основных классов неорганической химии |
|
|
|
|
|
Практическая часть |
|||||
|
1. Работа студентов по методическим рекомендациям для студентов практического занятия по аналитической химии Фронтальный опрос |
Выполняют задания для студентов по рекомендациям · Развитие логического мышления, внимания, памяти · Формирование интереса к предмету Формирование самооценки и самоконтроля |
|
|
1.Практическая часть 2. Выполняют задания в тетрадях |
|
|
Закрепление материала |
|||||
|
Проверка самостоятельной работы мультимедийной презентации Microsoft Office Power Point Фронтальный опрос
Кроссворд по теме |
· Формирование логики суждений · Повышение интереса к предмету · Актуализация опорных знаний и подготовка воспроизведения теоретического материала на занятии · Определение степени усвоения изученного материала Развитие логического мышления, внимания, памяти |
|
|
Кроссворд |
|
|
Ситуационные задачи |
Определение степени усвоения материла по теме ««Приготовление стандартного раствора К2Сr2О7. Определение точной концентрации раствора Na2S2O3» |
|
|
Задачи |
|
|
Итоговая оценка |
· |
|
|
|
|
Приложение 3
Фронтальные вопросы для студентов по мультимедийной презентации по аналитической химии «Количественный анализ по йодометрии»
1 В какой среде проводят титрование?
2 Восстановили титруют каким методом?
3 Почему титрование нельзя проводить в щелочной среде?
4 Формула для определения концентрации вещества в растворе?
5 Малярная масса эквивалента дихромата калия?
6 Формула для нахождения массы навески?
Приложение 4
Методическая рекомендация для студентов при выполнении практической работы ОП.10 Аналитической химии
Приготовление стандартного раствора К2Сr2О7.
Определение точной концентрации раствора Na2S2O3.
Задание. Приготовить 100 мл 0,1 М раствора К2Сr2О7. Определить точную концентрацию Na2S2O3.
Алгоритм выполнения.
I. Приготовить 100 мл 0,1 М раствора К2Сr2О7
1) Рассчитать массу навески для приготовления 100 мл 0,1 М р-ра К2Сr2О7
2) Взвесить на ручных весах рассчитанную навеску (0,49г).
3) Взвесить на аналитических весах сухое часовое стекло, затем часовое стекло с навеской.
4) Высчитать массу навески с точностью до 4-го знака после запятой.
5) Навеску К2Сr2О7 перенести количественно в мерную колбу с помощью сухой воронки, смыть остатки с воронки и часового стекла горячей очищенной водой, налить воды две трети колбы, растворить соль, перемешивая круговыми движениями. Охладить до комнатной температуры, осторожно довести объем до метки с помощью пипетки.
6) Рассчитать титр К2Сr2О7, практическую молярную концентрацию р-ра К2Сr2О7, поправочный коэффициент.
Дано: V=100 мл, См К2Сr2О7 =0,1М, Мr К2Сr2О7=294,19 г, УЧ К2Сr2О7=1/6,
-------------------------------
ат - ? апр- ? Тпракт-? Тт-? См практ.-? Кп -?
------------------------------
Решение.
а) Метод оксидиметрия, метод йодометрия, способ титрования по заместителю.
б) К2Сr2О7 + 6КI + 7H2SO4--- 3I2+ Cr2(SO4)3 +7H2O+4К2SO4 УЧ К2Сr2О7=1/6
I2 +2 Na2S2O3 = 2NaI + Na2S4O6 УЧ I2=1/2, f=1
в) индикатор: крахмал, переход окраски из белого до синего.
г) установочное в-во: К2Сr2О7, рабочий р-р или титрант: Na2S2O3.
Ттеор=Мr *См*УЧ / 1000, атеор=Т* V,
Тпракт=апр/ V, См практ К2Сr2О7.=Тпракт*1000/М r *УЧ
Кп=апр/ атеор Кп= Тпр/Ттеор
Кп=Смпр/ Смтеор
II. Определить точную концентрацию Na2S2O3 по установочному веществу
Порядок титрования
7) Отмерить пипеткой аликвотную часть 1мл приготовленного р-ра К2Сr2О7 и перенести в колбу для титрования.
8) Добавить мерной пробиркой 5 мл КI (5%), затем добавить мерной пробиркой 1,5-2мл H2SO4. дать постоять 5 мин. в темном месте (до появления бурого цвета). После добавить 3-4мл воды очищенной (всего объем полученного раствора 8-9мл).
9) Титровать 0,1М раствором Na2S2O3 до появления бледно-желтого с зеленым оттенком р-ра, при этом записывают объем пошедший на титрование (V1) . После добавить2-3 капли крахмала и продолжать титровать до перехода окраски от темно-синего (черного или фиолетового) до светло сине-зеленого (голубого) (V2).
10) Рассчитать титр Na2S2O3, практическую молярную концентрацию р-ра Na2S2O3, поправочный коэффициент.
Дано: V Na2S2O3 1=--- мл, V Na2S2O3 2=--- мл, V ср= V Na2S2O3 1 + V Na2S2O3 2 = мл,
См К2Сr2О7=______М, V К2Сr2О7.= 1 мл, См теор Na2S2O3 =0,1М, Мr Na2S2O3 *5Н2О=248,2
-------------------------------------------
Тпракт Na2S2O3 -? См практ Na2S2O3 -? Кп -?
------------------------------------------
Решение.
См1 · V1 = См2 · V2, См Na2S2O3 = V К2Сr2О7* См К2Сr2О7/ V Na2S2O3 ,
Тпр NaOH = См · Э /1000 ТтеорNa2S2O3=См Na2S2O3·Мr Na2S2O3.УЧ Na2S2O3 /1000
Кп=Смпр Na2S2O3 / Смтеор Na2S2O3 Кп=ТпрNa2S2O3/Ттеор Na2S2O3
Домашнее задание:
Выполнить задания
1.Методом электронного баланса составьте уравнения окислительно-восстановительных реакций, которые протекают по схемам:
а) H2S + K2Cr2O7 + H2SO4 → S + Cr2(SO4)3 + K2SO4 + H2O;
б) C + HNO3 → CO2 + NO + H2O;
в) NaI + NaIO3 + H2SO4 → I2 + Na2SO4 + H2O;
г) Mg + HNO3 → Mg(NO3)2 + N2O + H2O.
Индивидуальный подход с целью повышения разития.
2.Двое учеников получают задание записать уравнение реакции между перманганатом калия и пероксидом водорода в кислой среде:
2KMnO4 + H2O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 4H2O + 8O2;
6KMnO4 + H2O2 + 9H2SO4 = 3K2SO4 + 6MnSO4 + 10H2O + 8O2.
Приложение 5
Физкультминутка. Комплексы упражнений для глаз.
Упражнения выполняются сидя или стоя, отвернувшись от экрана, при ритмичном дыхании, с максимальной амплитудой движения глаз.
1. Закрыть глаза, сильно напрягая глазные мышцы, на счёт 1-4, затем раскрыть глаза, расслабив мышцы глаз, посмотреть вдаль на счёт 1-6. Повторить 4-5 раз.
2. Не поворачивая головы, посмотреть направо и зафиксировать взгляд на счёт 1-4, затем посмотреть вдаль прямо на счет 1-6. Аналогичным образом проводятся упражнения, но с фиксацией взгляда влево, вверх и вниз. Повторить 3-4 раза.
3. Перенести взгляд быстро по диагонали: направо вверх, налево вниз, потом прямо вдаль на счет 1-6; затем налево вверх, направо вниз и посмотреть вдаль на счет 1-6. Повторить 4-5 раз.
Кроссворд
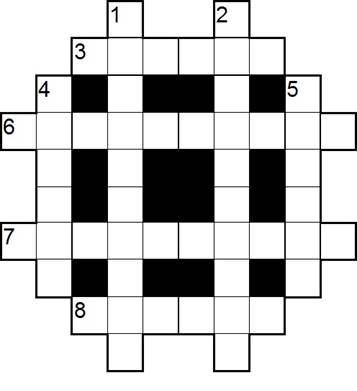
Вопросы:
По горизонтали: 3. Химический элемент с атомным номером 41, обозначается символом Nb, блестящий металл серебристо-серого цвета.
6. Окислительно-восстановительный метод титрования в основе лежит рабочий раствор йода, тиосульфат натрия.
7. Переход или перевод поверхности металла в неактивное, пассивное состояние путём образования на поверхности тонкого защитного слоя.
8. Рабочим раствором является раствор йода, какой способ титрования .
![]()
![]()
![]() По вертикали: 1. Анион, соль
или эфир пирофосфорной кислоты. 2. Переход окраски
при титровании бурый. Соломенно-желтый+крахмал синий
?
По вертикали: 1. Анион, соль
или эфир пирофосфорной кислоты. 2. Переход окраски
при титровании бурый. Соломенно-желтый+крахмал синий
?
4. Эфир карбаминовой кислоты и её производных.
5. При определении окислителей раствор крахмала добавляют в конце титрования при этом раствор приобретает какую окраску.
Ответы: По горизонтали: 3. Ниобий. 6. Йодометрия. 7. Пассивация. 8. Прямой.
По вертикали: 1. Пирофосфат. 2. Бесцветный. 4. Уретан. 5. Жёлтая.
Приложение 6
Решить задачи
Задача№1
Раствор объемом 500 мл содержит NaOH массой 5 г. Определить молярную концентрацию этого раствора.
Задача№2
Вычислить массу хлорида натрия, содержащегося в растворе объемом 200 мл, если его молярная концентрация 2 моль/л.
Задача№3
Какую навеску гидроксида натрия необходимо взять для приготовления 200 мл 0,1 н. раствора?
Задача №4
Какие массы йода и спирта необходимы для приготовления 300 г раствора с массовой долей йода 5%?
Задача №5
Какие массы воды и нитрата аммония необходимо взять для приготовления 3 л раствора с массовой долей NH4NO3 8%? Плотность раствора 1,06 г/мл.
Задача №6
Какую массу серной кислоты надо взять для приготовления раствора объемом 2,5 л, если C(H2SO4) = 0,1 моль/л?
Скачано с www.znanio.ru
© ООО «Знанио»
С вами с 2009 года.
![]()

