
|
Рассмотрено и утверждено на заседании ЦМК «Общих гуманитарных, социально-экономических, математических и естественнонаучных дисциплин» Протокол № ________от «____»______________2025___г. Председатель ЦМК Мутыгуллина М.Б.._______
|
Составлено в соответствии с Федеральными требованиями к минимуму содержания и уровню подготовки выпускников по специальности 31.02.01. Лечебное дело Зав. отделом по УР «____»____________2025___ г. ________________Е.С. Кузьмина
|
|
Методист ------------------- Богданова А.Д. «--- »---------2025г. |
Составитель:
Серикова Т.Н. – преподаватель первой квалификационной категории ГБПОУ ТМедК «Тольяттинский медицинский колледж»
Содержание.
|
№п\п |
Наименование |
Стр. |
|
1 |
Пояснительная записка |
3-7 |
|
2 |
I.Материал лекции №1. |
8 |
|
3 |
Тема 1.1 Предмет органической химии. Теория химического строения органических веществ А.М. Бутлерова. (Теоретическое занятие). |
8-10 |
|
4 |
1.2. Значение органической химии. |
11 |
|
5 |
1.3. Основы теории строения |
12 |
|
6 |
1.4.. Основные положения теории химического строения А.М.Бутлерова |
12 |
|
7 |
1.5. Формулы строения органических веществ. |
13 |
|
8 |
II. Контрольные вопросы. (с эталонами ответов) |
13-14 |
|
9 |
III .Материал лекции №2. |
14 |
|
10 |
3.1 Изомерия органических соединений. Природа связей в молекулах. |
15-19. |
|
11 |
3.2.Рабочая тетрадь для практических работ по химии .для студентов 1 курса, (2семестр) Практическое занятие №1. |
20-24 |
|
12 |
3.3. Практические задания с эталонами ответов. |
25-35 |
|
13 |
IV. Задания для самостоятельная работа. |
21 |
|
14 |
Рекомендуемая литература. |
38-39 |
|
15 |
Приложение 1. Органические вещества и медицина |
40-41 |
|
16 |
Приложение 2. Сравнение органических и неорганических соединений. |
42 |
|
17 |
Приложение 3 Гомологический ряд алканов. |
43 |
|
18 |
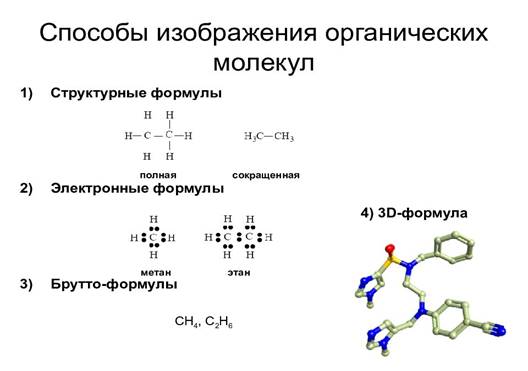
Приложение 4 Способы изображения органических молекул. |
44 |
Пояснительная записка.
Учебно методическое пособие разработано в соответствии с ФГОС СПО по дисциплине ОУД 12. «Химия» и предназначено для преподавателей и студентов I курса специальности 31.02.01 « Лечебное дело».
В соответствии с тематическим планом дисциплины учебно методическое пособие рассчитано на 6 часов, из них четыре часа теоретических занятий и два часа практических занятий.
Основной учебной целью предлагаемого пособия является формирование прочных знаний по органической химии. Одновременно продолжается развитие умений самостоятельно работать с литературой, систематически заниматься решением задач, работать с тестами различных типов. Полученные знания закрепляются серией упражнений, задач, тестов.
В процессе освоения данных тем и в рамках федерального компонента государственного образовательного стандарта среднего полного общего образования в пределах ОПОП СПО по естественнонаучному профилю: студенты должны овладеть формированием личностных, метапредметных и предметных результатов
Личностные результаты освоения химии в СПО включают:
Ø чувство гордости и уважения к истории и достижениям отечественной химической науки;
Ø химически грамотное поведение в профессиональной деятельности и в быту при обращении с химическими веществами, материалами и процессами;
Ø готовность к продолжению образования и повышения квалификации в избранной профессиональной деятельности и объективное осознание роли химических компетенций в этом;
Ø умение использовать достижения современной химической науки и химических технологий для повышения собственного интеллектуального развития в выбранной профессиональной деятельности.
Метапредметные результаты освоения химии в СПО включают:
Ø использование различных видов познавательной деятельности и основных интеллектуальных операций (постановки задачи, формулирования гипотез, анализа и синтеза, сравнения, обобщения, систематизации, выявления причинно-следственных связей, поиска аналогов, формулирования выводов) для решения поставленной задачи;
Ø применение основных методов познания (наблюдения, научного эксперимента) для изучения различных сторон химических объектов и процессов, с которыми возникает необходимость сталкиваться в профессиональной сфере;
Ø использование различных источников для получения химической информации, умение оценить её достоверность для достижения хороших результатов в профессиональной сфере.
Предметные результаты освоения химии в СПО включают:
Ø сформированность представлений о месте химии в современной научной картине мира; понимание роли химии в формировании кругозора и функциональной грамотности человека для решения практических задач;
Ø владение основополагающими химическими понятиями, теориями, законами и закономерностями; уверенное пользование химической терминологией и символикой;
Ø владение основными методами научного познания, используемыми в химии: наблюдением, описанием, измерением, экспериментом;
Ø умение обрабатывать, объяснять результаты проведённых опытов и делать выводы; готовность и способность применять методы познания при решении практических задач;
Ø сформированность умения давать количественные оценки и производить расчёты по химическим формулам и уравнениям;
Ø владение правилами техники безопасности при использовании химических веществ;
Ø сформированность собственной позиции по отношению к химической информации, получаемой из разных источников.
В процессе освоения дисциплины у студентов должны формироваться и общие компетенции (ОК) в рамках федерального компонента государственного образовательного стандарта среднего полного общего образования в пределах ОПОП СПО по естественнонаучному профилю:
Ø ОК -1 - Понимать сущность и социальную значимость своей будущей профессии, проявлять к ней устойчивый интерес.
Ø ОК 2 – организовывать собственную деятельность, выбирать типовые методы и способы выполнения профессиональных задач, оценивать их выполнение и качество;
Ø ОК 3 – принимать решения в стандартных и нестандартных ситуациях и нести за них ответственность;
Ø ОК 4 – осуществлять поиск и использование информации, необходимой для эффективного выполнения профессиональных задач, профессионального и личностного развития;
Ø ОК 5 – использовать информационно – коммуникационные технологии в профессиональной деятельности;
Ø ОК 6 – работать в коллективе и команде, эффективно общаться с коллегами, руководством, потребителями;
Ø ОК 7 – брать на себя ответственность за работы членов команды (подчинённых), за результат выполнения заданий;
Ø ОК 8 – самостоятельно определять задачи профессионального и личностного развития, заниматься самообразованием, осознанно планировать и осуществлять повышение квалификации;
Задачи учебно методического пособия:
образовательные:
Изучив раздел студент должен:
Знать:
Ø важнейшие химические понятия: пространственное строение молекул, углеродный скелет, функциональная группа, гомология, структурная и пространственная изомерия, индуктивный и мезомерный эффекты, электрофил, нуклеофил, основные типы реакций в органической химии;
Ø основные теории химии; строения органических соединений;
Ø классификацию и номенклатуру органических соединений.
Уметь:
Ø определять: изомеры и гомологи, принадлежность веществ к разным классам органических соединений; характер взаимного влияния атомов в молекулах, типы реакций в органической химии;
Ø объяснять: зависимость реакционной способности органических соединений от строения их молекул.
развивающие:
продолжить развитие исследовательской компетентности студентов:
Ø через поиск необходимой информации в учебной, дополнительной литературе, Интернете;
Ø развивать умение работать со схемами, рисунками, слайдами презентации;
Ø развивать умение сравнивать (на примере сравнения различных классов углеводородов);
Ø умение анализировать (умения выдвигать гипотезу на основе мысленного эксперимента для ответа на вопросы проблемного характера);
Ø развивать творческие способности студентов с помощью самостоятельной работы по переносу полученных знаний и умений в новую ситуацию;
воспитательные:
Ø развивать коммуникативные способности студентов при работе в парах, в группе;
Ø воспитывать культуру умственного труда - развивать внутреннюю мыслительную активность и самостоятельность;
Целью и основными задачами организации и осуществления самостоятельной работы студентов является:
Ø систематизация и закрепление полученных теоретических знаний и практических умений;
Ø углубление и расширение теоретических знаний;
Ø формирование общих компетенций;
Ø формирование умений использовать специальную и дополнительную литературу, периодическую печать;
Ø развитие познавательных способностей и активности обучающихся;
Ø формирование самостоятельности мышления;
Ø развитие исследовательских умений.
межпредметные:
Ø использование различных видов познавательной деятельности и основных интеллектуальных операций (постановки задачи, формулирования гипотез, анализа и синтеза, сравнения, обобщения, систематизации, выявления причинно-следственных связей, поиска аналогов, формулирования выводов) для решения поставленной задачи, применение основных методов познания (наблюдения, научного эксперимента) для изучения различных сторон химических объектов и процессов, с которыми возникает необходимость сталкиваться в профессиональной сфере;
Ø
![]() использование различных источников для получения
химической информации, умение оценить ее достоверность для достижения хороших
результатов в профессиональной сфере;
использование различных источников для получения
химической информации, умение оценить ее достоверность для достижения хороших
результатов в профессиональной сфере;
предметные:
Ø сформированность представлений о месте химии в современной научной картине мира; понимание роли химии в формировании кругозора и функциональной грамотности человека для решения практических задач;
Ø владение основополагающими химическими понятиями, теориями, законами и закономерностями; уверенное пользование химической терминологией и символикой;
Ø владение основными методами научного познания, используемыми в химии: наблюдением, описанием, измерением, экспериментом; умение обрабатывать, объяснять результаты проведенных опытов и делать выводы; готовность и способность применять методы познания при решении практических задач;
Ø сформированность умения давать количественные оценки и производить расчеты по химическим формулам и уравнениям;
Ø владение правилами техники безопасности при использовании химических веществ;
Ø сформированность собственной позиции по отношению к химической информации, получаемой из разных источников.
В учебно методическое пособие раздела входят следующие материалы: лекционный материал теоретических занятий, практическая работа по данной теме, задания с эталонами ответов, тестовые задания, разно уровневые задания.
Оборудование и наглядные пособия: компьютер, экран, мультимедийный проектор, комплекты опорных конспектов, презентация «Теория А.М.Бутлерова».
http://www.yandex.ru/clck/jsredir?
I.Материал лекции №1.
Тема 1.1 Предмет органической химии. Теория химического строения органических веществ А.М. Бутлерова. (Теоретическое занятие).
1.Органическая химия - это раздел химической науки, в котором изучаются соединения углeрода - их строение, свойства, способы получения и практического использования. Соединения, в состав которых входит углерод, называются органическими.
Кроме углерода, они почти всегда содержат водород, довольно часто - кислород, азот и галогены, реже - фосфор, серу и другие элементы. Однако сам углерод и некоторые простейшие его соединения, такие как оксид углерода (II), оксид углерода (IV), угольная кислота, карбонаты, карбиды и т.п., по характеру свойств относятся к неорганическим соединениям. Поэтому часто используется и другое определение:
Органические соединения - это углеводороды (соединения углерода с водородом) и их производные.
Благодаря особым свойствам элемента углерода, органические соединения очень многочисленны. Ученым известно более 18 млн. органических веществ, в то время как неорганических около 100 тыс. Многообразие органических соединений объясняется способностью атомов углерода образовывать цепи, прямые и разветвленные, а также замкнутые циклы. Кроме того, они могут образовывать между собой двойные и тройные связи.
Органическая химия - химия углеводородов и их производных, то есть продуктов, образующихся при замене атомов водорода другими атомами или группами атомов.
Формулы в органической химии.
|
C3H |
||
|
Пол полная структурная - |
|
||
|
Сок сокращенная структурная – |
СН3 СН3 - СН2 - СН3 |
Сейчас известно свыше 10 миллионов синтетических и природных органических веществ, и их число постоянно возрастает.
Углерод
Символ. С, элемент IVA группы 2-го периода Периодической системы элементов); порядковый номер 6; атомная масса 12,01115.
Электронная конфигурация в основном состоянии 1s22s22p2.
Углерод - особый элемент. Ни один другой химический элемент не способен
образовывать такое многообразие соединений. Причина этого многообразия в том, что атомы углерода способны:
1) соединяться друг с другом в цепи различного строения: открытые (неразветвленные, разветвленные), замкнутые:
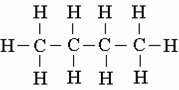
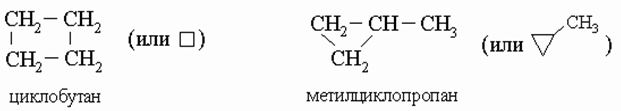
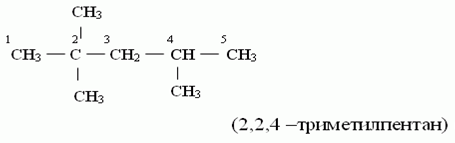
2) образовывать не только простые (одинарные), но и кратные (двойные, тройные) связи:
3) образовывать прочные связи почти с любым другим элементом.
Эти уникальные свойства углерода объясняются сочетанием двух факторов:
Ø наличие на внешнем энергетическом уровне (2s и 2p) четырех электронов (поэтому атом углерода не склонен ни терять, ни приобретать свободные электроны с образованием ионов);
Ø малый размер атома (в сравнении с другими элементами IV группы).
Вследствие этого углерод образует главным образом ковалентные, а не ионные связи, и проявляет валентность, равную 4.
Органические соединения.
Критерием деления соединений на органические и неорганические служит
их элементный состав.
К органическим соединениям относятся химические вещества, содержащие в своем составе углерод, например.
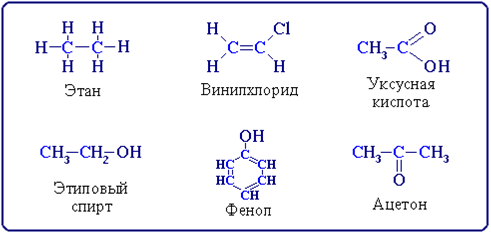
Органические соединения отличаются от неорганических рядом характерных особенностей:
Ø почти все органические вещества горят или легко разрушаются при нагревании с окислителями, выделяя СО2 (по этому признаку можно установить принадлежность исследуемого вещества к органическим соединениям);
Ø в молекулах органических соединений углерод может быть соединен почти с любым элементом Периодической системы;
Ø органические молекулы могут содержать последовательность атомов углерода, соединенных в цепи (открытые или замкнутые);
Ø молекулы большинства органических соединений не диссоциирует на достаточно устойчивые ионы;
Ø реакции органических соединений протекают значительно медленнее и в большинстве случаев не доходят до конца;
Ø среди органических соединений широко распространено явление изомерии ;
Ø органические вещества имеют более низкие температуры фазовых переходов (т.кип., т.пл.).
1.2.Значение органической химии.
Органическая химия имеет исключительно важное познавательное и народно хозяйственное значение.
Природные органические вещества и их превращения лежат в основе явлений Жизни. Поэтому органическая химия является химическим фундаментом биологической химии и молекулярной биологии - наук, изучающих процессы, происходящие в клетках организмов на молекулярном уровне. Исследования в этой области позволяют глубже понять суть явлений живой природы. Множество синтетических органических соединений производится промышленностью для использования в самых разных отраслях человеческой
деятельности.
Это - нефтепродукты, горючее для различных двигателей, полимерные материалы (каучуки, пластмассы, волокна, пленки, лаки, клеи и т.д.), поверхностно-активные вещества, красители, средства защиты растений, лекарственные препараты, вкусовые и парфюмерные вещества и т.п. Без знания основ органической химии современный человек не способен экологически грамотно использовать все эти продукты цивилизации.
Сырьевыми источниками органических соединений служат: нефть и природный газ, каменный и бурый угли, горючие сланцы, торф, продукты сельского и лесного хозяйства.
1.3. Основы теории строения.
Основой современной органической химии является ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ, созданная на базе теории химического строения А.М. Бутлерова и электронных (квантовохимических) представлений о строении атома и природе химической связи.
Современная теория строения позволяет предсказывать основные химические и
физические свойства органических соединений, исходя из их химического, пространственного и электронного строения. Теория строения играет ключевую роль в изучении и систематизации огромного фактического материала органической химии.
1.4. Основные положения теории химического строения А. М .Бутлерова.
1. Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения).
2. Химическое строение можно устанавливать химическими методами. (В настоящее время используются также современные физические методы).
3. Свойства веществ зависят от их химического строения.
4. По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства.
5. Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга.
Теория Бутлерова явилась научным фундаментом органической химии и способствовала быстрому ее развитию. Опираясь на положения теории, А.М. Бутлеров дал объяснение явлению изомерии, предсказал существование различных изомеров и впервые получил некоторые из них.
1.5. Формулы строения
Формула строения (структурная формула) описывает порядок соединения атомов в молекуле, т.е. ее химическое строение. Химические связи в структурной формуле изображают черточками. Связь между водородом и другими атомами обычно не указывается.
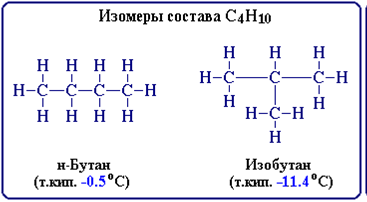
Структурные формулы отличаются от молекулярных (брутто) формул, которые показывают только, какие элементы и в каком соотношении входят в состав вещества (т.е. качественный и количественный элементный состав), но не отражают порядка связывания атомов.
Например, н-бутан и изобутан имеют одну молекулярную формулу C4H10, но разную последовательность связей . Таким образом, различие веществ обусловлено не только разным качественным и количественным элементным составом, но и разным химическим строением, которое можно отразить лишь структурными формулами.
II.Контрольные вопросы (с эталонами ответов)
Для закрепления и осмысления учебного материала попытайтесь ответить на
следующие вопросы:
1.Какие из приведенных соединений относятся к органическим?
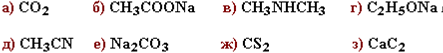
Варианты ответов (выберите правильный):
Ответ а : все приведенные соединения
Ответ б : б, в, г, д
Ответ в : б, в, д, е, ж
Ответ г : все, кроме "е" и "з"
2.Валентность углерода в органических соединениях равна?
А) трем; б) одному; в) четырем; г) двум
3.Чтоотображает молекулярная формула ?
а) последовательность соединения атомов в молекуле
б) последовательность соединения атомов углерода в молекуле
в) пространственное расположение атомов в молекуле
г) состав молекулы ( качественный и количественный)
4.Какие вещества в органической химии называются гомологами ?
а) схожие по строению, имеющие одинаковый качественный состав;
б) одинакового качественного, но разного количественного состава, отличающиеся на одну или несколько ─СН2─ групп и обладающие схожими свойствами;
в) с одинаковым качественным и количественным составом, но разным химическим строением и разными свойствами;
г) различного качественного и количественного состава, но схожего строения
5. Укажите элемент, атомы которого способны соединяться друг с другом в длинные цепи: а) водород; б) азот; в) кислород; г) углерод.
6. Структурная формула показывает:
а) последовательность соединения атомов в молекуле
б) последовательность соединения атомов углерода в молекуле
в) пространственное расположение атомов в молекуле
г) пространственное расположение атомов углерода в молекуле
7. Изомеры – это вещества:
а) схожие по строению, имеющие одинаковый качественный состав, количественно отличающиеся на одну или несколько ─СН2─ групп
б) одинакового качественного, но разного количественного состава, обладающие схожими свойствами
в) с одинаковым качественным и количественным составом, но разным химическим строением и разными свойствами
г) различного качественного и количественного состава, но схожего строения
Эталон ответа:
1.А.
2.В.
3..Г.
4.В.
5.Г.
6.В.
7.Б.
III Лекция №2.
Тема 1.2 Изомерия органических соединений. Природа связей в молекулах. (Теоретическо занятие)
Понятие о изомерии.
Изомеры – вещества, имеющие одинаковый состав молекул, но различное химическое строение и, обладающие поэтому разными свойствами.
1. Изомерия углеродного скелета.
Упражнение: составить формулы пяти изомеров вещества, имеющего состав С6Н14.
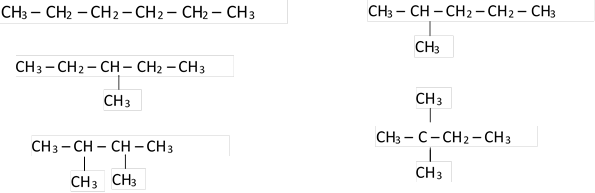
Еще до создания теории строения были известны вещества одинакового элементного состава, но c разными свойствами. Такие вещества были названы изомерами, а само это явление - изомерией.
В основе изомерии, как показал А.М. Бутлеров, лежит различие в строении молекул, состоящих из одинакового набора атомов. Таким образом, · изомерия - это явление существования соединений, имеющих одинаковый качественный и количественный состав, но различное строение и, следовательно, разные свойства.
Например, при содержании в молекуле 4-х атомов углерода и 10-ти атомов водорода возможно существование 2-х изомерных соединений:
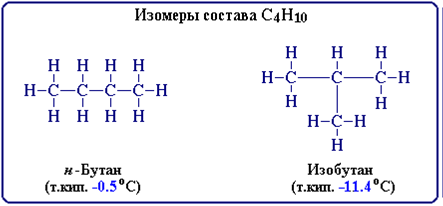
В зависимости от характера отличий в строении изомеров различают структурную и пространственную изомерию.
Структурные изомеры
Структурные изомеры - соединения одинакового качественного и количественного состава, отличающиеся порядком связывания атомов, т.е. химическим строением.
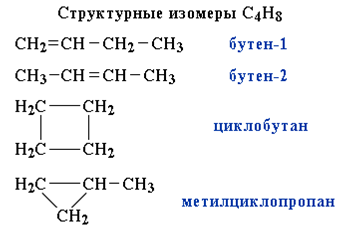
Стереоизомеры.
Пространственные изомеры (стереоизомеры) при одинаковом составе и одинаковом
химическом строении различаются пространственным расположением атомов в молекуле. Пространственными изомерами являются оптические (зеркальные) и цис-транс изомеры
(шарики разного цвета обозначают разные атомы или атомные группы): Молекулы таких изомеров несовместимы в пространстве. Стереоизомерия играет важную роль в органической химии. Подробнее эти вопросы будут рассматриваться при изучении соединений отдельных классов.
Пространственная изомерия.
Пространственные изомеры – это вещества с одинаковым составом и химическим строением, но с разным пространственным расположением атомов в молекуле. Виды пространственной изомерии – геометрическая (цис—транс) и оптическая изомерия.
Геометрическая изомерия (или цис-транс-изомерия).
Геометрическая изомерия характерна для соединений, в которых различается положение заместителей относительно плоскости двойной связи или цикла. Например, для алкенов и циклоалканов.
Двойная связь не имеет свободного вращения вокруг своей оси.
Поэтому заместители у атомов углерода при двойной связи могут быть расположены либо по одну сторону от плоскости двойной связи (цис-изомер), либо по разные стороны от плоскости двойной связи (транс-изомер). При этом никаким вращением нельзя получить из цис-изомера транс-изомер, и наоборот.
Например, бутен-2 существует в виде цис— и транс-изомеров
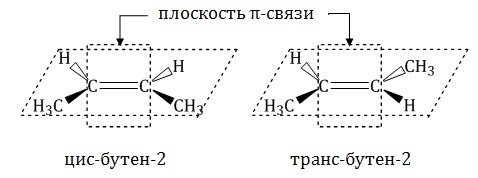
1,2-Диметилпропан также образует цис-транс-изомеры:

Геометрические изомеры различаются по физическим свойствам (температура кипения и плавления, растворимость, дипольный момент и др.). Например, температура кипения цис-бутена-2 составляет 3,73 оС, а транс-бутена-2 0,88оС.
При этом цис—транс-изомерия характерна для соединений, в которых каждый атом углерода при двойной связи С=С (или в цикле) имеет два различных заместителя.
Природа связей в молекулах.
Одна из характеристик химических связей — тип перекрывания
орбиталей атомов в молекуле.
По характеру перекрывания различают σ-(сигма) и π‑(пи)
связи.
|
σ-С вязь — это связь, в которой перекрывание орбиталей происходит вдоль оси, соединяющей ядра атомов. |
σ-Связь может быть образована любыми типами орбиталей (s, p, d, гибридизованными).
σ-Связь — это основная связь в молекуле, которая преимущественно образуется между атомами.
Между двумя атомами возможна только одна σ-связь.
Виды σ-связей
|
|
|
|
|
|
|
|
|
|
π-Связь — это связь, в которой перекрывание орбиталей происходит в плоскости, перпендикулярной оси, соединяющей ядра атомов, сверху и снизу от оси связи. |
π-Связь образуется при перекрывании только р- (или d) орбиталей, перпендикулярных линии связи и параллельных друг другу.
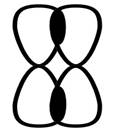
π-Связь является дополнительной к σ-связи, она менее прочная и легче разрывается при химических реакциях.
|
Одинарная связь С–С, С–Н, С–О |
Двойная связь С=С, С=О |
Тройная связь С≡С, С≡N |
|
σ-связь |
σ-связь + π-связь |
σ-связь + две π-связи |
Таким образом, число сигма-связей (σ-связей) в молекуле метана равно четырем:
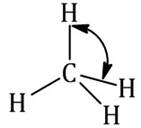
В молекуле этилена число сигма-связей равно пяти, а также есть одна пи-связь (между атомами углерода):
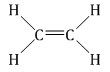
В молекуле ацетилена всего три сигма-связи и две пи-связи:
H–C≡C–H
Рабочая тетрадь для практических работ по химии .для студентов 1 курса, (2семестр)
Практическое занятие №1.
Тема: « Изомерия органических соединений. Природа связей в молекулах».
Цель урока:
Работа с терминами: Дописать определения;
1) Органическая химия -------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
2) углеводороды-------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
3) 1 положение теории А.М.Бутлерова,------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
4) 2 положение теории А.М.Бутлерова ------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
5) 3 положение теории А.М.Бутлерова ---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
6) изомерия ----------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Задание 1.Изготовление моделей молекул органических веществ.
Оборудование:
· деревянные стержни,
· материал для лепки (пластилин),
· набор шаростержневых моделей.
Общие указания.
Для построения моделей используйте детали готовых наборов или пластилин с палочками. Изготовьте шарики, имитирующие атомы углерода, готовят обычно из пластилина темной окраски, шарики, имитирующие атомы водорода, - из светлой окраски, атомы хлора – из зеленого или синего цвета. Для соединения шариков используют палочки (спички, зубочистки). Написав формулу органического соединения, изготовьте его пространственную структуру, используя заранее приготовленные модели атомов и применяя знания о строении молекул предельных углеводородов (угол связи, длина связи, форма молекулы).
Задание 2.
Перечислите основные виды изомерии:
1)…………………………………………………………………………………..
2)…………………………………………………………………………………..
3)………………………………………………………………………..……….
4)…………………………………………………………………………………..
Нарисуйте электронную структуру и валентные состояния атома углерода в органических соединениях.
Атом углерода в невозбужденном состоянии
Атом углерода в возбужденном состоянии
Закончите определение.
Гибридизация - это
………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Нарисуйте атомы углерода в трех валентных состояниях. Укажите виды гибридизации. Какие валентные углы характерны для атомов углерода в данных состояниях?
|
I валентное состояние |
II валентное состояние |
III валентное состояние |
|
….-гибридизация |
….-гибридизация |
….-гибридизация |
|
Валентный угол- ….. |
Валентный угол- ….. |
Валентный угол- ….. |
|
|
|
|
Закончите предложение.
Для неорганических соединений более характерны ионные связи, а для органических - ……………………………………………………………….
Дайте определение данному виду связи.
…………………………………связь - это…………………………………………
………………………………………………………………………………………………………………………………………………………………………………........
Закончите следующие определения.
σ-связь - ……………………………………………………………………
……………………………………………………………………………………………………………………………………………………………………
π-связь - ………………………………………...………………………..…
……………………………………………………………………………………………………………………………………………………………………
Задание 3.
Напишите структурные формулы всех возможных изомеров веществ
пентана, гексана, этана, дихлорметана CH2Cl2, в соответствии с ними сделайте шаровидные модели изомеров на примере бутана и изобутана
 Н Н H H
Н Н H H
| | | |
Н – С – C – C – C – H
| | | |
Н Н H H
Н H H
 | | |
| | |
Н – С – C – C – H
| | |
H | H
H – C – H
|
H
|
|
Условия выполнения задания
1. Место (время) выполнения задания: задание выполняется на занятие в аудиторное время
2. Максимальное время выполнения задания: ____90_______ мин.
3. Вы можете воспользоваться учебником, конспектом лекций
Шкала оценки образовательных достижений:
Критерии оценки: Выполнение работы более 90% –оценка «5»,
70-90% - оценка «4»,
50 -70% - оценка «3»,
Менее 50% - оценка «2».
Оценка-------------------подпись---------------------
IV. Практические задания с эталонами ответов.
Задание №1
Охарактеризуйте научное и практическое значение теории А.М. Бутлерова.
Эталон ответа:
Теория химического строения позволила объяснить многие факты, накопившиеся в органической химии в начале второй половины Х I Х в., доказала, что с помощью химических методов ( синтеза, разложения и других реакций) можно установить порядок соединения атомов в молекулах ( этим самым была доказана возможность познания строения вещества).
Внесла новое в атомно-молекулярное учение ( порядок расположения атомов в молекулах, взаимное влияние атомов, зависимость свойств от строения молекул вещества). Теория рассматривала молекулы вещества как упорядоченную систему, наделенную динамикой взаимодействующих атомов. В связи с этим атомно-молекулярное учение получило свое дальнейшее развитие, что имело большое значение для науки химии.
Дала возможность предвидеть свойства органических соединений на основании строения, синтезировать новые вещества, придерживаясь плана.
Позволила объяснить многообразие органических соединений.
Дала мощный толчок синтезу органических соединений, развитию промышленности органического синтеза ( синтез спиртов, эфиров, красителей, лекарственных веществ и др.).
Советы:
Теория Бутлерова позволила предсказать существование многих соединений, предвидеть их свойства, осуществить их синтез. Она указала путь внутрь строения молекулы.
Задание №2. Изобразите структурные формулы всех изомеров гексана С6Н14.
Эталон ответа:
Гексан (C6H14C6H14) имеет 5 изомеров. Вот их структурные формулы и названия:
1.
н-Гексан (нормальный гексан)
CH3−CH2−CH2−CH2−CH2−CH3CH3−CH2−CH2−CH2−CH2−CH3
2.
2-Метилпентан
CH3−CH2−CH2−CH(CH3)−CH3CH3−CH2−CH2−CH(CH3)−CH3
3.
3-Метилпентан
CH3−CH2−CH(CH3)−CH2−CH3CH3−CH2−CH(CH3)−CH2−CH3
4.
2,3-Диметилбутан
CH3−CH(CH3)−CH(CH3)−CH3CH3−CH(CH3)−CH(CH3)−CH3
5.
2,2-Диметилбутан
CH3−C(CH3)2−CH2−CH3CH3−C(CH3)2−CH2−CH3
Все эти соединения являются насыщенными углеводородами (алканами) и отличаются друг от друга порядком связи атомов углерода, при этом имеют одинаковую молекулярную формулу C6H14C6H14.
Задание №3.
Тест по теме Теория строения органических соединений А.М. Бутлерова.
Вопрос 1
Какой химический элемент в обязательном порядке входит в состав органических веществ?
Варианты ответов
Вопрос 2
Правильно соотнесите событие с годами
1. 1842
2. 1889
3. 1806
4. 1861
Варианты ответов
Эталон ответа:
1—1
2—2
3—3
4-- 4
Вопрос 3
Валентность углерода в органических веществах равна
Варианты ответов
Эталон ответа:
4-- 4
Вопрос 4
Как называется формула, в которой показан порядок связывания атомов между собой?
Варианты ответов
Эталон ответа: 2.
Вопрос 5
Одна из причин многообразия органических веществ.
Варианты ответов
Эталон ответа: 2
Вопрос 6
Какие вещества называют изомерами?
Варианты ответов
Эталон ответа: 1
Вопрос 7
В каком году была сформулирована теория строения органических соединений?
Варианты ответов
Эталон ответа: 2
Вопрос 8
Укажите число атомов водорода, которое входит в состав молекулы, скелет которой имеет строение
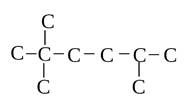
Варианты ответов
Эталон ответа: 4
Вопрос 9
В число положений теории химического строения органических соединений не входит утверждение:
Варианты ответов
Эталон ответа: 4
Вопрос 10
![]() Сколько
веществ изображено с помощью формул
Сколько
веществ изображено с помощью формул 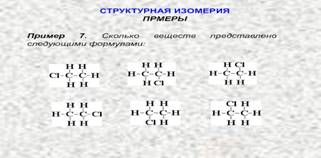
Варианты ответов
Эталон ответа: 4.
Вопрос 11
Для изомеров одинаковы:( выберите 2 верных ответа)
Варианты ответов
Эталон ответа: 3. 4.
Вопрос 12
По структурам углеродного скелета углеводородов укажите одинаковые вещества:(через запятую, по порядку.)
Варианты ответов
1.
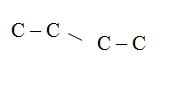
2. 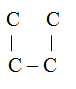
3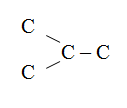
4.![]()
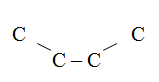
Варианты ответов
Эталон ответа: 4
Задние №4. Тест по теме Теория строения органических соединений А.М.
Бутлерова.
С выбором одного правильного ответа.
1. Какая была первая теория строения органических соединений?
1. Теория радикалов
2. Теория типов
3. Теория химического строения
2. Что такое радикал в теории радикалов?
1. Неизменяемая группа атомов
2. Атом с неспаренным электроном
3. Оба ответа верны
3. На какую теорию сменилась теория радикалов?
1. Теория типов
2. Теория химического строения
3. Теория резонанса
4. Каким ученым принадлежит теория типов?
1. Жерар, Дюма
2. Жерар, Либих
3. Полинг, Жерар
5. Какой ученый ввел понятие о валентности?
1. Франкланд
2. Шееле
3. Полинг
6. Кому принадлежит современная теория строения органических соединений?
1. Бутлеров
2. Менделеев
3. Ломоносов
7. Какова валентность углерода в органических соединениях?
1. 2
2. 4
3. 6
8.Какие пары веществ являются изомерами?
1. н-бутан, изобутан
2. ацетилен, этилен
3. анилин, п-толуидин
9. Какая молекула является разветвленной?
1. 2-метилпропан
2. Пропан
3. Метан
10. Какой спирт синтезировал Бутлеров и доказал его изомерию?
1. Трет-бутиловый
2. Втор-бутиловый
3. Фенол
Эталон ответа:
1-1
2-1
3-1
4-1
5-1
6-1
7-2
8-1
9-1
10-1
Задание №5
Тест по химии на тему "Теория Бутлерова"
Инструкция:
Пожалуйста, выберите один правильный вариант ответа на каждый вопрос и запишите его номер.
Вопрос 1: Кто является основоположником теории
бутлерова?
a) Дмитрий Менделеев
b) Алексей Бутлеров
c) Анри Лавуазье
d) Роберт Бунзен
Ответ: b) Алексей Бутлеров
Вопрос 2: Какое понятие описывает, что молекулы
органических соединений имеют структуру, определяемую связями между атомами?
a) Структурная формула
b) Химическая связь
c) Структура молекулы
d) Молекулярная масса
Ответ: a) Структурная формула
Вопрос 3: В каком году Бутлеров представил свою
теорию?
a) 1850
b) 1861
c) 1871
d) 1880
Ответ: b) 1861
Вопрос 4: Что такое изомерия в контексте теории
Бутлерова?
a) Наличие разных форм одного вещества
b) Процесс образования новых веществ
c) Соответствие молекулы формуле
d) Изменение цвета веществ
Ответ: a) Наличие разных форм одного вещества
Вопрос 5: Какой из следующих типов изомерии НЕ
относится к изомерии, описанной Бутлеровым?
a) Пространственная изомерия
b) Составная изомерия
c) Геометрическая изомерия
d) Оптическая изомерия
Ответ: b) Составная изомерия
Вопрос 6: Какой из предложенных принципов
объясняет, почему молекулы органических соединений имеют различные свойства?
a) Закон сохранения массы
b) Принцип дополнительности
c) Принцип симметрии
d) Структурный принцип
Ответ: d) Структурный принцип
Вопрос 7: Какой вид структурной формулы чаще
всего используют в химии для обозначения органических соединений?
a) Графическая формула
b) Систематическая формула
c) Структурная формула
d) Эмпирическая формула
Ответ: c) Структурная формула
Вопрос 8: Какое из соединений, по теории
Бутлерова, может иметь разные изомеры?
a) Метан
b) Этанол
c) Бутан
d) Тетраметилгексадекан
Ответ: c) Бутан
Вопрос 9: Что подчеркивает теория Бутлерова в
отношении химических свойств соединений?
a) Свойства зависят исключительно от состава
b) Свойства зависят от структуры
c) Свойства зависят от физического состояния
d) Свойства зависят от температуры
Ответ: b) Свойства зависят от структуры
Вопрос 10: Какой фактор не влияет на свойство различных
изомеров по теории Бутлерова?
a) Положение функциональных групп
b) Количество атомов углерода
c) Форма молекулы
d) Наличие водорода в составе
Ответ: d) Наличие водорода в составе
1. Порядок связи атомов в молекуле отражает
1. эмпирическая формула
2. молекулярная формула
3. структурная формула +
4. брутто-формула
2. Какое из утверждений соответствует теории A.M. Бутлерова?
1. все вещества имеют постоянный качественный и количественный состав
2. атомы и группы атомов в молекулах взаимно влияют друг на друга +
3. все вещества состоят из молекул
4. органические вещества образуются только в природе
3.Атомы в молекулы органических веществ соединяются в определенной последовательности согласно их
1. электроотрицательности
2. алфавитному порядку
3. валентности +
4. атомным массам
4.. Тип связи между атомами углерода и водорода
1. ковалентный неполярный
2. ковалентный сильнополярный
3. ковалентный слабополярный +
4. ионный +
5. Какие из утверждений верны?
1. верно только А
2. верно только В
3. оба утверждения верны +
4. оба утверждения неверны
6. Какое из утверждений не соответствует теории A.M. Бутлерова?
1. строение вещества определяет его свойства
2. все вещества имеют постоянный качественный и количественный состав +
3. атомы соединены в молекулы согласно их валентности
4. атомы в молекулах оказывают взаимное влияние друг на друга
7. Структурная формула отражает
1. пространственное расположение атомов
2. порядок связи атомов в молекуле +
3. только качественный состав молекулы
4. только количественный состав молекулы
8. Изомерия — это явление существования нескольких веществ, имеющих
1. одинаковый качественный и разный количественный
2. состав одинаковый качественный и количественный +
3. состав одинаковое строение и разный состав
4. разное строение и разный состав
9. Закончите формулировку положения теории A.M. Бутлерова:
1. «Атомы и группы атомов в молекулах вещества взаимно влияют друг на друга +
2. соединяются по алфавиту
3. взаимодействуют друг с другом
4. взаимозависят друг от друга
10. Ковалентная слабополярная связь возникает между атомами
1. углерода и водорода +
2. углерода и углерода
3. углерода и кислорода
4. углерода и фтора
11. Наименее полярная связь возникает между атомами
1. углерода и водорода
2. углерода и углерода +
3. углерода и кислорода
4. углерода и фтора
12. Закончите формулировку положения теории A.M. Бутлерова: «По свойствам данного вещества можно определить строение его молекулы,
1. а по строению молекулы предвидеть свойства +
2. также и пространственное строение
3. также и валентные углы между атомами
4. по строению молекулы определить валентность атомов
13. Порядок соединения атомов в молекуле и характер их связей называют
1. валентностью
2. химическим строением +
3. изомерией
4. гомологией
14. Формулы, показывающие порядок соединения атомов в молекуле, называют
1. эмпирическими
2. молекулярными
3. структурными +
4. брутто-формулами
15. Какое из утверждений соответствует теории A.M. Бутлерова?
1. все вещества имеют постоянный качественный и количественный состав
2. все вещества состоят из молекул
3. органические вещества образуются только в природе
4. атомы в молекулах оказывают взаимное влияние друг на друга +
Задание №6
Тест по химии на тему "Теория Бутлерова"
Инструкция:
Пожалуйста, выберите один правильный вариант ответа на каждый вопрос и запишите его номер.
Вопрос:
1.Укажите утверждение, соответствующее теории А.М. Бутлерова
2. Строение вещества определяет его свойства
3. Все вещества состоят из молекул
4.Все вещества имеют постоянный качественный и количественный состав
5.Органические вещества образуются только в природе
Эталон
ответа:
Пропуски:
Теория строения органических веществ
Порядок
соединения атомов в молекуле и характер их связей А.М. Бутлеров назвал.
При составлении структурных формул органических веществ учитывают, что в
органических соединениях углерод всегда.
- это явление,
заключающееся в существовании нескольких веществ, имеющих один и тот же состав
и одну и ту же молекулярную массу, но различающихся строением молекул.
Различают три основных типа углеродного скелета :,и.
IV Задания для самостоятельной работы.
Тема «Теория строения органических соединений. Изомерия»
Задание №1.
1. Укажите, какие из структурных формул отвечают одним и тем же соединениям:
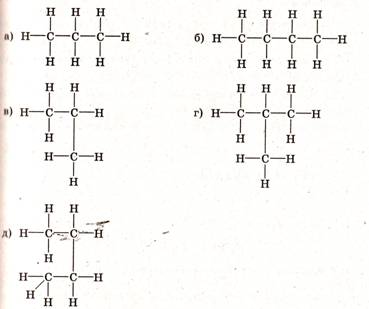
Углеводород имеет нормальное строение, если каждый их углеродных атомов в цепочке (кроме крайних) соединен ковалентными связями с двумя другими атомами углерода. Напишите структурные формулы предельных углеводородов нормального строения с четырьмя, пятью и семью атомами углерода.
Задание №2.
Найдите среди приведенных структурных формул написанные неправильно и исправьте их:
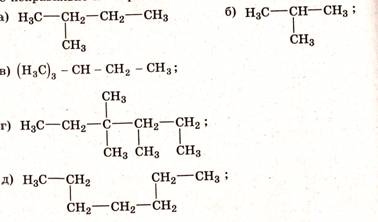
Задание №3
.Укажите, какие из веществ являются изомерами:
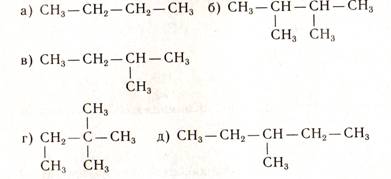
Задание №4.
Сколько соединений изображено формулами а-е?
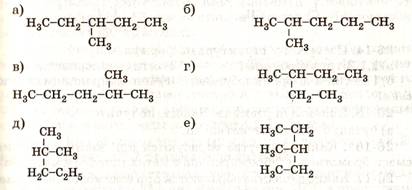
Рекомендуемая литература.
Для студентов обязательная литература.
1. Химия : учебник для среднего профессионального образования / Ю. А. Лебедев, Г. Н. Фадеев, А. М. Голубев, В. Н. Шаповал ; под общей редакцией Г. Н. Фадеева. — 2-е изд., перераб. и доп. — Москва : Издательство Юрайт, 2023.
2. Хомченко И.Г. Общая химия .Учебник для СПО М РИО «Новая волна» Издатель Умеринков. 463 стр 2022 год
3. Габриелян О.С. Химия: учеб. для студ. проф. учеб. заведений / О.С. Габриелян, И.Г. Остроумов. – М., 2021.
4. Габриелян О.С. Общая химия: учеб. для 11 кл. общеобразоват. учреждений с углубл. изучением химии / О.С. Габриелян, И.Г. Остроумов, С.Н. Соловьев, Ф.Н. Маскаев – М., 2023 г..
Дополнительная литература.
1. Габриелян О.С. Химия в тестах, задачах, упражнениях: учеб. пособие для студ. сред. проф. учебных заведений / О.С. Габриелян, Г.Г. Лысова – М., 2021г.
2. Габриелян О.С. Практикум по общей, неорганической и органической химии: учеб. пособие для студ. сред. проф. учеб. заведений / Габриелян О.С., Остроумов И.Г., Дорофеева Н.М. – М., 20224
3. Габриелян О.С., Воловик В.В. Единый государственный экзамен: Химия: Сб. заданий и упражнений. – М., 2023.
Для преподавателей.
1.Химия : учебник для среднего профессионального образования / Ю. А. Лебедев, Г. Н. Фадеев, А. М. Голубев, В. Н. Шаповал ; под общей редакцией Г. Н. Фадеева. — 2-е изд., перераб. и доп. — Москва : Издательство Юрайт, 2023.
2.Хомченко И.Г. Общая химия .Учебник для СПО М РИО «Новая волна» Издатель Умеринков. 463 стр 2022 год
3.Габриелян О.С. Химия: учеб. для студ. проф. учеб. заведений / О.С. Габриелян, И.Г. Остроумов. – М., 2021.
5. Габриелян О.С. Общая химия: учеб. для 11 кл. общеобразоват. учреждений с углубл. изучением химии / О.С. Габриелян, И.Г. Остроумов, С.Н. Соловьев, Ф.Н. Маскаев – М., 2023 г.
6. OnlineSchool-1.ru›encyclopedia/10-klass/himiya/- Конспект урока: Основные положения теории химического строения. Автор: Додонова Елена Владимировна.
Авторы: Рудзитис Г.Е., Фельдман Ф.Г. Издательство: Просвещение 2014
Приложение 1
Органические вещества и медицина.
Органические вещества используются в медицине в разных областях: для создания лекарственных средств, диагностических препаратов, медицинских материалов и в биотехнологиях. Для успешного применения в медицине важно учитывать не только химические свойства вещества, но и его биохимическую активность, стабильность и способность проникать в целевые органы.
Лекарственные средства
· Синтетические производные органических соединений. Например:
o антибактериальные препараты нитрофуранового ряда (фурацилин, фурадонин, фуразолидон);
o вазодилататоры и антигипертензивные средства дигидропиридинового типа (никардипин, нифедипин, фелодипин); транквилизаторы группы 1,4-бензодиазепина (диазепам, оксазепам, нитразепам, феназепам, элениум).
· Модификации структуры существующих соединений для повышения активности. Например, введение в молекулу спиртового гидроксила, альдегидной и кетогрупп повышает фармакологический эффект.
Диагностические препараты
· Рентгеноконтрастные препараты — содержат нетоксичные компоненты (чаще на основе йода), которые задерживают рентгеновские лучи при прохождении через ткани.
· Препараты на основе радиоактивно меченых аминокислот — повышенное накопление которых сигнализирует об активном росте тканей (опухолей или их метастазов). Например, 11С-метионин (11С-МЕТ) и 18F-фторэтилтирозин (18F-ФЭТ) — аналоги природных незаменимых аминокислот метионина и тирозина.
Медицинские материалы
· Полимеры природного и синтетического происхождения — используются в стоматологии в качестве пломбировочных материалов для реставрации зубов, создания оттисков, базисов, искусственных зубов.
· Биоразлагаемые полимерные композиционные материалы — применяются при остеосинтезе — хирургическом методе сращивания кости.
Биотехнологии
· Создание новых лекарственных биопрепаратов — они продуцируются генетически модифицированными микроорганизмами, трансгенными растениями и животными. Например, рекомбинантные инсулин, интерферон, соматотропин, эритропоэтин, интерлейкины и другие препараты пептидной природы.
· Использование ферментов микробного, растительного и животного происхождения — они применяются в медицинской практике как биопрепараты для диагностики, лечения и профилактики различных болезней человека. Особенно они эффективны при терапии наследственной патологии, обусловленной отсутствием либо недостаточностью того или иного фермента в организме.
Приложение 2
Таблица №1.
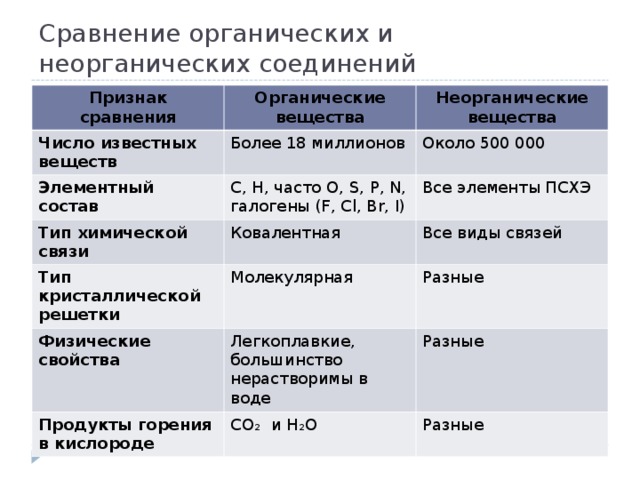
Таблица №2.

Приложение 3.
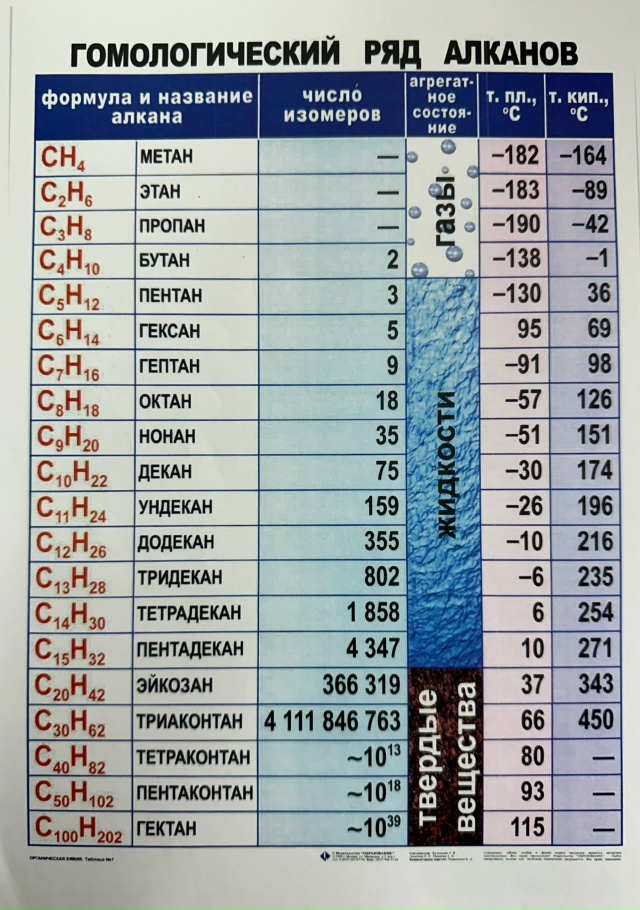
Приложение 4
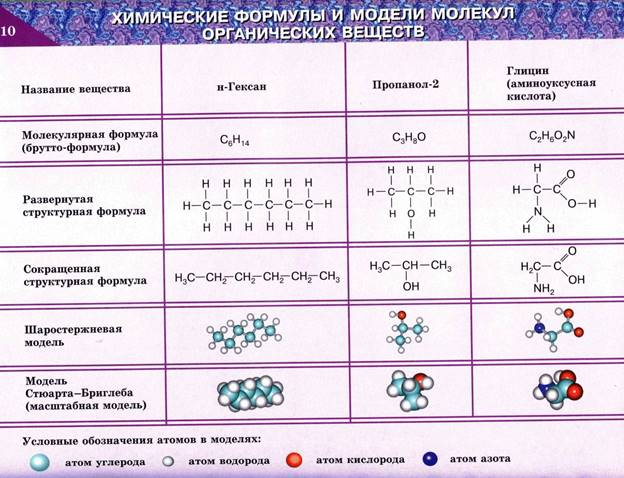
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.