
ГОУ ЛНР «СЛСШ ПГТ ПЕТРОВКА»
РАБОЧАЯ ТЕТРАДЬ по теме:
«Ненасыщенные углеводороды. Этен и этин. Изомерия, гомология, номенклатура ненасыщенных углеводородов. Физические и химические свойства. Применение»
Фамилия Имя ученика:_____________________________________________

2023-2024
уч.год
I. Проверка домашнего задания. Графический диктант
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 2 3 4 5 6 7 8 9 10
![]() Обозначте значком « » правильный
ответ, а значком « » неправильный.
Обозначте значком « » правильный
ответ, а значком « » неправильный.
1. Алканы относят к химически активным веществам.
2. Наличие в молекулах алканов только одинарных (простых) связей обуславливает особые химические свойства алканов.
3. Под действием метана фиолетовый раствор калий перманганата обесцвечивается.
4. Все алканы горят, освобождая большое количество теплоты, реакции горения – это экзотермические реакции.
5. Реакция С2Н6 + Cl2 → С2Н5Cl + НCl называется реакцией хлорирования.
6. Метан и его гомологи разлагаются при сильном нагревании без доступа кислорода, на водород и сажу.
7. Алканы могут вступать в реакции присоединения галогенов.
8. Алканы применяют как топливо благодаря способности вступать в реакции термического разложения.
9. Если через раствор брома, у которого бурая окраска, пропустить метан, то раствор обесцветится.
10. Гомологи метана С5 ─ С10 являются основой топлива для автомобильных двигателей.
II. Понятие о ненасыщенных УВ. «Ассоциативный куст»
![]()
![]()

![]()

![]()
![]() Органические
соединения
Органические
соединения
 Ненасыщенные
УВ
Ненасыщенные
УВ
_________________________ __________________________
_________________________ __________________________
_________________________ __________________________
_________________________ __________________________

Работа в группах. Изготовить из шаростержневого набора молекулу этана, этена, этина. Сравнить подвижность связей, расстояние между атомами углерода, валентный угол.
Используя информацию из учебника и своих наблюдений заполнить таблицу:
|
Углеводороды |
Алканы (этан) |
Алкены (этен, этилен) |
Алкины (этин, ацетилен) |
|
Структурная формула |
|
|
|
|
Тип гибридизации |
|
|
|
|
Валентный угол |
|
|
|
|
Подвижность связей |
|
|
|
|
Расстояние между атомами углерода |
|
|
|
III. Номенклатура, гомологи „Два, четыре, вместе”
Составить схему-шпаргалку: І группа – алкены, IІ группа – алкины
|
Алканы СnН2n+2 |
Алкены СnН2n |
Алкины СnН2n-2 |
|
СН4 метан |
- |
- |
|
С2Н6 этан |
|
|
|
С3Н8 пропан |
|
|
|
С4Н10 бутан |
|
|
|
С5Н12 пентан |
|
|
|
С6Н14 гексан |
|
|
|
С7Н16 гептан |
|
|
|
С8Н18 октан |
|
|
|
С9Н20 нонан |
|
|
|
С10Н22 декан |
|
|
Алгоритм названия ненасыщенных УВ:

|
СН3-СН=СН-СН2-СН-СН3 | СН3
|
СН3-С=СН-СН-СН3 | | СН3 СН3
|
|
________________________________ |
_______________________________ |
|
СН3-СН=С-СН2-СН2-СН3 | СН3
|
СН3-С=СН-СН2-СН3 | СН3
|
|
________________________________ |
_______________________________ |
Алгоритм написания формулы соединения по его названию
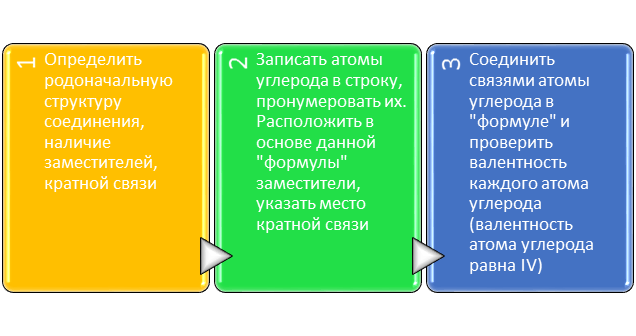
2-метил-3-этилпентен-2 4-метилпентин-2
______________________ __________________________
______________________ __________________________
4-метилпентен-2 2-метилбутен-2
______________________ __________________________
______________________ __________________________
2,4-диметилгексен-2 4,4-диметил-3-этилгептен-2
______________________ __________________________
______________________ __________________________
3,3-диметилбутин-1 2,2-диметилгексин-3
______________________ __________________________
______________________ __________________________
2,2,5-триметилгептин-3 4-метил-3,4-дихлорпентин-1
______________________ __________________________
______________________ __________________________
Изомерия ненасыщенных УВ
1. Изомерия углеводородного скелета:
|
1 2 3 4 5 СН3-СН=С-СН2-СН3 | СН3
|
1 2 3 4 5 СН3-СН=СН-СН-СН3 | СН3
|
|
3-метилпентен-2 |
4-метилпентен-2 |
2. Изомерия положения кратной связи:
|
1 2 3 4 5 СН3-СН=СН-СН-СН3 | СН3
|
1 2 3 4 5 СН2=СН-СН2-СН-СН3 | СН3
|
|
4-метилпентен-2 |
4-метилпентен-2 |
3. Межклассовая изомерия
4. Пространственная изомерия
Физические свойства ненасыщенных УВ
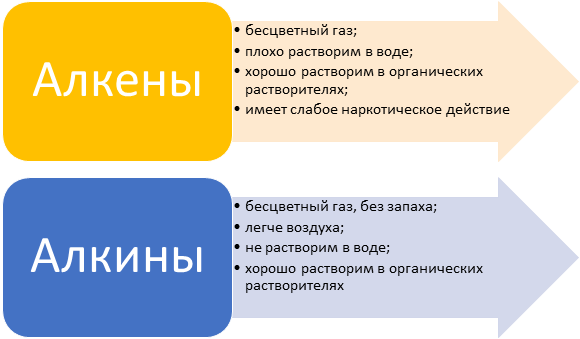
Круги Вена. Исходя из приведенной информации о физических свойствах ненасыщенных УВ, составьте следующую диаграмму: слева запишите все свойства алкенов, которые отличаются от свойств алкинов. По центру напишите общие свойства характерные и для алкенов, и для алкинов.

Химические свойства ненасыщенных УВ
1. Реакции горения:
_____________________________ _____________________________
2. Реакции присоединения:
_____________________________ _____________________________
_____________________________ _____________________________
_____________________________ _____________________________
Правило Марковникова (присоединение молекул типа НХ к нессиметричным ненасыщенным УВ) Присоединение молекул типа НХ к нессиметричным алкенам происходит по месту разрыва двойной связи, атом водорода присоединяется к наиболее гидрогенизированному атому углерода:
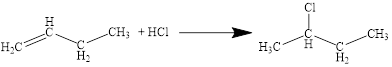
3. Реакции полимеризации:
Реакция полимеризации – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения низкомолекулярного вещества (мономера)
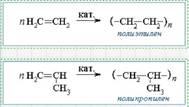
_____________________________ _____________________________
_____________________________ _____________________________
Применение ненасыщенных УВ
Этилен-
· производство взрывоопасных веществ,
· пластмасс,
· ускорение созревания плодов,
· производство топлива для самолетов,
· антифризов,
· тефлона
Ацетилен –
· производство парфюма, лаков,
· уксусной ктслоты,
· искусственных волокон,
· синтез красителей,
· сварка металлов,
· производство ПВХ
Задания для самоконтроля:
1.Дать название алкенам:
CH3—CH2—C=CH—CH3 CH3—CH2—CH—CH—CH=CH2
| | |
СH3 CH3 CH3
_____________________________________________________________________________
CH3—CH2—CH—C=CH—CH—CH3 CH3—CH2—CH=CH—CH3
| | |
C2H5 CH3 CH3
_____________________________________________________________________________
CH3- CH2—CH—CH2- CH=CH2 CH3—CH = CH—CH2 —CH3
|
C2H5
_____________________________________________________________________________
CH3—CH2—CH—CH=C—CH—CH3 CH3—CH —C=CH—CH3
| | | | |
CH3 CH3 CH3 CH3 CH3
_____________________________________________________________________________
2. Написать структурные формулы следующих соединений:
2-хлорбутен-1
2,3-диметилпентен-1
3-метилгексин-1
3,3-диэтилпентин-1
2,5-диметилгептен-3
2,2-диметилгексин-3
2-метилгексин-3
4,4-диметилгексен-1
3-этилоктен-1
3.Используя алкен, в формуле которого шесть атомов углерода составьте:
А) формулу гомолога с меньшим числом атомов углерода
Б) формулу гомолога с большим числом атомов углерода
В) формулу изомера углеродного скелета
Г) формулу изомера положения связи. Все вещества назовите.
4.Используя алкен, в формуле которого семь атомов углерода составьте:
А) формулу гомолога с меньшим числом атомов углерода
Б) формулу гомолога с большим числом атомов углерода
В) формулу изомера углеродного скелета
Г) формулу изомера положения связи. Все вещества назовите.
5.Допишите уравнения реакций, характеризующих химические свойства алкенов:
CH3-CH=CH-CH3+Cl2 à________________________________________________________
CH3-CH=CH-CH3+H2 à________________________________________________________
CH3-CH=CH-CH3+H2Oà_______________________________________________________
CH3-CH=CH-CH3+HClà_______________________________________________________
CH3-CH=CH2+O2 à___________________________________________________________
CH3-CH=CH-CH3+H2O(KMnO4)à_______________________________________________
CH3-CH=CH-CH3+Br2 à_______________________________________________________
CH3-CH=CH-CH3+H2 à_______________________________________________________
CH3-CH=CH-CH3+H2Oà_______________________________________________________
CH3—CH=CH – CH3 + O2à____________________________________________________
CH3-CH=CH-CH3+HBrà______________________________________________________
CH3-CH=CH-CH3+H2O(KMnO4)à_______________________________________________
6.Определите молекулярную формулу газообразного углеводорода, если известно, что он вдвое тяжелее воздуха, а содержание в нем углерода составляет 82,76% (Мгвозд=29).
|
Дано:
|
Решение:
|
|
Найти:
|
7. В углеводороде массовая доля углерода составляет 92,3%. Относительная плотность паров углеводорода по углекислому газу равна 0,59. Определите формулу углеводорода, напишите реакцию его взаимодействия с хлором.
|
Дано:
|
Решение:
|
|
Найти:
|
8. Выведите формулу углеводорода, если массовая доля углерода равна 85,7% и у него относительная плотность газа по метану 2,625. Как экспериментально отличить это вещество от метана?
|
Дано:
|
Решение:
|
|
Найти:
|
9. Вычислить массовые доли углерода в молекулах этена и этина.
|
Дано:
|
Решение:
|
|
Найти:
|
10.Какой объем кислорода (н.у) прореагировал с ацетиленом, если образовалось 0,75 моль углекислого газа?
|
Дано:
|
Решение:
|
|
Найти:
|
11. Вычислить плотность ацетилена (н.у.)
|
Дано:
|
Решение: |
|
Найти:
|
12. Вычислить относительную плотность этена по гелию.
|
Дано:
|
Решение: |
|
Найти:
|
13. Вычислить массу 336мл (н.у) этина.
|
Дано:
|
Решение: |
|
Найти:
|
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.