
ҚАЗАҚСТАН РЕСПУБЛИКАСЫНЫҢ ДЕНСАУЛЫҚ САҚТАУ МИНИСТРЛІГІ
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ КАЗАХСТАН
ҚОСТАНАЙ ЖОҒАРЫ МЕДИЦИНАЛЫҚ КОЛЛЕДЖІ
КОСТАНАЙСКИЙ ВЫСШИЙ МЕДИЦИНСКИЙ КОЛЛЕДЖ

Бекітемін
Қостанай облысы әкімдігі денсаулық сақтау басқармасының Қостанай жоғары медициналық колледжі Коммуналды мемлекеттік кәсіпорнының ОЖ директордың орынбасары
_________________ А.А.Жарматова
20__ж. «____»___________
СТУДЕНТТЕР ҮШІН ПӘН БОЙЫНША ОҚУ ЖҰМЫС БАҒДАРЛАМАСЫ (СИЛЛАБУС)
учебная программа ДИСЦИПЛИНЫ ДЛЯ СТУДЕНТОВ
(СИЛЛАБУС)
|
Модуль: Модуль: |
2 Жаратылыстану-ғылыми пәндер циклі 2 Цикл естественнонаучных дисциплин |
|
Субмодуль: Субмодуль: |
АП01 Бейорганикалық химия СД 01 Неорганическая химия |
|
Мамандық: Специальность: |
0306000 «Фармация» 0306000 «Фармация» |
|
Біліктілігі: Квалификация: |
0306013 «Фармацевт» 0306013 «Фармацевт» |
|
Білім деңгейі: Уровень знания: |
Орта - арнайы білім Средне - специальное образование |
|
Оқу мерзімі: Период обучения: |
I курс, II семестр
|
|
Оқу нысаны: Форма обучения: |
Күндізгі Очная |
|
Академиялық сағаттар саны (кредиттер): Количество академических часов (кредитов): |
120/4 |
|
Олардың ішінен: Из них: |
|
|
Аудиториялық сабақтар Аудиторные занятия |
20 |
|
СӨЖ Самостоятельная работа обучающихся (СРО) |
30 |
|
СОӨЖ Самостоятельная работа обучающихся с преподавателем (СРОП) |
10 |
|
Симуляциялар Симуляции |
60 |
|
Бақылау нысаны: Форма контроля: |
Емтихан Экзамен |
Құрастырушы: Кужахметова А.Ж.
Студенттерге арналған пәннің оқу бағдарламасы (силлабус) ҚР денсаулық сақтау Министрінің 201_ жылғы _______№___ бұйрығымен бекітілген «Фармация» мамандығы бойынша ҚР МЖМБС сәйкес құрастырылды.
Студенттерге арналған (силлабус) пәннің оқу бағдарламасы № 4 циклдік әдістемелік комиссиясының отырысында қарастырылды
201__ жылғы «____» ____________ №___ хаттамасы
ЦӘК төрайымы: ___________ Шулейко С.В.
Составитель: Кужахметова А.Ж.
Учебная программа дисциплины для студентов (силлабус) составлена в соответствии с ГОСО РК по специальности «Фармация», утвержденного приказом Министра здравоохранения РК № ___ от «___» _______ 201__ года.
Учебная программа дисциплины для студентов (силлабус) рассмотрена на заседании цикловой методической комиссии №4
Протокол №___ от «____» ____________ 201___ г.
Председатель: ___________ Шулейко С.В.
1. ОБЩИЕ СВЕДЕНИЯ
Количество академических часов:
Из них: 120
Аудиторные занятия: 20
Самостоятельная работа обучающихся (СРС): 30
Самостоятельная работа обучающихся с преподавателем (СРОП): 10
Практические занятия: 60
Форма контроля: экзамен
Сведения о преподавателях данной дисциплины:
Кужахметова А.Ж., вторая квалификационная категория
Контактная информация: кабинет 510, время и место проведения занятий 8.00 – 18.00, сайт колледжа www.komeco.kz
Политика курса, академического поведения и этики:
Обязанности студента:
1.Овладевать теоретическими знаниями и практическими навыками по избранной специальности;
2. Уважать труд и достоинство преподавателей;
3. Бережно обращаться с помещениями, мебелью, оборудованием и материалами, принадлежащими колледжу, нести материальную ответственности за их порчу;
4. Студенты должны быть дисциплинированными и опрятными в колледже;
5. Выполнять в установленные сроки все виды заданий, предусмотренные учебным планом и обязательными программами;
6. За пропуски аудиторных занятий студент должен предоставить оправдательный документ. Пропуски должны быть отработаны в течение 10 дней;
7. Во время учебных занятий отключать сотовые телефоны и прочие гаджеты, внимательно слушать объяснения преподавателей и ответы товарищей, не разговаривать, не отвлекаться, выполнять все указания преподавателя;
8. Входить и выходить во время занятий из аудитории студенты могут только с разрешения преподавателя;
9. Во время занятий и во время практики студенты пользуются только теми пособиями, приборами и инструментами, которые указаны руководителем занятия, обязаны обращаться с ними бережно и соблюдать правила техники безопасности;
10. Во время экзамена запрещается пользоваться сотовыми телефонами, гаджетами и шпаргалками.
2. ПРОГРАММА
2.1 Введение
Неорганическая химия является фундаментальной базой для изучения других химических дисциплин и специальных дисциплин. Неорганическая химия состоит из двух разделов: теоретические основы химии, изучающих основные понятия химии, строение атомов и молекул, закономерности протекания химических реакций, свойства и превращения веществ в растворах – кислотно-основные реакции и химия элементов, изучающих s-, p – и d-блоки периодической системы элементов.
2.2 Цель курса
Целью изучения неорганической химии является формирование у студентов представления взаимосвязи структуры и химических свойств основных классов неорганических соединений, материальном единстве химических элементов и веществ, взаимосвязи качественных и количественных изменений.
2.3 Задачи обучения курса
Задачами курса неорганической химии являются обеспечение студентов знаниями, способствующими формированию научно- материалистического мировоззрения, развития мышления, создание прочной базы, на которой строится изучение специальных и профессиональных дисциплин, а также приобретение навыков работы в химической лаборатории.
2.4 Компетенции, формируемые у студентов в процессе обучения курса согласно ГОСО
Базовые компетенции:
|
№ |
Компетенции |
№ К |
Результаты обучения программы. Выпускник будет способен: |
|
БК-1 |
ЭМОЦИОНАЛЬНО ПСИХОЛОГИЧЕСКИЕ. Проявляет самосознание, понимает свои потребности и побуждения. |
БК-1.1 |
Понимает сущность и социальную значимость своей будущей профессии, проявляет к ней устойчивый интерес. |
|
БК-2 |
РЕГУЛЯТИВНО-АНАЛИТИЧЕСКИЕ. Организует и оценивает собственную деятельность при выполнении профессиональных задач. |
БК-2.1 |
Определяет задачи и планирует собственную деятельность, выбирает типовые методы и способы выполнения профессиональных задач базовой категории сложности с учетом поставленной цели, оценивает их эффективность и качество |
|
БК-2.2 |
Самостоятельно решает практические задачи базовой категории сложности в области фармацевтической деятельности в пределах компетенции, анализирует рабочую ситуацию и ее предсказуемые изменения, производит текущий и итоговый контроль, оценку и коррекцию. |
Профессиональные компетенции:
|
ПК-1 |
ОРГАНИЗАЦИЯ И ЭКОНОМИКА ФАРМАЦЕВТИЧЕСКОЙ ДЕЯТЕЛЬНОСТИ. Демонстрирует навыки оптовой и розничной реализации лекарственных средств и товаров аптечного ассортимента, организации и руководства отделами аптеки или аптечного склада.
|
ПК-1.1 |
Организовывает прием, хранение лекарственных средств, лекарственного растительного сырья и товаров аптечного ассортимента в соответствии с требованиями нормативно-правовой базы. |
|
ПК-2 |
ФАРМАЦЕВТИЧЕСКИЕ ТЕХНОЛОГИИ. Изготавливает и отпускаетлекарственные препараты, осуществляет контроль их качества. |
ПК-2.1 |
Изготавливает лекарственные формы по рецептам и требованиям медицинских организаций. |
2.5 Результаты обучения
В результате освоения дисциплины студент должен:
Знать:
- цели и задачи неорганической химии;
- основные понятия химии;
- структуру и строение периодической системы;
- виды химической связи;
- основные термодинамические величины;
- способы выражения концентрации растворов;
- классификацию растворов;
- характерные свойства элементов группы и их важнейших соединений;
- применение важнейших неорганических соединений в медицине и фармации;
- правила техники безопасности при выполнении практических работ.
Уметь:
- рассчитывать молекулярные и молярные массы веществ, эквивалент, массу веществ, количество вещества;
- давать характеристику элементу по положению в периодической системе химических элементов;
- определять направление химической реакции по значению энергии Гиббса и энтропии;
- рассчитывать массу навески вещества для приготовления раствора заданной концентрации, приготовить раствор;
- определять направление ОВР по разности стандартных электродных потенциалов полупар.
2.6 Список пре- и постреквизитов
|
№ |
Пререквизит (название курса) |
Постреквизит (название курса) |
|
1 |
Латинский язык в фармации |
Фармацевтическая химия |
2.7 Тематический план по дисциплине «Неорганическая химия»
|
№ |
Тема |
Литература |
Количество часов |
Оснащение |
|||
|
Самостоятельная работа студентов |
Аудиторные занятия |
Практические занятия
|
|||||
|
СРО |
СРОП |
||||||
|
1 |
Предмет, задачи и стехиометрические законы в неорганической химии. |
О: 1. Бабков А.В., Барабанова Т.И., Попков В.А. «Общая и неорганическая химия», стр.11-22; 2. Пустовалова Л.М., Никанорова И.Е. «Общая и неорганическая химия», стр.4-19 Д: 1. Чернобельская Г.М., Чертков И.Н. «Химия», стр.7-11 |
8 |
3 |
4 |
14 |
флипчарт |
|
2 |
Учение о растворах. |
О: 1. Бабков А.В., Барабанова Т.И., Попков В.А. «Общая и неорганическая химия», стр.121-134 2. Пустовалова Л.М., Никанорова И.Е. «Общая и неорганическая химия», стр.108-114 Д: 1. Чернобельская Г.М., Чертков И.Н. «Химия», стр.38-42 |
8 |
3 |
4 |
14 |
флипчарт |
|
3 |
Рубежный контроль |
|
|
|
2 |
|
|
|
4 |
Химия s-, p-, d- элементов и их соединений |
О: 1. Бабков А.В., Барабанова Т.И., Попков В.А. «Общая и неорганическая химия», стр.199-214 2. Пустовалова Л.М., Никанорова И.Е. «Общая и неорганическая химия», стр.186-316 Д: 1. Чернобельская Г.М., Чертков И.Н. «Химия», 213-224 |
14 |
4 |
4 |
32 |
флипчарт |
|
5 |
Рубежный контроль |
|
|
|
2 |
|
|
|
6 |
Экзамен |
|
|
|
4 |
|
|
|
|
Итого |
|
30 |
10 |
20 |
60 |
|
2.8 Краткое содержание курса
2.8.1 Аудиторные занятия
|
№ |
Тема |
Содержание |
Количество часов |
|
1 |
Предмет, задачи и стехиометрические законы в неорганической химии. |
История развития неорганической химии. Роль неорганической химии в фармации. Основные законы химии (закон сохранения массы веществ, закон сохранения энергии, закон эквивалентов, закон Авогадро). Основные понятия химии (материя, вещество, молекула, атом, изотоп, эквивалент, моль, молярная масса, атомная масса, молекулярная масса). Современная номенклатура неорганических веществ.
|
4 |
|
2 |
Учение о растворах. |
Определения «раствор», «растворитель», «растворенное вещество». Способы выражения концентрации растворов. Роль водных растворов в биосфере, жизнедеятельности организма, приготовления лекарственных препаратов. Классификация растворов (электролиты, неэлектролиты, концентрированные, разбавленные, насыщенные, ненасыщенные, истинные, коллоидно-дисперсные, грубодисперсные). Коллигативные свойства растворов неэлектролитов. Диффузия, осмос, осмотическое давление. Роль осмотического давления в биологических системах (гипо-, изо-, гипертонические растворы, плазмолиз, гемолиз, тургор). Понижение температуры замерзания и повышение температуры кипения растворов.
|
4 |
|
3 |
Рубежный контроль |
|
2 |
|
4 |
Химия s-, p-, d- элементов и их соединений |
Общая характеристика s-, p- элементов. Особенности положения в ПСХЭ. Лабораторные, промышленные способы получения s-, p-, физические и химические свойства. Важнейшие соединения s-, p-элементов. Их свойства, получение, применение в медицине и биологическая роль.
|
4 |
|
5 |
Рубежный контроль |
|
2 |
|
6 |
Экзамен |
|
4 |
|
|
Итого |
|
20 |
|
|
|
|
|
2.8.2 Практические занятия
|
№ |
Тема |
Содержание |
Количество часов |
|
1 |
Правила ТБ при работе в химической лаборатории. Периодический закон Д.И.Менделеева. Теория строения веществ. |
Правила работы и ТБ в химической лаборатории. Виды химической посуды. Правила работы химической посудой, реактивами, нагревательными приборами. Правила оказания первой помощи при химических ожогах и отравлениях химическими веществами. Характеристика элемента по положению в периодической системе и строению атома.
|
4 |
|
2 |
Свойства основных классов неорганических соединений. |
Химические свойства и способы получения неорганических веществ: оксидов, оснований, амфотерных гидроксидов, кислот и солей. |
4 |
|
3 |
Комплексные соединения |
Комплексные соединения. Координационная теория Вернера. Строение, классификация и номенклатура комплексных соединений. Диссоциация комплексных соединений в растворах. Свойства комплексных соединений. Биологическая роль комплексных соединений и применение их в медицине и фармации. |
4 |
|
4 |
Расчет теплового эффекта химических реакций. Изучение зависимости скорости реакции от различных факторов.
|
Расчет теплового эффекта химических реакций по закону Гесса, по уравнению реакции. Зависимость скорости реакции от концентрации веществ, от температуры, от наличия катализатора, от степени дисперсности вещества.
|
4 |
|
5 |
Растворы. Массовая доля растворенного вещества. |
Способы выражения концентрации растворов, расчетные формулы. |
4 |
|
6 |
Растворы. Молярная концентрация |
Расчеты для приготовления растворов определенной молярной концентрации и молярной концентрации растворов. |
4 |
|
7 |
Реакции ионного обмена |
Свойства электролитов в растворе. Условия, при которых реакции ионного обмена протекают до конца. |
4 |
|
8 |
Окислительно-восстановительные реакции |
Степени окисления атомов элементов, правила их расчетов. Составление уравнений окислительно-восстановительных реакций методом электронного баланса и полуреакций. Классификагщя ОВР. Стандартные электродные потенциалы полуреакций. Определение направления реакции по ОВР по разности стандартных потенциалов. Влияние среды на направление ОВР и характер образующихся продуктов. Роль окислительно-восстановительных реакций в биосистемах, в анализе лекарственных препаратов, применение в клинических исследованиях.
|
4 |
|
9 |
Свойства галогенов и их соединений. |
Химические реакции, характеризующие свойства галогенов и их соединений. Качественные реакции на Cl-, Br-, I- ионы. |
4 |
|
10 |
Свойства соединений серы. |
Реакции, характеризующие свойства серной кислоты. Качественные реакции на сульфат-, сульфит-, сульфид- и тиосульфат- ионы. |
4 |
|
11 |
Свойства соединений азота и фосфора. |
Химические реакции, характеризующие соединения азота и фосфора. Качественные реакции на ионы NH4+, NO3-, PO43- |
4 |
|
12 |
Свойства соединений s-элементов I и II групп |
Свойства соединений натрия и кальция. Химические реакции, характеризующие свойства этих соединений. |
4 |
|
13 |
Свойства соединений d-элементов I и II групп |
Химические реакции, характеризующие свойства соединений меди, цинка, серебра. |
4 |
|
14 |
Свойства соединений хрома и марганца. |
Свойства соединений хрома и марганца. Химические реакции, характеризующие свойства соединений хрома и марганца. |
4 |
|
15 |
Свойства соединений железа (II и III ) |
Химические реакции, характеризующие свойства соединений железа (II) |
4 |
|
|
Итого |
|
60 |
2.8.4 Самостоятельная работа обучающихся (СРО)
|
№ |
Тема |
Содержание задания |
Форма контроля |
Количество часов |
|
1 |
Типы химической связи
|
Химическая связь. Типы химической связи: ковалентная, ионная, металлическая, водородная. Типы межмолекулярного взаимодействия. Характеристики химической связи. Гибридизация атомных орбиталей и виды гибридизации. |
Заполнение таблицы |
2 |
|
2 |
Валентность элементов с точки зрения атомов и химичкой связи. Степень окисления. |
Валентность элемента. Степень окисления. Низшая и высшая степени окисления. |
Опорный конспект |
2 |
|
3 |
Оксиды и основания |
Состав, название, свойства и способы получения оксидов и оснований |
Фишбоун, составление задач. |
2 |
|
4 |
Кислоты и соли |
Состав, название, свойства и способы получения кислот и солей |
Синквейн, решение задач. |
2 |
|
5 |
Дисперсные системы. Коллоидные и истинные растворы. |
Виды дисперсных систем, коллоидные растворы, растворитель, растворенное вещество |
Сравнительная таблица |
3 |
|
6 |
Концентрации и основные единицы, необходимые для расчета концентрации |
Молярная концентрация, молярная концентрация эквивалента, титр раствора, массовая концентрация, массовая доля, объемная доля. |
Глоссарий, опорный конспект |
3 |
|
7 |
Теория электролитической диссоциации |
Механизм электролитической диссоциации. Степень и константа электролитической диссоциации. |
Презентация, опорный конспект |
2 |
|
8 |
Элементы VII A группы. |
Общая характеристика галогенов. Химические соединения галогенов. |
Составление тестовых заданий. |
2 |
|
9 |
Элементы VI A группы. |
Особенности строения атомов элементов группы VI A, получение и свойства простых веществ кислорода и серы и важнейших типов их соединений, биологическое значение элементов группы. |
Составление схемы. |
2 |
|
10 |
Элементы IIIA, IVA и VA групп |
Свойства элементов IIIA, IVA и VA групп |
Сравнительная таблица |
2 |
|
11 |
Элементы IA и IIA групп |
Свойства элементов IA и IIA |
Диаграмма Венна |
1 |
|
12 |
Элементы IB и IIB групп |
Cвойства элементов IB и IIB групп |
Опорный конспект |
2 |
|
13 |
Элементы VIB и VIIB групп |
Свойства элементов VIB и VIIB групп |
Составление задач |
3 |
|
14 |
Элементы VIII B группы |
Общая характеристика элементов и их соединений. Медико-биологическое значение. |
Презентация |
2 |
|
|
Итого |
|
|
30 |
2.8.5 Самостоятельная работа студентов под руководством преподавателя
|
№ |
Тема |
Содержание задания |
Форма контроля |
Количество часов |
|
1 |
Периодический закон и периодическая система химических элементов Д.И.Менделеева.
|
Структура периодической системы. Основные характеристики атома: атомный радиус, энергия ионизации, сродство к электрону, электроотрицательность. |
Индивидуальные карточки, проверка самостоятельной работы |
1 |
|
2 |
Основные классы неорганических соединений. |
Важнейшие классы неорганических веществ. Способы получения, физические и химические свойства. |
Просмотр и проверка выполнения самостоятельной работы, тестирование. |
1 |
|
3 |
Комплексные соединения |
Центральный атом. Лиганды. Типы, номенклатура, образование комплексных соединений |
Индивидуальные карточки |
1 |
|
4 |
Концентрация растворов. Массовые доли. |
Способы выражения концентрации растворов. Массовая доля растворенного вещества. |
Индивидуальное собеседование. Проверка выполнения самостоятельной работы. |
1 |
|
5 |
Молярная концентрация и молярная концентрация эквивалента. |
Способы выражения концентрации растворов. Молярная концентрация и молярная концентрация эквивалента. |
Индивидуальные карточки, проверка выполнения самостоятельной работы. |
1 |
|
6 |
Реакции обмена в водных растворах электролитов. |
Ионные реакции и уравнения. |
Индивидуальные карточки, проверка выполнения самостоятельной работы |
1 |
|
7 |
Галогены. |
Общая характеристика p-элементов и их соединений. Медико-биологическое значение. |
Устный опрос, проверка выполнения самостоятельной работы. |
1 |
|
8 |
Халькогены. |
Общая характеристика халькогенов. Кислород и его соединения. Сера и ее соединения. |
Тестирование, проверка выполнения самостоятельной работы. |
1 |
|
9 |
Элементы IB и IIB групп. |
Свойства соединений, способы получения и медико-биологическое значение. |
Индивидуальная беседа, проверка выполнения самостоятельной работы. |
1 |
|
10 |
Свойства соединений d - элементов. |
Свойства соединений d-элементов, способы получения и медико-биологическое значение. |
Тестирование, проверка выполнения самостоятельной работы. |
1 |
|
|
Итого |
|
|
10 |
2.9 Методические указания по выполнению СРО
Рекомендации по заполнению таблицы.
Таблица. Типы химической связи.
|
Связь |
Определение |
Схема образования |
Примеры соединений |
|
1 |
2 |
3 |
4 |
|
Ковалентная |
|
|
|
|
Ковалентная неполярная |
|
|
|
|
Ковалентная полярная |
|
|
|
|
Ионная |
|
|
|
|
Металлическая |
|
|
|
|
Водородная |
|
|
|
|
Ван-дер-Ваальсова |
|
|
|
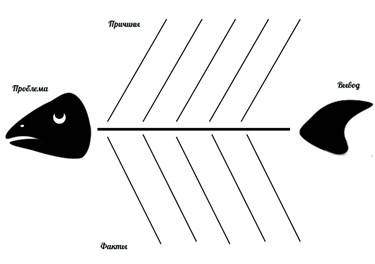
Рекомендации по составлению фишбоун
Фишбоун — установление причинно-следственных взаимосвязей между объектом анализа и влияющими на него факторами, совершение обоснованного выбора.
Рекомендации по составлению синквейн
Синквейн — это методический прием, который представляет собой составление стихотворения, состоящего из 5 строк.
Первая строчка стихотворения — это его тема. Представлена она всего одним словом и обязательно существительным.
Вторая строка состоит из двух слов, раскрывающих основную тему, описывающих ее. Это должны быть прилагательные. Допускается использование причастий.
В третьей строчке, посредством использования глаголов или деепричастий, описываются действия, относящиеся к слову, являющемуся темой синквейна. В третьей строке три слова.
Четвертая строка — это уже не набор слов, а целая фраза, при помощи которой составляющий высказывает свое отношение к теме. В данном случае это может быть как предложение, составленное учеником самостоятельно, так и крылатое выражение, пословица, поговорка, цитата, афоризм, обязательно в контексте раскрываемой темы.
Пятая строчка — всего одно слово, которое представляет собой некий итог, резюме. Чаще всего это просто синоним к теме стихотворения.
Рекомендации по составлению глоссария
Глоссарий - вид самостоятельной работы, выражающейся в подборе и систематизации терминов, непонятных слов и выражений, встречающихся при изучении темы. Способность выделять главные понятия темы и формулировать их. Оформляется письменно, включает название и значение терминов, слов и понятий в алфавитном порядке.
Рекомендации по составлению диаграммы Венна
Диаграмма Венна - схематичное
изображение всех возможных отношений.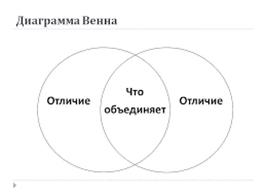
Вопросы первого рубежного контроля
1. Введение. Предмет и задачи неорганической химии.
2. Периодический закон Д.И.Менделеева. Теория строения веществ.
3. Типы химической связи.
4. Валентность элементов с точки зрения атомов и химической связи. Степень окисления.
5. Свойства основных классов неорганических соединений.
6. Оксиды и основания.
7. Кислоты и соли.
8. Комплексные соединения.
9. Расчет теплового эффекта химических реакций. Изучение зависимости скорости реакции от различных факторов.
10. Учение о растворах.
11. Концентрация растворов. Массовые доли.
12. Молярная концентрация и молярная концентрация эквивалента.
13. Теория электролитической диссоциации.
14. Реакции обмена в водных растворах электролитов.
15. Дисперсные системы. Коллоидные и истинные растворы.
16. Окислительно-восстановительные реакции.
Вопросы второго рубежного контроля
1. Химия s-, p- элементов и их соединений.
2. Свойства галогенов и их соединений.
3. Свойства соединений серы.
4. Свойства соединений азота и фосфора.
5. Свойства соединений s-элементов I и II групп.
6. Свойства соединений d-элементов I и II групп.
7. Свойства соединений хрома и марганца.
8. Элементы IB и IIB групп.
9. Элементы VIB и VIIB групп.
10. Элементы VIII B группы.
11. Свойства соединений железа (II и III)
Вопросы итогового контроля
1. Введение. Предмет и задачи неорганической химии.
2. Периодический закон Д.И.Менделеева. Теория строения веществ.
3. Типы химической связи.
4. Валентность элементов с точки зрения атомов и химической связи. Степень окисления.
5. Оксиды и основания.
6. Кислоты и соли.
7. Комплексные соединения.
8. Расчет теплового эффекта химических реакций. Изучение зависимости скорости реакции от различных факторов.
9. Концентрация растворов. Массовые доли.
10. Молярная концентрация и молярная концентрация эквивалента.
11. Теория электролитической диссоциации.
12. Реакции обмена в водных растворах электролитов.
13. Дисперсные системы. Коллоидные и истинные растворы.
14. Окислительно-восстановительные реакции.
15. Свойства галогенов и их соединений.
16. Свойства соединений серы.
17. Свойства соединений азота и фосфора.
18. Свойства соединений s-элементов I и II групп.
19. Свойства соединений d-элементов I и II групп.
20. Свойства соединений хрома и марганца.
21. Элементы IB и IIB групп.
22. Элементы VIB и VIIB групп.
23. Элементы VIII B группы.
24. Свойства соединений железа (II)
25. Свойства соединений железа (III)
2.10 Литература
Основная:
1. Бабков А.В., Барабанова Т.И., Попков В.А. «Общая и неорганическая химия». М; 2014
2. Пустовалова Л.М., Никанорова И.Е. «Общая и неорганическая химия». Ростов н/Д; 2015
Дополнительная:
1. Чернобельская Г.М., Чертков И.Н. «Химия». М.; 1991
2.11 Критерии и правила оценивания знаний студентов
Критерии оценки, предъявляемые к обучающимся на аудиторных и практических занятиях.
|
№ |
Критерии оценивания |
Пояснение |
|
1 |
Отлично «А» |
Обучающийся, проявивший всестороннее и глубокое знание учебно-программного материала, умение свободно в нем ориентироваться, самостоятельно и правильно выполнять задания в полном объеме. |
|
2 |
Хорошо «В» |
Обучающийся, проявивший хорошее знание учебно-программного материала, успешно выполнивший предусмотренные в программе задания, показавший систематический характер знаний по дисциплине, но имеющий незначительные пробелы, которые он способен самостоятельно пополнить. |
|
3 |
Удовлетворительно «C, D» |
Обучающийся, усвоивший основной учебно-программный материал в объеме, необходимом для дальнейшей учебы, но при этом допустившему в ответе несколько погрешностей. Этот обучающийся способен устранить отмеченные недостатки под руководством преподавателя и далее самостоятельно справляться с выполнением заданий. |
|
4 |
Неудовлетворительно «F» |
Обучающийся, у которого обнаружены пробелы в знании основного учебно-программного материала, принципиальные ошибки в выполнении предусмотренных программой заданий. Оценка Неудовлетворительно «F» означает, что студент не сможет продолжать обучение без дополнительной работы по дисциплине под руководством преподавателя (дополнительные занятия, консультации) и самостоятельно. |
Итоговый контроль: экзамен
Текущая оценка влияет на R 60%, итоговая оценка влияет на E 40%,
Формула оценки: І = R x 0.6 + E x 0.4, где R – текущий контроль E – итоговый контроль. В экзаменационную ведомость оценки вставляются согласно таблице указанной ниже.
Буквенная система оценки учебных достижений обучающихся, соответствующая цифровому эквиваленту по четырехбалльной системе
|
Оценка по буквенной системе |
Цифровой эквивалент баллов |
Процентное содержание % |
Оценка по традиционной системе |
|
А |
4,0 |
95-100 |
Отлично |
|
А- |
3,67 |
90-94 |
|
|
В+ |
3,33 |
85-89 |
Хорошо |
|
В |
3,0 |
80-84 |
|
|
В- |
2,67 |
75-79 |
|
|
С+ |
2,33 |
70-74 |
Удовлетворительно |
|
С |
2,0 |
65-69 |
|
|
С- |
1,67 |
60-64 |
|
|
D+ |
1,33 |
55-59 |
|
|
D |
1,0 |
50-54 |
|
|
F |
0 |
0-49 |
Неудовлетворительно |
2.12 Сокращения и обозначения
БК - базовая компетенция– способность управлять собой и собственной деятельностью, склонность к самомотивации и самоорганизации.
ПК - профессиональная компетенция – способность специалиста решать совокупность профессиональных задач на основе знаний, умений и навыков, а также личностных качеств, позволяющих эффективно осуществлять профессиональную деятельность.
ПП - профессиональная практика – вид учебной деятельности, направленной на закрепление теоретических знаний, умений, приобретение и развитие практических навыков и компетенций в процессе выполнения определенных видов работ, связанных с будущей профессиональной деятельностью.
ОК - обязательный компонент – перечень учебных дисциплин и соответствующих минимальных объемов кредитов, установленных типовым учебным планом и изучаемых студентами в обязательном порядке по программе обучения;
Компонент по выбору – перечень учебных дисциплин и соответствующих минимальных объемов кредитов (или академических часов), предлагаемых высшими учебными заведениями, самостоятельно выбираемых студентами в любом академическом периоде с учетом их пререквизитов и постреквизитов.
КЭД - каталог элективных дисциплин – систематизированный аннотированный перечень всех дисциплин компонента по выбору, содержащий их краткое описание с указанием цели изучения, краткого содержания (основных разделов) и ожидаемых результатов изучения (приобретаемые студентами знания, умения, навыки и компетенции).
СРО - Самостоятельная работа обучающихся - работа по определенному перечню тем, отведенных на самостоятельное изучение, обеспеченных учебно-методической литературой и рекомендациями, контролируемая в виде тестов, контрольных работ, коллоквиумов, рефератов, сочинений и отчетов.
СРОП - самостоятельная работа обучающихся под руководством преподавателя – внеаудиторная работа обучающегося под руководством преподавателя, проводимая по утвержденному графику.
Постреквизиты - дисциплины, для изучения которых требуются знания, умения и навыки, приобретаемые по завершении изучения данной дисциплины;
Пререквизиты - дисциплины, содержащие знания, умения и навыки, необходимые для освоения изучаемой дисциплины.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.