
Текст к уроку
Источник: http://ru.solverbook.com/spravochnik/uravneniya-po-fizike/uravnenie-puassona/
Уравнение Пуассона описывает адиабатный процесс, протекающий в идеальном газе. Адиабатным называют такой процесс, при котором отсутствует теплообмен между рассматриваемой системой и окружающей средой Q=0
Уравнение Пуассона имеет вид:
![]()
![]()
Здесь V – объем, занимаемый газом, p – его давление, а k (γ) –величина, которая называется показателем адиабаты.
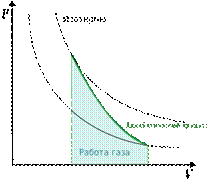
График адиабатного процесса:
 |
Показатель адиабаты можно рассчитать, как отношение изобарной теплоемкости газа к его изохорной теплоемкости:
![]()
В практических расчётах удобно помнить, что для
идеального газа показатель адиабаты равен ![]() , для двухатомного –
, для двухатомного – ![]() , а для трёхатомного –
, а для трёхатомного – ![]() .
.
Как же быть с реальными газами, когда важную роль
начинают играть силы взаимодействия между молекулами? В этом случае показатель
адиабаты для каждого исследуемого газа можно получить экспериментально. Один из
таких методов был предложен в 1819 году Клеманом и Дезормом. Мы наполняем
баллон холодным газом, пока давление в нём не достигнет ![]() . Затем
открываем кран, газ начинает адиабатически расширяться, а давление в баллоне
падает до атмосферного
. Затем
открываем кран, газ начинает адиабатически расширяться, а давление в баллоне
падает до атмосферного ![]() . После того, как газ изохорно
прогреется до температуры окружающей среды, давление в баллоне повысится
до
. После того, как газ изохорно
прогреется до температуры окружающей среды, давление в баллоне повысится
до ![]() . Тогда показатель адиабаты можно рассчитать за формулой:
. Тогда показатель адиабаты можно рассчитать за формулой:
![]()
Показатель адиабаты всегда больше 1, поэтому при адиабатическом сжатии газа – как идеального, так и реального – до меньшего объема температура газа всегда возрастает, а при расширении газ охлаждается. Это свойство адиабатического процесса, называемое пневматическим огнивом, применяется в дизельных двигателях, где горючая смесь сжимается в цилиндре и воспламеняется от высокой температуры. Вспомним первый закон термодинамики: Q=ΔU+A, где ΔU — внутренняя энергия системы, а А – выполняемая над ней работа. Поскольку Q=0, то работа, осуществляемая газом, идёт только на изменение его внутренней энергии – а значит, температуры. Из уравнения Пуассона можно получить формулу для расчёта работы газа в адиабатном процессе:
![]()
Здесь n – количество газа в молях, R – универсальная газовая постоянная, Т – абсолютная температура газа.
Уравнение Пуассона для адиабатического процесса применяется не только при расчётах двигателей внутреннего сгорания, но и в проектировании холодильных машин.
Стоит помнить, что уравнение Пуассона точно описывает только равновесный адиабатный процесс, состоящий из непрерывно сменяющих друг друга состояний равновесия. Если же мы в реальности откроем кран в баллоне, чтобы газ адиабатически расширился, возникнет нестационарный переходной процесс с завихрениями газа, которые затухнут из-за макроскопического трения.
Реальный процесс можно считать адиабатный, если он протекает очень быстро и не успевает осуществиться теплообмен с окружающей средой.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.