
Тема урока: «Алкены: строение молекул, гомология и изомерия».
Андриянова Ольга Станиславна, учитель химии МОУ «Каракокшинская СОШ им. С.В.Тартыкова»
Класс: 10
Тип урока: урок открытия новых знаний
Цели:
- изучение строения алкенов; выявление их существенных отличий от алканов; изучение видов изомерии алкенов;
- прогнозирование химических свойств алкенов на основе их строения.
Планируемые результаты:
Личностные
- проявление эмоционально-ценностного отношения к учебной проблеме;
- проявление творческого отношения к процессу обучения.
Метапредметные
Познавательные: умение находить сходство и различие между алкенами и алканами, обобщать полученную информацию, делать выводы.
Регулятивные:
- умение выполнять учебное задание в соответствии с поставленной целью;
- умение соотносить учебные действия с известными правилами;
- умение выполнять учебное действие в соответствии с алгоритмом.
Коммуникативные:
- умение формулировать высказывание;
- умение согласовывать позиции и находить общее решение;
- умение адекватно использовать речевые средства и символы для представления результата.
Предметные:
-умение характеризовать строение алкенов;
- умение сравнивать строение алкенов с алканами;
- умение называть вещества;
- умение определять вид изомерии.
Используемые технологии: ИКТ, технология развивающего обучения.
Информационно-технологические ресурсы:
Г.Е. Рудзитис, Ф.Г. Фельдман. Химия. 10 класс: учебник для общеобразовательных учреждений, базовый уровень/ Г.Е. Рудзитис, Ф.Г. Фельдман. – М.: Просвещение, 2019; компьютер, мультимедиа проектор, презентация по теме “Алкены”.
Ход урока
1. Организационный этап – проверка готовности обучающихся к уроку, положительный настрой на урок.
2. Актуализация знаний
Фронтальная беседа:
- Какие вещества называются углеводородами?
- На какие группы делят углеводороды?
- Дайте определение алканы.
- Что такое изомеры?
- Какие виды изомерии характерны для алканов?
- Какие вещества называются гомологами?
Самостоятельная работа обучающихся:
1. Выпишите формулы алканов: C4H8, CH4, C2H2, C5H12, C2H4, C3H6, C7H16, C8H18, C8H16, C5H10. Назовите вещества. (слайд № 1)
Самопроверка, (слайд №2)
/CH4 – метан, C5H12-пентан, C7H16- гептан, C8H18-октан/
2. Назовите вещества (проверка слайд № 3):
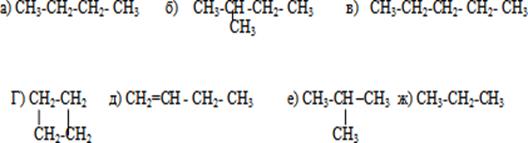
- Какие трудности вы испытали при выполнении данного задания?
3. Мотивация и постановка учебной задачи.
Будет ли УВ, формула которого представлена под буквой Д, относиться к предельным УВ? Почему? (Не отвечает общей формуле алканов). К какому классу УВ его можно отнести?
Самостоятельная работа обучающихся: Составьте структурную формулу данного УВ, исходя из того, что валентность углерода в органических соединениях равна четырём.
Постановка целей урока
4. Открытие нового знания
1. Запись темы в тетрадь: Алкены: строение молекул, гомология и изомерия.
2. Самостоятельная работа обучающихся с текстом учебника:
- Найдите в тексте определение Алканы, запишите общую формулу алканов.
- Используя понятия гомологи, гомологическая разность, составьте гомологический ряд алкенов.
Может ли гомологический ряд алкенов начинаться с УВ, в состав которого входит только один атом углерода. Почему?
3. Работа в парах: (слайд №4)
Выпишите формулы веществ, которые можно отнести к алкенам:
С4Н8, СН4, С5Н12, С2Н4, С3Н4, С7Н16, СН2, С6Н6, С8Н16, С5Н10. Назовите алкены (изменяя -ан на –ен)
Самопроверка, (слайд №5)
|
4. Работа в парах: Назовите вещества по систематической номенклатуре:
|
|||||||||||||||||||
|
5. Самостоятельная работа: Напишите
структурные формулы: |
|||||||||||||||||||
|
6. Объяснение по таблице: Электронное и пространственное строение этилена. В молекуле этилена СН2 = СН2 оба атома углерода, связанные двойной связью, находятся в состоянии sp2 – гибридизации. То есть в гибридизации участвует 1 s-облако и 2 p-облака (в отличие от этана у которого в гибридизации участвуют 1 s-облако и 3 p-облака), и по одному p-облаку у каждого атома углерода остаются негибридизованными. Оси sp2 - орбиталей лежат в одной плоскости (в отличие от алканов, в которых атом углерода имеет объемную форму - тетраэдр). Угол между ними составляет 1200 (в алканах 109028/). Длина двойной связи меньше одинарной и составляет 0,133 нм (у алканов l=0,154 нм). Из-за наличия двойной связи свободное вращение относительно связи С=С невозможно (тогда как у алканов возможно свободное вращение вокруг одинарной связи).
1.Назовите вещества: 1) СН2 = СН – СН2 – СН3 2) СН3 – СН = СН – СН2 – СН3 3) СН3 – С = СН – СН2 – СН3
СН3
2. Гомологом пропена является: а) С3 Н8 б) С5 Н10 в) С4 Н8 г) С4 Н10 3. Вещество СН2 = С – СН2 – СН3 имеет название:
СН3 а) 2 – метилбутан б) 2,2 – диметилбутан в) бутен – 1 г) 2 – метилбутен – 1 4. Двойная связь имеется в молекулах: а) алканов б) циклоалканов в) алкенов г) алкинов. 5. Алкены имеют общую формулу: а) Сn H2n+2 б) Сn H2n в) Сn H2n-2 г) Сn H2n+1 6. В молекулах алканов связи: а) двойные; б) одна тройная; в) одинарные; г) две двойные. 7. Двойная связь в алкенах состоит из: а) одной сигма-связи и одной пи- связи б) двух пи-связей в) двух сигма-связей г) верного ответа среди перечисленных нет. 6. Подведение итогов, рефлексия.
|
|||||||||||||||||||
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.