
Входной контроль 11 класс
Вариант 1.
1. Число электронных слоев и число электронов на внешнем электронном слое атомов брома соответственно равны:
1) 7 и 4; 2) 4 и 7; 3) 35 и 7; 4) 4 и 35.
2. Электронная конфигурация атома железа:
1) ls22s22p63s23p6 ;2) 1s22s22p63s23p64s24p 2 ; 3) ls22s22p63s23p63d8 ;
4) 1s22s22p63s23p63d64s2 .
3. Номер периода элемента в периодической системе соответствует
1) заряду ядра атома этого элемента
2) числу электронов на валентной оболочке атома этого элемента
3) числу электронных уровней атома этого элемента
4) среднему значению массовых чисел изотопов этого элемента
4. Элементу, электронная формула атома которого ls22s22p63s23p63d54s2 соответствует высший оксид, формула которого: 1) Вг2О7; 2) MnО2; 3) MnO; 4) Mn2О7.
5. Наибольшую электроотрицательность имеет:
1) фосфор; 2) хлор; 3) кремний; 4) сера.
6. В ряду химических элементов фтор → хлор → бром:
1) усиливаются неметаллические свойства;
2) увеличивается радиус атома;
3) увеличивается степень окисления в летучих водородных соединениях;
4) увеличивается электроотрицательность.
7. Ряд химических элементов, в котором неметаллические свойства усиливаются:
1) фтор → бром → иод;
2) кремний → фосфор → хлор;
3) кислород → сера → селен
8. Вещества только с ионной связью приведены в ряду:
1) F2, ССl4, КС1
2) NaBr, Na2O, KI
3) SO2. P4 , CaF2
4) H2S, Br2, K2S
9. Установите соответствие между формулой вещества и степенью окисления атома хлора в нём.
ФОРМУЛА ВЕЩЕСТВА
A) Ca(OCl)2
Б) KClO3
B) HClO2
Г) FeCl3
СТЕПЕНЬ ОКИСЛЕНИЯ ХЛОРА
1) +1
2) +3
3) -1
4) +5
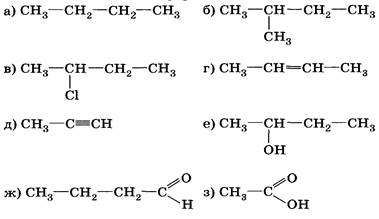
10. Распредели вещества, формулы которых приведены по классам соединений и назови их.
Входной контроль 11 класс
Вариант 2.
1. Число электронных слоев и число электронов на внешнем электронном слое атомов марганца соответственно равны: 1) 4 и 7; 2) 4 и 2; 3) 7 и 4; 4) 4 и 5.
2. Электронная конфигурация атома ванадия: 1) ls22s22p63s23p63d5 ;
2) ls22s22 p63s23p63d34s2 ; 3) ls22s22p63s23p63d44s1 ; 4) ls 22s22p63s23p64s24p 3
3. Номер группы элемента в периодической системе соответствует
1) заряду ядра атома этого элемента
2) числу электронов на валентной оболочке атома этого элемента
3) числу электронных уровней атома этого элемента
4) среднему значению массовых чисел изотопов этого элемента
4. Наименьшую электроотрицательность имеет:
1) фтор; 3) бром; 2) хлор; 4) иод.
5. В ряду химических элементов барий → кальций → магний:
1) увеличивается радиус атома; 2) усиливаются металлические свойства;
3) уменьшается радиус атома; 4) увеличивается степень окисления в высших оксидах.
6. Ряд химических элементов, в котором металлические свойства ослабевают:
1) литий → бериллий → бор;
2) натрий → магний → алюминий;
3) углерод → кремний → германий
7. Элементу, электронная формула атома которого ls22s22p63s23p4 , соответствует высший оксид, формула которого: 1) SО2; 2) SO3; 3) SeO2; 4) CrО3.
8. В каком ряду все вещества имеют ковалентную полярную связь?
1) HCl, NaCl, Cl2
2) O2, H2O, CO2
3) H2O.NH3.CH4
4) CH3OH, HBr, CO
9. Установите соответствие между формулой вещества и степенью окисления атома азота в нём.
ФОРМУЛА ВЕЩЕСТВА СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТА
A) NH4Cl 1) -3
Б) HNO3 2) +3
B) NH4NO3 3) +5
Г) N2O3 4) -3, +5
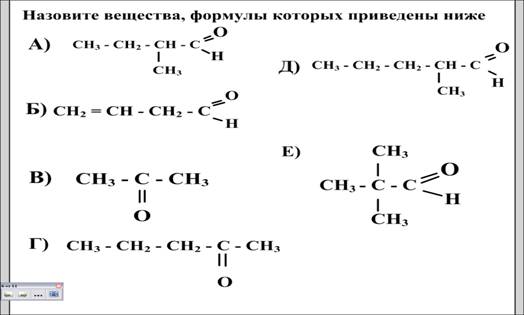
10. Распредели вещества, формулы которых приведены по классам соединений и назови их.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.